修回日期: 2019-11-14
接受日期: 2019-11-20
在线出版日期: 2019-11-28
伊立替康(camptothecin-11, CPT-11)为晚期结肠癌的一线化疗用药, 但CPT-11耐药性限制了CPT-11的化疗效果. 研究结肠癌CPT-11耐药的机制, 并恢复结肠癌细胞对CPT-11的敏感性, 对延长结肠癌患者的生命时间具有十分重要的临床价值.
探讨长链基因间非编码RNA-p21(long intergenic non-coding RNA-p21, lincRNA-p21)对结肠癌细胞CPT-11耐药的作用和机制.
采用结肠癌HCT-8细胞和SW480细胞利用CPT-11持续接触浓度递增法分别构建伊立替康耐药HCT-8/CPT-11细胞和SW480/CPT-11细胞, 并利用实时定量聚合酶链式反应(real-time quantitative polymerase chain reaction, RT-qPCR)检测细胞内lincRNA-p21表达. HCT-8/CPT-11细胞和SW480/CPT-11细胞分别转染pcDNA-lincRNA-p21或si-lincRNA-p21后, 细胞计数试剂盒-8(cell counting kit-8, CCK-8)实验检测CPT-11对细胞活性的影响; 蛋白质免疫印迹(Western blot)初步分析了lincRNA-p21对磷脂酰肌醇3-激酶/蛋白激酶B(phosphoinositide 3-kinase/protein kinase B, PI3K/AKT)通路是否有调节作用. 采用PI3K/AKT通路抑制剂LY294002预处理已转染si-lincRNA-p21的HCT-8/CPT-11细胞和SW480/CPT-11细胞或采用PI3K/AKT通路激动剂Recilisib预处理已转染pcDNA-lincRNA-p21的HCT-8/CPT-11细胞和SW480/CPT-11细胞, CCK-8实验检测CPT-11对细胞活性的影响.
与亲本细胞相比, CPT-11耐药细胞中lincRNA-p21表达明显降低. 过表达lincRNA-p21抑制HCT-8/CPT-11细胞和SW480/CPT-11细胞对CPT-11耐药性, 而敲低lincRNA-p21增强HCT-8/CPT-11细胞和SW480/CPT-11细胞对CPT-11耐药性. Western blot结果显示, lincRNA-p21过表达抑制PI3K/AKT通路活性; 而敲低lincRNA-p21增强PI3K/AKT通路活性. LY294002能抑制lincRNA-p21敲低对CPT-11耐药的促进作用; Recilisib能抑制lincRNA-p21过表达对CPT-11耐药的抑制作用.
上调lincRNA-p21能抑制结肠癌细胞CPT-11耐药性, 而下调lincRNA-p21能增强结肠癌细胞CPT-11耐药性, 这种调节作用可能与lincRNA-p21调控PI3K/AKT信号通路活性相关.
核心提要: lincRNA-p21在HCT-8/CPT-11和SW480/CPT-11细胞中低表达. 过表达lincRNA-p21能部分逆转HCT-8/CPT-11和SW480/CPT-11细胞的CPT-11耐药性并伴随抑制磷脂酰肌醇3-激酶/蛋白激酶B活性; 敲减lincRNA-p21以上指标呈相反结果.
引文著录: 戴丹平, 余灵芝, 叶梦飞. LincRNA-p21调控PI3K/AKT信号通路逆转结肠癌细胞伊立替康耐药性. 世界华人消化杂志 2019; 27(22): 1356-1364
Revised: November 14, 2019
Accepted: November 20, 2019
Published online: November 28, 2019
Irinotecan (camptothecin-11, CPT-11) is a first-line chemotherapy drug for advanced colon cancer, but CPT-11 resistance limits its efficacy. Studying the mechanism of CPT-11 resistance in colon cancer and restoring the sensitivity of colon cancer cells to CPT-11 are of great clinical value in prolonging the life time of colon cancer patients.
To investigate the effect and mechanism of long intergenic non-coding RNA-p21 (lincRNA-p21) on CPT-11 resistance in colon cancer cells.
HCT-8 and SW480 cells were used to construct irinotecan-resistant HCT-8/CPT-11 and SW480/CPT-11 cell lines by continuously exposing them to increasing concentrations of CPT-11, and the expression of lincRNA-p21 in the cells was detected by real-time quantitative polymerase chain reaction (RT-qPCR). After transfection with pcDNA-lincRNA-p21 or si-lincRNA-p21, the effect of CPT-11 on the viability of HCT-8/CPT-11 cells or SW480/CPT-11 cells was measured by cell counting kit-8 (CCK-8) assay. The regulatory effect of lincRNA-p21 on the phosphoinositide 3-kinase/protein kinase B (PI3K/AKT) pathway was preliminarily analyzed by Western blot. After pretreatment with PI3K/AKT pathway inhibitor LY294002 prior to transfection with si-lincRNA-p21, or pretreatment with PI3K/AKT pathway agonist Recilisib prior to transfection with pcDNA-lincRNA-p21, the effect of CPT-11 on cell viability in HCT-8/CPT-11 cells or SW480/CPT-11 cells was measured by CCK-8 assay.
LincRNA-p21 expression in CPT-11 resistant cells was significantly lower than that in parental cells. Overexpression of lincRNA-p21 inhibited the resistance of HCT-8/CPT-11 cells and SW480/CPT-11 cells to CPT-11, while knockdown of lincRNA-p21 enhanced the resistance of HCT-8/CPT-11 cells and SW480/CPT-11 cells to CPT-11. Western blot results showed that overexpression of lincRNA-p21 inhibited the activity of the PI3K/AKT pathway, while knockdown of lincRNA-p21 enhanced the activity of the PI3K/AKT pathway. LY294002 inhibited the promotive effect of lincRNA-p21 knockdown on CPT-11 resistance, while Recilisib inhibited the inhibitive effect of lincRNA-p21 overexpression on CPT-11 resistance.
Up-regulation of lincRNA-p21 can inhibit the CPT-11 resistance of colorectal cancer cells, while down-regulation of lincRNA-p21 can promote their CPT-11 resistance, which may be related to the regulation of the PI3K/AKT signaling activity by lincRNA-p21.
- Citation: Dai DP, Yu LZ, Ye MF. LincRNA-p21 reverses irinotecan resistance in colon cancer cells via the PI3K/AKT signaling pathway. Shijie Huaren Xiaohua Zazhi 2019; 27(22): 1356-1364
- URL: https://www.wjgnet.com/1009-3079/full/v27/i22/1356.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v27.i22.1356
结肠癌是一种常见的消化道肿瘤, 是全球癌症患者死亡的常见原因[1]. 化疗是常见的结肠癌治疗手段之一, 但结肠癌的化疗效果常受到化疗药物耐药性的制约[2]. 而鉴定逆转结肠癌化疗耐药的生物标志物并阐明潜在的分子机制有助于开发新的治疗结肠癌的策略[3]. 伊立替康(camptothecin-11, CPT-11)为晚期结肠癌的一线用药, 但经过一段时间化疗后, 往往造成化疗耐药性增加. 因此, 深入研究结肠癌CPT-11耐药的机制, 并恢复结肠癌细胞对CPT-11的敏感性, 对延长结肠癌患者的生命时间具有十分重要的临床价值及社会意义.
长链基因间非编码RNA-p21(long intergenic non-coding RNA-p21, lincRNA-p21)被称为p53直接转录靶, 已发现其在多种人类实体瘤中下调[4,5], 且lincRNA-p21可以抑制肝癌、肺癌和胃癌等肿瘤的发生发展[5-7]. 而, lincRNA-p21在结肠癌中对化疗耐药性影响的研究尚少. 因此本实验主要研究lincRNA-p21对结肠癌细胞CPT-11耐药性的调节作用, 并初步研究其作用机制.
人结肠癌细胞HCT-8和SW480购自于美国典型培养物保藏中心(american type culture collection, ATCC); 胎牛血清(fetal bovine serum, FBS)和PRMI-1640培养基购于美国Gibco公司; 细胞计数试剂盒-8(cell counting kit-8, CCK-8)、辣根过氧化物酶(horseradish peroxidase, HRP)耦合的二抗和二喹啉甲酸(bicinchoninic acid disodium, BCA)试剂盒购于江苏碧云天公司; CPT-11粉剂由江苏恒瑞公司赠予; TRIZol试剂、逆转录试剂盒和SYBR GreenⅠ购于日本Takara公司; 磷脂酰肌醇3-激酶(phosphoinositide 3-kinase, PI3K)、磷酸化PI3K(phospho-PI3K, p-PI3K)、蛋白激酶B(protein kinase B, AKT)和磷酸化AKT(phospho-AKT, p-AKT)抗体购于美国CST公司. PI3K/AKT通路抑制剂LY294002和激动剂Recilisib购自美国Med Chem Express公司; 包含全长lincRNA-p21的克隆载体(pcDNA-lincRNA-p21)和靶向抑制lincRNA-p21的siRNA(si-lincRNA-p21) (序列为: GAUAGAUAAUGUUCCUCAA)以及pcDNA空载体(pcDNA-vector)和阴性siRNA(siRNA-Negative control, si-NC) (序列为: UUCUCCGAACGUGUCACGU)由上海吉玛公司合成.
1.2.1 CPT-11耐药的细胞株的诱导与构建: 按照文献[8]中描述的方法, 采用药物持续接触浓度递增法逐步诱导HCT-8细胞和SW480细胞对CPT-11耐药. 取对数期生长状态良好的HCT-8细胞和SW480细胞用胰酶消化, 离心后弃上清并重悬, 取约1×106细胞数的细胞接种于含CPT-11初浓度为5 μmol/L的培养基中, 每48 h后换液一次. 同一浓度的药物反复处理3代细胞, 当细胞能维持生长且存活率大于80%时, 根据细胞存活状况不断增加药物浓度, 并依此反复处理, 直至其能在50 μmol/L的药物浓度中稳定生长, 命名为HCT-8/CPT-11细胞和SW480/CPT-11细胞. 使用耐药细胞株前, 将其培养在含有25 μmol/L CPT-11的细胞培养液中持续培养1 wk.
1.2.2 细胞培养: HCT-8、SW480、HCT-8/CPT-11和SW480/CPT-11细胞在含有10%FBS的PRMI-1640培养液中, 置在37 ℃和5%CO2的条件下培养, 并且每隔2 d换液一次, 每周用0.25%胰蛋白酶消化传代.
1.2.3 结肠癌CPT-11耐药细胞转染: HCT-8/CPT-11和SW480/CPT-11细胞接种于6孔板中, 贴壁后利用Lipofectamine 3000辅助转染si-lincRNA-p21、si-NC、pcDNA-lincRNA-p21和pcDNA-vector, 6 h后更换为新鲜培养基, 继续培养细胞48 h. 细胞经实时定量聚合酶链式反应(real-time quantitative polymerase chain reaction, RT-qPCR)确定已经转染成功后, 用于后续实验.
1.2.4 RT-qPCR实验: 使用TRIZol试剂提取待测细胞的总RNA, 利用逆转录试剂盒合成基因cDNA链. 以cDNA为模板, 加入SYBR GreenⅠ及引物混合后用7500 Fast Applied Biosystems进行RT-qPCR实验. LincRNA-p21反应条件: 95 ℃ 5 min, 40个循环: 95 ℃ 1min, 74 ℃ 30s, 72 ℃ 34s. GAPDH引物(5'-3'): 正向引物: GGGAAATTCAACGGCACAGT , 反向引物: AGATGGTGATGGGCTGCCC; lincRNA-P21引物(5'-3'): 正向引物: GGGTGGCTCACTCTTCTGGC, 反向引物: TGGCCTTGCCCGGGCTTGTC. 以GAPDH为内参, 行2-ΔΔCt法进行量化lincRNA-p21表达.
1.2.5 CCK-8检测细胞活性: 细胞按照4000个/孔的密度接种于96孔板培养板中, 按照实验指定的要求, 采用或者不采用LY294002(10 μmol/L)[9]和Recilisib(10 μmol/L)[10]预处理细胞30 min, 再采用不同浓度(25, 50, 100, 150, 200 μmol/L)[8] CPT-11培养细胞24 h. 实验达到终点时间后, 加入10 μL CCK-8染色液, 在细胞培养箱中孵育2 h后, 在450 nm处测定各孔吸光度.
1.2.6 蛋白质免疫印迹(Western blot): 以裂解液(10 mmol/ L Tris-HCl、150 mmol/ L NaCl、0.11% SDS、1% Triton-100、2 μg/mL Aprotinin、2 μg/mL Leupeptin、1 mmol/L PMSF)抽提已转染细胞的总蛋白, BCA法定量蛋白含量. 每样品取20 μg细胞总蛋白进行电泳, 然后转移蛋白至聚偏二氟乙烯(polyvinylidene fluoride, PVDF)膜上, 5%脱脂奶粉室温封闭2 h, 随后, 将膜与p-PI3K、PI3K、p-AKT、AKT一抗(稀释度1:500)在4 ℃温育过夜. 第二天, 洗涤膜后, 将膜与HRP标记的二抗(稀释度1:10000)一起室温孵育1 h. 洗涤膜后, 使用Tanon GIS凝胶成像系统ECL显影, 曝光成像. 用Image J软件扫描灰度值, 以GAPDH内参灰度值为对照, 用其比值作图.
统计学处理 采用SPSS 20.0统计软件进行数据分析, 符合正态分布的数据表示为mean±SD. 俩组数据比较, 采用成组t检验; 多组间数据两两比较, 先行方差分析齐性检验, 满足方差齐的条件下, 运用方差分析的后续检验. P<0.05为差异有统计学意义.
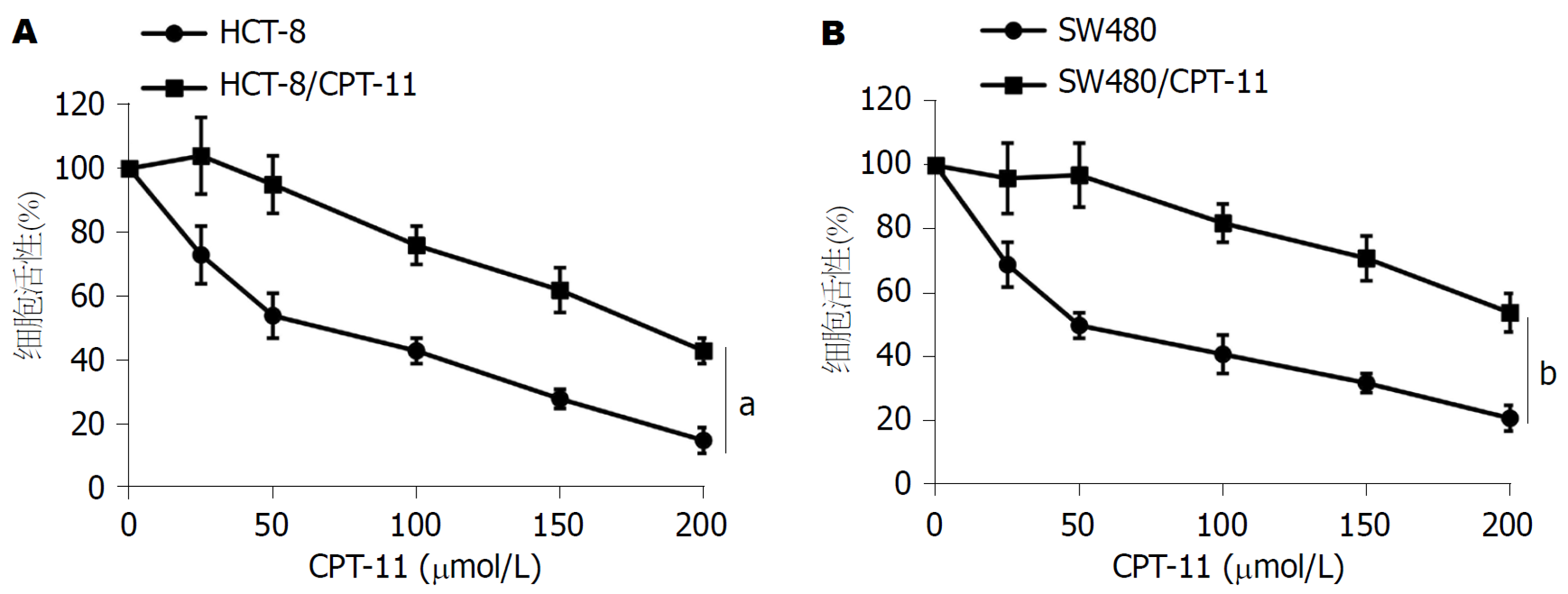
HCT-8细胞的IC50值为44.62 μmol/L±5.14 μmol/L, HCT-8/CPT-11细胞的IC50值为172.35 μmol/L±8.26 μmol/L, 耐药指数为3.86; SW480细胞的IC50值为47.83 μmol/L±4.02 μmol/L, SW480/CPT-11细胞的IC50值为219.64 μmol/L±11.18 μmol/L, 耐药指数为4.59; 与HCT-8细胞或SW480细胞比较, HCT-8/CPT-11细胞(图1A)或的SW480/CPT-11细胞(图1B)的细胞活性均明显升高(P<0.01). 以上结果表明CPT-11耐药细胞构建成功.
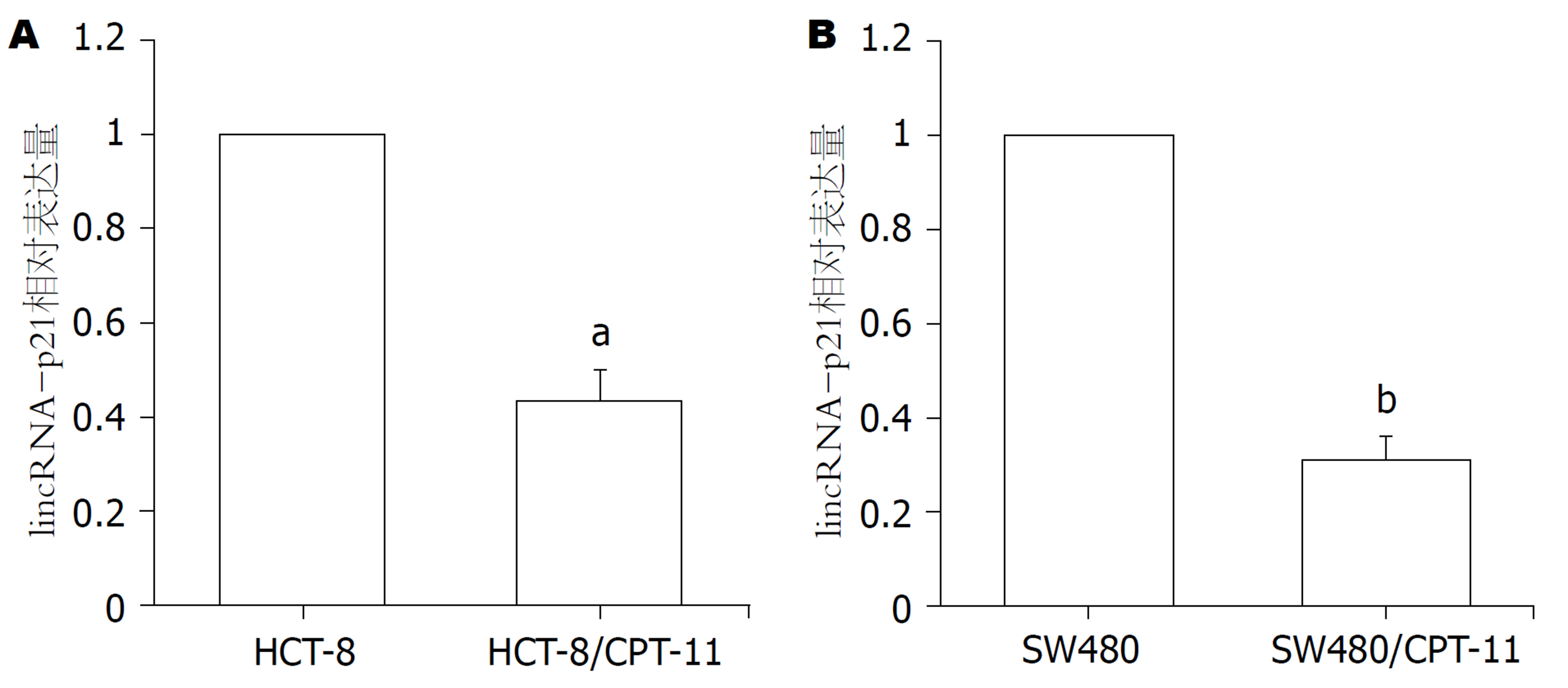
通过RT-qPCR检测CPT-11耐药细胞和亲本细胞中lincRNA-p21相对表达量. 结果如图2显示, 分别与HCT-8细胞或SW480细胞比较, HCT-8/CPT-11细胞(图2A)或SW480/CPT-11细胞(图2B)中lincRNA-p21的相对表达量均明显降低(P<0.01).
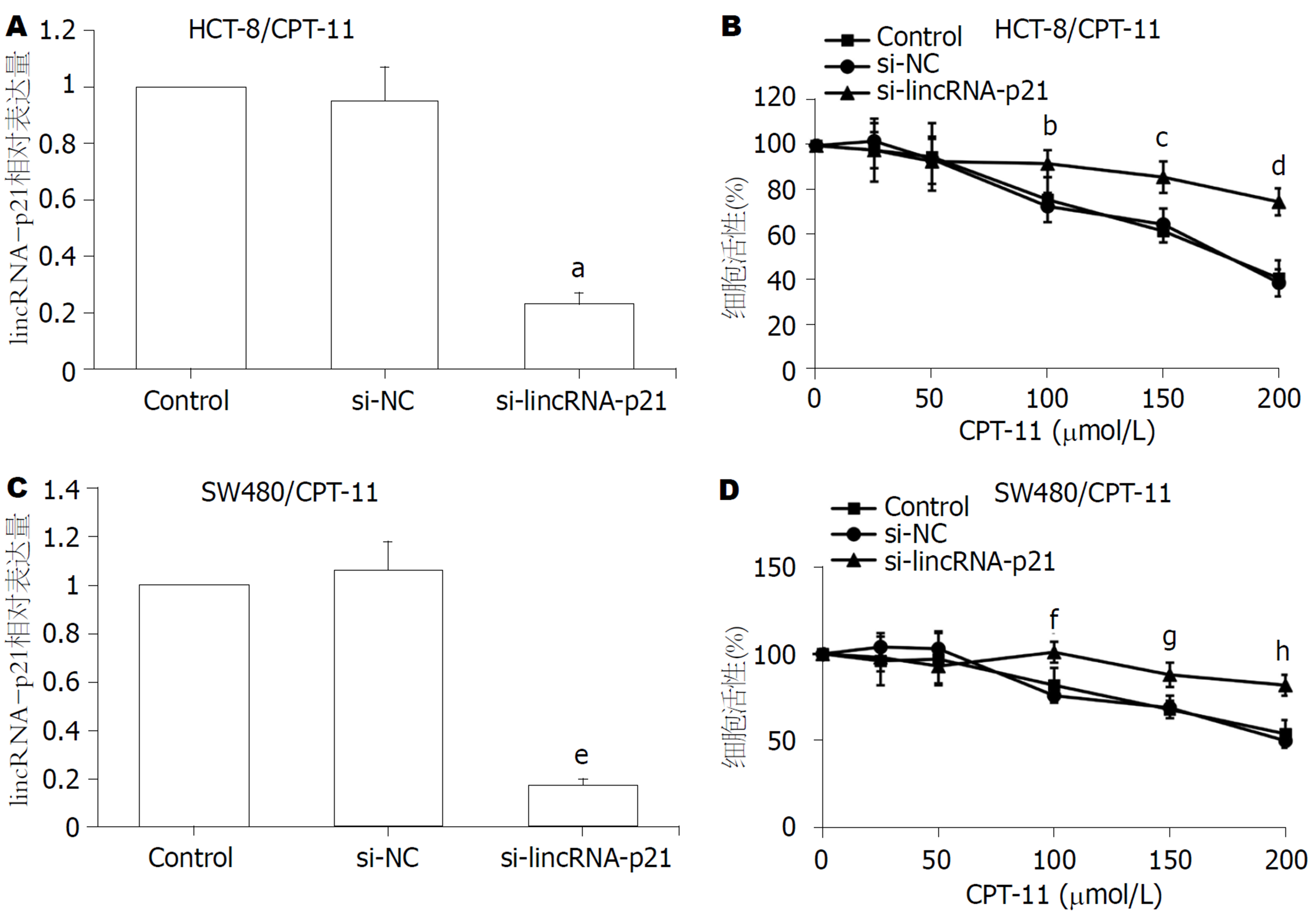
分别对HCT-8/CPT-11细胞或SW480/CPT-11细胞转染si-lincRNA-p21, CCK-8法检测敲低lincRNA-p21对CPT-11耐药细胞的敏感性的影响. HCT-8/CPT-11细胞敲低lincRNA-p21(图3A)后, 与si-NC组比较, si-lincRNA-p21组HCT-8/CPT-11细胞在100、150、200 μmol/L CPT-11浓度下的细胞活性均明显升高(P<0.05; P<0.01; P<0.001), 见图3B. 在SW480/CPT-11细胞中也得到了类似的结果, 见图3C和3D. 以上结果提示, lincRNA-p21敲低能增强CPT-11耐药性.
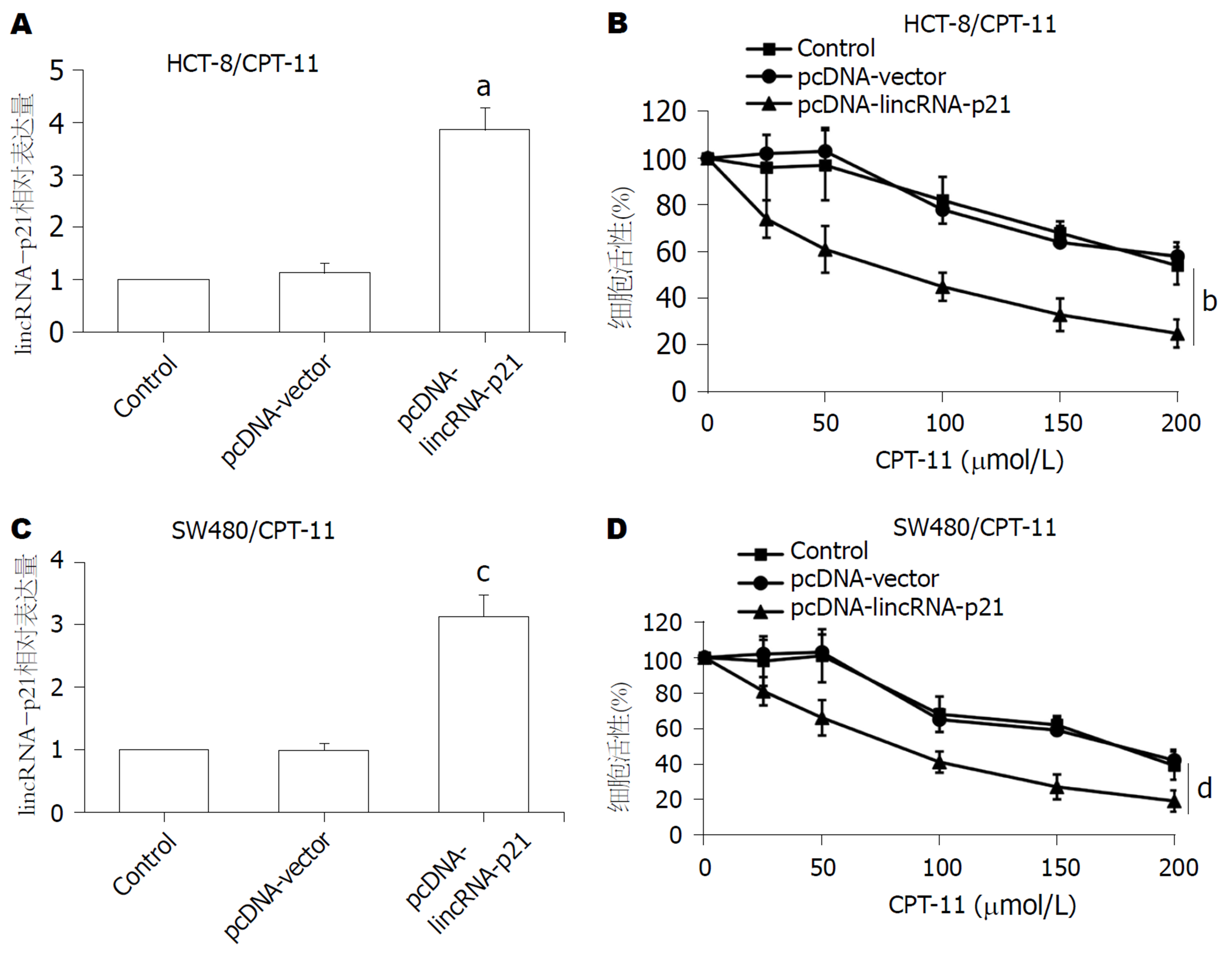
分别对HCT-8/CPT-11细胞或SW480/CPT-11细胞转染pcDNA-lincRNA-p21, CCK-8法检测过表达lincRNA-p21对CPT-11耐药细胞的敏感性的影响. HCT-8/CPT-11细胞过表达lincRNA-p21(图4A)后,与pcDNA-vector组比较, pcDNA-lincRNA-p21组HCT-8/CPT-11细胞在CPT-11处理下的细胞活性均明显降低(P<0.001), 见图4B. 在SW480/CPT-11细胞中也得到了类似的结果, 见图4C和4D. 以上结果提示, lincRNA-p21过表达能对CPT-11增敏.
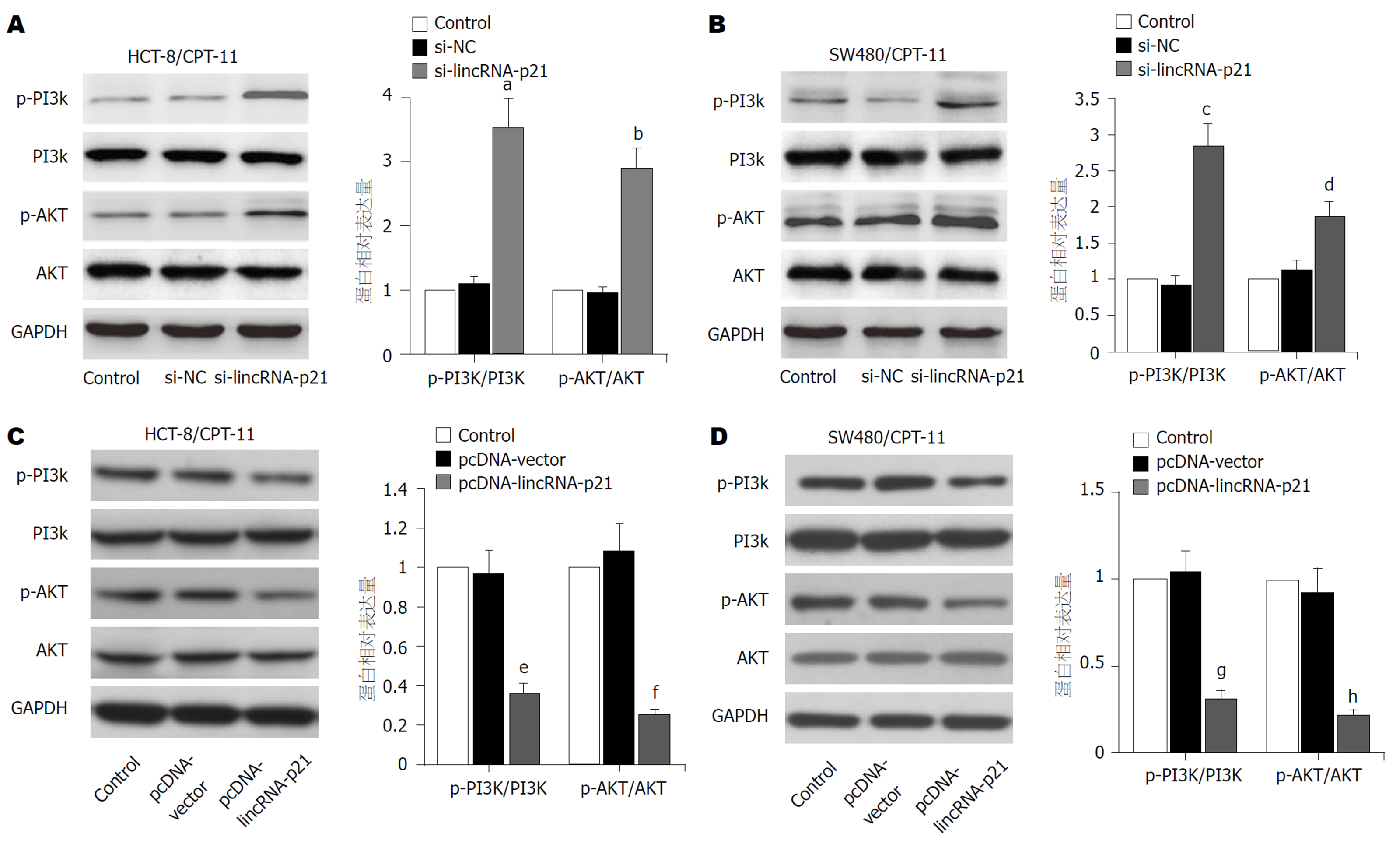
Western blot检测敲低或过表达lincRNA-p21对PI3K/AKT通路的调控作用: 转染si-lincRNA-p21后, 与si-NC组比较, si-lincRNA-p21组HCT-8/CPT-11细胞(图5A)或SW480/CPT-11细胞(图5B)中p-PI3K和p-AKT的相对表达量均明显升高(P<0.01). 转染pcDNA-lincRNA-p21后, 与pcDNA-vector组比较, pcDNA-lincRNA-p211组HCT-8/CPT-11细胞(图5C)或SW480/CPT-11细胞(图5D)中p-PI3K和p-AKT的相对表达量均明显降低(P<0.01). 结果提示, lincRNA-p21敲低促进CPT-11耐药细胞p-PI3K和p-AKT的表达, 而lincRNA-p21过表达抑制CPT-11耐药细胞p-PI3K和p-AKT的表达.
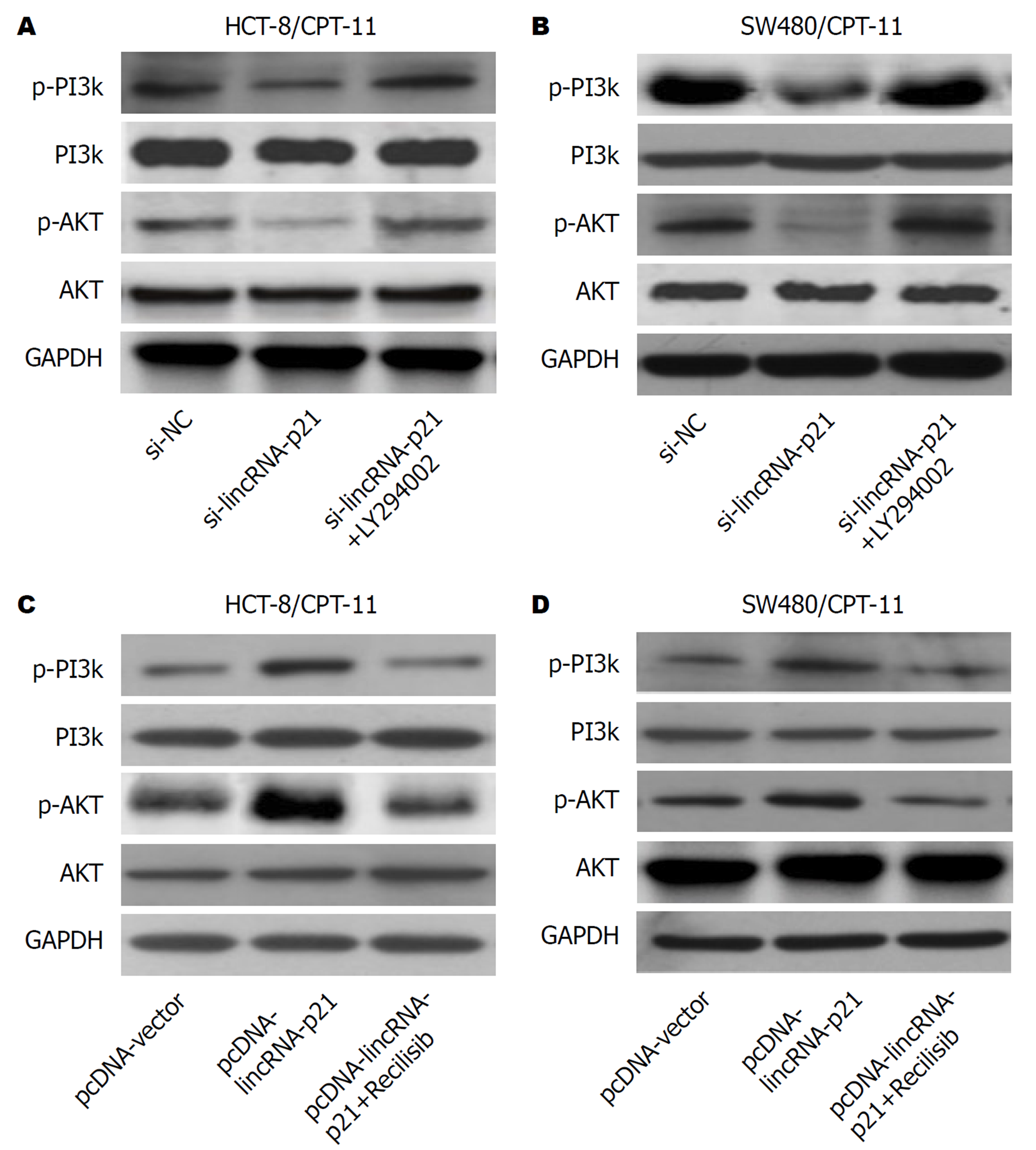
LY294002预处理的转染si-lincRNA-p21的CPT-11耐药细胞或Recilisib预处理的转染pcDNA-lincRNA-p21的CPT-11耐药细胞对PI3K/AKT通路信号的影响见图6.
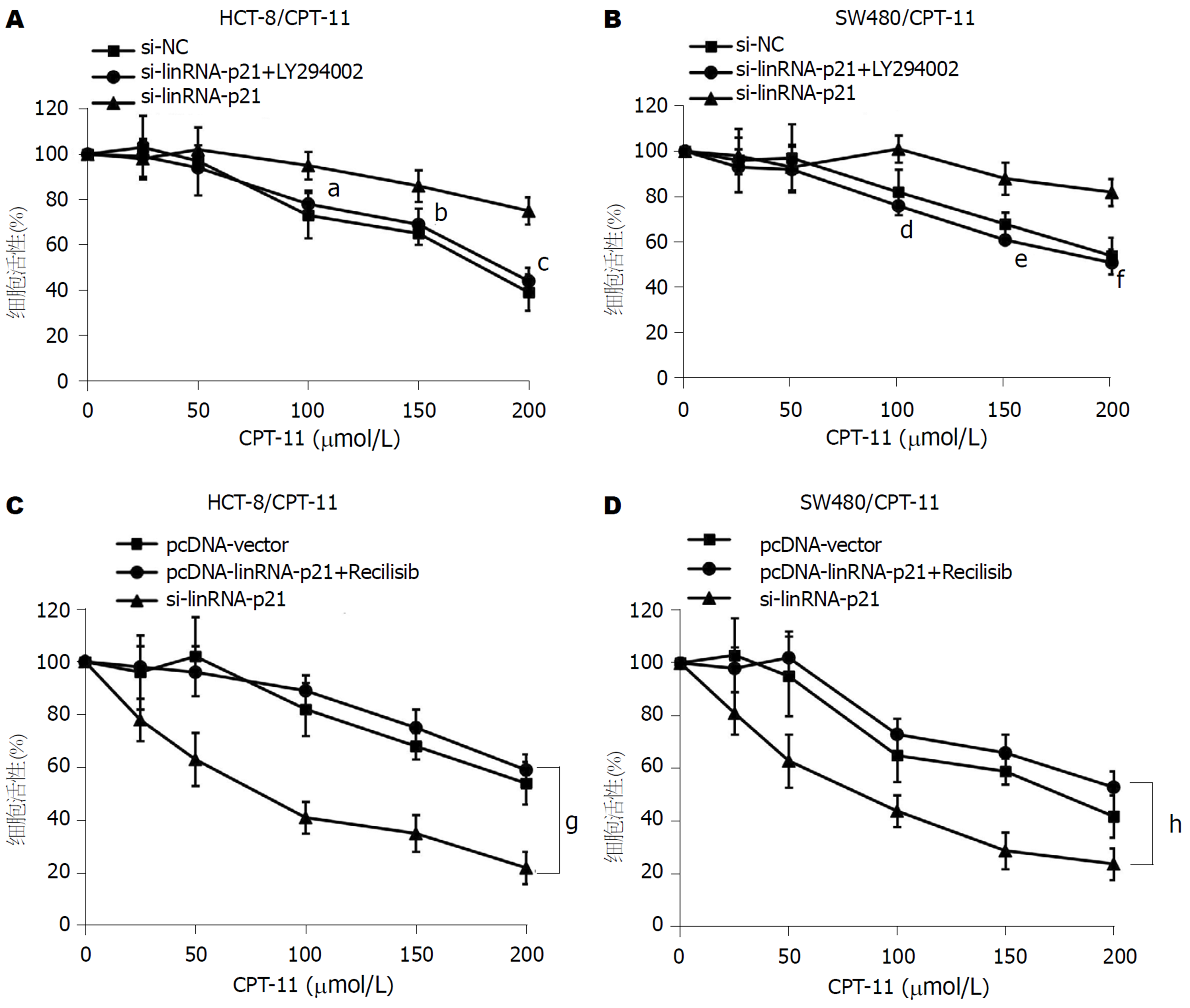
采用CCK-8检测LY294002预处理的转染si-lincRNA-p21的CPT-11耐药细胞对CPT-11敏感性的影响. 结果显示,与si-lincRNA-p21组比较, si-lincRNA-p21+LY294002组HCT-8/CPT-11细胞(图7A)或SW480/CPT-11细胞(图7B)分别在100、150、200 μmol/L CPT-11下的细胞活性均明显降低(P<0.05或P<0.01或P<0.001). 提示, LY294002预处理能抑制lincRNA-p21敲低对CPT-11耐药性的促进作用.
采用CCK-8检测Recilisib预处理的转染pcDNA-lincRNA-p21的CPT-11耐药细胞对CPT-11敏感性的影响. 结果显示, 与pcDNA-lincRNA-p21组比较, pcDNA-lincRNA-p21+Recilisib组HCT-8/CPT-11细胞(图7C)或SW480/CPT-11细胞(图7D)在CPT-11下的细胞活性均明显升高(P<0.001). 结果提示, Recilisib预处理能抑制lincRNA-p21过表达对CPT-11增敏作用.
以上实验结果共同提示, PI3K/AKT信号通路参与lincRNA-p21对CPT-11耐药性的调节作用.
CPT-11耐药是晚期结肠癌患者治疗失败的主要原因之一[11]. 而探索逆转结肠癌CPT-11耐药的机制有助于对延长结肠癌患者的生命时间. 近年研究[6,12,13]发现, lincRNA-p21在非小细胞肺癌, 食管癌和结直肠癌等多种肿瘤中下调表达, 而上调lincRNA-p21抑制肿瘤细胞的生长和侵袭. 有研究[14]报道lincRNA-p21具有增强结直肠癌细胞对放疗敏感性的作用, 然而lincRNA-p21对缓解结肠癌细胞CPT-11耐药性的作用目前尚未见报道. 本研究发现, 相对于结肠癌亲本细胞, lincRNA-p21在结肠癌CPT-11耐药细胞上低表达, 且敲低lincRNA-p21表达增强结肠癌CPT-11耐药细胞的耐药性, 而过表达lincRNA-p21能部分恢复结肠癌CPT-11耐药细胞对CPT-11的敏感性. 这一结果提示, lincRNA-p21是治疗结肠癌CPT-11耐药潜在的靶点.
本研究对lincRNA-p21调控结肠癌CPT-11耐药的机制进行了探索, 结果显示敲低lincRNA-p21促进p-PI3K和p-AKT的表达; 而过表达lincRNA-p21则抑制p-PI3K和p-AKT表达. 而PI3K/AKT信号传导在结肠癌发生发展中起着重要作用[15,16], 并且有已有研究报道化疗耐药结直肠癌组织或奥沙利铂耐药结直肠癌细胞中p-PI3K和p-AKT高表达, 而抑制PI3K/AKT信号活性能抑制顺铂耐药性[17]. 故, 我们推测lincRNA-p21调节CPT-11耐药性可能与其调控PI3K/AKT信号活性相关. 并且本研究进一步研究发现, PI3K/AKT抑制剂LY294002能逆转lincRNA-p21敲低对CPT-11耐药性的促进作用, PI3K/AKT激动剂Recilisib能抑制lincRNA-p21过表达对CPT-11增敏作用. 以上结果说明, lincRNA-p21通过调节PI3K/AKT信号活性来调控CPT-11耐药性.
另外, 众所周知PI3K/AKT抑制剂可以抑制肿瘤生长、侵袭、转移以及逆转多种化疗药物耐药性[18], 但PI3K/AKT信号活性同样也是正常细胞赖以生存、生长、代谢与维持功能的重要信号[19]. 在正常的组织或细胞中, PI3K/AKT信号同样也处于激活状态, 而抑制此信号活性可能会造成一系列级联的副作用[18,19]. 另外, 一些研究[20-22]数据显示, 高活性的PI3K/AKT信号能对抗老年痴呆、帕金森和抑郁等中枢神经疾病, 而PI3K/AKT抑制剂可加重这类疾病. 目前, 仅有西罗莫司和哌立福新应用于临床, 而其他PI3K/AKT抑制剂仍处于研究阶段. 而lincRNA-p21不但在众多肿瘤中下调[5-7,12,13], 并且也在其他非肿瘤疾病如动脉硬化与冠心病等疾病中下调表达[23,24], 且上调lincRNA-p21表达能一定程度减轻该类疾病的进展. 虽然在本研究中, lincRNA-p21抑制结肠癌CPT-11耐药细胞的PI3K/AKT信号活性, 但若能开发针对特异性低表达lincRNA-p21疾病的靶向恢复lincRNA-p21表达的制剂, 可能会避开PI3K/AKT抑制剂的不良反应. 这项研究对于筛选PI3K/AKT抑制剂也起到了一定的启示作用. 当然, 靶向恢复lincRNA-p21表达是否真能应用于PI3K/AKT抑制剂的筛选仍需大量的研究, 毕竟在其他细胞、组织或不同的处理条件中lincRNA-p21也能影响众多信号通路活性.
综上所述, lincRNA-p21是结肠癌CPT-11耐药治疗的潜在靶点, 上调lincRNA-p21通过抑制PI3K/AKT信号传导抑制结肠癌细胞CPT-11耐药, 从而起到部分恢复CPT-11化疗敏感性的作用. 这些发现可能为结肠癌CPT-11化疗耐药患者提供了一个新的生物标记物和治疗策略.
伊立替康(camptothecin-11, CPT-11)耐药是晚期结肠癌患者CPT-11化疗失败的主要原因之一. 而探索逆转结肠癌CPT-11耐药的机制对提高晚期结肠癌患者的CPT-11化疗具有重大意义.
长链基因间非编码RNA-p21(long intergenic non-coding RNA-p21, lincRNA-p21)在多种人类实体瘤中下调, 且其可以抑制多种肿瘤的发生与进展. 而, 关于lincRNA-p21在结肠癌中对CPT-11耐药性影响的研究尚未见报道.
探讨lincRNA-p21在结肠癌CPT-11耐药细胞中对CPT-11化疗敏感性的调节作用和机制.
构建结肠癌CPT-11耐药细胞, 并利用实时定量聚合酶链式反应(real-time quantitative polymerase chain reaction, RT-qPCR)检测细胞lincRNA-p21表达. 敲减或过表达lincRNA-p21后, 通过细胞计数试剂盒-8(cell counting kit-8, CCK-8)法检测结肠癌CPT-11耐药细胞对CPT-11敏感性的变化; 并通过Western blot检测改变lincRNA-p21表达对磷脂酰肌醇3-激酶/蛋白激酶B(phosphoinositide 3-kinase/protein kinase B, PI3K/AKT)通路活性的影响.
结肠癌CPT-11耐药细胞中lincRNA-p21低表达. 上调lincRNA-p21表达增强CPT-11耐药细胞对CPT-11敏感性并伴随抑制PI3K/AKT通路活性, 下调lincRNA-p21表达降低CPT-11耐药细胞对CPT-11敏感性并伴随增强PI3K/AKT通路活性.
lincRNA-p21可通过调控PI3K/AKT信号通路活性进而调节结肠癌耐药细胞对CPT-11敏感性的变化.
本研究为结肠癌CPT-11化疗耐药患者提供了一个潜在靶点和治疗策略. 另外, 这项研究对于筛选PI3K/AKT抑制剂也起到了一定的启示作用.
学科分类: 胃肠病学和肝病学
手稿来源地:
同行评议报告分类
A级 (优秀): A
B级 (非常好): B
C级 (良好): C, C
D级 (一般): 0
E级 (差): 0
编辑: 王禹乔 电编:刘继红
| 2. | Hawkins AT, Hunt SR. Watch and Wait: Is Surgery Always Necessary for Rectal Cancer? Curr Treat Options Oncol. 2016;17:22. [PubMed] [DOI] |
| 3. | De Mattia E, Cecchin E, Toffoli G. Pharmacogenomics of intrinsic and acquired pharmacoresistance in colorectal cancer: Toward targeted personalized therapy. Drug Resist Updat. 2015;20:39-70. [PubMed] [DOI] |
| 4. | Chen S, Liang H, Yang H, Zhou K, Xu L, Liu J, Lai B, Song L, Luo H, Peng J, Liu Z, Xiao Y, Chen W, Tang H. LincRNa-p21: function and mechanism in cancer. Med Oncol. 2017;34:98. [PubMed] [DOI] |
| 5. | Ding G, Peng Z, Shang J, Kang Y, Ning H, Mao C. LincRNA-p21 inhibits invasion and metastasis of hepatocellular carcinoma through miR-9/E-cadherin cascade signaling pathway molecular mechanism. Onco Targets Ther. 2017;10:3241-3247. [PubMed] [DOI] |
| 7. | Chen Y, Wei G, Xia H, Yu H, Tang Q, Bi F. Down regulation of lincRNA-p21 contributes to gastric cancer development through Hippo-independent activation of YAP. Oncotarget. 2017;8:63813-63824. [PubMed] [DOI] |
| 8. | 苏 鹏飞, 陈 小伍, 朱 达坚, 王 国新, 黄 燕峰, 杨 勇, 罗 勇, 张 小聪. 姜黄素对结肠癌细胞耐药性的影响及机制. 中华实验外科杂志. 2018;35:450-452. [DOI] |
| 9. | Kim DH, Kim MJ, Sung B, Suh H, Jung JH, Chung HY, Kim ND. Resveratrol analogue, HS-1793, induces apoptotic cell death and cell cycle arrest through downregulation of AKT in human colon cancer cells. Oncol Rep. 2017;37:281-288. [PubMed] [DOI] |
| 10. | Kang AD, Cosenza SC, Bonagura M, Manair M, Reddy MV, Reddy EP. ON01210.Na (Ex-RAD®) mitigates radiation damage through activation of the AKT pathway. PLoS One. 2013;8:e58355. [PubMed] [DOI] |
| 12. | Castellano JJ, Navarro A, Viñolas N, Marrades RM, Moises J, Cordeiro A, Saco A, Muñoz C, Fuster D, Molins L, Ramirez J, Monzo M. LincRNA-p21 Impacts Prognosis in Resected Non-Small Cell Lung Cancer Patients through Angiogenesis Regulation. J Thorac Oncol. 2016;11:2173-2182. [PubMed] [DOI] |
| 13. | Wang J, Lei ZJ, Guo Y, Wang T, Qin ZY, Xiao HL, Fan LL, Chen DF, Bian XW, Liu J, Wang B. miRNA-regulated delivery of lincRNA-p21 suppresses β-catenin signaling and tumorigenicity of colorectal cancer stem cells. Oncotarget. 2015;6:37852-37870. [PubMed] [DOI] |
| 14. | Wang G, Li Z, Zhao Q, Zhu Y, Zhao C, Li X, Ma Z, Li X, Zhang Y. LincRNA-p21 enhances the sensitivity of radiotherapy for human colorectal cancer by targeting the Wnt/β-catenin signaling pathway. Oncol Rep. 2014;31:1839-1845. [PubMed] [DOI] |
| 15. | 唐 剑, 贺 菊乔, 杨 怡玲, 王 振冉. PI3K/Akt信号通路对人结肠癌HT-29细胞增殖的影响. 中华实用诊断与治疗杂志. 2018;32:218-221. [DOI] |
| 16. | 石 雪萍, 李 静, 冉 建华, 熊 伟, 李 海星, 郭 珮, 陈 地龙. 人参皂苷Rh2调控PI3K/AKT/GSK-3β信号通路诱导人结肠癌细胞凋亡. 中国药理学通报. 2017;33:114-119. [DOI] |
| 17. | Zhang Y, Xu Z, Sun Y, Chi P, Lu X. Knockdown of KLK11 reverses oxaliplatin resistance by inhibiting proliferation and activating apoptosis via suppressing the PI3K/AKT signal pathway in colorectal cancer cell. Onco Targets Ther. 2018;11:809-821. [PubMed] [DOI] |
| 18. | Brown JS, Banerji U. Maximising the potential of AKT inhibitors as anti-cancer treatments. Pharmacol Ther. 2017;172:101-115. [PubMed] [DOI] |
| 19. | Ersahin T, Tuncbag N, Cetin-Atalay R. The PI3K/AKT/mTOR interactive pathway. Mol Biosyst. 2015;11:1946-1954. [PubMed] [DOI] |
| 20. | Yi J, Chen B, Yao X, Lei Y, Ou F, Huang F. Upregulation of the lncRNA MEG3 improves cognitive impairment, alleviates neuronal damage, and inhibits activation of astrocytes in hippocampus tissues in Alzheimer's disease through inactivating the PI3K/Akt signaling pathway. J Cell Biochem. 2019;120:18053-18065. [PubMed] [DOI] |
| 21. | Nakano N, Matsuda S, Ichimura M, Minami A, Ogino M, Murai T, Kitagishi Y. PI3K/AKT signaling mediated by G proteincoupled receptors is involved in neurodegenerative Parkinson's disease (Review). Int J Mol Med. 2017;39:253-260. [PubMed] [DOI] |
| 22. | Pazini FL, Cunha MP, Rosa JM, Colla AR, Lieberknecht V, Oliveira Á, Rodrigues AL. Creatine, Similar to Ketamine, Counteracts Depressive-Like Behavior Induced by Corticosterone via PI3K/Akt/mTOR Pathway. Mol Neurobiol. 2016;53:6818-6834. [PubMed] [DOI] |
| 23. | 尹 来波, 刘 瑞英, 侯 量, 胡 思远, 朱 志军, 朱 佳龙. 长链非编码RNA-p21诱导细胞凋亡在动脉粥样硬化中的作用. 东南大学学报(医学版). 2017;36:816-821. [DOI] |
| 24. | Boon RA, Jaé N, Holdt L, Dimmeler S. Long Noncoding RNAs: From Clinical Genetics to Therapeutic Targets? J Am Coll Cardiol. 2016;67:1214-1226. [PubMed] [DOI] |