修回日期: 2025-06-28
接受日期: 2025-08-25
在线出版日期: 2025-08-28
肝脏肿瘤性质的无创鉴别是当前临床面临的难题. 超声造影(contrast-enhanced ultrasounds, CEUS)和血清甲胎蛋白(alpha-fetoprotein, AFP)/总胆汁酸(total bile acid, TBA)各具优势, 但联合诊断价值尚不明确, 本研究假设二者联合可提高肝脏肿瘤无创鉴别诊断效能, 并与病理结果一致.
研究CEUS联合血清AFP/TBA鉴别肝血管瘤、原发性肝癌及肝转移瘤与病理活检的一致性.
选取2023-07/2025-03杭州市临安区第四人民医院收治的291例肝脏肿瘤患者作为研究对象, 建立CEUS联合血清AFP/TBA的鉴别诊断模型, 其中经组织病理确诊恶性198例(原发性肝癌135例, 肝转移瘤63例)为恶性组, 良性93例(肝血管瘤)为良性组. 另选本中心2025-04/2025-06, 124例肝脏肿瘤(组织病理学提示恶性88例, 良性36例)患者作为外部验证数据. 比较2组常规超声表现、CEUS结果及血清AFP/TB, 构建Logistic回归模型分析恶性病变的影响因素, 使用受试者工作特征(receiver operating characteristic, ROC)曲线分析CEUS、血清AFP/TBA单独及联合应用在病灶性质鉴别诊断中的价值, 并采用ROC曲线、一致性分析对联合诊断效能进行内、外部评价.
恶性组形态不规则占比、边界不清晰占比、内部回声不均匀占比、病灶及周围血流信号Ⅱ级+Ⅲ级占比、增强速率及血清AFP/TBA分别为32.83%、46.46%、60.10%、91.92%、(0.85±0.19)、(6.07±2.02), 显著高于良性组20.43%、31.18%、24.73%、19.33%、(0.57±0.16)、(1.64±0.53), 50%倾斜率、达峰时间分别为(0.59±0.12)、(35.40±7.62), 显著低于良性组(0.80±0.24)、(44.93±10.51), 差异均有统计学意义(P<0.05); Logistic回归模型分析显示, 形态不规则、边界不清晰、内部回声不均匀、病灶及周围血流信号Ⅱ级+Ⅲ级、增强速率、血清AFP/TBA是恶性病变的危险因素, 50%倾斜率、达峰时间是其保护因素(P<0.05); ROC曲线分析显示, CEUS联合血清AFP/TBA鉴别诊断病灶性质的曲线下面积为0.928, 内、外部评价结果显示, 净改善了86.50%的分类正确率及对病灶性质的区分能力(均P<0.001); 一致性分析发现, CEUS与血清AFP/TBA鉴别诊断结果与病理活检结果一致性好(Kappa = 0.819)(P<0.001).
CEUS联合血清AFP/TBA对肝血管瘤、原发性肝癌及肝转移瘤具有一定鉴别诊断价值, 且与病理活检结果具有良好一致性, 可为临床无创鉴别诊断肝脏肿瘤性质提供参考, 并可指导后续临床决策.
核心提要: 本研究发现肿瘤形态、血流信号、增强速率及甲胎蛋白(alpha-fetoprotein, AFP)/总胆汁酸(total bile acid, TBA)是肝脏恶性病变关键指标, 论证了超声造影联合血清AFP/TBA可高效鉴别肝血管瘤、原发性肝癌及肝转移瘤, 且与病理活检结果具有较高一致性(Kappa = 0.819).
引文著录: 许建军. 超声造影联合血清AFP/TBA鉴别肝血管瘤、原发性肝癌及肝转移瘤与病理活检一致性研究. 世界华人消化杂志 2025; 33(8): 657-665
Revised: June 28, 2025
Accepted: August 25, 2025
Published online: August 28, 2025
The noninvasive differentiation of liver tumor nature remains a clinical challenge. While contrast-enhanced ultrasound (CEUS) and serum alpha-fetoprotein (AFP)/total bile acid (TBA) each have their advantages, the diagnostic value of their combined use remains unclear. This study hypothesized that combining these two modalities can improve the efficacy of noninvasive differential diagnosis of liver tumors while maintaining the consistency with pathological results.
To investigate the performance of CEUS combined with serum AFP/TBA in differentiating hepatic hemangioma, primary liver cancer, and liver metastases by using pathological biopsy as the golden standard.
A total of 291 patients with liver tumors admitted to the Fourth People's Hospital of Lin'an District from July 2023 to March 2025 were selected as the study subjects to establish a differential diagnosis model combining CEUS with serum AFP/TBA. Among them, 198 cases (135 cases of primary liver cancer and 63 cases of liver metastases) were histopathologically confirmed as malignant, forming a malignant group, while 93 cases (hepatic hemangioma) were benign, forming a benign group. Another 124 patients with liver tumors (88 malignant and 36 benign according to histopathology) from April 2025 to June 2025 in our center were selected for external validation. Conventional ultrasound findings, CEUS results, and serum AFP/TBA were compared between the two groups. A Logistic regression model was constructed to analyze the influencing factors of malignant lesions. Receiver operating characteristic (ROC) curve analysis was conducted to evaluate the value of CEUS and serum AFP/TBA alone and in combination for the differential diagnosis of lesion nature. Internal and external evaluation of diagnostic efficacy of the combination modality was conducted using ROC curves and consistency analysis.
In the malignant group, the proportions of tumors with an irregular morphology, unclear boundaries, uneven internal echoes, and surrounding blood flow signals of grade Ⅱ + Ⅲ, as well as the enhancement rate and serum AFP/TBA levels, were 32.83%, 46.46%, 60.10%, 91.92%, (0.85 ± 0.19), and (6.07 ± 2.02), respectively, which were significantly higher than those of the benign group [20.43%, 31.18%, 24.73%, 19.33%, (0.57 ± 0.16), and (1.64 ± 0.53), P < 0.05]; and the 50% inclination rate and time to peak were (0.59 ± 0.12) and (35.40 ± 7.62), respectively, which were significantly lower than those of the benign group [(0.80 ± 0.24) and (44.93 ± 10.51), P < 0.05]. Logistic regression analysis showed that irregular morphology, unclear boundaries, uneven internal echoes, surrounding blood flow signals of grade Ⅱ + Ⅲ, enhancement rate, and serum AFP/TBA were risk factors for malignant lesions, while 50% inclination rate and time to peak were protective factors (P < 0.05). ROC curve analysis revealed that the area under the curve for CEUS combined with serum AFP/TBA in distinguishing lesion nature was 0.928. Internal and external evaluation results indicated a net improvement in classification accuracy and lesion property differentiation of 86.50% (P < 0.001). Consistency analysis revealed good agreement between CEUS plus serum AFP/TBA diagnostic results and pathological biopsy results (Kappa = 0.819) (P < 0.001).
CEUS combined with serum AFP/TBA has appreciated diagnostic value in differentiating hepatic hemangioma, primary liver cancer, and liver metastases, and shows good consistency with pathological biopsy results. It can provide a reference for non-invasive clinical diagnosis of liver tumor nature and guide subsequent clinical decision-making.
- Citation: Xu JJ. Contrast-enhanced ultrasound combined with serum AFP/TBA in differentiating hepatic hemangioma, primary liver cancer, and liver metastases. Shijie Huaren Xiaohua Zazhi 2025; 33(8): 657-665
- URL: https://www.wjgnet.com/1009-3079/full/v33/i8/657.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v33.i8.657
近年来肝脏肿瘤具有较高发病率, 但肝血管瘤、原发性肝癌、肝转移瘤等不同性质肿瘤在超声、CT等常规影像学中存在特征重叠, 而病理活检亦存在有创及采样误差缺陷, 临床应用受限, 故肝脏肿瘤的性质鉴别在临床中仍存在较大挑战[1,2]. 因此, 早期、无创、准确鉴别肝脏肿瘤性质, 并选择合理治疗方案, 以获取最佳疗效、防控病情进展, 已成为当前临床亟待解决的难题. 超声造影(contrast-enhanced ultrasounds, CEUS)基于超声技术, 结合造影剂注射增强显影, 具有较高的时间、空间分辨率, 可通过动态血流监测区分不同性质肿瘤血供模式差异, 为临床诊疗提供参考信息[3]. 甲胎蛋白(alpha-fetoprotein, AFP)是肝癌特异性蛋白类标志物, 机体肝脏受损可致使AFP水平升高[4]. 总胆汁酸(total bile acid, TBA)为胆固醇代谢最终产物, 可参与调控脂质代谢, 亦可反映肝细胞摄取、分泌等功能状态[5]. 既往研究多聚焦于CEUS或血液指标在肝脏肿瘤鉴别中的单一应用价值, 但影像学检查结果易受操作者主观影响, 且对微小病灶的诊断精确度尚有待提高, 而血清学结果易受药物等多种因素影响[6,7]. 因此, 本研究首次分析CEUS与血清AFP/TBA联合应用对肝脏肿瘤性质的鉴别诊断价值, 以期为临床工作提供更可靠依据.
选取2023-07/2025-03杭州市临安区第四人民医院收治的291例肝脏肿瘤患者作为研究对象建立CEUS联合血清AFP/TBA的鉴别诊断模型, 其中经组织病理确诊恶性198例(原发性肝癌135例, 肝转移瘤63例)为恶性组, 良性93例(肝血管瘤)为良性组. 纳入标准: (1)恶性组均符合肝癌诊断标准[8], 并经病理结果证实为原发性肝癌或肝转移瘤; (2)良性组均经临床诊断为良性肝血管瘤, 并经病理结果证实; (3)既往无肝脏手术史; (4)对本研究方案风险及获益知情同意. 排除标准: (1)存在语言沟通障碍或心理、精神疾病, 无法配合相关检查; (2)对本研究所用造影剂过敏; (3)同时参与其他临床研究; (4)合并艾滋病等严重感染性疾病; (5)合并凝血功能障碍等循环系统病变; (6)伴其他重要脏器损伤; (7)伴自身免疫缺陷; (8)近3个月内服用损伤肝功能药物. 脱落标准: (1)突发其他重大疾病、失联或意外死亡; (2)自行退出研究者. 其中, 恶性组: 男性126例, 女性72例; 年龄41-69(55.14±6.83)岁; 体质量指数(body mass index, BMI)21.7-26.8(24.28±1.25) kg/m2; 肿瘤直径15.8-28.4(22.08±3.14) mm; 基础病: 肝癌家族史12例; 高血压61例, 高脂血症52例, 糖尿病45例. 良性组: 男性55例, 女性38例; 年龄39-68(53.79±7.02)岁; BMI 21.5-26.3(23.89±1.18) kg/m2; 肿瘤直径15.5-27.4(21.49±2.96) mm; 肝癌家族史3例; 基础病: 高血压24例, 高脂血症20例, 糖尿病30例. 两组基线资料均衡可比(P>0.05). 本研究经我院医学伦理委员会批准.
1.2.1 CEUS检查: 使用超声诊断仪(飞利浦Q7, 通用电气医疗系统(中国)公司, 国械注准20223061027), 设置频率2.0-5.0 MHz、机械指数0.04-0.10. (1)常规超声扫描肝脏, 观察并记录肿瘤病灶形态、大小、边界、数量、内部回声强度及血流信号等情况; (2)切换至造影状态, 自肘静脉团注微泡型造影剂(Sono Vue, 意大利Bracco公司), 注射完毕后续注5 mL生理盐水, 注射即刻至注射后30 s、30-90 s、90 s后分别为动脉相、门脉相及延迟相, 分析并记录达峰时间、峰值增强速率及50%倾斜率.
1.2.2 肿瘤病灶及周围血流信号分级标准: (1)0级: 未见明显血流信号; (2)Ⅰ级: 可见1-2个短棒状、点状血流信号; (3)Ⅱ级: 显示较长血管, 或3-4个短棒状、点状血流信号; (4)Ⅲ级: 显示丰富血流信号, 可见至少2条血, 或超过4个短棒状、点状血流信号[9].
1.2.3 血清AFP/TBA检测: 使用真空无菌采集管, 抽取所有受检者入院时清晨空腹外周静脉血约5 mL, 使用离心机(Avanti JXN-30型, 美国贝克曼库尔特公司, 国食药监械(进)字2013第1400407号)于4 ℃条件下离心10 min, 离心半径10 cm、转速3500 r/min, 取上层清液, 立即送往检验科检测. 采用高效液相色谱-串联质谱法检测AFP水平, 采用双抗体夹心法测定AFP水平, 并计算AFP/TBA比值. 检测试剂盒均购自北京健安生物公司, 所有步骤按试剂盒说明书要求严格操作.
(1)比较2组常规超声表现、CEUS结果及血清AFP/TB; (2)分析恶性病变的影响因素; (3)分析CEUS、血清AFP/TBA单独及联合应用在病灶性质鉴别诊断中的价值, 并进行内、外部评价.
统计学处理 应用SPSS 27.0统计学软件进行数据分析. 计数资料以n(%)表示, 行χ2检验; 计量资料经正态分布(Kolmogorov-Smirnov法)检查, 近似服从正态分布时以(mean±SD)表示, 行t检验; 等级资料采用Ridit分析, 以U表示; Logistic回归模型分析影响因素, 以Bonferroni法校正: 显著性阈值调整为0.05/8 = 0.00625; 采用受试者工作特征(receiver operating characteristic, ROC)曲线分析诊断价值, 曲线下面积(area under the curve, AUC)评估诊断效能, 以DeLong检验+Bonferroni校正: 在比较多个AUC时, 调整P值阈值; 通过Kappa值进行一致性分析. 以P<0.05为差异有统计学意义.
恶性组形态不规则、边界不清晰、内部回声不均匀患者占比显著高于良性组, 且病灶及周围血流信号分级分布高于良性组, 差异均有统计学意义(P<0.05). 见表1.
| 组别 | 例数 | 形态 | 边界 | 内部回声 | 病灶及周围血流信号 | ||||||
| 规则 | 不规则 | 清晰 | 不清晰 | 均匀 | 不均匀 | 0级 | Ⅰ级 | Ⅱ级 | Ⅲ级 | ||
| 恶性组 | 198 | 133(67.17) | 65(32.83) | 106(53.54) | 92(46.46) | 79(39.90) | 119(60.10) | 1(0.51) | 15(7.58) | 134(67.68) | 48(24.24) |
| 良性组 | 93 | 74(79.57) | 19(20.43) | 64(68.82) | 29(31.18) | 70(75.27) | 23(24.73) | 28(30.11) | 47(50.54) | 11(11.83) | 7(7.53) |
| χ2/u | 4.737 | 6.084 | 31.683 | 9.970 | |||||||
| P值 | 0.030 | 0.014 | 0.000 | 0.000 | |||||||
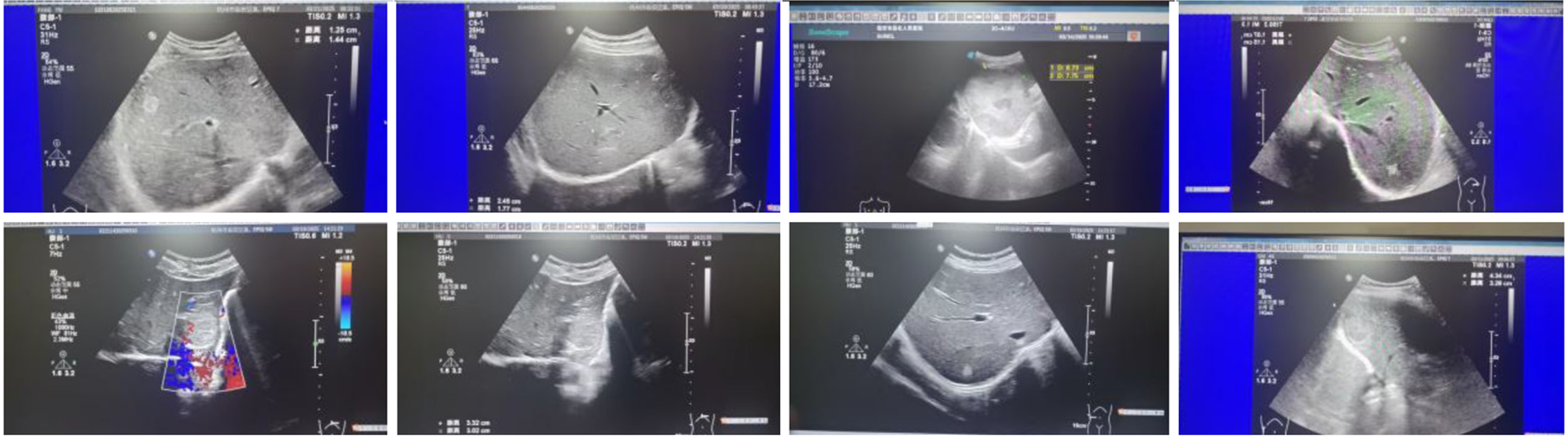
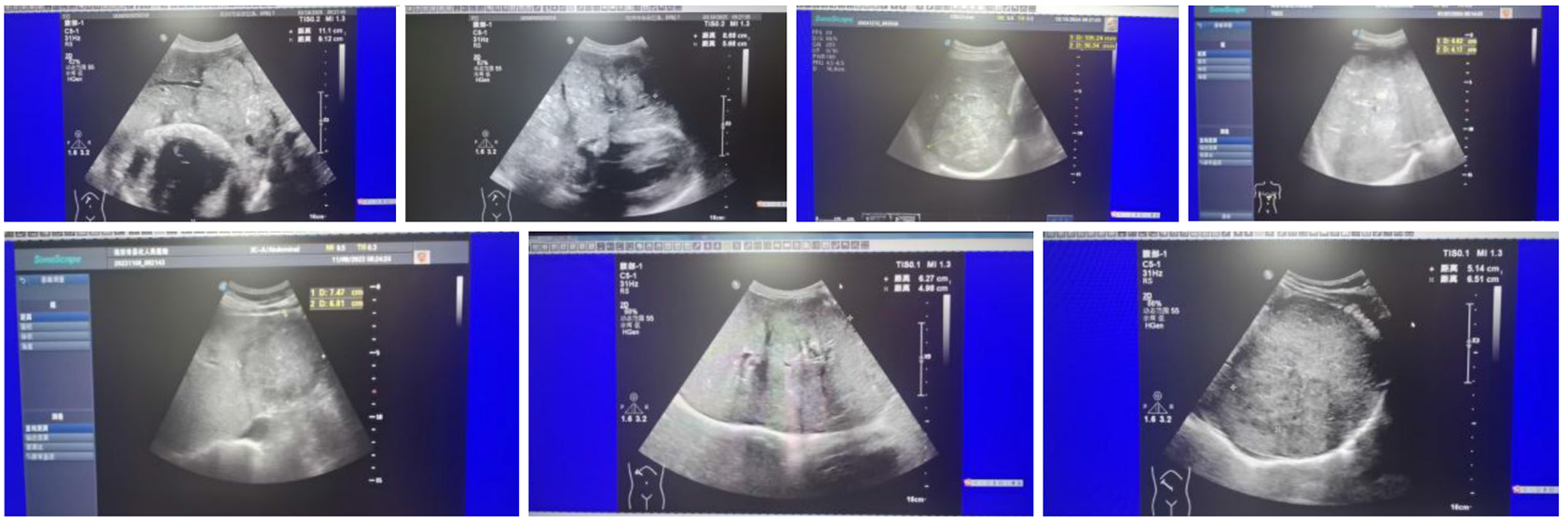
恶性组增强速率、血清AFP/TBA显著高于良性组, 50%倾斜率、达峰时间显著低于良性组, 差异均有统计学意义(P<0.05). 见表2. 两组部分患者超声表现见图1和图2.
| 组别 | 例数 | 增强速率 | 50%倾斜率 | 达峰时间(s) | AFP/TBA |
| 恶性组 | 198 | 0.85±0.19 | 0.59±0.12 | 35.40±7.62 | 6.07±2.02 |
| 良性组 | 93 | 0.57±0.16 | 0.80±0.24 | 44.93±10.51 | 1.64±0.53 |
| t | 12.306 | -9.956 | -8.769 | 20.798 | |
| P值 | 0.000 | 0.000 | 0.000 | 0.000 |
2.3.1 使用Logistic回归模型拟合多个变量: 以病灶性质为因变量(良性 = 0, 恶性 = 1), 形态(X1)、边界(X2)、内部回声(X3)、病灶及周围血流信号(X4)、增强速率(X5)、50%倾斜率(X6)、达峰时间(X7)、AFP/TBA(X8)作为协变量, 建立CEUS联合血清AFP/TBA鉴别诊断模型, 模型表达式为: Logit(P) = -3.608+0.401×X1+0.632×X2+0.499×X3+1.245×X4+0.297×X5-0.556×X6-0.822×X7+0.492×X8, 其中形态不规则、边界不清晰、内部回声不均匀、病灶及周围血流信号Ⅱ级+Ⅲ级、增强速率、血清AFP/TBA是恶性病变的危险因素, 50%倾斜率、达峰时间是其保护因素(P<0.05). 见表3.
| 影响因素 | β | SE | Wald χ2 | OR | 95%CI | P值 | |
| 下限 | 上限 | ||||||
| 形态(X1)不规则 | 0.401 | 0.140 | 8.217 | 1.494 | 1.025 | 2.177 | <0.001 |
| 边界(X2)不清晰 | 0.632 | 0.165 | 14.666 | 1.881 | 1.178 | 3.004 | <0.001 |
| 内部回声(X3)不均匀 | 0.499 | 0.187 | 7.110 | 1.646 | 1.106 | 2.451 | 0.002 |
| 病灶及周围血流信号(X4)Ⅱ级+Ⅲ级 | 1.245 | 0.326 | 14.575 | 3.471 | 2.314 | 5.208 | <0.001 |
| 增强速率(X5) | 0.297 | 0.103 | 8.309 | 1.346 | 1.113 | 1.627 | <0.001 |
| 50%倾斜率(X6) | -0.556 | 0.192 | 8.373 | 0.574 | 0.399 | 0.825 | <0.001 |
| 达峰时间(X7) | -0.822 | 0.203 | 16.388 | 0.440 | 0.253 | 0.764 | <0.001 |
| AFP/TBA(X8) | 0.492 | 0.153 | 10.341 | 1.636 | 1.367 | 1.957 | <0.001 |
| 常数项 | -3.608 | 0.084 | 27.956 | - | - | - | <0.001 |
2.3.2 CEUS联合血清AFP/TBA鉴别诊断模型的生成及最佳临界值的确定: 在Stata 10.0软件通过输入"Predict pre1"命令, 将原始协变量X1-X8拟合, 生成联合诊断因子, 并输入"roctab sepsis New, d"命令, 列出所生成的CEUS联合血清AFP/TBA鉴别诊断模型取不同值时对应的敏感度、特异度, 当约登指数最大时, 联合预测因子对应的数值为最佳临界值, 即0.127, >0.127为恶性, ≤0.127为良性.
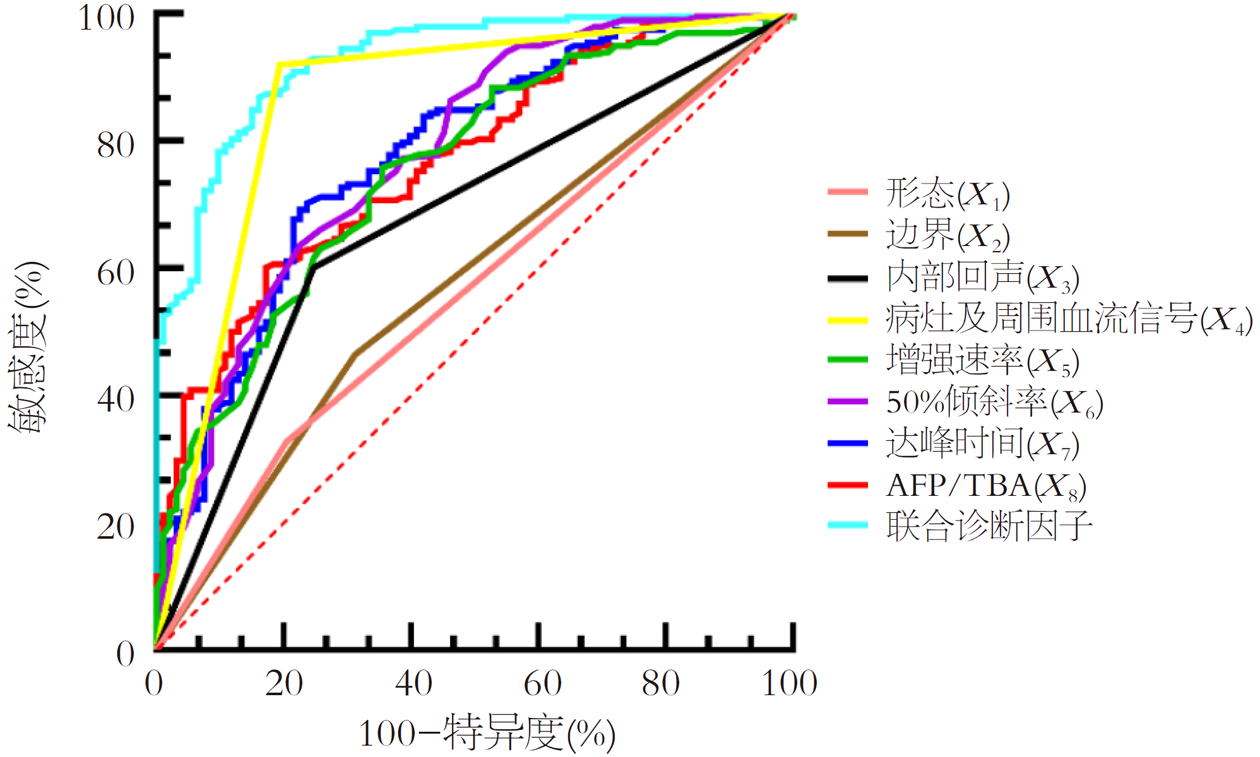
2.3.3 联合诊断因子及各协变量的诊断价值: 原始协变量X1-X8的AUC值介于0.562-0.863, 其中病灶及周围血流信号(X4)的AUC最大; 将各原始协变量拟合建立CEUS联合血清AFP/TBA鉴别诊断模型后, 诊断AUC值进一步提高至0.928, 联合诊断因子的AUC显著大于原始协变量病灶及周围血流信号(X4)的AUC值(Z = 2.566, P = 0.024), 由于病灶及周围血流信号(X4)的AUC是单一变量中最高的, 所以联合诊断因子的AUC亦显著高于其他单独的原始协变量, 诊断价值显著提升, 见图3和表4.
| 指标 | AUC | 95%CI | 最佳截断值 | 敏感度(%) | 特异度(%) | P值 |
| 形态(X1) | 0.562 | 0.503-0.620 | 32.83 | 79.57 | <0.001 | |
| 边界(X2) | 0.576 | 0.517-0.634 | 46.46 | 68.82 | <0.001 | |
| 内部回声(X3) | 0.677 | 0.620-0.730 | 60.10 | 75.27 | <0.001 | |
| 病灶及周围血流信号(X4) | 0.863 | 0.818-0.900 | 91.92 | 80.65 | <0.001 | |
| 增强速率(X5) | 0.754 | 0.701-0.803 | 0.73 | 75.76 | 64.52 | <0.001 |
| 50%倾斜率(X6) | 0.780 | 0.728-0.826 | 0.62 | 63.64 | 77.42 | <0.001 |
| 达峰时间(X7) | 0.777 | 0.725-0.824 | 38.02 | 69.19 | 77.42 | <0.001 |
| AFP/TBA(X8) | 0.769 | 0.716-0.816 | 5.87 | 60.10 | 82.80 | <0.001 |
| 联合诊断因子 | 0.928 | 0.892-0.955 | 0.127 | 86.87 | 83.87 | <0.001 |
2.3.4 联合诊断因子的内部评价: 由于联合诊断因子的AUC最大, 为最优方案, 所以对该方案进行进一步分析, 获得净重新分类指数(net reclassification index, NRI)、综合判别改善指数(integrated discrimination improvement, IDI)对联合诊断价值进行内部评价, 结果显示, NRI = 0.865(P<0.001), 提示与AUC最大的原始协变量病灶及周围血流信号(X4)单独应用相比, 联合诊断净改善了86.50%的分类正确率; IDI = 0.802(P<0.001), 提示联合诊断概率差异整体扩大了80.20%, 因此联合诊断方案将更多人正确分类, 并能整体提高对恶性和良性的区分能力, 诊断能力有明显改善.
2.3.5 联合诊断因子的外部评价: 在124例肝脏肿瘤外部验证数据集中, 组织病理学提示恶性88例, 良性36例. 采用CEUS联合血清AFP/TBA鉴别诊断模型准确判断恶性85例, 良性30例. Kappa值分析显示, CEUS联合血清AFP/TBA鉴别诊断结果与病理活检一致性为92.74%, Kappa值为0.819(P<0.001), 见表5.
| 病理检查 | CEUS联合血清AFP/TBA | 总计 | 一致性 | χ2 | P值 | Kappa值 | 95%CI | |
| 恶性 | 良性 | |||||||
| 恶性 | 85 | 3 | 88 | 92.74% | 79.520 | 0.000 | 0.819 | 0.644-0.995 |
| 良性 | 6 | 30 | 36 | |||||
| 总计 | 91 | 33 | 124 | |||||
随着人们生活及工作压力增加, 肝脏肿瘤发病率呈逐年升高趋势, 严重危害国民健康[10,11]. 不同性质肿瘤, 治疗方式亦不相同, 肝血管瘤通常生长缓慢, 可密切观察、随访, 而原发性肝癌及肝转移瘤病情重、进展快, 若未早期识别并对症积极治疗, 肿瘤细胞可逐步转移至全身各器官, 具有较高致死风险[12]. 病理活检是临床诊断肝脏肿瘤性质的"金标准", 但因具有有创、癌细胞针道种植等风险, 部分患者难以接受, 因此, 探索影像与血清学结合的无创、多模态鉴别诊断方式, 并分析其与病理活检结果的一致性, 对优化诊疗路径、提高肝脏恶性肿瘤检出率具有重要意义.
本研究结果显示, 恶性组形态不规则占比、边界不清晰占比、内部回声不均匀占比、病灶及周围血流信号分级分布、增强速率高于良性组, 50%倾斜率、达峰时间显著低于良性组. CEUS通过注射微泡型造影剂增强后散射回声, 可实时动态显示肝脏不同灌注阶段的血供状态, 明确病灶内微血管构筑特点, 对部分微小、隐匿病灶亦可清晰成像, 微气泡结构造影剂半衰期仅数十分钟, 经呼吸代谢, 无肝肾毒性, 对结节定性诊断的敏感度、准确度堪比增强CT、增强MRI, 且与CT、MRI等诊断方法相比, CEUS亦具有无辐射、费用低廉、操作更简单、可重复性更高等优势, 在临床中的应用越来越广泛[13,14]. 肝血管瘤多为海绵状血窦结构, 血管网由扁平内皮细胞血管管道组成, 血管密度大, 但内部血流差, 且难以形成新生血管, 故病灶及周围微血流信号小, Ⅱ级+Ⅲ级占比低, 造影剂进入血液循环后"向心性"填充, 呈现"慢进慢出"特征, 增强速率较小、达峰时间长、50%倾斜率小[15]; 而原发性肝癌及肝转移癌是癌细胞经狄氏间隙及血池呈浸润性生长, 病灶及周围微血管密度大、血流信号强, 微泡造影剂作为血池显影剂, 可随血流进入浸润途径, 清晰显示微小血管及血源性组织浸润范围, 且不易向周围组织间隙弥散, 呈现"快进快退"特征, 故增强速率大、达峰时间短、50%倾斜率小[16,17]. Logistic回归模型分析显示, 形态不规则、边界不清晰、内部回声不均匀、病灶及周围血流信号Ⅱ级+Ⅲ级、增强速率是恶性病变的危险因素, 50%倾斜率、达峰时间是其保护因素, 进一步印证了上述结论. Safai Zadeh等[18]经临床研究指出, CEUS在恶性血液性肝脏病变及良性病变中存在影像特征及数据差异, 可为本研究结果提供参考. 但CEUS检查结果易受操作者临床经验及技术水平的影响, 具有一定主观缺陷, 单独应用具有一定局限性, 故本研究进一步分析血清学客观指标与肝脏肿瘤的关系.
本研究结果显示, 血清AFP/TBA与肝脏肿瘤性质具有紧密联系. AFP属胚胎期肝脏合成糖蛋白, 而成熟肝细胞无法合成、分泌AFP, 故在正常肝脏及良性肝脏病变中, AFP在血液中的含量极低, 而恶性肝脏肿瘤患者伴肝功能障碍, 癌基因异常激活可重新恢复胎儿期表观遗传特征, 幼嫩肝细胞增加, 启动AFP合成机制, 故AFP在肝脏恶性肿瘤中呈高表达[19,20]. 但临床实践显示, AFP在肝炎等良性病变中可短暂升高, 诊断敏感度较低, 单独应用价值较为有限[21]. 胆汁酸是胆固醇最终代谢产物, 恶性肝脏肿瘤伴肝细胞结构异常及胆管压迫, 可引起胆汁酸代谢异常及肝-肠循环障碍, 肝细胞摄取胆汁酸能力下降, 致使TBA含量持续升高, 但升高幅度低于AFP[22]; 此外, 肿瘤微环境多存在不同程度炎症、氧化应激反应, NF-κB等信号通路被激活, 可进一步加重胆汁酸代谢失衡状态, 并抑制其再循环, 胆汁酸蓄积逐步增加, TBA水平升高, 而高浓度胆汁酸介导局部炎症及氧化应激, 形成恶性循环[23]. 而良性肝脏肿瘤侵袭性较弱, 对肝细胞合成、分泌及摄取功能的干扰相对较小, TBA水平波动幅度及毒性作用均有限, 普遍呈现轻度升高趋势[24]. 故AFP/TBA在肝脏恶性肿瘤中的比值相对较高. 进一步数据分析显示, 血清AFP/TBA与恶性病变独立相关, AFP/TBA比值增大, 肿瘤恶性病变风险随之升高. He等[25]经临床研究指出, TBA与肝癌分级及肝功能损伤密切相关, 可为本研究观点提供数据支持.
基于上述结果, 推测CEUS与血清AFP/TBA联合可突出各自优势, 提高整体鉴别诊断效能, 诸玮等[26]近期研究也表明, CEUS联合糖类抗原199等肿瘤标志物可提高对肿瘤良恶性的鉴别效能, 但仍存在一定误诊、漏诊率. 故本研究绘制ROC曲线, 发现联合诊断因子可明显提高对病灶性质的鉴别诊断价值, 净改善了86.50%的分类正确率及对病灶性质的区分能力, 且CEUS与血清AFP/TBA鉴别诊断结果与病理活检结果一致性好, 可作为临床鉴别诊断肝脏肿瘤性质的新型方案, 这也是本研究创新性所在. CEUS检查及血清AFP、TBA检测均无创、无辐射、可重复性较高, 因此, 建议临床将二者联合应用作为肝脏肿瘤患者常规检测项目, 有助于早期、准确、无创鉴别肿瘤性质, 从而指导临床进行更合理、精细化治疗. 本研究局限于诊断性临床试验及单中心选例, 原发性肝癌样本量较小, 且缺乏长期随访数据, 考虑肝转移瘤与原发性肝癌虽起源不同, 但生物学行为、临床表现等存在一定共性, 故将二者同时纳入, 以补充样本量, 但可能影响结果稳定性及外推性, 未来仍需累积原发性肝癌病例及长期随访数据, 进一步验证本研究结果.
综上所述, CEUS联合化血清AFP/TBA对肝血管瘤、原发性肝癌及肝转移瘤具有一定鉴别诊断价值, 且与病理活检结果具有良好一致性, 可作为临床鉴别诊断肝脏肿瘤性质的新型方案, 并对后续临床决策具有一定指导作用.
肝血管瘤、原发性肝癌和肝转移瘤的准确鉴别对临床实施个体化诊疗极为重要, 而病理活检作为诊断"金标准", 存在有创、出血、感染等风险. 超声造影(contrast-enhanced ultrasounds, CEUS)及甲胎蛋白(alpha-fetoprotein, AFP)、总胆汁酸(total bile acid, TBA)等血清标志物均是无创诊断手段, 但单独应用时诊断效能有限. 既往研究多聚焦单一超声技术或血清学技术, 关于多模态联合鉴别诊断的深入验证仍较为缺乏, 亟需探索CEUS联合血清标志物的综合鉴别诊断价值, 从而为无创诊断提供参考价值.
探索无创、有效鉴别诊断方案, 从而可为临床实施精准、个体化治疗提供依据, 并可减少活检需求、降低医疗风险.
构建CEUS联合AFP/TBA的鉴别诊断模型, 评估其对肝血管瘤、原发性肝癌及肝转移瘤的鉴别诊断价值, 并分析鉴别结果与病理活检结果的一致性.
采用前瞻性队列研究, 分析CEUS表现及血清AFP/TBA在肝脏良恶性病变中差异, Logistic回归方程筛选恶性病变的独立影响因素, 并使用受试者工作特征曲线及Kappa值分析、验证CEUS联合血清AFP/TBA模型的鉴别诊断效能.
本研究结果显示, CEUS联合血清AFP/TBA鉴别肝脏肿瘤性质的曲线下面积为0.928, 且鉴别诊断结果与病理活检结果一致性好(Kappa = 0.819), 可作为临床无创鉴别诊断肝脏肿瘤良恶性的无创、有效方案.
本研究整合了超声表现及血清学指标, 证实CEUS联合血清AFP/TBA可鉴别肝脏肿瘤性质, 且鉴别效能接近于病理活检结果, 可为临床无创诊断提供更多可靠信息.
本研局限于单中心、小样本量, 可能影响统计学效能, 从而影响结果稳定性及外推性, 未来将持续累积病例、扩大样本量、开展多中心研究, 并可纳入人工智能技术, 从而验证本研究结果.
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C, C
D级 (一般): D
E级 (差): E
科学编辑: 刘继红 制作编辑:张砚梁
| 1. | Revsine M, Wang L, Forgues M, Behrens S, Craig AJ, Liu M, Tran B, Kelly M, Budhu A, Monge C, Xie C, Hernandez JM, Greten TF, Wang XW, Ma L. Lineage and ecology define liver tumor evolution in response to treatment. Cell Rep Med. 2024;5:101394. [PubMed] [DOI] |
| 2. | 罗 咏萍, 古 代娇, 陈 宗华, 刘 毅, 张 键, 黄 洁, 郑 学颖, 杨 志慧, 黄 亚娜, 曹 敏, 唐 欢. 食管静脉曲张一级预防对首诊原发性肝细胞癌患者预后的影响. 临床误诊误治. 2024;37:31-35. |
| 3. | Abushamat F, Dietrich CF, Clevert DA, Piscaglia F, Fetzer DT, Meloni MF, Shiehmorteza M, Kono Y. Contrast-Enhanced Ultrasound (CEUS) in the Evaluation of Hemoperitoneum in Patients With Cirrhosis. J Ultrasound Med. 2023;42:247-253. [PubMed] [DOI] |
| 4. | Norman JS, Li PJ, Kotwani P, Shui AM, Yao F, Mehta N. AFP-L3 and DCP strongly predict early hepatocellular carcinoma recurrence after liver transplantation. J Hepatol. 2023;79:1469-1477. [PubMed] [DOI] |
| 5. | Wu L, Zhou J, Zhou A, Lei Y, Tang L, Hu S, Wang S, Xiao X, Chen Q, Tu D, Lu C, Lai Y, Li Y, Zhang X, Tang B, Yang S. Lactobacillus acidophilus ameliorates cholestatic liver injury through inhibiting bile acid synthesis and promoting bile acid excretion. Gut Microbes. 2024;16:2390176. [PubMed] [DOI] |
| 6. | Lyshchik A, Fetzer DT, Kono Y, Wilson SR, Dietrich CF, Clevert DA, Meloni MF, Jang HJ, Kim TK, Lee JM, Minami Y, Kudo M, Piscaglia F. Liver Imaging Reporting and Data System Contrast-Enhanced US Nonradiation Treatment Response Assessment Version 2024. Radiology. 2024;311:e232369. [PubMed] [DOI] |
| 7. | Möller K, Stock B, Ignee A, Zadeh ES, De Molo C, Serra C, Jenssen C, Lim A, Görg C, Dong Y, Klinger C, Tana C, Meloni MF, Sparchez Z, Francica G, Dirks K, Hollerweger A, Kinkel H, Weskott HP, Montagut NE, Srivastava D, Dietrich CF. Comments and illustrations of the WFUMB CEUS liver guidelines: Rare focal liver lesions - non-infectious, non-neoplastic. Med Ultrason. 2023;25:435-444. [PubMed] [DOI] |
| 9. | Ware MB, Zaidi MY, Yang J, Turgeon MK, Krasinskas A, Mace TA, Keenan K, Farren MR, Ruggieri AN, Li Y, Zhang C, Chen Z, Young GS, Elnaggar O, Che Z, Maithel SK, Bekaii-Saab T, El-Rayes B, Lesinski GB. Suppressive myeloid cells are expanded by biliary tract cancer-derived cytokines in vitro and associate with aggressive disease. Br J Cancer. 2020;123:1377-1386. [PubMed] [DOI] |
| 10. | Velliou RI, Legaki AI, Nikolakopoulou P, Vlachogiannis NI, Chatzigeorgiou A. Liver endothelial cells in NAFLD and transition to NASH and HCC. Cell Mol Life Sci. 2023;80:314. [PubMed] [DOI] |
| 11. | Toniutto P, Shalaby S, Mameli L, Morisco F, Gambato M, Cossiga V, Guarino M, Marra F, Brunetto MR, Burra P, Villa E; Special Interest Group Gender in Hepatology of the Italian Association for the Study of the Liver (AISF). Role of sex in liver tumor occurrence and clinical outcomes: A comprehensive review. Hepatology. 2024;79:1141-1157. [PubMed] [DOI] |
| 12. | Zhao G, Ma Q, Yang H, Jiang H, Xu Q, Luo S, Meng Z, Liu J, Zhu L, Lin Q, Li M, Fang J, Ma L, Qiu W, Mao Z, Lu Z. Base editing of the mutated TERT promoter inhibits liver tumor growth. Hepatology. 2024;79:1310-1323. [PubMed] [DOI] |
| 13. | Dietrich CF, Albrecht T, Becher H, Harvey CJ, Jenssen C, Lim AK, Möller K, Greis C. History of contrast enhanced ultrasound (CEUS). Med Ultrason. 2024;26:405-416. [PubMed] [DOI] |
| 14. | Sugimoto K, Kamiyama N, Kakegawa T, Takahashi H, Wada T, Abe M, Yoshimasu Y, Takeuchi H, Itoi T. Modified CEUS LI-RADS using Sonazoid for the diagnosis of hepatocellular carcinoma. Ultrasonography. 2023;42:388-399. [PubMed] [DOI] |
| 15. | Kacała A, Dorochowicz M, Matus I, Puła M, Korbecki A, Sobański M, Jacków-Nowicka J, Patrzałek D, Janczak D, Guziński M. Hepatic Hemangioma: Review of Imaging and Therapeutic Strategies. Medicina (Kaunas). 2024;60:449. [PubMed] [DOI] |
| 16. | Ying X, Dong S, Zhao Y, Chen Z, Jiang J, Shi H. Research Progress on Contrast-Enhanced Ultrasound (CEUS) Assisted Diagnosis and Treatment in Liver-Related Diseases. Int J Med Sci. 2025;22:1092-1108. [PubMed] [DOI] |
| 17. | Moller K, Zadeh ES, Görg C, Jenssen C, Hocke M, De Molo C, Serra C, Dong Y, Cui XW, Lim A, Thees-Laurenz R, Faiss S, Dietrich CF. Comments and illustrations of the WFUMB CEUS liver guidelines: Rare vascular pathology, part II. Med Ultrason. 2023;25:189-200. [PubMed] [DOI] |
| 18. | Safai Zadeh E, Görg C, Huber KP, Dirks K, Jenssen C, Lim A, Möller K, Götzberger M, Dong Y, Cui XW, Fetzer DT, Klinger C, Clevert DA, Dietrich CF. Comments and illustrations of the WFUMB CEUS liver guidelines: Rare malignant hematological liver lesions. Med Ultrason. 2024;26:383-390. [PubMed] [DOI] |
| 19. | Lu X, Deng S, Xu J, Green BL, Zhang H, Cui G, Zhou Y, Zhang Y, Xu H, Zhang F, Mao R, Zhong S, Cramer T, Evert M, Calvisi DF, He Y, Liu C, Chen X. Combination of AFP vaccine and immune checkpoint inhibitors slows hepatocellular carcinoma progression in preclinical models. J Clin Invest. 2023;133:e163291. [PubMed] [DOI] |
| 20. | Tayob N, Kanwal F, Alsarraj A, Hernaez R, El-Serag HB. The Performance of AFP, AFP-3, DCP as Biomarkers for Detection of Hepatocellular Carcinoma (HCC): A Phase 3 Biomarker Study in the United States. Clin Gastroenterol Hepatol. 2023;21:415-423.e4. [PubMed] [DOI] |
| 21. | Lee S, Jeon H, Han J, Song IK, Baek SH, Shim S, Eun H, Park MS, Jang H, Shin JE, Ihn K. Management of Neonatal Hepatic Hemangiomas: A Single-Center Experience Focused on Challenging Cases. J Clin Med. 2024;13:2839. [PubMed] [DOI] |
| 22. | Zhang XF, Niu XF, Li LX, He X, Li ZJ, Liu ZW, Zhang DL, Ren H. Total bile acid is a useful tool for evaluating the risk of portal hypertension in patients with hepatocellular carcinoma who have undergone hepatectomy. Curr Med Res Opin. 2025;41:253-259. [PubMed] [DOI] |
| 23. | Ma Y, Zou C, Yang Y, Fang M, Guan Y, Sun J, Gao Y, Shang Z, Zhang X. Arachidonic acid enhances hepatocyte bile acid uptake and alleviates cholestatic liver disease by upregulating OATP1 expression. Food Funct. 2024;15:9916-9927. [PubMed] [DOI] |
| 24. | Fitzinger J, Rodriguez-Blanco G, Herrmann M, Borenich A, Stauber R, Aigner E, Mangge H. Gender-Specific Bile Acid Profiles in Non-Alcoholic Fatty Liver Disease. Nutrients. 2024;16:250. [PubMed] [DOI] |
| 25. | He X, Zhang X, Li Z, Niu X, Li L, Liu Z, Ren H, Zhang D. Total bile acid as a preoperative risk factor for post-hepatectomy liver failure in patients with hepatocellular carcinoma and normal bilirubin. Cir Esp (Engl Ed). 2024;102:642-648. [PubMed] [DOI] |