修回日期: 2019-07-01
接受日期: 2019-08-02
在线出版日期: 2019-08-08
食管胃底静脉曲张破裂出血是肝硬化严重及危急的并发症, 相对于食道静脉曲张, 孤立胃底静脉曲张发生率低, 但一旦发生出血, 出血量大且死亡率高. 急诊出血时可考虑行内镜下组织胶注射治疗, 但对于非结节型曲张静脉内镜下注射治疗效果差, 且病因多为左侧门脉高压. 左侧门静脉高压最常见原因为胰源性, 其中慢性胰腺炎的发生率最高. 免疫球蛋白G(immunoglobulin G, IgG)4相关自身免疫性胰腺炎(autoimmune pancreatitis, AIP)为慢性胰腺炎的特殊类型, 其引起胃底静脉曲张破裂出血的报道相对较少.
一例以胃底静脉曲张破裂出血就诊患者, 最终诊断为IgG4相关AIP, 合并脾静脉及肠系膜上静脉血栓形成, 经激素治疗后, 胰腺体积、血清IgG4明显好转, 未再出血, 但脾静脉及肠系膜静脉血栓较前好转, 胃底曲张静脉未完全消失.
对于孤立胃底静脉曲张破裂出血, 左侧门脉高压的患者, 在止血治疗后应积极寻找病因. AIP患者, 脾静脉血栓治疗对于胃底静脉曲张的消失可能起关键作用. 对于影响脾静脉血栓治疗效果的因素期待更多病例数及更长时间随访的报道.
核心提要: 对于孤立胃底静脉曲张破裂出血的病例, 在出血时应积极行止血治疗, 待患者出血停止后积极寻找病因. 对于免疫球蛋白G4相关自身免疫性胰腺炎, 激素的治疗改善胰腺肿胀同时, 可减轻脾静脉及肠系膜血栓和胃底静脉曲张程度. 激素治疗时间, 是否加用抗血栓治疗及是否会加重患者再次出血风险, 本病例资料有限, 期待更多的病例及报道.
引文著录: 梅雪灿, 王曦, 孔德润. IgG4相关自身免疫性胰腺炎合并脾静脉血栓导致胃底静脉曲张破裂出血: 1例病例报告. 世界华人消化杂志 2019; 27(15): 967-971
Revised: July 1, 2019
Accepted: August 2, 2019
Published online: August 8, 2019
Bleeding from isolated gastric varices, though uncommon, may be life-threatening. There are few reports of autoimmune pancreatitis (AIP) with splenic vein thrombosis and subsequent left-sided portal hypertension complicated by gastric varices, and the effect of steroid therapy on gastric varices is unknown. We herein present one case of AIP complicated by gastric varices.
A 43-year-old man was diagnosed with AIP complicated by gastric varices, splenic vein obstruction, and splenomegaly. Although the AIP was improved after steroid therapy, gastric varices and splenic vein obstruction did not resolve.
For bleeding from isolated gastric varices with left portal hypertension, the cause should be actively sought after hemostasis therapy. Gastric varices or splenic vein obstruction may be an indication for steroid therapy, and splenic vein thrombosis may play a key role in the disappearance of gastric varices. Factors affecting the efficacy in splenic vein thrombosis are expected to be explored by future studies with more cases and longer follow-up.
- Citation: Mei XC, Wang X, Kong DR. IgG4-related autoimmune pancreatitis combined with splenic vein thrombosis leading to variceal bleeding of the fundus: A case report. Shijie Huaren Xiaohua Zazhi 2019; 27(15): 967-971
- URL: https://www.wjgnet.com/1009-3079/full/v27/i15/967.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v27.i15.967
自身免疫性胰腺炎(autoimmune pancreatitis, AIP)在近50年来逐渐被认识, 其主要特点是胰腺淋巴浆细胞浸润、慢性炎症性席文状纤维化、闭塞性静脉炎和高球蛋白血症, 但因胃底静脉曲张破裂出血为首发症状就诊病例较少, 且其引起胃底静脉曲张的原因, 激素治疗时间和效果仍存在争议. 本文报道了一列胃底静脉曲张破裂出血为首发症状的免疫球蛋白G(immunoglobulin G, IgG) 4相关AIP的病例, 经激素治疗后未再发生消化道出血, 胃底静脉曲张较前改善.
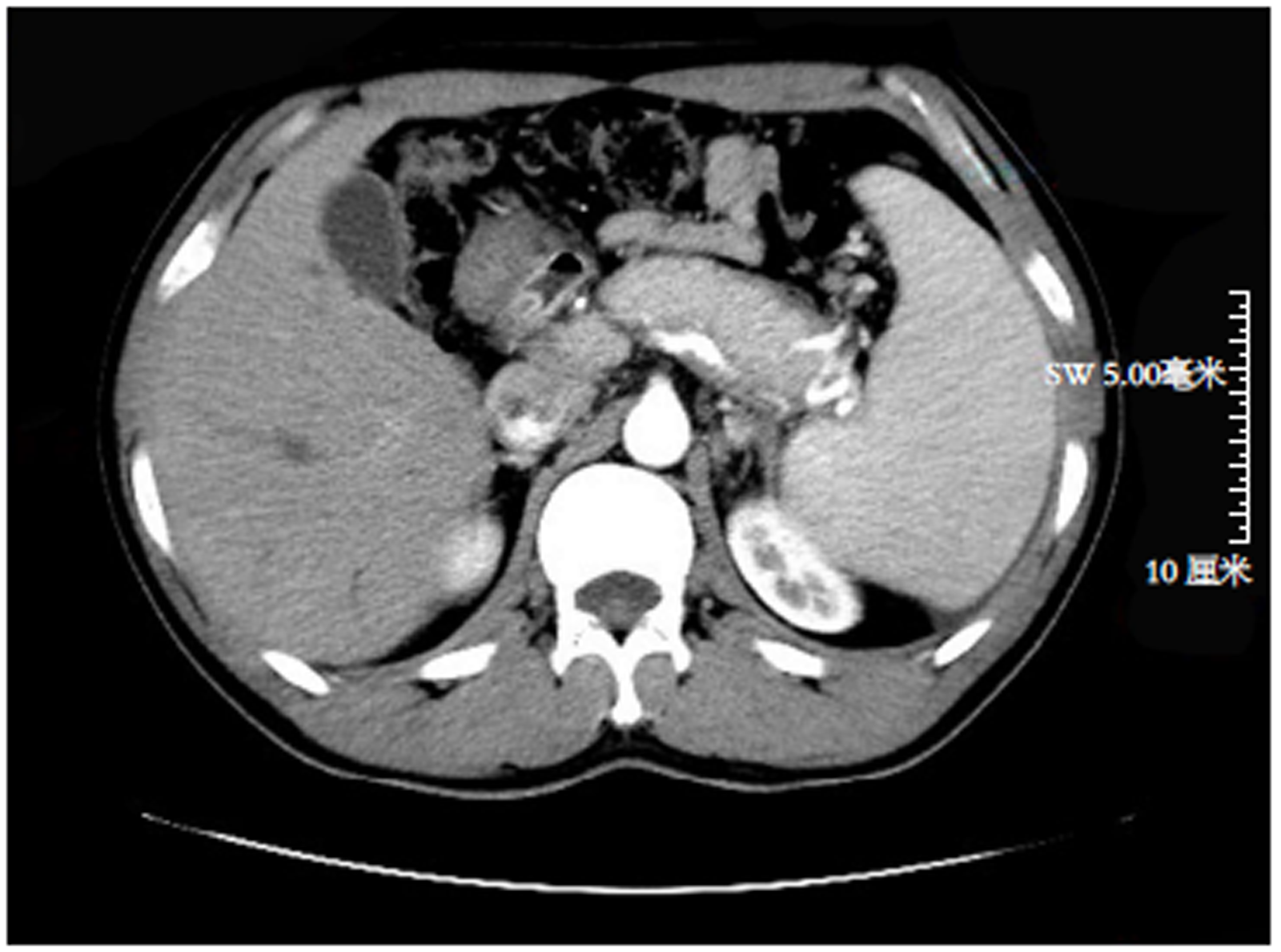
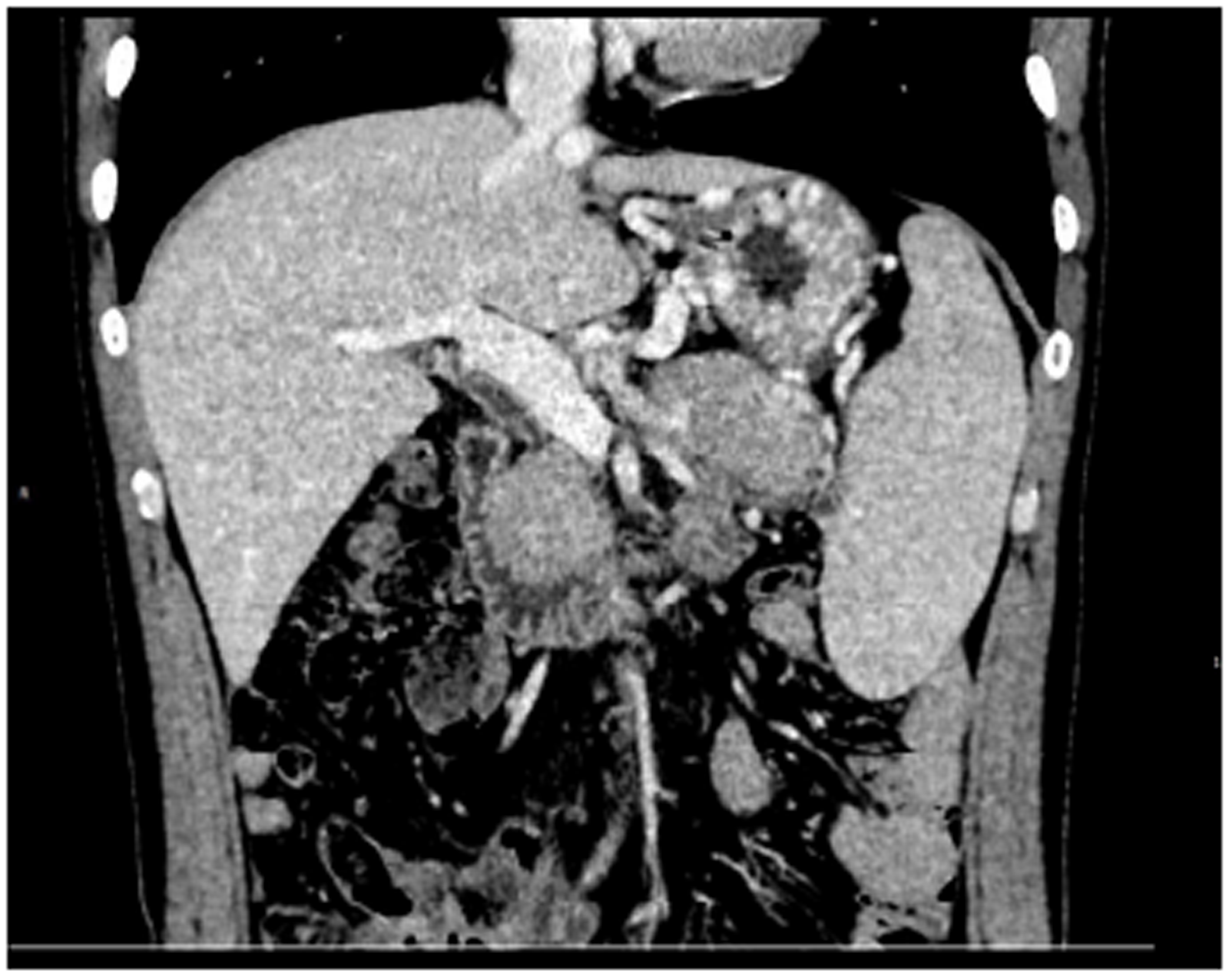
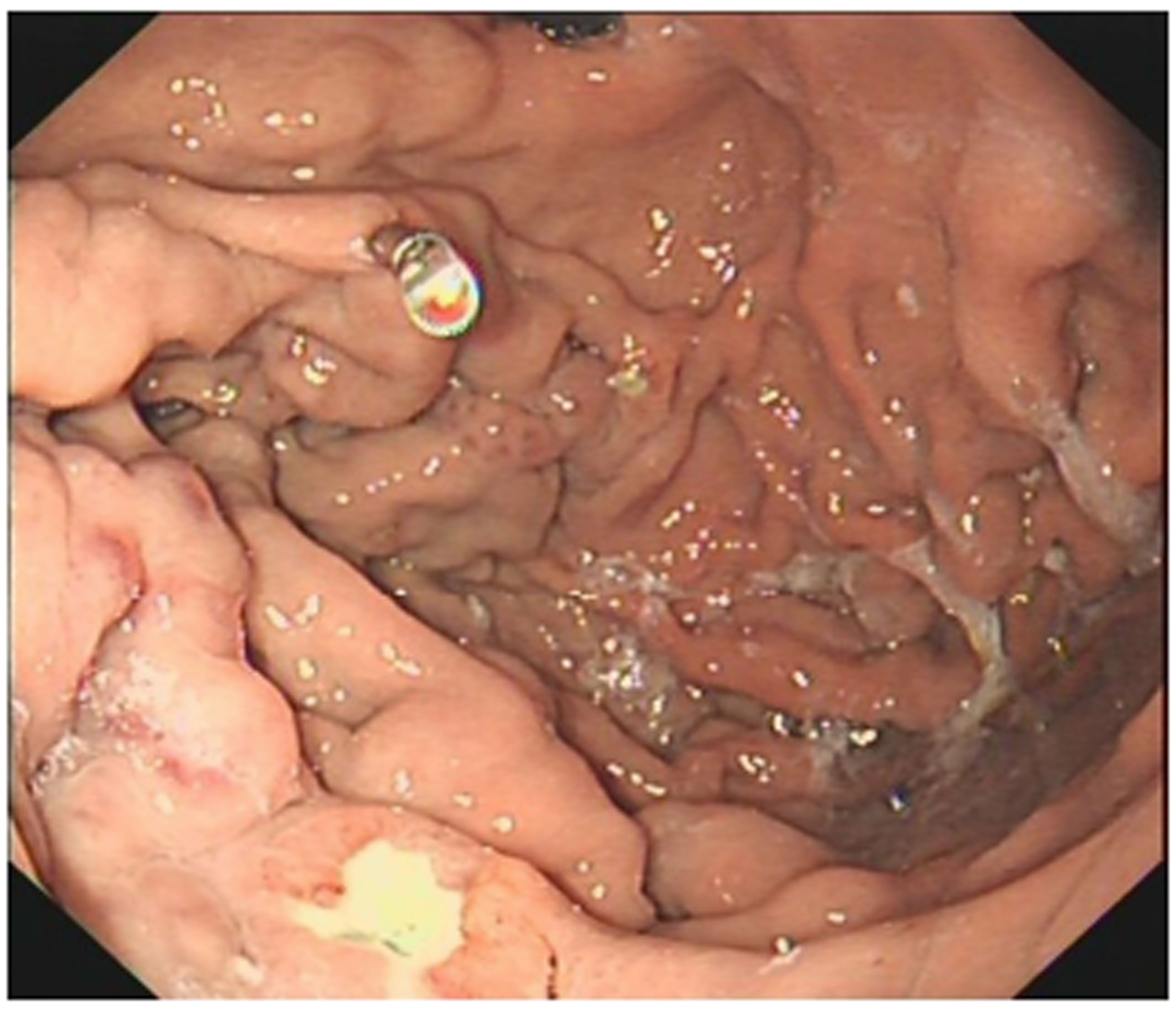
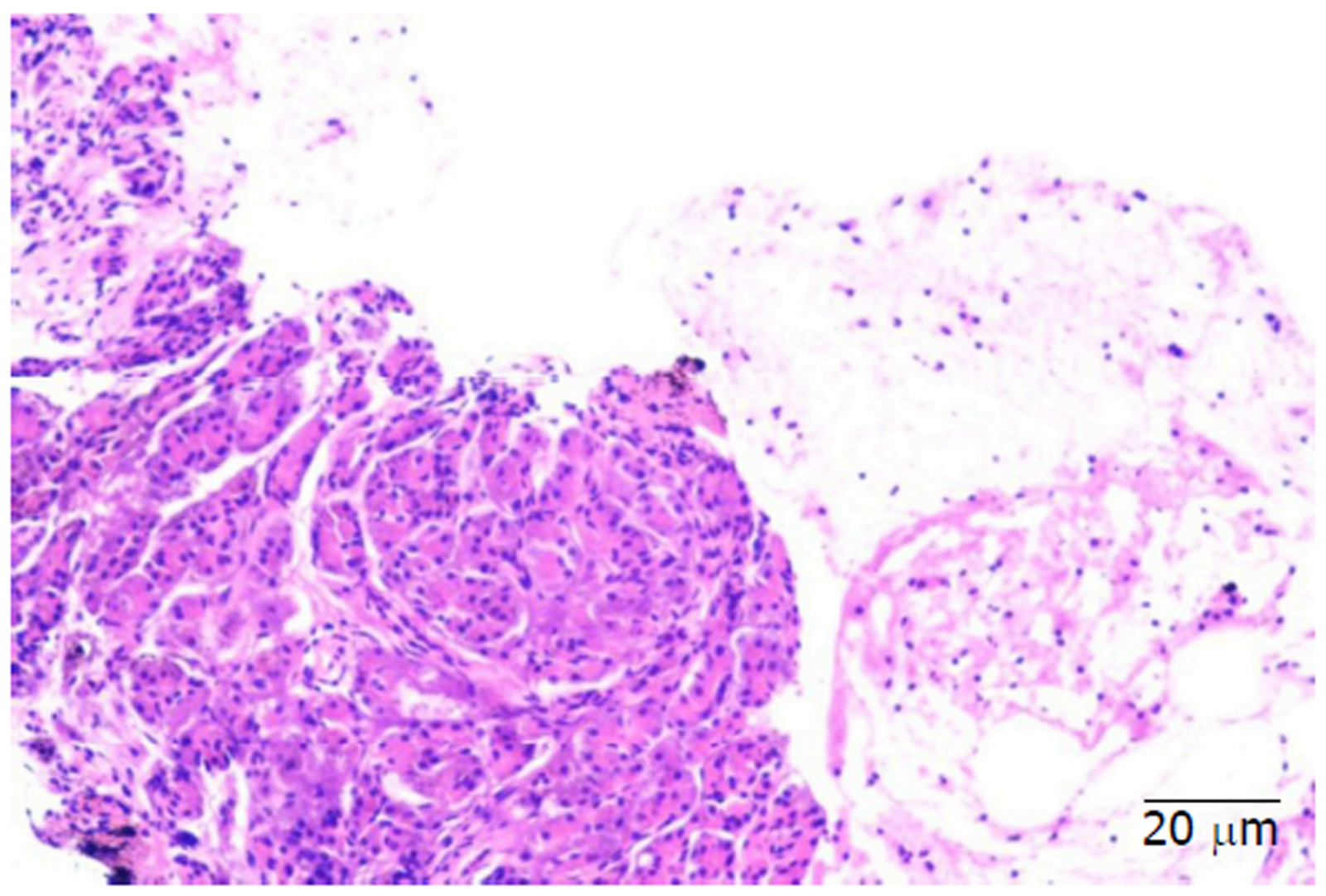
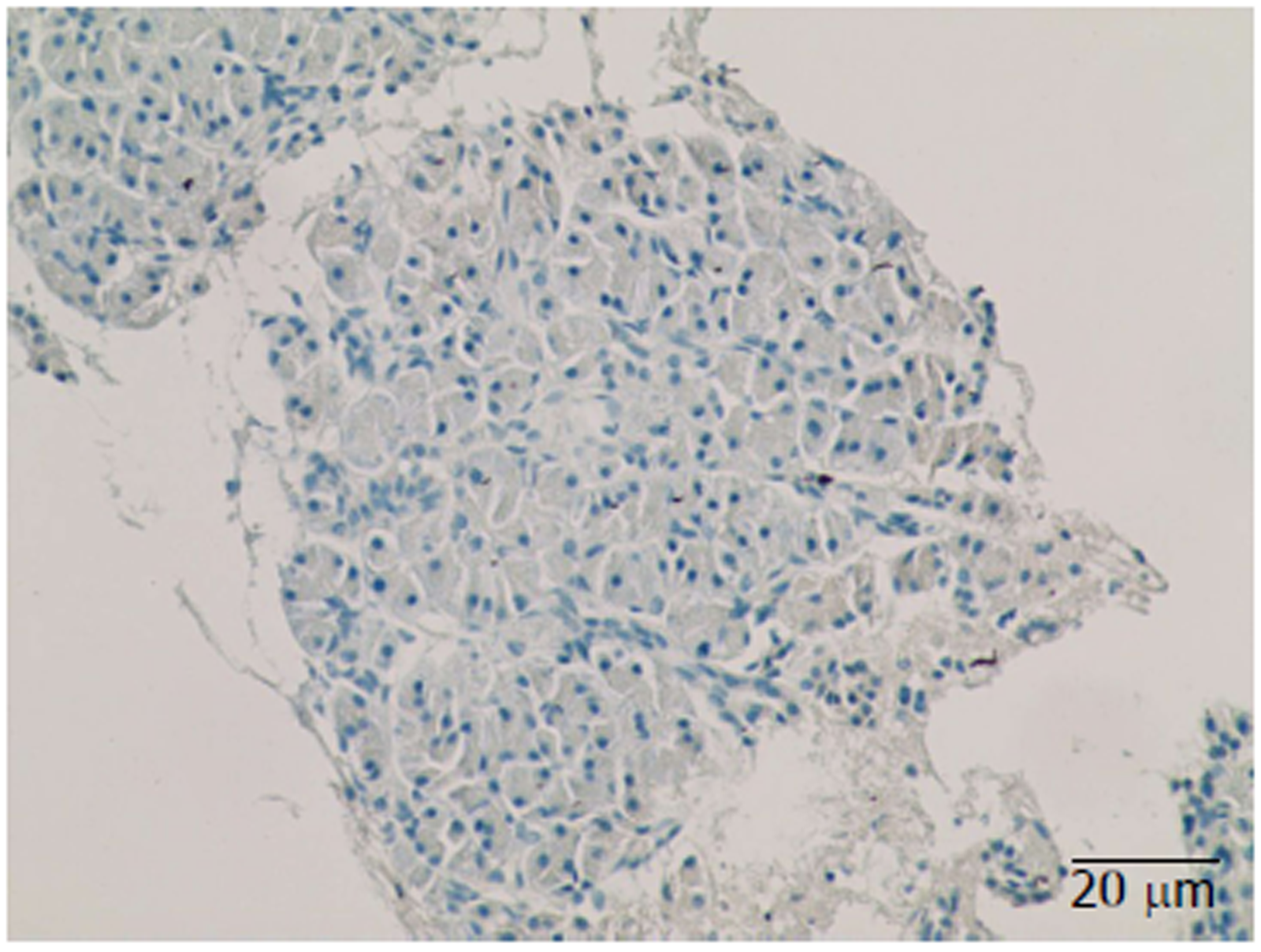
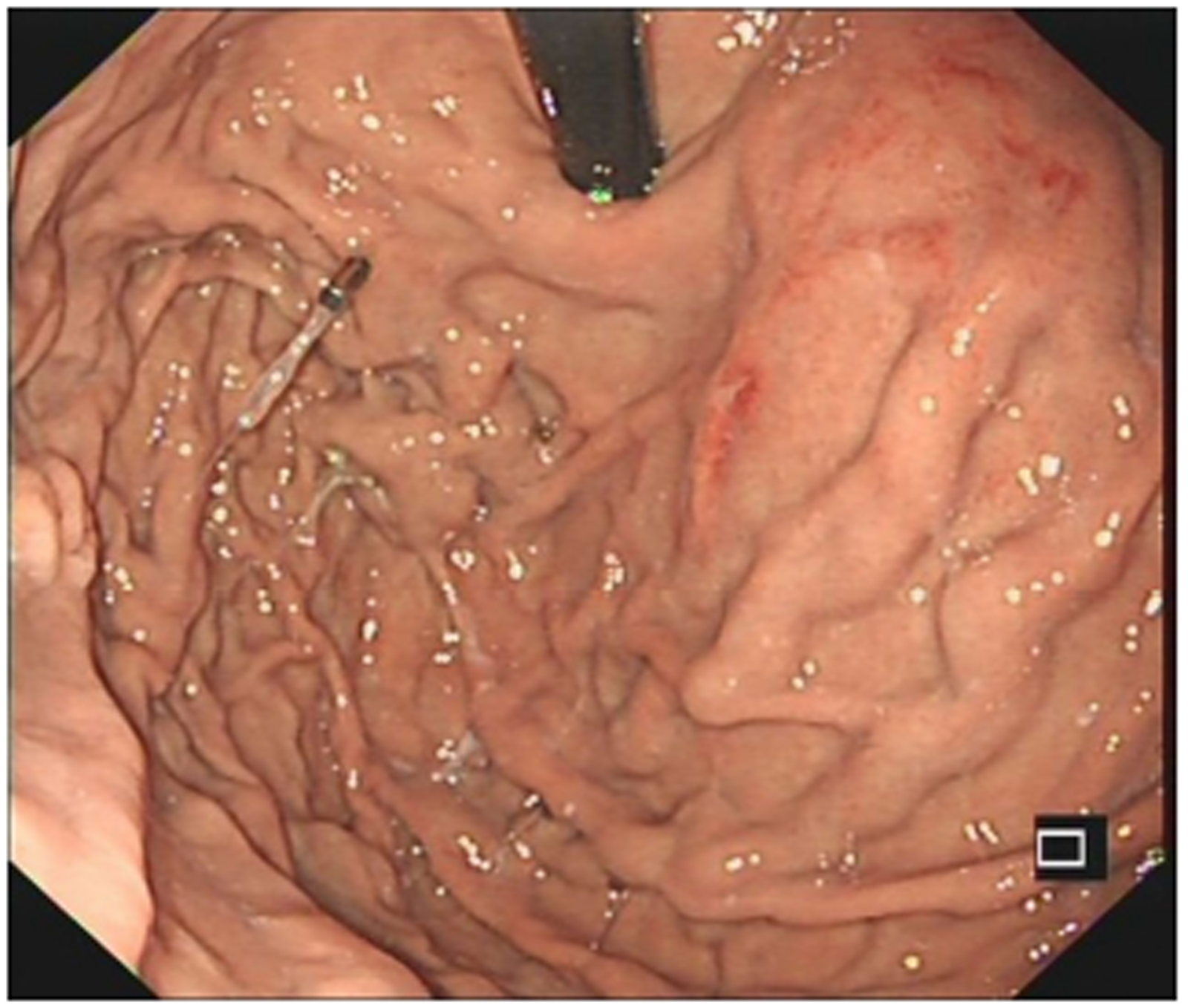
患者, 男, 43岁, 因"黑便1 mo余"入院. 患者1 mo前无明显诱因下解稀糊状黑便3次, 总量约500 mL左右, 当地医院查血红蛋白74 g/L, 血小板84×109/L, 抑酸、补液对症治疗后患者黑便停止. 胃镜提示食管静脉未见曲张, 胃底见数条蔓状分布曲张静脉, 并有可疑的出血病灶. 腹部电子计算机断层扫描(computed tomography, CT)示脾稍大, 未见肝硬化征象. 于当地医院行胃底曲张静脉组织胶+硬化剂治疗. 后无呕血及黑便, 为进一步诊治入住我科. 查体: 入院时脾肋下2 cm. 血常规示白细胞 3.87×109/L, 中性粒细胞百分比53.90%, 血红蛋白70 g/L, 血小板80×109/L, 肝功能示白蛋白38.3 g/L, 球蛋白29.2 g/L, 总胆红素6.96 μmol/L, 谷丙转氨酶9 U/L, 谷草转氨酶12 U/L, 碱性磷酸酶56 U/L, γ-谷氨酰转移酶20 U/L. 甲乙丙丁戊肝炎及肿瘤指标均阴性. 腹部增强CT示胰腺形态饱满, 呈"腊肠样改变", 边缘条状低密度影, 密度均匀(图1), 脾静脉及肠系膜上静脉血栓形成, 胰腺段狭窄, 脾动脉见血栓形成(图2). 胃镜示胃底静脉曲张, 内镜治疗后改变(图3). 完善抗核抗体阳性(核均质1:320), 自免肝全套、抗中性粒细胞胞浆抗体、抗心磷脂抗体均阴性, IgG 16.26 g/L, IgG 4种亚型: IgG1 9.07 g/L, IgG2 5.69 g/L, IgG3 0.540 g/L, IgG4 3.940 g/L. 超声内镜示胰腺体积明显肿大, 形态尚规则, 呈低回声改变, 散在强回声点, 胰管规整, 黏膜层回声增强, 内未见强回声. 穿刺病理提示为胰腺组织及炎症细胞浸润, 未见肿瘤细胞(图4), 免疫组化示取材较少, 未见IgG4阳性浆细胞(图5).
IgG4相关AIP左侧门脉高压, 胃底静脉曲张, 脾静脉血栓, 肠系膜静脉血栓, 脾动脉血栓, 贫血.
口服强的松40 mg/d, 持续4 wk后, 每周减量5 mg, 至5 mg后继续维持治疗. 口服激素期间同时口服艾斯奥美拉唑20 mg/d.
口服激素40 mg/d, 持续4 wk后, 复查IgG 12.64 g/L, IgG4 2.55 g/L, 后激素每周减量5 mg-5 mg/d维持疗程3 mo后复查, 患者无呕血黑便, 血红蛋白较前明显升高(103 g/L), 胃镜示曲张静脉较3 mo前改善(图6), CT示胰腺肿胀较前好转, 脾静脉及肠系膜静脉胰腺段血栓较前改善.
孤立胃底静脉曲张形态分为结节隆起型、条索型、葡萄串型及树枝型. 临床常见结节隆起型, 对于非结节型曲张静脉, 病因多为区域性门脉高压(regional portal hypertension, RPH), 应该积极寻找及针对原发病治疗, 内镜下组织胶及硬化剂治疗效果差[1,2]. 通常胃底体的静脉血通过两条途径回流至门静脉, (1)胃贲门区附近的静脉血→胃左静脉→门静脉; (2)胃底体静脉血→胃短静脉及胃后静脉或胃网膜左静脉→脾静脉→门静脉, 当脾静脉及肠系膜上静脉受阻时, 胃底静脉回流不畅, 则会出现侧支循环开放及胃底静脉曲张形成. 而RPH最常见原因为胰源性门脉高压, 其中慢性胰腺炎的发生率最高, 约占总病例的60%, 胰腺肿瘤是第二个最常见的原因(约10%). RPH的其他不太常见的原因是腹膜后肿瘤, 恶性淋巴结肿大, 淋巴瘤和医源性原因, 如脾切除术和部分胃切除术[3]. 而我们此次报道的是一例特殊的慢性胰腺炎, 罕见的IgG4相关AIP合并胃底静脉曲张破裂出血的病例.
自1995年Yoshida等[4]人首次提出AIP的概念, 现在AIP已被世界公认为一种特殊类型的慢性胰腺炎AIP分为1型和2型两种亚型, 其中1型AIP在亚洲人群更常见. 特点是淋巴细胞和浆细胞的大量浸润, 尤其是IgG4阳性浆细胞, 席文状纤维化, 闭塞性静脉炎, 和其他脏器的受累. 本病例患者有典型CT下AIP表现包括胰腺弥漫性肿大及包膜样的低密度边缘[5]、IgG4升高大于135 mg/dL, 符合AIP国际诊断共识及JPS-2011标准[6]. 诊断为1型AIP明确. 关于AIP引起胃底静脉曲破裂出血的报道很少, 考虑原因可能是脾静脉及肠系膜上静脉的闭塞或血栓形成, Agarwal等[7]人报道了156例AIP中34例出现门静脉血栓, 其中15%病人出现胃底静脉曲张破裂出血Ishikawa等[8]报道中AIP发生胰周血管病变的概率在44%(24/54), 其中胰腺呈弥漫性改变, 其胰周血管发生闭塞概率增加, 发生血管病变的机制暂未完全明确. 静脉闭塞可由外在因素引起, 因脾静脉在胰腺包膜内, 伴随胰腺背面走形, 在胰腺弥漫性肿大或局灶性病变时可导致脾静脉受压而闭塞. 而对于脾静脉内血栓形成, Kamisawa等[9]人6例AIP组织学中发现胰周静脉几乎完全闭塞, 具有淋巴浆细胞浸润和壁内及周围的成纤维细胞增殖, 呈闭塞性静脉炎样改变, 另有4例发现门静脉狭窄及8例发现胰周小动脉的改变. 无论脾静脉阻塞是由机械性还是炎性浸润形成, 脾静脉内皮损伤, 及脾静脉血流速度减慢等都增加脾静脉血栓发生的几率, 且随着时间推移, 可形成不可逆的血栓, 从而进一步加重左侧门脉高压及胃底静脉曲张. 在日本的3例AIP合并脾静脉血栓形成的报道, 病例1无脾脏肿大, 治疗后曲张静脉消失, 病例3合并脾肿大及门脉血栓, 治疗后脾静脉血栓及曲张静脉均未消失. 类固醇激素治疗可改善闭塞性静脉炎及患者免疫状况, 进而改善脾静脉血栓, 且建议对于有脾静脉血栓的病人尽早加用激素的治疗[10]. 同样近期报道也建议对于有胰周血管病变, 尚未出现血栓及胃底静脉曲张的AIP患者可早期加用类固醇治疗, 因为早期类固醇治疗可减少脾静脉血栓的发生, 从而降低胃底静脉曲张破裂出血等并发症的发生[11]. 近期庞桃红等也报道一例AIP合并胃底静脉曲张, 脾静脉受压但无脾静脉血栓形成的病例, 再使用激素治疗后, 胃底静脉曲张静脉迅速得到缓解, 该患者胃底静脉曲张迅速改善可能为脾静脉受压导致狭窄, 无血栓形成, 在胰腺肿大缓解后, 脾静脉血流恢复, 胃底静脉曲张缓解明显[12]. Lin等[13]也报道了一例因黑便就诊, 诊断为AIP合并胃底和十二指肠静脉曲张的病例, 同时因胰腺肿大至十二指肠狭窄行胃空肠吻合术, 术中见脾静脉及肠系膜上静脉血栓形成. 口服类固醇激素治疗3 mo后再次出现黑便并追加内镜下套扎治疗, 出血停止后继续口服激素治疗, 随访一年未再出血, 但未复查血栓及血管消失情况本例病例口服激素前脾静脉及肠系膜静脉重度狭窄, 脾静脉胰腺段几乎完全闭塞, 同时肠系膜静脉及脾动脉也发现有血栓形成及狭窄, 3 mo后胃镜见胃底曲张静脉好转, 复查CT提示胰腺肿胀较前明显好转, 脾静脉及肠系膜静脉狭窄较前好转, 但脾静脉血栓尚未完全消失. 目前尚未有对AIP合并脾静脉血栓使用低分子肝素及华法林等溶栓治疗报道. Loffredo等[14]人的一个大型系统回顾和Meta分析显示低分子肝素对于肝硬化合并门脉血栓形成病例有较好的疗效, 且不增加其食管胃底静脉曲张破裂出血风险. 合并脾静脉血栓的AIP患者, 在使用激素治疗的同时是否可使用低分子肝素抗凝治疗改善血栓情况, 期待更多的病例报道及长期的随访.
对于孤立胃底静脉曲张破裂出血, 左侧门脉高压的患者, 在止血治疗后应积极寻找病因. AIP患者, 脾静脉血栓治疗对于胃底静脉曲张的消失可能起关键作用. 对于影响脾静脉血栓治疗效果的因素和更多治疗方法, 期待更多病例数及更长时间随访的报道.
学科分类: 胃肠病学和肝病学
手稿来源地: 安徽省
同行评议报告分类
A级 (优秀): 0
B级 (非常好): B, B
C级 (良好): C, C
D级 (一般): D
E级 (差): E
编辑: 崔丽君 电编:刘继红
| 1. | Sarin SK, Lahoti D, Saxena SP, Murthy NS, Makwana UK. Prevalence, classification and natural history of gastric varices: a long-term follow-up study in 568 portal hypertension patients. Hepatology. 1992;16:1343-1349. [PubMed] |
| 2. | 朱 燕华, 吴 云林, 吴 巍, 范 嵘, 孙 萍胡, 李 晨, 胡 月亮. 孤立性胃脉曲张的内下形态分型及临床特点. 胃肠病学和肝病学杂志. 2017;20:637-640. [DOI] |
| 3. | Liu QD, Zhou NX, Zhang WZ, Wang MQ. Diagnosis and management of regional portal hypertension. Chin J Dig Dis. 2005;6:87-92. [PubMed] [DOI] |
| 4. | Yoshida K, Toki F, Takeuchi T, Watanabe S, Shiratori K, Hayashi N. Chronic pancreatitis caused by an autoimmune abnormality. Proposal of the concept of autoimmune pancreatitis. Dig Dis Sci. 1995;40:1561-1568. [PubMed] |
| 5. | Suzuki K, Itoh S, Nagasaka T, Ogawa H, Ota T, Naganawa S. CT findings in autoimmune pancreatitis: assessment using multiphase contrast-enhanced multisection CT. Clin Radiol. 2010;65:735-743. [PubMed] [DOI] |
| 6. | Sumimoto K, Uchida K, Mitsuyama T, Fukui Y, Kusuda T, Miyoshi H, Tomiyama T, Fukata N, Koyabu M, Sakaguchi Y, Ikeura T, Shimatani M, Fukui T, Matsushita M, Takaoka M, Nishio A, Okazaki K. A proposal of a diagnostic algorithm with validation of International Consensus Diagnostic Criteria for autoimmune pancreatitis in a Japanese cohort. Pancreatology. 2013;13:230-237. [PubMed] [DOI] |
| 7. | Agarwal AK, Raj Kumar K, Agarwal S, Singh S. Significance of splenic vein thrombosis in chronic pancreatitis. Am J Surg. 2008;196:149-154. [PubMed] [DOI] |
| 8. | Ishikawa T, Itoh A, Kawashima H, Ohno E, Itoh Y, Nakamura Y, Hiramatsu T, Miyahara R, Ohmiya N, Haruta J, Goto H, Hirooka Y. Peripancreatic vascular involvements of autoimmune pancreatitis. J Gastroenterol Hepatol. 2012;27:1790-1795. [PubMed] [DOI] |
| 9. | Kamisawa T, Egawa N, Nakajima H. Extrapancreatic Lesions in Autoimmune Pancreatitis. J Clin Gastroenterol. 2009;10:904-907. |
| 10. | Goto N, Mimura J, Itani T, Hayashi M, Shimada Y, Matsumori T. Autoimmune pancreatitis complicated by gastric varices: a report of 3 cases. World J Gastroenterol. 2012;18:4228-4232. [PubMed] [DOI] |
| 11. | Juarez LA, Gupta RR, Ruhnke GW. Gastric varices and splenic vein obstruction during steroid treatment for autoimmune pancreatitis: A case report and literature review. Medicine (Baltimore). 2018;97:e11940. [PubMed] [DOI] |
| 12. | 庞 桃红, 胡 青青, 曹 守莉, 吕 瑛, 王 雷, 诸葛 宇征, 邹 晓平, 徐 桂芳. 自身免疫性胰腺炎合并左侧门静脉高压胃底静脉曲张破裂出血一例. 中华消化内镜杂志. 2018;35:446-447. [DOI] |
| 13. | Lin TC, Chang WL. Multifocal gastrointestinal varices: a rare manifestation of immunoglobulin G4-related disease. Postgrad Med. 2019;131:176-181. [PubMed] [DOI] |
| 14. | Loffredo L, Pastori D, Farcomeni A, Violi F. Effects of Anticoagulants in Patients With Cirrhosis and Portal Vein Thrombosis: A Systematic Review and Meta-analysis. Gastroenterology. 2017;153:480-487.e1. [PubMed] [DOI] |