修回日期: 2015-12-27
接受日期: 2016-01-06
在线出版日期: 2016-02-08
目的: 评价乳果糖预防肝硬化消化道出血后肝性脑病的疗效.
方法: 检索1990-01/2015-08 Medline、Embase、SCI、CBM以及Cochrane图书馆数据库, 不限语种纳入所有关于乳果糖预防消化道出血后肝性脑病的随机对照试验(randomized controlled trials, RCT)文献, 对搜索到的RCT以及参考文献进行二次筛选, 对纳入的研究进行质量评价, 采用RevMan软件进行Meta分析.
结果: 共有11篇RCT文献符合纳入标准. Meta分析结果显示, 增加乳果糖治疗可以减少肝硬化上消化道出血后肝性脑病的发生率(RR = 0.24, 95%CI: 0.16-0.35, P<0.00001), 减少SHE的发生率(RR = 0.15, 95%CI: 0.06-0.38, P<0.0001), 缩短数字连接试验时间(WMD = -12.55, 95%CI: -17.23--7.87, P<0.00001), 降低血氨浓度(WMD = -6.44, 95%CI: -8.26--4.61, P<0.00001).
结论: 乳果糖可以降低肝硬化合并消化道出血时肝性脑病以及SHE的发生率, 降低血氨水平、改善数字连接试验(number connection test, NCT)时间, 不良反应率低, 可以推荐用来预防肝硬化消化道出血患者肝性脑病的发生. 目前需要大样本量、多中心、高质量的RCT来支持这一循证医学结论.
核心提示: Meta分析表明, 乳果糖可以降低肝硬化合并上消化道出血时肝性脑病(hepatic encephalopathy, HE)以及亚临床肝性脑病(subclinical hepatic encephalopathy)的发生率, 降低血氨水平、改善数字连接试验时间, 不良反应率低,可以推荐用来预防肝硬化消化道出血患者HE的发生.
引文著录: 夏亮, 陈文欣, 喻永明, 吕农华, 胡杨. 乳果糖预防肝硬化消化道出血后肝性脑病疗效的系统评价. 世界华人消化杂志 2016; 24(4): 594-600
Revised: December 27, 2015
Accepted: January 6, 2016
Published online: February 8, 2016
AIM: To evaluate the efficacy of lactulose in preventing hepatic encephalopathy after digestive tract hemorrhage in liver cirrhosis.
METHODS: All the randomized controlled trials (RCTs) published in all languages concerning lactulose in preventing hepatic encephalopathy after upper digestive tract hemorrhage published from January 1990 to August 2015 were retrieved from the databases of Medline, Embase, SCI, CBM and Cochrane Library. The retrieved RCTs experienced a secondary screening before quality assessment, and Meta-analysis was carried out using the RevMan software.
RESULTS: A total of 11 RCTs met the inclusion criteria. Meta-analysis showed that additional lactulose administration could reduce the incidence rate of hepatic encephalopathy after liver cirrhosis-induced upper digestive tract hemorrhage (RR = 0.24, 95%CI: 0.16-0.35, P<0.00001) and subclinical hepatic encephalopathy (RR = 0.15, 95%CI: 0.06-0.38, P<0.0001). It can shorten the time for the number connection test (NCT) (WMD = -12.55, 95%CI: -17.23--7.87, P<0.00001) and decrease blood ammonia concentration (WMD = -6.44, 95%CI: -8.26--4.61, P<0.00001).
CONCLUSION: Lactulose can lower the incidence rate of hepatic encephalopathy after upper digestive tract hemorrhage in liver cirrhosis and subclinical hepatic encephalopathy, and improve patients' performance in NCT with a lower rate of adverse reactions. Therefore, use of lactulose is recommended for prevention of hepatic encephalopathy after upper digestive tract hemorrhage in liver cirrhosis. Multi-center and high-quality RCTs based on larger sample size are needed to confirm this evidence-based medical conclusion.
- Citation: Xia L, Chen WX, Yu YM, Lv NH, Hu Y. Efficacy of lactulose in prophylaxis of hepatic encephalopathy after acute gastrointestinal bleeding: A meta-analysis. Shijie Huaren Xiaohua Zazhi 2016; 24(4): 594-600
- URL: https://www.wjgnet.com/1009-3079/full/v24/i4/594.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v24.i4.594
严重的肝病可能会继发肝性脑病(hepatic encephalopathy, HE), 风险因素包括脱水、便秘、肾功能衰竭、电解质平衡紊乱、感染、胃肠道出血以及肝细胞癌[1,2]. 接近50%的肝硬化患者都有静脉曲张, 而肝硬化患者食管静脉曲张出血的发生率为25%-35%[3]. 胃肠道出血可认为是HE最常见的诱因之一. 由于胃肠道的蛋白过度生成的机制, 出血参与了HE的发生. 肠道吸收过多的血红蛋白分解的氨, 是肝硬化消化道出血后HE的主要病理生理机制[4]. 乳果糖常用于HE的治疗, 其为不可吸收的双糖, 可以减少肠道细菌产氨, 日常饮食添加乳果糖可以产生对结肠氨代谢有利的双歧因子效应[5-7]. 近年来, 国内外一些学者开展了应用乳果糖预防肝硬化消化道出血后HE发生的临床研究, 但为小样本研究, 疗效不一致, 本研究通过现有的相关随机对照试验(randomized controlled trials, RCT)进行系统评价, 探讨乳果糖预防消化道出血后HE发生的疗效.
检索策略: 检索相关的数据库(Medline、Embase、SCI、CBM以及Cochrane 图书馆)研究限定在成年患者, 时间由1990-01/2015-08, 不限语种. 检索词为: 英文: lactulose、hepatic encephalopathy、bleeding、 randomized controlled trials; 中文: 乳果糖, 消化道出血, 肝性脑病. 不限语种, 纳入所有关于乳果糖预防消化道出血后HE的RCT, 对搜索到的RCT以及参考文献进行二次筛选.
1.2.1 文献纳入与排除标准: 纳入标准: (1)研究对象: 肝硬化患者合并消化道出血; (2)RCT, 不论选取的试验是否采用了分配隐藏或者盲法; (3)干预措施: 探讨乳果糖预防出血后HE的研究均被纳入, 药物开始的时间、疗程、剂量、给药途径不限; (4)结局指标: 以治疗前后乳果糖组和对照组的HE及亚临床肝性脑病(subclinical hepatic encephalopathy, SHE)发生率、数字连接试验(number connection test, NCT)、血氨浓度数据作为两组疗效指标, 以两组患者的不良反应发生率作为判断安全性的指标. 排除标准: (1)存在重复发表情况的文献; (2)无法获得文献全文也无法从摘要中获取所需要数据的文献; (3)未公开发表的文献.
1.2.2 资料提取: 2名独立研究者阅读所得文献的题目和摘要, 排除不符合纳入标准的文献后, 再对有可能符合标准的文献行全文阅读, 最终确定所需要纳入的文献将所需要记录信息填入预先制定好的数据提取表中, 再将所得数据进行整理. 如遇分歧, 则通过讨论来决定是否将文献纳入研究.
1.2.3 文献质量评价: 由研究者将纳入研究的文献进行整理, 对文献中所涉及的方法学如随机方法、分配隐藏、盲法等内容用Jadad评分表进行质量评价. 如遇分歧, 则互相讨论解决[8].
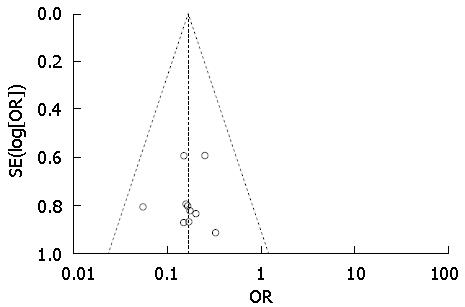
统计学处理 本研究所采用的统计分析软件是由Cochrane协作网提供的RevMan5.3软件. 对纳入研究结果之间的异质性进行卡方检验(Chi-square test, χ2)和I2检验. 若P>0.05, I2<50%, 表明异质性不明显, 选用固定效应模型估计合并效应量; 若P<0.05, I2>50%, 表明异质性明显, 可采用随机效应模型估计合并效应量, 若异质性过于明显, 则需进一步分析异质性原因和来源, 必要时进行亚组分析、敏感性分析. 计数资料的效应量表达采用RR及其95%CI, 连续性变量采用MD及其95%CI, P<0.05为差异具有统计学意义. 采用倒漏斗图分析是否存在潜在的发表性偏倚[9].
2.1.1 纳入文献的基本情况: 共检出相关文献26篇, 经阅读文题和摘要, 排除不符合本研究要求的文献, 初步筛选得到对照试验13篇, 经阅读全文对照纳入和排除标准排除2篇研究, 其中1篇联用了巴龙霉素, 1篇对照组为利福昔明且未报告HE发生率, 最终纳入11篇RCT文献. 在11篇RCT文献中, 共纳入肝硬化失代偿期患者755例(乳果糖组379例, 对照组376例), 文献基本特征如表1.
2.1.2 纳入研究的质量评价: 本研究纳入的11篇文献, 英文文献质量更高, 表现为: 英文2篇文献均详细描述了随机化以及分配隐藏方案, 中文文献均在文中提及随机而未进行详细描述; 所有文献未采用盲法, 中文文献均未描述有无失访和退出病例、均未报道随机化隐藏情况. 因此, 2篇英文RCT的Jadad评分>3分, 其余均为2分, 为低质量研究文献(表1).
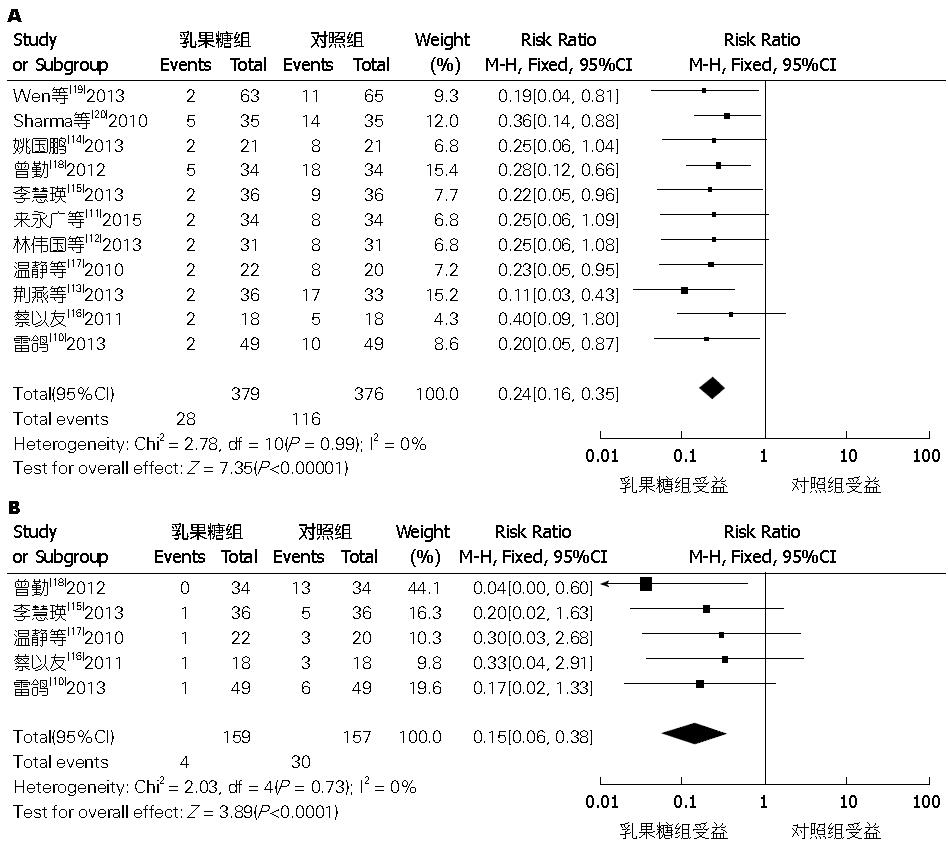
2.2.1 HE: 对纳入的11项临床研究[10-20]进行异质性检验, 结果显示各研究间不存在异质性(P = 0.99, I2 = 0%). 因此使用固定效应模型合并效应量, Meta分析显示, 治疗组的HE发生率显著下降(RR = 0.24, 95%CI: 0.16-0.35, P<0.00001)(图1A).
有5个RCT[10,15-18]进行了SHE的观察, 对纳入的5项临床研究进行异质性检验, 结果显示各研究间不存在异质性(P = 0.73, I2 = 0%). 因此使用固定效应模型合并效应量, Meta分析显示, 乳果糖组的SHE发生率也比对照组显著下降(RR = 0.15, 95%CI: 0.06-0.38, P<0.0001)(图1B).
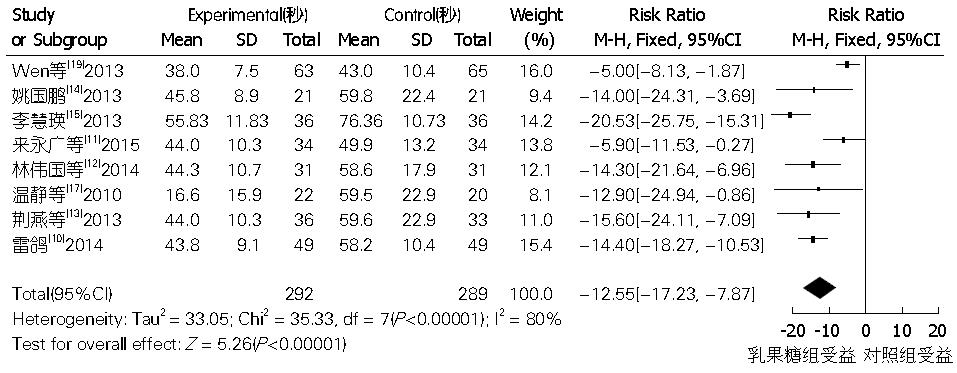
2.2.2 NCT: 有8个研究[10-15,17,19]包括了NCT的数据, 对这些临床研究进行异质性检验, 结果显示各研究间存在异质性(P<0.00001, I2 = 80%), 遂进行敏感性分析: 分别排除英文研究[19](排除后异质性P<0.05, I2 = 58%)、1个[15]联合了枯草杆菌治疗的研究(排除后异质性P = 0.002, I2 = 70%)及2011年前的研究[17](排除后异质性P<0.00001, I2 = 83%)后亚组仍存在异质性, 且异质性对结果无明显影响, 因此使用随机效应模型合并效应量, Meta分析显示, 治疗组的NCT比对照组明显缩短(WMD = -12.55, 95%CI: -17.23--7.87, P<0.00001)(图2).
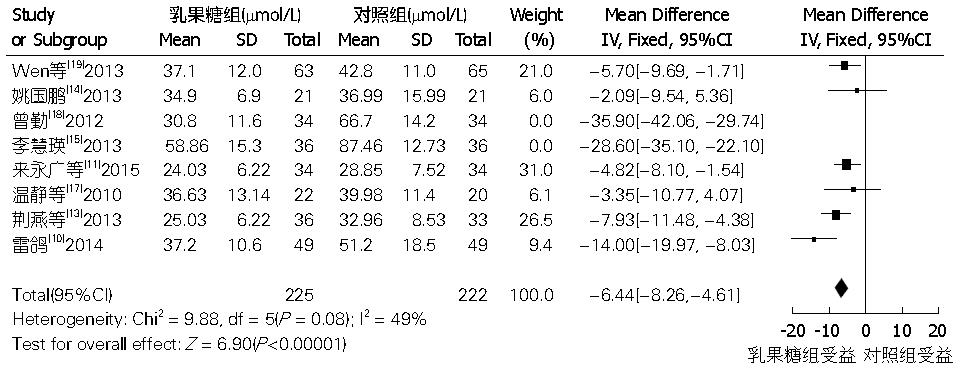
2.2.3 血氨浓度: 对纳入报告了血氨浓度的8个临床研究[10,11,13-15,17-19]进行异质性检验, 结果显示各研究间存在异质性(P<0.00001, I2 = 94%), 由于统计学异质性较高, 遂进行临床异质性分析: (1)本研究已经对纳入的RCT中血氨浓度结果进行换算, 统一使用μmol/L为单位, 计算公式为1 μmol/L = 0.714 μg/dL[21]; (2)排除2个[15,18]联合了枯草杆菌治疗的RCT后, 亚组内异质性明显降低(P = 0.08, I2 = 49%), 因此使用固定效应模型合并亚组的效应量, Meta分析显示, 乳果糖组的血氨浓度比对照组明显下降(WMD = -6.44, 95%CI: -8.26--4.61, P<0.00001)(图3).
HE是因肝功能衰竭后的生化学异常所导致的一种代谢性脑病. 氨代谢紊乱是HE病理生理的一个重要机制. 中枢神经系统积累的血氨升高会引起神经传导功能的显著改变[22]. 因为治疗手段有限, 积极消除诱因仍然是防治HE的主要原则之一.
肝硬化患者食管胃底静脉曲张破裂出血的发生率为25%-30%, 且其肠道内腐败菌大量生长繁殖, 消化道出血后, 血液中所含的蛋白质聚集在肠道内经腐败菌分解后产生氨, 弥散进入血液, 而肝硬化患者肝脏代谢氨的能力减退且存在门体分流, 最终引起血氨增高[23]. 出血还会形成适于肠道细菌繁殖的环境. 细菌的毒素可能会导致机体感染从而引起组织分解, 进一步增加氨的生成. 血尿素氮在上消化道出血后数小时内开始升高(每100 mL血含有20 g蛋白质), 并在24-48 h达到峰值. 大多数HE的药物治疗都着眼于通过抑制氨生成或者促进氨分解而减少氨的水平[24].
由于乳果糖对血氨水平的降低作用, 其被广泛用来治疗HE. 小肠上皮微绒毛膜上无二糖酶, 所以乳果糖基本不被小肠吸收; 在结肠内, 乳果糖易被细菌酵解为乳酸, 这种酸环境首先可以促使氨转化为铵离子随之从粪便排出, 减少氨的吸收; 其次, 促进肠蠕动, 缩短有害物质在肠腔内停留的时间, 使其能及时排出体外; 其三, 可以抑制含氮化合物分解为氨[25]. 有一个研究[20]结果显示出乳果糖治疗组的中位氨浓度要比对照组低. 乳果糖还作为益生元能促进益生菌的繁殖, 调节肠道的微环境, 抑制肠道致病菌从而减少氨的生成[26]. 根据大量的研究以及美国研究学会调查, 乳果糖公布为轻微HE的第一位标准治疗[27].
预防肝硬化患者的HE发作在肝硬化治疗上具有重要的意义[1,28]. 这篇Meta分析纳入评价了肝硬化消化道出血后乳果糖预防HE疗效的RCT研究. 通过检索国内外关于乳果糖防治肝硬化消化道出血患者发生HE的RCT, 研究结果显示, 乳果糖可以降低HE及SHE的发生率, 可以改善肝硬化消化道出血患者的相关指标, 可以常规应用于预防肝硬化消化道出血后的HE发生. 因此扩展了以往对乳果糖仅用于治疗肝硬化并发HE的认识[20]. 同时, 对SHE发病率的Meta分析显示, 乳果糖也能够用于改善肝硬化出血患者SHE的发生. 但是, 由于目前SHE的诊断缺乏统一的标准, 其诊断受到许多因素的影响包括患者的教育水平、酒精性肝硬化患者的酒精性脑病等, 我们对SHE的Meta分析结果可能存在偏倚.
与其他Meta分析比较, 本研究没有排除乳果糖联合门冬氨酸鸟氨酸等药物的临床试验, 因为该类药物已经作为HE的标准治疗之一, 在HE的治疗中使用广泛, 而且在我们对纳入试验的异质性检验中, 敏感性分析认为该研究对异质性和Meta分析结果无明显影响. 也因此纳入了更多的临床试验. 而我们的研究结果显示, 这些试验的NCT结果、血氨水平异质性较大, 排除合并枯草杆菌的研究后亚组的血氨指标异质性明显减少, 这提示: (1)NCT结果受到医师培训专业程度、患者年龄、患者文化程度的影响较大, 容易产生较大的异质性; (2)如前文所述, 益生菌可能通过协助调解肠道微环境、酸化肠道等途径减少肠道氨的生成与吸收, 因而对研究结果产生较大的影响.
在纳入试验的报道中, 没有患者因为发生严重的乳果糖不良反应退出研究, 但有一些患者出现明显腹泻. 因此, 长期使用乳果糖治疗可能会增加腹泻的严重度和频率.
本研究的局限性在于: (1)纳入文献的质量, 尤其是中文, 有待进一步提高, 英文文献的样本量较多, 有助于减少偏倚发生, 但纳入文献数较少; (2)肝硬化出血后HE的病死率涉及的因素多, 不能直接与HE相关, 且纳入研究的研究时间非常短(1 wk), 因此本研究不能做病死率的评价; (3)由于乳果糖具有甜味以及腹泻的作用, 难以设计安慰剂, 无法进行盲法设计, 可能会造成主观偏倚; (4)国外与国内的肝硬化病因不同, 因此对于酒精性脑病与HE是否会对研究有干扰这一点目前尚无法确定; (5)NCT的异质性较大, 系因其影响因素复杂, 对该指标的Meta分析有一定的局限性.
总之, 乳果糖可以减少肝硬化消化道出血患者的HE及SHE发病率, 降低血氨水平、改善NCT时间, 不良反应率低, 可以推荐用来预防肝硬化消化道出血患者HE的发生, 目前需要大样本量、多中心、高质量的RCT来支持这一循证医学结论.
近年来, 国内外一些学者开展了应用乳果糖预防肝硬化消化道出血后肝性脑病(hepatic encephalopathy, HE)发生的临床研究, 但为小样本研究, 疗效不一致, 本研究通过现有的国内外相关随机对照试验(randomized controlled trials, RCT)进行系统评价, 探讨乳果糖预防消化道出血后HE发生的有效性.
许钟, 副主任医师, 贵州省人民医院消化内科
消化道出血后, 会增加氨的生成, 而肝硬化患者肝脏代谢氨的能力减退, 最终引起血氨增高. 目前大多数HE的药物治疗都着眼于通过抑制氨生成或者促进氨分解而减少氨的水平.
Clausen等分析认为乳果糖作为益生元能促进益生菌的繁殖, 改善肠道菌群从而减少氨的生成. 根据美国研究学会调查, 乳果糖公布为轻微HE的第一位标准治疗.
通过检索国内外的RCT, 本文的研究结果显示, 乳果糖可以常规应用于预防肝硬化消化道出血后的HE发生. 因此扩展了以往对乳果糖仅用于治疗肝硬化并发HE的认识.
临床应用中, 乳果糖可以缩短肝硬化消化道出血患者的数字连接试验(number connection test, NCT)时间、降低其血氨水平, 不良反应率低, 可以推荐用来预防肝硬化消化道出血患者HE的发生.
NCT: 是公认诊断轻微型HE的简单易行和最有价值的智力检测指标. 国内外一直沿用1978年Conn建立的卡片式检测, 是测定将随机排列的1-25个数字按顺序连接起来所用的时间, 包括纠正错误所用的时间.
本文对于乳果糖预防肝硬化出血患者HE的研究纳入全面, 反应了目前国内外在该方向上的研究结果. 但其中一部分纳入的文献质量偏低, 一定程度上影响了本研究的意义.
编辑: 郭鹏 电编: 闫晋利
| 1. | Munoz SJ. Hepatic encephalopathy. Med Clin North Am. 2008;92:795-812, viii. [PubMed] [DOI] |
| 2. | Sundaram V, Shaikh OS. Hepatic encephalopathy: pathophysiology and emerging therapies. Med Clin North Am. 2009;93:819-836, vii. [PubMed] [DOI] |
| 3. | Calès P, Zabotto B, Meskens C, Caucanas JP, Vinel JP, Desmorat H, Fermanian J, Pascal JP. Gastroesophageal endoscopic features in cirrhosis. Observer variability, interassociations, and relationship to hepatic dysfunction. Gastroenterology. 1990;98:156-162. [PubMed] |
| 4. | Hassan SN, Townsend JL, Curry SB. Hepatic encephalopathy: a retrospective analysis. J Natl Med Assoc. 1982;74:521-523. [PubMed] |
| 5. | Blei AT, Córdoba J. Hepatic Encephalopathy. Am J Gastroenterol. 2001;96:1968-1976. [PubMed] [DOI] |
| 6. | Riordan SM, Williams R. Treatment of hepatic encephalopathy. N Engl J Med. 1997;337:473-479. [PubMed] [DOI] |
| 7. | Bouhnik Y, Attar A, Joly FA, Riottot M, Dyard F, Flourié B. Lactulose ingestion increases faecal bifidobacterial counts: a randomised double-blind study in healthy humans. Eur J Clin Nutr. 2004;58:462-466. [PubMed] [DOI] |
| 8. | Jadad AR, Moore RA, Carroll D, Jenkinson C, Reynolds DJ, Gavaghan DJ, McQuay HJ. Assessing the quality of reports of randomized clinical trials: is blinding necessary? Control Clin Trials. 1996;17:1-12. [PubMed] |
| 9. | Moher D, Cook DJ, Eastwood S, Olkin I, Rennie D, Stroup DF. Improving the quality of reports of meta-analyses of randomised controlled trials: the QUOROM statement. Quality of Reporting of Meta-analyses. Lancet. 1999;354:1896-1900. [PubMed] |
| 17. | 温 静, 梁 浩, 常 宇峰, 彭 丽花, 郭 明洲. 乳果糖预防消化道出血后诱发肝性脑病的疗效观察. 胃肠病学和肝病学杂志. 2010;19:360-361. |
| 19. | Wen J, Liu Q, Song J, Tong M, Peng L, Liang H. Lactulose is highly potential in prophylaxis of hepatic encephalopathy in patients with cirrhosis and upper gastrointestinal bleeding: results of a controlled randomized trial. Digestion. 2013;87:132-138. [PubMed] [DOI] |
| 20. | Sharma P, Agrawal A, Sharma BC, Sarin SK. Prophylaxis of hepatic encephalopathy in acute variceal bleed: a randomized controlled trial of lactulose versus no lactulose. J Gastroenterol Hepatol. 2011;26:996-1003. [PubMed] [DOI] |
| 22. | Butterworth RF. The neurobiology of hepatic encephalopathy. Semin Liver Dis. 1996;16:235-244. [PubMed] [DOI] |
| 23. | Vaquero J, Chung C, Blei AT. Brain edema in acute liver failure. A window to the pathogenesis of hepatic encephalopathy. Ann Hepatol. 2003;2:12-22. [PubMed] |
| 24. | Foster KJ, Lin S, Turck CJ. Current and emerging strategies for treating hepatic encephalopathy. Crit Care Nurs Clin North Am. 2010;22:341-350. [PubMed] [DOI] |
| 25. | Weber FL. Effects of lactulose on nitrogen metabolism. Scand J Gastroenterol Suppl. 1997;222:83-87. [PubMed] |
| 26. | Clausen MR, Mortensen PB. Lactulose, disaccharides and colonic flora. Clinical consequences. Drugs. 1997;53:930-942. [PubMed] |
| 27. | Bajaj JS, Etemadian A, Hafeezullah M, Saeian K. Testing for minimal hepatic encephalopathy in the United States: An AASLD survey. Hepatology. 2007;45:833-834. [PubMed] [DOI] |
| 28. | Poordad FF. Review article: the burden of hepatic encephalopathy. Aliment Pharmacol Ther. 2007;25 Suppl 1:3-9. [PubMed] [DOI] |