修回日期: 2014-12-07
接受日期: 2014-12-18
在线出版日期: 2015-01-28
目的: 评价替吉奥胶囊(S-1)联合热疗治疗老年晚期胃癌的临床疗效及不良反应, 旨在为65岁以上的老年晚期胃癌患者寻找有效、不良反应轻的治疗方式.
方法: 选择2010-02/2012-09的石河子大学医学院第一附属医院的老年胃癌晚期患者(年龄≥65岁)90例, 采用随机对照研究将90例患者随机分为3组. A组给予替吉奥胶囊单药化疗, B组给予替吉奥联合热疗, C组给予卡培他滨联合热疗, 治疗时间超过两周期, 观察近期、远期疗效以及不良反应, 进行统计学分析.
结果: A、B、C组临床获益率分别是50%、80%, 70%, B组较A组临床获益率高(P<0.05), 与C组差异无统计学意义(P>0.05). 远期疗效评价: B组、C组中位无进展生存时间(6.6、5.8 mo)较A组(3.8 mo)有所延长(P<0.05). 替吉奥较卡培他滨化疗不良反应轻, 主要是乏力、腹泻、手足综合症反应较轻, 差异有统计学意义(P<0.05).
结论: 替吉奥联合热疗或卡培他滨联合化疗治疗老年晚期胃癌比替吉奥单药疗效好, 替吉奥联合热疗与卡培他滨联合热疗疗效无差异, 但替吉奥较卡培他滨不良反应轻, 老年患者耐受性好.
核心提示: 替吉奥胶囊(S-1)为口服氟尿嘧啶类新药, 近来一些Ⅱ、Ⅲ期临床试验研究显示, S-1单药或联合其他药物治疗晚期胃癌均显示较高的疗效, S-1联合热疗在老年晚期胃癌的临床应用值得期待.
引文著录: 李娜, 李勇, 巩平, 李晶, 王于理. 热疗联合替吉奥治疗老年晚期胃癌的临床疗效. 世界华人消化杂志 2015; 23(3): 445-450
Revised: December 7, 2014
Accepted: December 18, 2014
Published online: January 28, 2015
AIM: To evaluate the clinical effects of gimeracil and oteracil porassium tablet (S-1) combined with hyperthermia in the treatment of elderly patients with advanced gastric cancer.
METHODS: Ninety elderly gastric cancer patients treated from February 2010 to September 2012 were randomly divided into three groups: A, B and C. Group A received S-1 chemotherapy alone, group B was given S-1 combined with hyperthermia, and group C was given capecitabine combined with hyperthermia. After more than two cycles of treatment, the short-term and long-term curative effects and adverse reactions were analyzed.
RESULTS: The clinical benefit rate in group B was significantly higher than that in group A (80% vs 50%, P < 0.05), but was not significantly different with that in group C (70%, P > 0.05). Compared with group A (3.8 mo), median progression-free survival times in groups B (6.6 mo) and C (5.8 mo) were significantly prolonged (P < 0.05). Compared with capecitabine, S-1 was associated with significantly milder toxicity such as fatigue, diarrhea, and hand-foot syndrome (P < 0.05).
CONCLUSION: Compared with S-1 chemo-therapy alone, capecitabine or S1 combined with hyperthermia therapy has a better therapeutic effect in the treatment of elderly patients with advanced gastric cancer. The efficacy between S-1 combined with hyperthermia and capecitabine combined with hyperthermia has no difference. Compared with capecitabine, S-1 has less toxic side effects and is well tolerated in elderly patients.
- Citation: Li N, Li Y, Gong P, Li J, Wang YL. Clinical effects of hyperthermia combined with S-1 chemotherapy in elderly patients with advanced gastric cancer. Shijie Huaren Xiaohua Zazhi 2015; 23(3): 445-450
- URL: https://www.wjgnet.com/1009-3079/full/v23/i3/445.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i3.445
胃癌是全世界最常见的恶性肿瘤之一, 居恶性肿瘤死因第4位, 居我国恶性肿瘤死亡率第3位, 全世界平均每年死亡病例约700000例[1], 严重危害人类健康, 给家庭、社会造成巨大负担. 且有半数以上的患者在发现时已为肿瘤晚期, 不能行手术治疗或根治性手术切除, 因此化疗则是晚期胃癌的主要治疗方式之一. 晚期胃癌患者广泛存在体能评分差和化疗耐受性差的特点, 尤其是老年患者, 虽然顺铂(奥沙利铂)、5-氟尿嘧啶(5-fluorouracil, 5-Fu)、阿霉素等药物的联合方案具有一定的疗效, 但由于其不良反应较大, 许多晚期患者尤其是老年晚期患者不能耐受, 导致病情迅速恶化. 该研究在石河子大学医学院第一附属医院肿瘤内科老年晚期胃癌患者中开展了单药替吉奥胶囊(S-1)、替吉奥胶囊联合热疗、卡培他滨联合热疗3种不同方式的治疗, 从疗效、不良反应等方面进行比较, 报道如下.
纳入标准: (1)年龄≥65岁, 均有明确病理诊断; (2)至少有1个>2 cm的明确的可测病灶; (3)东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)评分 ≤ 3分, 预计生存期>3 mo, 不能耐受两药及以上联合方案化疗者; (4)全血细胞计数、肝肾功能、凝血功能正常; (5)临床症状明显, 临床分型为Ⅳ期[根据美国癌症联合委员会(American Joint Committeeon Cancer, AJCC)2010年分期[2], 既往未接受过氟尿嘧啶类药物治疗; (6)患者均填写知情同意书. 根据以上标准自2010-02/2012-09共收治石河子大学医学院第一附属医院老年晚期胃癌患者90例, 其中男56例, 女34例, 年龄73.00岁±4.47岁; 均为Ⅳ期患者, 其中腹腔淋巴结转移者40例, 左锁骨上淋巴结转移者20例, 肝转移28例, 骨转移8例, 胰腺转移4例(有多发转移的患者); 治疗前所有患者均完善全血细胞计数、肝肾功能、凝血功能、胸、腹部计算机断层扫描(computed tomography, CT)平扫、腹部彩超及骨扫描等相关检查. 将患者随机分为3组: A组30例, B组30例, C组30例. 3组年龄、性别、ECOG评分比较均差异无统计学意义(P>0.05)(表1), 有可比性, 观察截点时间2013-09.
1.2.1 化疗治疗: A组: 替吉奥胶囊80 mg/(m2·d), 分2次在早、晚餐后半小时用温水吞服, 第1-14天[3], 休息1 wk, 每3 wk为1个周期, 重复至患者病情进展或其他原因停药. B组: 替吉奥胶囊每日80 mg/m2, 分2次在早、晚餐后半小时用温水吞服, 第1-14天, 休息1 wk, 每3 wk为1个周期, 重复至患者病情进展或其他原因停药. 化疗期间加用射频热疗, 每周3次, 每次1 h. C组: 卡培他滨每日2500 mg/m2, 分2次在早晚餐后半小时用温水吞服, 第1-14天化疗, 休息1 wk, 每3 wk为1个周期, 重复至患者病情进展或其他原因停药. 化疗期间加用射频热疗, 3次/wk, 每次1 h.
1.2.2 热疗: 采用NRL-Ⅱ型内生场热疗机(吉林迈达科技发展有限公司). 患者取平卧位, 结合患者CT明确的胃部原发病灶部位, 将病变部位置于热疗机两极板之间,调节上电极距离人体约3-6 cm, 将温度控制在40 ℃-43 ℃之间, 每次热疗时间为1 h.
1.2.3 疗效评定标准: 近期疗效评价: 采用CT或核磁共振观察病灶大小, 根据实体瘤疗效评价标准进行疗效评价[3]. 完全缓解(complete remission, CR): 可见病灶完全消失; 部分缓解(partial remission, PR): 瘤灶缩小>30%; 稳定(stable disease, SD): 非PR/PD; 肿瘤进展(progression disease, PD): 肿瘤继续增大>20%或出现新发病灶[4]. 以(CR+PR)计为治疗有效, 以(CR+PR+SD)为临床获益. 近期疗效评价在患者使用以上方案治疗4周期后进行或≥2周期不足4周期因各种原因退出治疗的患者. 远期疗效评价用CT或磁共振成像(magnetic resonance imaging, MRI)观察病灶大小, 随访患者至病情进展, 评价指标无进展生存(progression-free survival, PFS)时间.
1.2.4 治疗不良反应观察: 按照美国国家癌症研究所常见不良反应标准(National Cancer Institute Common Toxicity Criteria, NCI-CTC)3.0版进行评价[4].
统计学处理 采用SPSS13.0统计软件进行统计学分析, 计量资料采用方差分析, 计数资料采用χ2检验、非参数检验、Fisher确切概率法等, 检验水准α = 0.05, 采用Kaplan-Meier法绘制生存曲线. P<0.05为差异具有统计学意义.
90例患者有效率(CR+PR)3组比较差异无统计学意义(均P>0.05). 临床获益率(CR+PR+SD)比较, B、C组高于A组(P<0.05), B组与C组比较差异无统计学意义(P>0.05)(表2). 说明热疗增加替吉奥化疗的疗效, 且替吉奥联合热疗与卡培他滨联合热疗疗效无明显差异(表2).
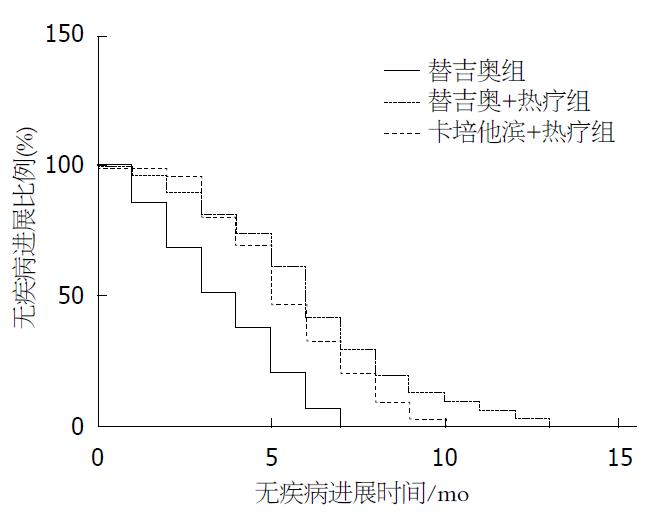
90例患者PFS (表3, 图1), A组PFS 1-7 mo, 中位时间3.8 mo(3.77 mo±1.85 mo), B组PFS 1-13 mo, 中位时间6.6 mo(6.30 mo±2.94 mo), C组PFS 2-12 mo, 中位时间5.8 mo(5.60 mo±2.08 mo). B、C组PFS较A组均延长, 差异有统计学意义(F = 9.367, P<0.000), B、C组差异无统计学意义. 说明替吉奥联合热疗远期疗效优于替吉奥单药, 替吉奥联合热疗与卡培他滨联合热疗远期疗效差异无统计学意义.
| 分组 | 分级 | 粒细胞减少 | 血红蛋白减少 | 血小板减少 | 恶心、呕吐 | 腹泻 | 肝功损伤 | 乏力 | 手足综合症 | 食欲减退 |
| A组 | ||||||||||
| 0 | 20(66.7) | 15(50.0) | 26(86.7) | 21(70.0) | 20(66.7) | 20(66.7) | 19(63.3) | 23(6.7) | 22(73.3) | |
| Ⅰ | 8(26.7) | 10(33.3) | 3(10) | 7(23.3) | 7(23.3) | 7(23.3) | 8(26.7) | 7(23.3) | 5(16.7) | |
| Ⅱ | 2(6.7) | 5(16.7) | 1(3.3) | 2(6.7) | 3(10.0) | 3(10.0) | 3(10.0) | 0(0.0) | 0(0.0) | |
| Ⅲ | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | |
| Ⅳ | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | |
| B组 | ||||||||||
| 0 | 18(60.0) | 17(56.7) | 27(90.0) | 22(73.3) | 23(76.7) | 19(63.3) | 20(66.7) | 17(56.7) | 21(70.0) | |
| Ⅰ | 10(33.3) | 11(36.6) | 3(10.0) | 6(20.0) | 6(20.0) | 8(26.7) | 7(23.3) | 11(36.7) | 6(20.0) | |
| Ⅱ | 2(6.7) | 2(6.7) | 0(0.0) | 2(6.7) | 2(6.7) | 3(10.0) | 3(10.0) | 2(6.67) | 3(10.0) | |
| Ⅲ | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | |
| Ⅳ | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | |
| C组 | ||||||||||
| 0 | 15(50.0) | 13(43.3) | 23(76.7) | 16(53.3) | 17(57.6) | 14(45.7) | 13(43.3) | 12(40.0) | 17(56.7) | |
| Ⅰ | 8(26.7) | 12(40.0) | 6(20.0) | 5(16.7) | 5(16.7) | 3(10.0) | 4(13.3) | 6(20.0) | 3(10.0) | |
| Ⅱ | 6(20.0) | 5(16.7) | 1(0.3) | 5(16.7) | 7(23.3) | 10(33.3) | 10(33.3) | 8(26.7) | 8(26.7) | |
| Ⅲ | 1(3.3) | 0(0.0) | 0(0.0) | 3(10.0) | 1(3.0) | 3(10.0) | 3(10.0) | 4(13.3) | 2(6.7) | |
| Ⅳ | 0(0.0) | 0(0.0) | 0(0.0) | 1(0.3) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) |
随着我国医疗水平的提高及人口的老龄化日益加重, 老年癌症患者逐年增多. 由于老年患者各种生理机能、心、肺、肝、肾等重要器官功能减退, 合并各种急慢性疾病, 导致晚期患者治疗方案选择成为临床难题, 而老年晚期胃癌患者的治疗方式选择更为棘手, 近年来寻找高效低毒的治疗方式是临床研究的热点. 由于胃癌病理分型复杂, 人群种族差异, 目前, 胃癌治疗并没有标准方案, 主要以奥沙利铂(顺铂)、紫杉醇、5-Fu等药物组成联合化疗方案. 老年胃癌晚期患者, 由于年龄较大, 疾病分期较晚, 体质差, 很难耐受FOLFOX、ECF等多药联合静脉化疗方案, 因此临床预后极差. S-1是由日本Taibo制药公司研制的口服抗癌药物, 是一种复方制剂, 其主要成分是替加氟(tegafur, FT)、吉美斯特(gimeracil, CDHP)和奥替拉西钾(potassium oxonate, OXO). 其中奥替拉西钾经口服吸收后对5-Fu的代谢酶具有选择性的抑制作用, 可在胃肠道内选择性地作用于乳清酸磷酸核糖转移酶, 阻断5-Fu磷酸化, 减轻5-Fu引起的胃肠道不良反应, 与同类药物如氟尿嘧啶、卡培他滨等药物相比, 不良反应明显减轻, 因此增加化疗耐受性[5]. 目前在日本替吉奥胶囊已成为治疗晚期胃肠道恶性肿瘤的一线药物. 本研究比较了替吉奥胶囊与卡培他滨的化疗不良反应, 证实替吉奥较卡培他滨相比乏力、腹泻、手足综合症等不良反应轻, 患者耐受性好, 与其他学者[6-10]报道一致, 可明显改善老年晚期胃癌患者的生活质量[11,12].
相对于手术治疗、化疗、放疗、生物治疗, 肿瘤热疗被称之为第5种肿瘤治疗方法, 是一种利用高频电磁波、超声波等物理能量使人体全身或局部加热, 利用正常组织和肿瘤组织对温度耐受力的差异, 达到杀灭肿瘤, 不损伤正常组织的治疗方法, 目前已有较多研究证实热疗与放疗或化疗联合治疗肿瘤有很好的协同作用[13-17], 化疗药物配合热疗有相乘或相加的作用[18], 同时热疗还能够增加肿瘤组织对化疗、放疗的敏感性[19-21]. 本研究中3组临床有效率(CR+PR)分别为替吉奥单药16.6%, 替吉奥联合热疗33.3%, 卡培他滨联合热疗30.0%, 后两组较接近, 虽然3组比较无统计学差异(可能与样本数较小有关), 但替吉奥联合热疗临床获益率(CR+PR+SD)为80%, 与Koizumi等[6]、Lee等[7]研究结果较一致, 明显高于替吉奥单药组, 显示热疗联合替吉奥治疗老年晚期胃癌明显增加临床获益率, 延长患者无进展生存时间.
因此热疗联合替吉奥化疗, 为老年晚期胃癌患者的治疗带来了希望. 目前在肿瘤综合治疗和个体化治疗的时代, 肿瘤热疗已成为继手术、放疗、化疗和生物治疗之后又一重要的肿瘤治疗手段[2,22].
胃癌是全世界最常见的恶性肿瘤之一, 居恶性肿瘤死因第4位, 居我国恶性肿瘤死亡率第3位, 全世界平均每年死亡约700000例, 严重危害人类健康. 且有半数以上患者在发现时已为肿瘤晚期,化疗是晚期胃癌的主要治疗方式之一. 老年晚期患者多不能耐受联合方案化疗, 导致病情迅速恶化.因此寻找高效低毒的治疗方式是临床研究的热点.
邹小明, 教授, 哈尔滨医科大学附属第二医院普外二科
本文研究的重点是针对老年晚期胃癌患者应用替吉奥联合热疗方案, 观察其有效性和不良反应, 目的在于提高老年晚期患者生活质量, 延长生存期.
Wust、李征等已证实热疗与放疗或化疗联合治疗肿瘤有很好的协同作用, 化疗药物配合热疗有相乘或相加的作用, 吕亚蕾、Hayashi 等研究表明热疗还能够增加肿瘤组织对化疗、放疗的敏感性.
本研究不同在于设计了三组, 对比了替吉奥单药、替吉奥联合热疗、卡培他滨联合热疗的疗效及不良反应, 在临床治疗方面提供了一定的临床依据.
研究证实热疗能增加替吉奥的化疗疗效,并且替吉奥联合热疗与卡培他滨联合热疗疗效无明显差异, 但替吉奥的不良反应较卡培他滨明显减轻, 替吉奥联合热疗对老年晚期胃癌患者临床获益较高.
本文选题贴近临床需要, 实验设计合理, 数据翔实, 可靠, 研究结果具有一定临床指导意义和研究价值.
编辑:郭鹏 电编:都珍珍
| 1. | Rosati G, Ferrara D, Manzione L. New perspectives in the treatment of advanced or metastatic gastric cancer. World J Gastroenterol. 2009;15:2689-2692. [PubMed] |
| 2. | NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). v.1 2013. fort Washington. PA: NCCN 2013; . |
| 6. | Koizumi W, Akiya T, Sato A, Sakuyama T, Sasaki E, Tomidokoro T, Hamada T, Fujimori M, Kikuchi Y, Shimada K. Phase II study of S-1 as first-line treatment for elderly patients over 75 years of age with advanced gastric cancer: the Tokyo Cooperative Oncology Group study. Cancer Chemother Pharmacol. 2010;65:1093-1099. [PubMed] |
| 7. | Lee JL, Kang YK, Kang HJ, Lee KH, Zang DY, Ryoo BY, Kim JG, Park SR, Kang WK, Shin DB. A randomised multicentre phase II trial of capecitabine vs S-1 as first-line treatment in elderly patients with metastatic or recurrent unresectable gastric cancer. Br J Cancer. 2008;99:584-590. [PubMed] [DOI] |
| 11. | Sakurai Y, Kamoshida S, Furuta S, Sunagawa R, Inaba K, Isogaki J, Komori Y, Uyama I, Tsutsumi Y. [Predictive value of orotate phosphoribosyltransferase in chemoresistant patients with gastric carcinoma who underwent S-1-based neoadjuvant/adjuvant chemotherapy]. Gan To Kagaku Ryoho. 2008;35:1147-1155. [PubMed] |
| 12. | Koizumi W, Tanabe S, Azuma M, Ishido K, Nishimura K, Sasaki T, Nakatani K, Higuchi K, Nakayama N, Katada C. Impacts of fluorouracil-metabolizing enzymes on the outcomes of patients treated with S-1 alone or S-1 plus cisplatin for first-line treatment of advanced gastric cancer. Int J Cancer. 2010;126:162-170. [PubMed] [DOI] |
| 17. | Wust P, Hildebrandt B, Sreenivasa G, Rau B, Gellermann J, Riess H, Felix R, Schlag PM. Hyperthermia in combined treatment of cancer. Lancet Oncol. 2002;3:487-497. [PubMed] |
| 18. | Westermann AM, Wiedemann GJ, Jager E, Jager D, Katschinski DM, Knuth A, Vörde Sive Vörding PZ, Van Dijk JD, Finet J, Neumann A. A Systemic Hyperthermia Oncologic Working Group trial. Ifosfamide, carboplatin, and etoposide combined with 41.8 degrees C whole-body hyperthermia for metastatic soft tissue sarcoma. Oncology. 2003;64:312-321. [PubMed] |
| 20. | 沈 清, 王 中奇, 张 丽曼, 黄 晓东. 热疗联合FOLFOX4方案治疗晚期胃癌疗效观察. 同济大学学报(医学版). 2012;33:94-97. |
| 21. | Hayashi S, Koshiba K, Hatashita M, Sato T, Jujo Y, Suzuki R, Tanaka Y, Shioura H. Thermosensitization and induction of apoptosis or cell-cycle arrest via the MAPK cascade by parthenolide, an NF-κB inhibitor, in human prostate cancer androgen-independent cell lines. Int J Mol Med. 2011;28:1033-1042. [PubMed] [DOI] |