修回日期: 2012-06-12
接受日期: 2012-06-20
在线出版日期: 2012-06-28
目的: 探讨功能性消化不良(functional dyspepsia, FD)症状与近端胃敏感性、容受性及顺应性的关系.
方法: 记录32例健康志愿者和59例FD患者的基本人口学特征和消化不良症状, 患者空腹行电子恒压器检查, 将前端带有气囊的双腔聚乙烯导管经口插入受试者胃内, 给予等压扩张, 检测指标包括近端胃敏感性、容受性及顺应性; 同样, 所有受试者第二天空腹行胃排空功能检查, 利用核素闪烁法测定胃的固体排空功能, 得出全胃排空标准曲线并计算全胃半排时间. 利用χ2和Logistic回归分析消化不良症状与近端胃功能关系.
结果: 44.07%的FD患者存在内脏敏感性增加, 内脏敏感性正常组和增加组之间胃半排时间无差异. 内脏敏感性增加的患者上腹痛症状发生率高于内脏敏感性正常的患者(P<0.01); 上腹痛症状是内脏敏感性增加的相关因素(OR = 4.430, P<0.05). 37.29%的FD患者存在近端胃容受性减低, 容受性正常组和减低组胃半排时间无差异. 近端胃容受性减低的患者早饱症状的发生率高于近端胃容受性正常的患者(P<0.05); 早饱症状是近端胃容受性减低的独立相关因素(OR = 3.231, P<0.05). 54.24%的FD患者存在顺应性减低, 顺应性正常组和减低组之间胃半排时间及消化不良症状发生率均无显著差异(P>0.05).
结论: FD患者的症状与近端胃功能障碍有关, 上腹痛症状提示内脏敏感性增加, 早饱症状提示近端胃容受性减低.
引文著录: 郭文娟, 张艳丽, 姚树坤, 尹立杰, 颜珏, 李红磊. 功能性消化不良症状和近端胃功能的关系. 世界华人消化杂志 2012; 20(18): 1623-1629
Revised: June 12, 2012
Accepted: June 20, 2012
Published online: June 28, 2012
AIM: To investigate the prevalence of impaired proximal stomach function and its relationship to symptoms in patients with functional dyspepsia (FD).
METHODS: Fifty-nine patients with FD and 32 healthy subjects (HS) were enrolled in this study. After an overnight fast of at least 12 h, a double-lumen polyvinyl tube with an adherent plastic bag that was finely folded was introduced through the patient's mouth. A gastric barostat was used to evaluate proximal stomach function (sensitivity, accommodation and compliance). After an overnight fast, gastric emptying was measured by single photon emission computerized tomography (SPECT). The gastric emptying curve was plotted to calculate the gastric emptying half-time. Individual dyspepsia symptom scores were obtained for all patients and their relationship with proximal stomach function was assessed. Logistic regression analysis and χ2 statistics were used to identify the association between proximal stomach function and symptoms.
RESULTS: Visceral hypersensitivity to gastric distention was found in 44.07% of the patients, and their gastric emptying half-time did not significantly differ from that of patients with normal sensitivity. Epigastric pain was significantly more prevalent in patients with visceral hypersensitivity than in those with normal sensitivity (P < 0.01). Epigastric pain was independently and significantly associated with hypersensitivity to gastric distention (OR = 4.430, P < 0.05). Impaired gastric accommodation was found in 37.29% of the patients, and their gastric emptying half-time did not differ from that of other patients. Impaired gastric accommodation to gastric distention was associated with a higher prevalence of early satiety (P < 0.05). The presence of early satiety was the only symptom that was independently associated with impaired accommodation to gastric distention (OR = 3.231, P < 0.05). Reduced compliance was found in 54.24% of the patients; however, no relationship was found between reduced compliance and dyspeptic symptoms.
CONCLUSION: Symptoms are associated with impaired proximal stomach function in patients with FD. Epigastric pain and early satiety can be used to predict the presence of hypersensitivity and impaired accommodation, respectively.
- Citation: Guo WJ, Zhang YL, Yao SK, Yin LJ, Yan J, Li HL. Relationship between symptoms and proximal stomach function in patients with functional dyspepsia. Shijie Huaren Xiaohua Zazhi 2012; 20(18): 1623-1629
- URL: https://www.wjgnet.com/1009-3079/full/v20/i18/1623.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i18.1623
功能性消化不良(functional dyspepsia, FD)是指存在一种或多种起源于胃或十二指肠区域的消化不良症状, 包括餐后饱胀不适、早饱、上腹痛或上腹部烧灼感等症状, 并且缺乏能够解释这些症状的任何器质性、系统性和代谢性疾病[1]. 研究显示该病患病率为16%, 约占消化科门诊量的40%[2,3], 尽管不影响患者的寿命, 但严重影响患者生活质量并消耗大量医疗资源[4]. 目前, 该病发病机制尚不清楚. 研究发现, FD患者近端胃内食物滞留[5], 表明FD患者存在近端胃功能异常, 然而国内鲜有相关报道, 因此本研究采用恒压器技术分别对FD患者与健康志愿者的近端胃功能(敏感性、容受性及顺应性)进行检测[6], 并进一步探讨消化不良症状与近端胃功能的关系.
以消化不良症状为主诉于2010-09/2012-01就诊于我院消化内科的FD患者59例纳入研究, 其中男20例, 平均年龄38.57岁±12.13岁. 入组患者均符合功能性消化不良罗马Ⅲ诊断标准[1]. 健康志愿者32名, 其中男15例, 平均年龄27.34岁±7.47岁, 均接受胃镜和生化检查以排除可能存在的消化系疾病. 研究方案经卫生部中日友好医院医学伦理委员会批准, 并取得研究对象的知情同意.
1.2.1 FD症状问卷: 记录入组FD患者的人口统计学特征和消化不良症状. 该问卷包括8个消化不良症状, 分别为餐后饱胀不适、早饱、上腹痛、上腹部烧灼感、上腹胀气、恶心、呕吐、嗳气, 并分别将每个症状的强度分为4个等级, 分别为: 无症状; 轻度, 症状轻微, 只有关注时才能感觉到; 中度, 症状尚能忍受, 部分影响日常生活工作; 重度, 症状难以忍受, 明显影响日常生活工作[7]. FD患者根据最近3个月的情况填写该问卷.
1.2.2 近端胃功能研究: 利用电子恒压器检测胃的敏感性、容受性及顺应性. 所有受试者(FD患者59例及健康志愿者32例)禁食水12 h后于清晨接受电子恒压器检查, 检测近端胃功能. 前端带有气囊的双腔聚乙烯导管(Davol, Cranston, Rhode Island)经口插入受试者胃内, 通过X线透视检查确定气囊的位置. 人工向气囊内缓慢充入300 mL气体使前端气囊扩张, 此时缓慢往回牵拉导管使得气囊位于食管下括约肌以下, 然后再将导管往前插入2 cm. 用医用胶布将导管固定于受试者下颌. 将气囊放气, 并将双腔聚乙烯导管与电子恒压器装置连接. 受试者取舒适座位, 双膝关节弯曲呈80度, 上身保持直立微微后仰10度, 该姿势可以减少外来的腹部压力[8,9]. 受试者适应15 min后开始检查, 以每2 min增加1 mmHg压力使前端气囊扩张, 当气囊内容积达到30 mL时, 记录此时相应压力为MDP(minimal distending pressure), 该压力可平衡腹内压. 然后, 在MDP压力基础上, 按照每次升高1 mmHg压力并持续2 min的模式行等压扩张, 电脑记录相应压力时的气囊内容积. 在检查者的指导下, 受试者在每次扩张结束时记录其腹内感觉. 检查的终点为气囊内容积达到1 200 mL或受试者难以耐受进一步的扩张[10]. 本实验记录3种感觉阈值: 初始感觉, 不适感觉及最大耐受感觉. 初始感觉是指气囊内压力或相应的容积引起受试者初次感觉到胃部扩张; 另外两种感觉分别指受试者感觉到不适或难以耐受进一步扩张时气囊内的压力或相应的容积. 对于上述感觉阈值的理解均在检查前由检查者向受试者解释清楚[11].
1.2.3 胃固体排空试验: 所有受试者禁食水12 h后于清晨行核素胃固态排空试验, 受试者摄入99mTc-DTPA标记的标准试餐(非油炸面饼95 g, 2 m Ci 99mTc-DTPA标记油煎鸡蛋65 g, 植物油10 g, 加水500 mL冲泡), 总热量2 092 kJ, 10 min内服完. 进食结束后使用SPECT装置(Millennium VG Hawkeye; GE, USA)采集图像, 2 h内每隔15 min采集1帧, 共9帧图像. 采集条件为140 keV, 窗宽50%, 放大倍数1.5, 低能通用型准直器. 两次图像采集间期, 允许受试者座位休息. 女性受试者应避开月经期, 以免激素水平对胃排空速度的干扰[12-14].
由一位核医学科医师和一位消化科医师协同分析、处理所采集的数据, 勾画出每帧图像的全胃部感兴趣区(region of interest, ROI)轮廓, 计算ROI放射性计数, 经放射性衰变和前后位校正后, 得到全胃排空标准曲线. 观察指标为全胃半排空时间(min)[15].
统计学处理 感觉阈值均以球囊内的压力值减去MDP表示. 以HS不适阈值压力的mean-2SD为界, 将FD患者分为内脏高敏感性组和正常组. 同样, 将FD患者分为容受性正常组和减低组. 利用线性回归计算出压力-容积曲线斜率为顺应性[16]. 根据HS顺应性95%CI的下限, 将FD患者分为顺应性正常组和顺应性减低组[8]. 应用SPSS13.0统计软件, 根据数据分布特征和分析需要分别采用χ2检验、t检验、非参数检验和Logistic回归分析. 所有结果以mean±SD表示, 显著性水平设定为0.05(双侧).
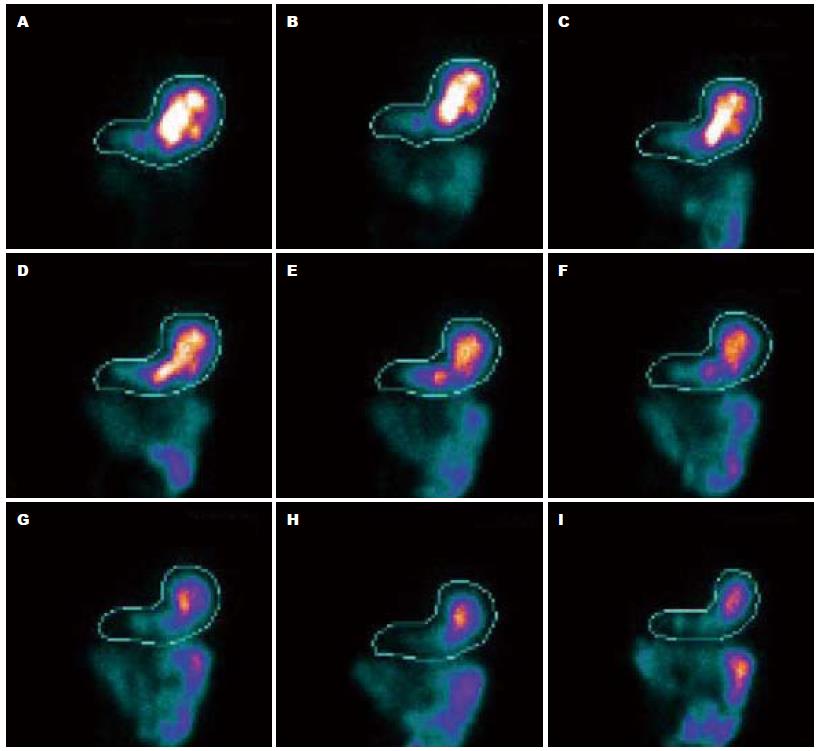
正常核素胃排空的动态图像如图1所示.
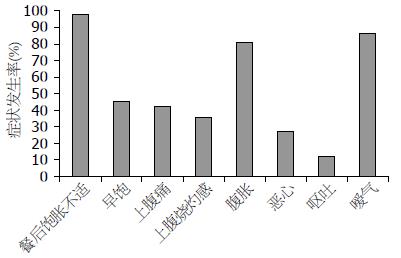
59例FD患者的平均年龄大于32例健康志愿者(38.58岁±12.12岁 vs 27.34岁±7.47岁, P<0.01), 但性别分布在两者之间无差异. FD患者各消化不良症状的发生率见图2. 餐后饱胀不适发生率最高(98.31%), 其次为嗳气(86.44%)与腹胀(81.36%), 恶心和呕吐症状的发生率最低, 分别为27.12%和11.86%.
2.2.1 FD患者及健康志愿者内脏胃敏感性的比较: FD患者与健康志愿者的MDP无差异(6.84 mmHg±1.77 mmHg vs 6.63 mmHg±2.52 mmHg, P>0.05). HS的初始感觉阈值和不适阈值分别为5.28 mmHg±1.91 mmHg和8.09 mmHg±2.31 mmHg. FD患者的初始感觉阈值和不适阈值分别为2.09 mmHg±1.40 mmHg和4.17 mmHg±1.54 mmHg. 统计学分析显示: FD患者的初始感觉阈值和不适阈值均低于健康志愿者(P<0.01). 以健康志愿者不适阈值的mean-2SD(3.47 mmHg)为正常值下限, 则FD患者中有26人(44.07%)存在内脏敏感性增高.
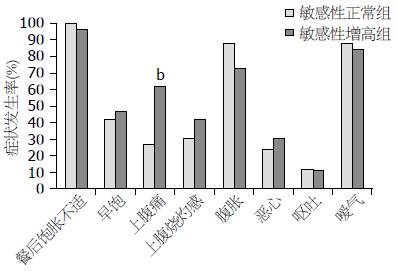
2.2.2 消化不良症状及人口学特征与内脏敏感性的关系: FD患者内脏敏感性增高组和正常组之间, 性别分布、BMI及胃半排时间无统计学差异. 但是内脏敏感性增高的FD患者年龄较正常组低(表1). 内脏敏感性增高组上腹痛症状的发生率高于正常组(16/26 vs 9/33, P<0.01), 其他消化不良症状在两组之间无统计学差异(图3). 以内脏敏感性为结局变量, 以年龄、性别、BMI、胃半排时间及是否存在8个消化不良症状为协变量, 利用Logistic分析发现: 上腹痛(OR = 4.430; 95%CI: 1.345-14.590, P<0.05)和年龄(OR = 0.940; 95%CI: 0.891-0.992, P<0.05)是内脏敏感性增高的相关因素, 其他消化不良症状及人口学特征均未进入最终的回归模型.
| 敏感性正常组(n = 33) | 敏感性增高组(n = 26) | |
| 年龄(岁) | 42.06±12.73 | 34.15±9.88a |
| 性别(男, n) | 10 | 10 |
| BMI(kg/m2) | 21.73 | 21.26 |
| 胃半排时间T1/2(min) | 117.54±40.79 | 123.63±40.08 |
2.3.1 FD患者及健康志愿者近端胃容受性的比较: 健康志愿者的初始感觉容积和不适容积分别为295.57 mL±94.60 mL和514.07 mL±133.9 mL. FD患者的初始感觉容积和不适容积分别为140.70 mL±76.42 mL和265.45 mL±124.16 mL. 统计学分析显示: FD患者的初始感觉容积和不适容积均低于健康志愿者(P<0.01). 以健康志愿者不适容积的mean-2SD(246.16 mL)为正常值下限, 则FD患者中有22人(37.29%)存在容受性减低.
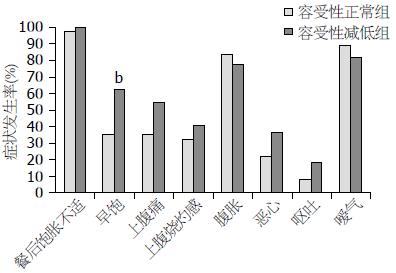
2.3.2 消化不良症状及人口学特征与近端胃容受性的关系: 在近端胃容受性正常组和减低组之间, 年龄、性别分布、BMI及胃半排时间均无统计学差异(表2). 近端胃容受性减低组早饱症状发生率高于正常组(14/22 vs 13/37, P<0.05), 而其他消化不良症状的发生率在两组之间无统计学差异(图4). 以胃容受性为结局变量, 以年龄、性别、BMI、胃半排时及是否存在8个消化不良症状为协变量, 利用Logistic分析证实只有早饱症状(OR = 3.231; 95%CI: 1.075-9.706, P<0.05)是近端胃容受性减低的独立相关因素.
| 容受性正常组(n = 37) | 容受性减低组(n = 22) | |
| 年龄(岁) | 40.22±12.92 | 35.82±10.36 |
| 性别(男, n) | 13 | 7 |
| BMI(kg/m2) | 21.81±2.51 | 21.04±3.27 |
| 胃半排时间T1/2(min) | 114.82±37.87 | 129.31±43.32 |
2.4.1 FD患者及健康志愿者近端胃顺应性的比较: 健康志愿者和FD患者的顺应性分别为59.01 mL/mmHg±18.78 mL/mmHg和49.95 mL/mmHg±20.58 mL/mmHg, 两者之间存在统计学差异(P<0.05). 以健康志愿者胃顺应性95%CI的下限(52.24 mL/mmHg)为正常值下限, 则32例FD患者(54.24%)存在顺应性减低.
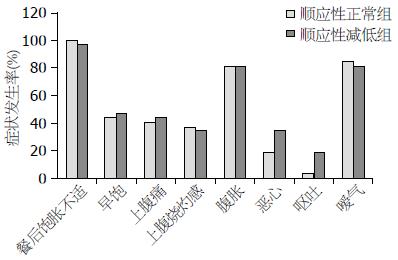
2.4.2 消化不良症状及人口学特征与近端胃顺应性的关系: 消化不良症状与近端胃顺应性关系的研究显示: 消化不良症状的发生率在顺应性正常组和减低组之间均无统计学差异(图5). 人口学特征及胃半排时间在两组之间未见显著统计学差异(表3).
| 顺应性正常组(n = 27) | 顺应性减低组(n = 32) | |
| 年龄(岁) | 40.11±12.33 | 37.28±11.99 |
| 性别(男, n) | 10 | 10 |
| BMI(kg/m2) | 22.06±2.93 | 21.07±2.68 |
| 胃半排时间T1/2(min) | 115.49±37.89 | 124.21±42.31 |
FD是最常见的功能性胃肠病, 由于其病因复杂, 发病机制尚未明确. 目前FD的治疗多为经验性治疗, 如促进胃动力、抑制胃酸分泌及消化酶促进消化等[17], 导致该病的疗效差及停药后易复发, 严重影响患者生活质量, 并造成医疗资源的严重浪费[18,19]. 深入研究FD症状与病理生理机制之间的相关性, 有望通过症状预测其发病机制, 具有重要的临床意义. 他使得针对病理生理机制的治疗措施简化为针对相关症状的治疗, 从而提高FD的临床疗效.
电子恒压器检查出现于20世纪80年代中期, 其通过研究敏感性、容受性及顺应性来探讨消化系的生理及病理生理机制, 目前已经广泛应用于临床研究[20]. 由于需要插入前端带有气囊的导管及检查过程的耗时, 有研究认为恒压器检查改变了胃的正常生理功能, 因此, 质疑该检查的可重复性[19]. Sarnelli等[6]利用恒压器检查健康志愿者和功能性消化不良患者的初始感觉阈、不适阈值及胃容受性, 发现同日及不同日的检查结果具有高度的可重复性. 同样, Jiande等的动物实验不仅证实恒压器检测胃的容受性具有可重复性, 同时也证实恒压器在检测胃的张力及顺应性方面也有可重复性. 同时, 该实验提示两次检查的差异可能是由于检查时胃处于移行性运动复合波的不同时期[21]. Talley等[22]对414例患者进行恒压器检查近端胃功能, 发现98%患者耐受良好, 在技术上94%满足条件(6%是由于气囊漏气或容积过低). 因此, 恒压器仍不失为评价胃敏感性、容受性及顺应性的"金标准"检测方法.
内脏敏感性与不同的消化不良症状是否存在相关性, 国内鲜有研究报道. 国外有研究显示进餐相关的FD患者存在不适阈值减低和近端胃敏感性增高[23,24]. 近端胃敏感性增高与上腹痛、嗳气、体质量减轻等相关[16]. 也有研究则未发现消化不良症状与内脏敏感性相关[25]. 我们的研究发现: FD患者不适阈值较健康志愿者低, 约44.07%的FD患者存在内脏敏感性增高; 并且上腹痛症状与内脏敏感性增高有关. 同时, 我们发现年龄与内脏敏感性增加呈负相关. Van Oudenhove等[26]报道过相似的研究结果, 其研究认为年龄、性虐待史和躯体化障碍均与内脏敏感性增加有关, 但对于年龄与内脏敏感性相关的机制有待于进一步的研究. 在我们的研究中未发现内脏敏感性与胃排空相关, 这与韩国的研究结果一致[27]. 内脏高敏感性与胃壁机械受体敏感性升高有关, Tack等[28,29]的研究中, 15名恒压器检查证实内脏敏感性增高的FD患者, 给予胃底松弛药舒马曲坛和可乐定治疗后, 恒压器复查胃对球囊扩张的敏感性, 结果显示近端胃的敏感性显著下降. 因此, 胃肠道机械受体在消化不良症状的产生中可能有重要意义.
容受性是指胃在一定时间内所能容纳食物的能力, 近端胃内压力没有明显变化而体积增大以容纳摄入的食物[20,30-32]. 有研究显示FD患者容受性减低与早饱、餐后饱胀不适有关[33]. 但Boeckxstaens等[34]研究未发现餐后消化不良症状与胃容受性减低有关. 我们的研究结果显示37.29%的FD患者存在容受性减低, 并且容受性减低与早饱有关, 这与Tack的研究结果一致. 但是我们的研究未发现容受性减低与餐后饱胀不适相关, 这可能是与本研究中FD患者样本量较小和餐后饱胀不适的发生率较高有关. 因此, FD患者早饱症状提示近端胃容受性的减低. 本研究进一步比较容受性与胃排空的关系, 结果未发现两者之间存在相关性. 容受性发生改变的原因尚不清楚, 可能与感觉神经元、迷走-迷走反射及近端胃的内在抑制神经元、平滑肌功能异常有关. 有研究发现在急性发病或感染后的功能性消化不良患者中, 容受性异常的比例显著增多[35]. 另外, 心理社会因素, 尤其是焦虑也影响胃的容受性[36].
与Rhee等[25]的研究结果一致, 胃的顺应性与消化不良症状之间未发现相关性. 但我们的研究发现, FD患者胃顺应性较健康志愿者减低, 这提示FD患者近端胃壁弹力发生变化, 对于胃壁顺应性改变的潜在机制需要进一步的研究.
总之, FD患者存在内脏敏感性增加, 容受性及顺应性减低; 并且, 上腹痛与近端胃敏感性增加有关, 早饱与近端胃容受性减低有关. 我们的结果进一步证实FD是一种异质性疾病, 不同的症状与不同的病理生理机制相关. 上腹痛和早饱症状分别提示内脏敏感性增加和容受性减低. 因此, 通过降低上腹痛患者内脏敏感性和增加早饱患者的容受性, 有望提高FD的临床疗效.
功能性消化不良(FD)是一种异质性疾病, 其病理生理机制与多种因素有关, 但目前研究仍不清楚. 阐明消化不良症状与机制的关系, 通过症状预测其潜在发病机制, 可以使该病的治疗更有针对性.
王小众, 教授, 福建医科大学附属协和医院消化内科
研究发现, FD患者近端胃内食物滞留, 表明FD患者存在近端胃功能异常, 然而国内鲜有相关报道.
Tack等利用恒压器技术研究160例功能性消化不良患者和80例健康志愿者的近端胃功能, 结果发现内脏敏感性增高的FD, 其腹痛、嗳气、体质量减轻的发生率高于内脏敏感性正常组.
本研究采用恒压器技术分别对FD患者与健康志愿者的近端胃功能(敏感性、容受性及顺应性)进行检测, 并进一步探讨消化不良症状与近端胃功能的关系.
容受性: 近端胃在一定时间内所能容纳食物的能力, 近端胃内压力没有明显变化而体积增大以容纳摄入的食物.
本文分析和探讨了功能性消化不良症状与近端胃敏感性、容受性及顺应性的关系, 为该病的临床治疗提供了理论基础和指导作用.
编辑: 李军亮 电编:闫晋利
| 1. | Tack J, Talley NJ, Camilleri M, Holtmann G, Hu P, Malagelada JR, Stanghellini V. Functional gastroduodenal disorders. Gastroenterology. 2006;130:1466-1479. [PubMed] [DOI] |
| 2. | Aro P, Talley NJ, Agréus L, Johansson SE, Bolling-Sternevald E, Storskrubb T, Ronkainen J. Functional dyspepsia impairs quality of life in the adult population. Aliment Pharmacol Ther. 2011;33:1215-1224. [PubMed] [DOI] |
| 3. | Okumura T, Tanno S, Ohhira M, Tanno S. Prevalence of functional dyspepsia in an outpatient clinic with primary care physicians in Japan. J Gastroenterol. 2010;45:187-194. [PubMed] [DOI] |
| 4. | Brook RA, Kleinman NL, Choung RS, Melkonian AK, Smeeding JE, Talley NJ. Functional dyspepsia impacts absenteeism and direct and indirect costs. Clin Gastroenterol Hepatol. 2010;8:498-503. [PubMed] [DOI] |
| 5. | Gonlachanvit S, Maurer AH, Fisher RS, Parkman HP. Regional gastric emptying abnormalities in functional dyspepsia and gastro-oesophageal reflux disease. Neurogastroenterol Motil. 2006;18:894-904. [PubMed] [DOI] |
| 6. | Sarnelli G, Vos R, Cuomo R, Janssens J, Tack J. Reproducibility of gastric barostat studies in healthy controls and in dyspeptic patients. Am J Gastroenterol. 2001;96:1047-1053. [PubMed] [DOI] |
| 7. | Sarnelli G, Caenepeel P, Geypens B, Janssens J, Tack J. Symptoms associated with impaired gastric emptying of solids and liquids in functional dyspepsia. Am J Gastroenterol. 2003;98:783-788. [PubMed] [DOI] |
| 8. | Tack J, Piessevaux H, Coulie B, Caenepeel P, Janssens J. Role of impaired gastric accommodation to a meal in functional dyspepsia. Gastroenterology. 1998;115:1346-1352. [PubMed] [DOI] |
| 9. | Van Oudenhove L, Vandenberghe J, Geeraerts B, Vos R, Persoons P, Demyttenaere K, Fischler B, Tack J. Relationship between anxiety and gastric sensorimotor function in functional dyspepsia. Psychosom Med. 2007;69:455-463. [PubMed] [DOI] |
| 10. | Tack J, Janssen P, Bisschops R, Vos R, Phillips T, Tougas G. Influence of tegaserod on proximal gastric tone and on the perception of gastric distention in functional dyspepsia. Neurogastroenterol Motil. 2011;23:e32-e39. [PubMed] [DOI] |
| 11. | Hou XH, Li Q, Zhu L, Xie X, Chen JD. Correlation of gastric liquid emptying with various thresholds of sensation in healthy controls and patients with functional dyspepsia. Dig Dis Sci. 2004;49:188-195. [PubMed] [DOI] |
| 12. | Zhang H, Xu X, Wang Z, Li C, Ke M. Correlation between gastric myoelectrical activity recorded by multi-channel electrogastrography and gastric emptying in patients with functional dyspepsia. Scand J Gastroenterol. 2006;41:797-804. [PubMed] [DOI] |
| 13. | Yang M, Fang DC, Li QW, Sun NX, Long QL, Sui JF, Gan L. Effects of gastric pacing on gastric emptying and plasma motilin. World J Gastroenterol. 2004;10:419-423. [PubMed] |
| 14. | Foxx-Orenstein A, Camilleri M, Stephens D, Burton D. Effect of a somatostatin analogue on gastric motor and sensory functions in healthy humans. Gut. 2003;52:1555-1561. [PubMed] [DOI] |
| 15. | Sachdeva P, Malhotra N, Pathikonda M, Khayyam U, Fisher RS, Maurer AH, Parkman HP. Gastric emptying of solids and liquids for evaluation for gastroparesis. Dig Dis Sci. 2011;56:1138-1146. [PubMed] [DOI] |
| 16. | Tack J, Caenepeel P, Fischler B, Piessevaux H, Janssens J. Symptoms associated with hypersensitivity to gastric distention in functional dyspepsia. Gastroenterology. 2001;121:526-535. [PubMed] [DOI] |
| 18. | Tack J, Bisschops R, Sarnelli G. Pathophysiology and treatment of functional dyspepsia. Gastroenterology. 2004;127:1239-1255. [PubMed] [DOI] |
| 19. | Miwa H, Watari J, Fukui H, Oshima T, Tomita T, Sakurai J, Kondo T, Matsumoto T. Current understanding of pathogenesis of functional dyspepsia. J Gastroenterol Hepatol. 2011;26 Suppl 3:53-60. [PubMed] [DOI] |
| 20. | Kindt S, Tack J. Impaired gastric accommodation and its role in dyspepsia. Gut. 2006;55:1685-1691. [PubMed] [DOI] |
| 21. | Xing JH, Chen JD. Reproducibility of gastric tone, compliance and gastric accommodation assessed with barostat in conscious dogs. Neurogastroenterol Motil. 2005;17:83-88. [PubMed] [DOI] |
| 22. | Talley NJ, Locke GR, Lahr BD, Zinsmeister AR, Tougas G, Ligozio G, Rojavin MA, Tack J. Functional dyspepsia, delayed gastric emptying, and impaired quality of life. Gut. 2006;55:933-939. [PubMed] [DOI] |
| 23. | Coffin B, Azpiroz F, Guarner F, Malagelada JR. Selective gastric hypersensitivity and reflex hyporeactivity in functional dyspepsia. Gastroenterology. 1994;107:1345-1351. [PubMed] |
| 24. | Bisschops R, Karamanolis G, Arts J, Caenepeel P, Verbeke K, Janssens J, Tack J. Relationship between symptoms and ingestion of a meal in functional dyspepsia. Gut. 2008;57:1495-1503. [PubMed] [DOI] |
| 25. | Rhee PL, Kim YH, Son HJ, Kim JJ, Koh KC, Paik SW, Rhee JC, Choi KW. Evaluation of individual symptoms cannot predict presence of gastric hypersensitivity in functional dyspepsia. Dig Dis Sci. 2000;45:1680-1684. [PubMed] [DOI] |
| 26. | Van Oudenhove L, Vandenberghe J, Vos R, Fischler B, Demyttenaere K, Tack J. Abuse history, depression, and somatization are associated with gastric sensitivity and gastric emptying in functional dyspepsia. Psychosom Med. 2011;73:648-655. [PubMed] [DOI] |
| 27. | Rhee PL, Kim YH, Son HJ, Kim JJ, Koh KC, Paik SW, Rhee JC, Choi KW. The etiologic role of gastric hypersensitivity in functional dyspepsia in Korea. J Clin Gastroenterol. 1999;29:332-335. [PubMed] [DOI] |
| 28. | Tack J, Caenepeel P, Corsetti M, Janssens J. Role of tension receptors in dyspeptic patients with hypersensitivity to gastric distention. Gastroenterology. 2004;127:1058-1066. [PubMed] [DOI] |
| 29. | Piessevaux H, Tack J, Wilmer A, Coulie B, Geubel A, Janssens J. Perception of changes in wall tension of the proximal stomach in humans. Gut. 2001;49:203-208. [PubMed] [DOI] |
| 30. | Gilja OH, Lunding J, Hausken T, Gregersen H. Gastric accommodation assessed by ultrasonography. World J Gastroenterol. 2006;12:2825-2829. [PubMed] |
| 31. | Choung RS, Talley NJ. Novel mechanisms in functional dyspepsia. World J Gastroenterol. 2006;12:673-677. [PubMed] |
| 32. | Fukudo S, Kuwano H, Miwa H. Management and pathophysiology of functional gastrointestinal disorders. Digestion. 2012;85:85-89. [PubMed] [DOI] |
| 33. | Kindt S, Dubois D, Van Oudenhove L, Caenepeel P, Arts J, Bisschops R, Tack J. Relationship between symptom pattern, assessed by the PAGI-SYM questionnaire, and gastric sensorimotor dysfunction in functional dyspepsia. Neurogastroenterol Motil. 2009;21:1183-e105. [PubMed] [DOI] |
| 34. | Boeckxstaens GE, Hirsch DP, Kuiken SD, Heisterkamp SH, Tytgat GN. The proximal stomach and postprandial symptoms in functional dyspeptics. Am J Gastroenterol. 2002;97:40-48. [PubMed] [DOI] |
| 35. | Tack J, Demedts I, Dehondt G, Caenepeel P, Fischler B, Zandecki M, Janssens J. Clinical and pathophysiological characteristics of acute-onset functional dyspepsia. Gastroenterology. 2002;122:1738-1747. [PubMed] [DOI] |
| 36. | Geeraerts B, Vandenberghe J, Van Oudenhove L, Gregory LJ, Aziz Q, Dupont P, Demyttenaere K, Janssens J, Tack J. Influence of experimentally induced anxiety on gastric sensorimotor function in humans. Gastroenterology. 2005;129:1437-1444. [PubMed] [DOI] |