修回日期: 2025-06-26
接受日期: 2025-08-18
在线出版日期: 2025-08-28
结直肠癌(colorectal cancer, CRC)预后评估需有效的生物标志物. 鉴于现有炎症指标预测效能存在局限, 本研究假设术前改良中性粒细胞血小板评分(modified neutrophil-platelet score, MNPs)可独立预测CRC患者总生存期(overall survival, OS)和无复发生存期(recurrence free survival, RFS).
探究术前MNPs与CRC患者预后的预测价值.
回顾性分析哈尔滨医科大学附属第二医院普外科2016-10/2018-12的503例CRC患者的临床资料, 随访5年, 记录CRC患者的预后情况. 分析不同MNPs与OS和RFS的关联. 采用Kaplan Meier法绘制生存曲线, Cox比例风险回归模型评价CRC患者预后的影响因素, 并计算C指数评估MNPs与其他炎症指标的预测效能差异.
共503例CRC患者纳入本研究. 单因素Cox回归分析结果显示, MNPs与OS相关, MNPs评分越高死亡风险越高; MNPs与RFS相关, MNPs评分越高复发风险越高. 多因素分析表明, MNPs为OS、RFS独立预测因子. C指数表明, MNPs对CRC患者的预后具有较好的预测能力.
MNPs是预测CRC患者预后的独立因素, 临床医师可通过检测术前MNPs为早期恶性肿瘤高危和复发转移患者提供更为个性化、精准的治疗方案.
核心提要: 本研究首次探索了术前中性粒细胞血小板评分(modified neutrophil-platelet score, MNPs)在结直肠患者预后中的临床价值. 我们的研究结果表明, 术前MNPs是结直肠癌(colorectal cancer, CRC)的独立预后因素, 高MNPs与CRC患者低总生存期和低无复发生存期相关. 而在临床预测结果方面, MNPs较NLR、PLR、SIR来说, 其预测价值更优.
引文著录: 唐研, 宗柏安, 张好刚. MNPs对结直肠癌患者总生存期及无复发生存期的预测效能. 世界华人消化杂志 2025; 33(8): 674-684
Revised: June 26, 2025
Accepted: August 18, 2025
Published online: August 28, 2025
Effective biomarkers are needed for the prognosis assessment of colorectal cancer (CRC). Given the limitations of existing inflammatory markers in predictive efficacy, we hypothesized that preoperative modified neutrophil-platelet score (MNPS) can independently predict overall survival (OS) and recurrence-free survival (RFS) in CRC patients.
To explore the value of preoperative MNPS for predicting the prognosis of patients with CRC.
A retrospective analysis was conducted on the clinical data of 503 CRC patients admitted to the Department of General Surgery of the Second Affiliated Hospital of Harbin Medical University between October 2016 and December 2018. These patients were followed up for a period of 5 years, and their prognoses were recorded. The association of MNPS with OS and RFS was then analyzed. The Kaplan-Meier method was used to plot survival curves, Cox proportional hazards regression model was used to evaluate the influencing factors of prognosis in CRC patients, and the C-index was calculated to assess the difference in predictive efficacy between MNPS and other inflammatory indicators.
A total of 503 patients with CRC were included in this study. The results of univariate Cox regression analysis showed that MNPS was associated with both OS and RFS, with higher MNPS indicating a higher risk of mortality and recurrence. Multivariate analysis revealed that MNPS served as an independent predictor of both OS and RFS. The C-index indicated that MNPS demonstrated superior predictive efficacy for the prognosis of CRC patients.
MNPS is an independent factor for predicting the prognosis of CRC patients. Clinicians can provide more personalized and accurate treatment plans for early-stage high-risk and recurrent metastatic patients by detecting preoperative MNPS.
- Citation: Tang Y, Zong BA, Zhang HG. Predictive efficacy of modified neutrophil-platelet score for overall survival and recurrence free survival in colorectal cancer patients. Shijie Huaren Xiaohua Zazhi 2025; 33(8): 674-684
- URL: https://www.wjgnet.com/1009-3079/full/v33/i8/674.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v33.i8.674
结直肠癌(colorectal cancer, CRC)是我国最常见的恶性肿瘤之一, 严重危害人类生命健康. 统计数据显示, 在中国, 2022年CRC发病率占恶性肿瘤第二位, 新发CRC病例约51.71万例; 死亡率居第四位, 每年约24万人死亡[1]. 尽管CRC患者的诊疗方法不断进步, 包括术前新辅助化疗、手术切除、术后辅助疗法、靶向药物疗法、免疫疗法以及针对晚期患者的姑息治疗. 但CRC的发生率和死亡率仍不断在上升, 尤其是术后复发和远处转移的CRC患者[2]. 在55岁以下的人群中, 尤其是年轻群体, 其发病率增加了近50%[3]. 目前已经发现了许多关于CRC患者的预后和预测标志物, 如微卫星不稳定性、基因突变和TNM分期等, 但这些标志物需要专门的实验室装置, 价格高昂. 随着CRC筛查不断改进, 研究者致力于开发可用于预测癌症不良预后的生物标志物. 这些生物标志物从常规的血液检测即可获得, 更容易被大多数患者接受[4].
早有研究发现全身炎症反应在恶性肿瘤的进展和转移中至关重要. 由于炎症指标更加容易获得、价格低廉, 而且在临床阶段具有更多的潜力, 越来越多的研究者致力于研究新的生物标志物在恶性肿瘤的诊断和预后方面的临床价值[5]. 近年来, 研究者发现了多种新的生物标志物, 如中性粒细胞、血小板、淋巴细胞、C反应蛋白(C-reactive protein, CRP)、中性粒细胞与淋巴细胞比值(neutrophil-to-lymphocyte ratio, NLR)、淋巴细胞与单核细胞比值(monocyte-to-lymphocyte ratio, LMR)、血小板与淋巴细胞比值(platelet-lymphocyte ratio, PLR)和中性粒细胞血小板评分(neutrophil-to-platelet ratio, NPS)等炎症指标[6]. 这些炎症标志物被广泛应用于临床, 且发现与传统生物标志物相比, NPS、NLR、PLR、CRP等指标能够更好的反应机体的炎症状态, 评估肿瘤患者的生存率, 指导治疗[7]. 改良中性粒细胞血小板评分(modified neutrophil-platelet score, MNPs)是Otani等[8]发现的一种基于中性粒细胞和血小板评估患者预后的生物标志物. 通过回顾性选取168例接受胃癌根治术的患者, 发现MNPs是胃癌患者总生存期(overall survival, OS)和无复发生存期(recurrence free survival, RFS)的独立预后因素. 这提示MNPs可作为胃癌治疗的参考指标, 但MNPs在其他恶性肿瘤的临床研究仍相对较少, 需要进一步验证其在其他肿瘤中的预测价值.
在本研究中, 我们通过分析MNPs与CRC患者的OS和RFS的相关性, 评估其在CRC患者中的的预后价值, 为指导CRC患者的治疗策略提供新的研究证据.
本研究回顾性选取了2016-2018于哈尔滨医科大学附属第二医院普外科行CRC根治手术的503例患者, 其中男性319例, 女性184例, 中位年龄为61岁. 该研究获得了所有患者的知情同意书, 并取得了哈尔滨医科大学附属第二医院医学伦理委员会的批准(YJSKY2024-267). 纳入标准: (1)年龄在18岁以上的个体; (2)术后病理证实为CRC; (3)入组前无放化疗等抗肿瘤治疗史; (4)术前一周内血液实验指标可用; (5)临床资料和随访资料完整; (6)术前无细菌、病毒、真菌等病原体感染、无发热症状等可能影响血常规计数的因素. 排除标准(排除0人): (1)心、肾、肝等脏器发生严重病变; (2)合并重大感染、免疫系统疾病或恶性肿瘤; (3)病灶远处转移, 无法切除; (4)患有血液系统疾病或自身免疫性疾病; (5)临床资料不全; (6)术前存在明确活动性感染或炎症性疾病. "无感染症状"的诊断基于以下综合评估: (1)临床症状与体征, 记录并排除术前存在发热、寒战、明确的局部感染症状(如咳嗽咳痰、伤口红肿热痛等)的患者; (2)实验室指标, 排除术前CRP水平显著升高且无法用非感染性原因(如近期创伤、手术等)合理解释的患者; 影像学检查, 排除术前影像学(如胸片/CT)提示明确活动性感染灶. 满足以上(1)-(2)中任何一条给予排除. 通过医院电子病历系统回顾性收集了患者的临床资料, 包括性别、年龄; 术前1周血液学参数, 包括中性粒细胞计数、血小板计数、CEA、CA199、淋巴细胞计数、单核细胞计数; 术后病理, 包括肿瘤大小、肿瘤部位、分化程度、病理形态、TNM分期、淋巴结侵犯数目、是否有神经侵犯、血管癌栓、淋巴管癌栓. MNPs的计算方法为中性粒细胞计数≤4170/μL和血小板计数≤26.6×104/μL的患者为0分, 中性粒细胞计数>4170/μL或血小板计数>26.6×104/μL的患者为1分, 中性粒细胞计数>4170/μL和血小板计数>26.6×104/μL的患者为2分[9]; NLR = 中性粒细胞计数/淋巴细胞计数; PLR = 血小板计数/淋巴细胞计数; SII = 血小板计数×中性粒细胞计数/淋巴细胞计数; SIRI = 单核细胞计数×中性粒细胞计数/淋巴细胞计数.
随访: 患者的随访信息通过电话或门诊复查及再次住院情况获得. 共随访5年, 该随访在患者死亡或2024-12结束. 主要终点为OS和RFS. OS定义为手术至任何原因死亡之间的时间. RFS定义为手术至复发之间的时间.
对于连续性定量资料, 如符合正态分布, 采用均数±标准差进行描述, 多组间比较采用单因素方差分析; 如不符合正态分布, 则采用中位数[P25,P75]进行统计描述, 组间比较采用秩和检验; 对于计数资料, 采用例数(%)进行描述, 组间比较采用卡方检验或Fisher精确概率法. 对于不同分组下的OS/RFS差异, 绘制KM曲线进行分析, 并进行Logrank检验比较组间差异. 并通过单变量和多变量Cox回归探索MNPs评分与OS/RFS之间的关联. 并计算C指数评估MNPs与其他炎症指标的预测效能差异. 所有统计学分析及相关图表绘制均在R语言(4.4.1版本)中进行, 双侧P<0.05被认为有统计学意义. 患者的MNPs值根据术前血细胞分析结果计算得出(公式如前所述). 本研究采用Okugawa等[9]最初在胃癌患者中建立并验证的临界值, 选择该临界值是基于其在预测胃癌预后方面的潜力.考虑到本研究目的是评估术前MNPs在CRC中的预测价值并与现有的生物标志物(如NLR、PLR等)进行比较, 而非重新定义最优截断点, 我们未在本队列中进行ROC曲线分析以确定CRC特异性的最佳截断值.
本研究共纳入503例研究对象, 中位年龄为61岁, 男性319例, 中位随访时间为75.5 mo(95%CI: 75.2 to 77.1), TNM1、2、3分别占15.7%、45.5%、38.8%, 分化程度以中分化为主401例(79.7%)、低分化76例(15.1%)、高分化26例(5.2%), 其他基线信息详见下表. 根据MNPs评分分为三组(0分: n = 275; 1分: n = 156; 2分: n = 72), 三组性别、年龄、 身体质量指数、肿瘤部位、临床分期、N、M等资料差异无统计学意义, 见表1.
| 变量 | 总计(n = 503) | 0(n = 275) | 1(n = 156) | 2(n = 72) | P值 |
| 癌胚抗原中位数(Q1,Q3) | 3.30(2.00, 7.62) | 3.15(1.92, 5.99) | 3.43(2.01, 8.08) | 4.56(2.42, 10.03) | 0.021 |
| 碳水化合物抗原199中位数(Q1,Q3) | 7.45(3.74, 17.83) | 6.72(3.86, 14.79) | 9.03(3.58, 25.75) | 8.70(3.23, 25.59) | 0.285 |
| 血小板与淋巴细胞比值中位数(Q1,Q3) | 132.82(100.97, 176.39) | 117.70(91.65, 148.02) | 150.48(113.38, 208.08) | 191.49(139.74, 225.44) | <0.001 |
| 中性粒细胞与淋巴细胞比值中位数(Q1,Q3) | 1.86(1.45, 2.64) | 1.73(1.39, 2.26) | 1.87(1.44, 2.64) | 3.08(2.40, 4.32) | <0.001 |
| 全身炎症反应指数中位数(Q1,Q3) | 0.67(0.47, 1.01) | 0.57(0.43, 0.83) | 0.68(0.45, 1.03) | 1.24(0.93, 2.24) | <0.001 |
| 全身免疫炎症指数中位数(Q1,Q3) | 249.85(154.01, 446.61) | 198.31(132.60, 313.92) | 269.21(185.53, 473.09) | 585.82(351.11, 901.23) | <0.001 |
| 中性粒细胞中位数(Q1,Q3) | 3.51(3.04, 4.14) | 3.31(2.88, 3.64) | 3.66(3.02, 4.72) | 5.62(4.83, 7.04) | <0.001 |
| 血小板中位数(Q1,Q3) | 245.00(207.00, 288.50) | 218.00(191.00, 241.00) | 286.00(257.00, 319.25) | 325.00(287.25, 394.25) | <0.001 |
| 淋巴细胞中位数(Q1,Q3) | 1.86(1.46, 2.33) | 1.79(1.42, 2.27) | 1.91(1.49, 2.37) | 1.92(1.55, 2.42) | 0.240 |
| 单核细胞百分比中位数(Q1,Q3) | 0.35(0.28, 0.45) | 0.33(0.26, 0.43) | 0.35(0.28, 0.43) | 0.44(0.34, 0.54) | <0.001 |
| 性别 | 0.124 | ||||
| 女性 | 184(36.6) | 91(33.1) | 67(42.9) | 26(36.1) | |
| 男性 | 319(63.4) | 184(66.9) | 89(57.1) | 46(63.9) | |
| 年龄中位数(Q1,Q3) | 61.00(53.50, 67.00) | 61.00(54.00, 67.00) | 62.00(54.00, 67.00) | 60.00(49.75, 66.00) | 0.378 |
| 身体质量指数中位数(Q1,Q3) | 23.23(21.22, 25.41) | 23.39(21.30, 25.71) | 23.12(20.98, 25.44) | 22.67(20.80, 24.79) | 0.303 |
| 肿瘤部位 | 0.088 | ||||
| 结肠 | 254(50.5) | 134(48.7) | 75(48.1) | 45(62.5) | |
| 直肠 | 249(49.5) | 141(51.3) | 81(51.9) | 27(37.5) | |
| 肿瘤最大直径中位数(Q1,Q3) | 4.50(3.50, 5.90) | 4.00(3.50, 5.25) | 5.00(3.50, 6.00) | 5.00(3.50, 6.12) | 0.003 |
| 病理形态 | 0.501 | ||||
| 溃疡性 | 365(72.6) | 195(70.9) | 114(73.1) | 56(77.8) | |
| 隆起型 | 138(27.4) | 80(29.1) | 42(26.9) | 16(22.2) | |
| 分化程度 | 0.059 | ||||
| 低 | 76(15.1) | 34(12.4) | 26(16.7) | 16(22.2) | |
| 中 | 401(79.7) | 228(82.9) | 118(75.6) | 55(76.4) | |
| 高 | 26(5.2) | 13(4.7) | 12(7.7) | 1(1.4) | |
| T | 0.004 | ||||
| 1 | 20(4) | 10(3.6) | 10(6.4) | 0(0) | |
| 2 | 79(15.7) | 52(18.9) | 22(14.1) | 5(6.9) | |
| 3 | 403(80.1) | 213(77.5) | 124(79.5) | 66(91.7) | |
| 4 | 1(0.2) | 0(0) | 0(0) | 1(1.4) | |
| N | 0.007 | ||||
| 0 | 309(61.4) | 175(63.6) | 95(60.9) | 39(54.2) | |
| 1 | 130(25.8) | 78(28.4) | 32(20.5) | 20(27.8) | |
| 2 | 64(12.7) | 22(8) | 29(18.6) | 13(18.1) | |
| M | 1.000 | ||||
| 0 | 503(100) | 275(100) | 156(100) | 72(100) | |
| 临床分期 | 0.106 | ||||
| Ⅰ | 79(15.7) | 47(17.1) | 28(17.9) | 4(5.6) | |
| Ⅱ | 229(45.5) | 128(46.5) | 67(42.9) | 34(47.2) | |
| Ⅲ | 195(38.8) | 100(36.4) | 61(39.1) | 34(47.2) | |
| 淋巴侵犯数目中位数(Q1,Q3) | 0.00(0.00, 2.00) | 0.00(0.00, 2.00) | 0.00(0.00, 2.00) | 0.00(0.00, 2.00) | 0.283 |
| 神经侵犯 | 0.425 | ||||
| 0 | 196(39) | 106(38.5) | 66(42.3) | 24(33.3) | |
| 1 | 307(61) | 169(61.5) | 90(57.7) | 48(66.7) | |
| 血管癌栓 | 0.960 | ||||
| 0 | 341(67.8) | 185(67.3) | 107(68.6) | 49(68.1) | |
| 1 | 162(32.2) | 90(32.7) | 49(31.4) | 23(31.9) | |
| 淋巴管癌栓 | 0.964 | ||||
| 0 | 381(75.7) | 209(76) | 117(75) | 55(76.4) | |
| 1 | 122(24.3) | 66(24) | 39(25) | 17(23.6) |
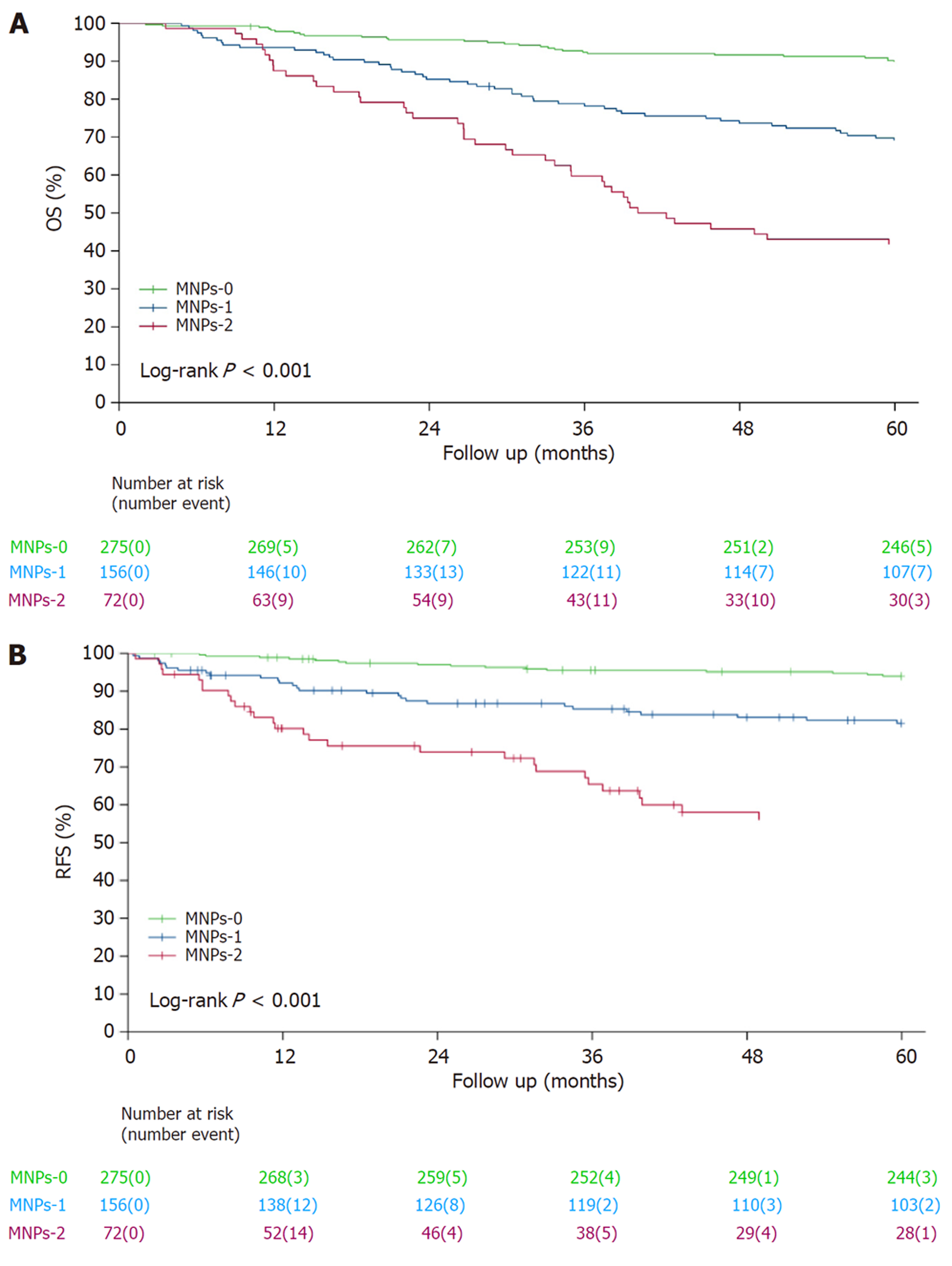
2.2.1 MNPs评分与OS的关联: 对不同MNPs评分分组下OS进行KM曲线分析, 结果显示: MNPs评分越高, OS越差(Logrank检验P<0.001), 三组(0分、1分、2分)的生存曲线分离明显, 见图1A.
2.2.2 MNPs评分与RFS的关联: 对不同MNPs评分分组下RFS进行KM曲线分析, 结果显示: MNPs评分越高, RFS越差(Logrank检验P<0.001), 三组(0分、1分、2分)的生存曲线分离更明显, 见图1B.
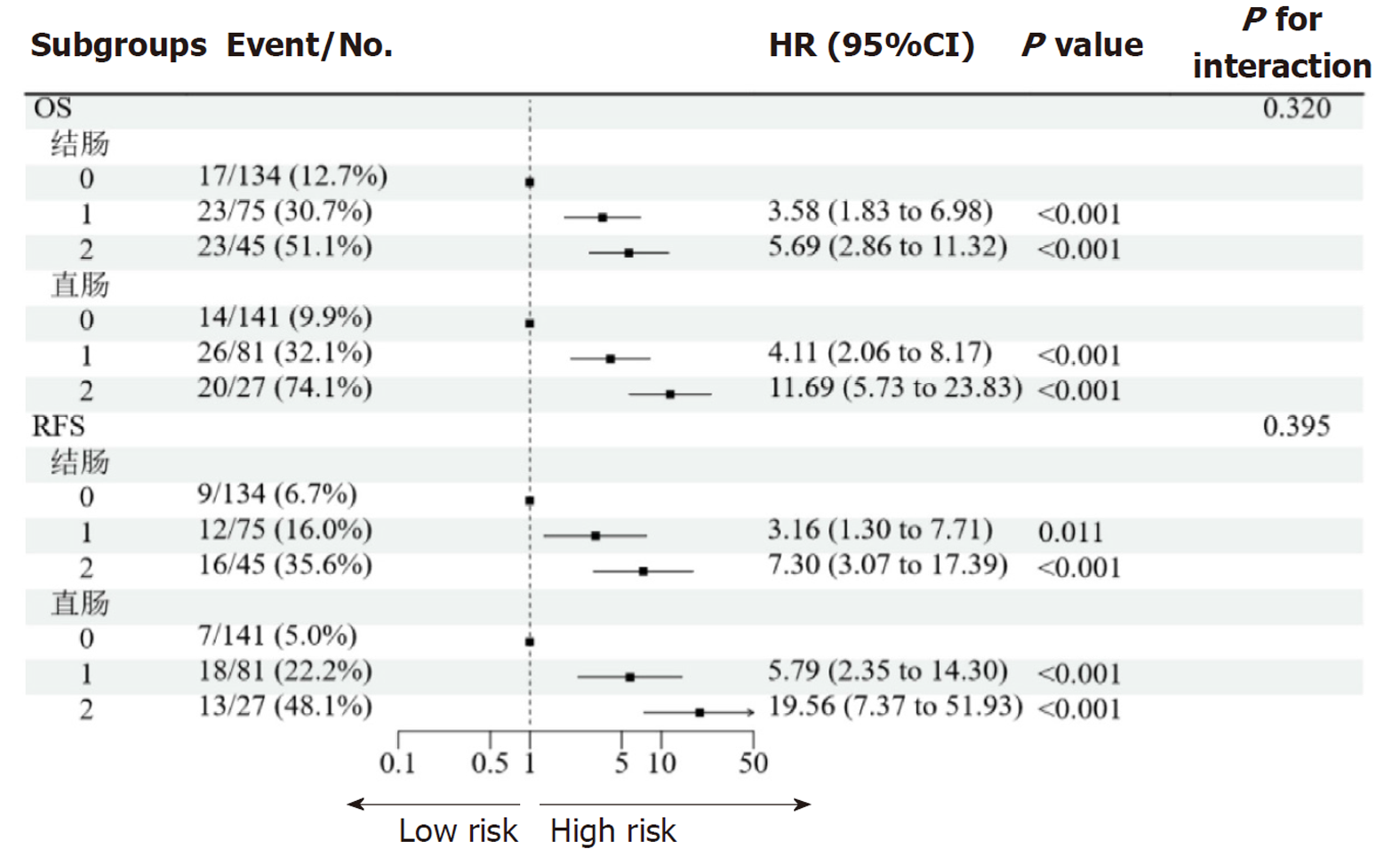
2.3.1 结肠癌与直肠癌的OS: 结肠癌低分险组生存率为12.7%, 中风险组为30.7%, 高风险组高达51.1%. 随着风险增加, 生存率显著下降. 直肠癌低分险组生存率为9.9%, 中风险组为32.1%, 高风险组高达74.1%. 同样呈现生存率随着风险增加而下降的趋势, 详见图2.
2.3.2 结肠癌与直肠癌的RFS: 结肠癌低分险组无复发生存率为6.7%, 中风险组为16.0%, 高风险组高达35.6%. 风险增加导致无复发生存率缩短. 直肠癌低分险组无复发生存率为5.0%, 中风险组为22.2%, 高风险组为48.1%. 无复发生存率同样随风险增加而减少, 详见图2.
2.4.1 MNPs与OS的单变量和多变量Cox回归分析: 单因素Cox回归分析结果显示: MNPs评分(1分 vs 0分: HR = 3.180, 95%CI: 2.028-4.988, P<0.001; 2分 vs 0分: HR = 7.430, 95%CI: 4.672-11.816, P<0.001)与OS相关, MNPs评分越高, 死亡风险越高; 在校正混杂因素(单因素中P<0.05的变量)后, MNPs评分仍为OS独立预测因子(1分 vs 0分: HR = 4.063, 95%CI: 2.443-6.757; 2分 vs 0分: HR = 10.094, 95%CI: 4.869-20.929, 均P<0.001), 见表2.
| 变量 | 单因素 | 多因素 | ||
| HR(95%CI) | P值 | HR(95%CI) | P值 | |
| 改良中性粒细胞血小板评分 | ||||
| 0 | 参考组 | 参考组 | ||
| 1 | 3.180(2.028, 4.988) | <0.001 | 4.063(2.443, 6.757) | <0.001 |
| 2 | 7.430(4.672, 11.816) | <0.001 | 10.094(4.869, 20.929) | <0.001 |
| 年龄 | 1.008(0.992, 1.025) | 0.337 | ||
| 身体质量指数 | 0.991(0.939, 1.046) | 0.740 | ||
| 肿瘤部位 | ||||
| 结肠 | 参考组 | |||
| 直肠 | 0.962(0.675, 1.370) | 0.830 | ||
| 肿瘤最大直径 | 1.013(0.924, 1.111) | 0.780 | ||
| 病理形态 | ||||
| 溃疡性 | 参考组 | 参考组 | ||
| 隆起型 | 0.410(0.248, 0.675) | <0.001 | 0.738(0.435, 1.252) | 0.260 |
| 分化程度 | ||||
| 低 | 参考组 | 参考组 | ||
| 中 | 0.422(0.283, 0.631) | <0.001 | 0.648(0.425, 0.989) | 0.044 |
| 高 | 0.212(0.065, 0.693) | 0.010 | 0.419(0.125, 1.401) | 0.158 |
| 临床分期 | ||||
| Ⅰ | 参考组 | 参考组 | ||
| Ⅱ | 5.101(1.580, 16.473) | 0.006 | 3.517(1.057, 11.699) | 0.040 |
| Ⅲ | 13.496(4.260, 42.756) | <0.001 | 6.608(1.956, 22.326) | 0.002 |
| 淋巴侵犯数目 | 1.169(1.120, 1.220) | <0.001 | 1.072(0.998, 1.151) | 0.057 |
| 神经侵犯 | ||||
| 0 | 参考组 | |||
| 1 | 1.381(0.947, 2.014) | 0.094 | ||
| 血管癌栓 | ||||
| 0 | 参考组 | 参考组 | ||
| 1 | 1.708(1.195, 2.441) | 0.003 | 1.222(0.833, 1.790) | 0.305 |
| 淋巴管癌栓 | ||||
| 0 | 参考组 | 参考组 | ||
| 1 | 1.805(1.243, 2.620) | 0.002 | 0.981(0.637, 1.511) | 0.931 |
| 癌胚抗原 | 1.007(1.002, 1.013) | 0.007 | 0.997(0.991, 1.004) | 0.401 |
| 碳水化合物抗原199 | 1.002(1.001, 1.002) | <0.001 | 1.001(1.000, 1.001) | 0.079 |
| 中性粒细胞 | 1.222(1.126, 1.325) | <0.001 | 0.938(0.810, 1.085) | 0.389 |
| 血小板 | 1.004(1.003, 1.006) | <0.001 | 0.998(0.995, 1.001) | 0.176 |
| 淋巴细胞 | 0.780(0.584, 1.042) | 0.093 | ||
| 单核细胞百分比 | 1.142(0.431, 3.027) | 0.790 | ||
2.4.2 MNPs与RFS的单变量和多变量Cox回归分析: 对MNPs等变量与OS进行Cox回归分析, 单因素Cox回归分析结果显示: MNPs评分(1分 vs 0分: HR = 3.790, 95%CI: 2.065-6.954, P<0.001; 2分 vs 0分: HR = 10.023, 95%CI: 5.428-18.510, P<0.001)与RFS相关, MNPs评分越高, 复发风险越高; 在校正混杂因素后, MNPs评分仍为RFS独立预测因子(1分 vs 0分: HR = 6.371, 95%CI: 3.220-12.604; 2分 vs 0分: HR = 31.086, 95%CI: 12.008-80.476, 均P<0.001), 见表3.
| 变量 | 单因素 | 多因素 | ||
| HR(95%CI) | P值 | HR(95%CI) | P值 | |
| 改良中性粒细胞血小板评分 | ||||
| 0 | 参考组 | 参考组 | ||
| 1 | 3.790(2.065, 6.954) | <0.001 | 6.371(3.220, 12.604) | <0.001 |
| 2 | 10.023(5.428, 18.510) | <0.001 | 31.086(12.008, 80.476) | <0.001 |
| 年龄 | 0.995(0.974, 1.016) | 0.610 | ||
| 身体质量指数 | 0.981(0.916, 1.052) | 0.595 | ||
| 肿瘤部位 | ||||
| 结肠 | 参考组 | |||
| 直肠 | 1.047(0.665, 1.646) | 0.844 | ||
| 肿瘤最大直径 | 1.000(0.888, 1.126) | 0.999 | ||
| 病理形态 | ||||
| 溃疡性 | 参考组 | 参考组 | ||
| 隆起型 | 0.503(0.277, 0.915) | 0.024 | 0.841(0.431, 1.638) | 0.610 |
| 分化程度 | ||||
| 低 | 参考组 | 参考组 | ||
| 中 | 0.495(0.290, 0.843) | 0.010 | 0.664(0.384, 1.149) | 0.143 |
| 高 | 0.264(0.061, 1.140) | 0.074 | 0.487(0.109, 2.166) | 0.344 |
| 临床分期 | ||||
| Ⅰ | 参考组 | 参考组 | ||
| Ⅱ | 1.928(0.740, 5.020) | 0.179 | 1.260(0.453, 3.508) | 0.658 |
| Ⅲ | 4.356(1.726, 10.993) | 0.002 | 2.705(0.941, 7.776) | 0.065 |
| 淋巴侵犯数目 | 1.125(1.056, 1.198) | <0.001 | 0.985(0.891, 1.088) | 0.764 |
| 神经侵犯 | ||||
| 0 | 参考组 | |||
| 1 | 1.515(0.927, 2.475) | 0.097 | ||
| 血管癌栓 | ||||
| 0 | 参考组 | 参考组 | ||
| 1 | 2.211(1.406, 3.477) | 0.001 | 1.916(1.189, 3.087) | 0.008 |
| 淋巴管癌栓 | ||||
| 0 | 参考组 | |||
| 1 | 1.230(0.737, 2.052) | 0.428 | ||
| 癌胚抗原 | 1.002(0.991, 1.012) | 0.753 | ||
| 碳水化合物抗原199 | 1.001(1.000, 1.002) | 0.212 | ||
| 中性粒细胞 | 1.193(1.069, 1.332) | 0.002 | 0.785(0.641, 0.962) | 0.020 |
| 血小板 | 1.004(1.002, 1.006) | <0.001 | 0.996(0.992, 1.000) | 0.034 |
| 淋巴细胞 | 0.855(0.594, 1.230) | 0.399 | ||
| 单核细胞百分比 | 0.695(0.172, 2.809) | 0.609 | ||
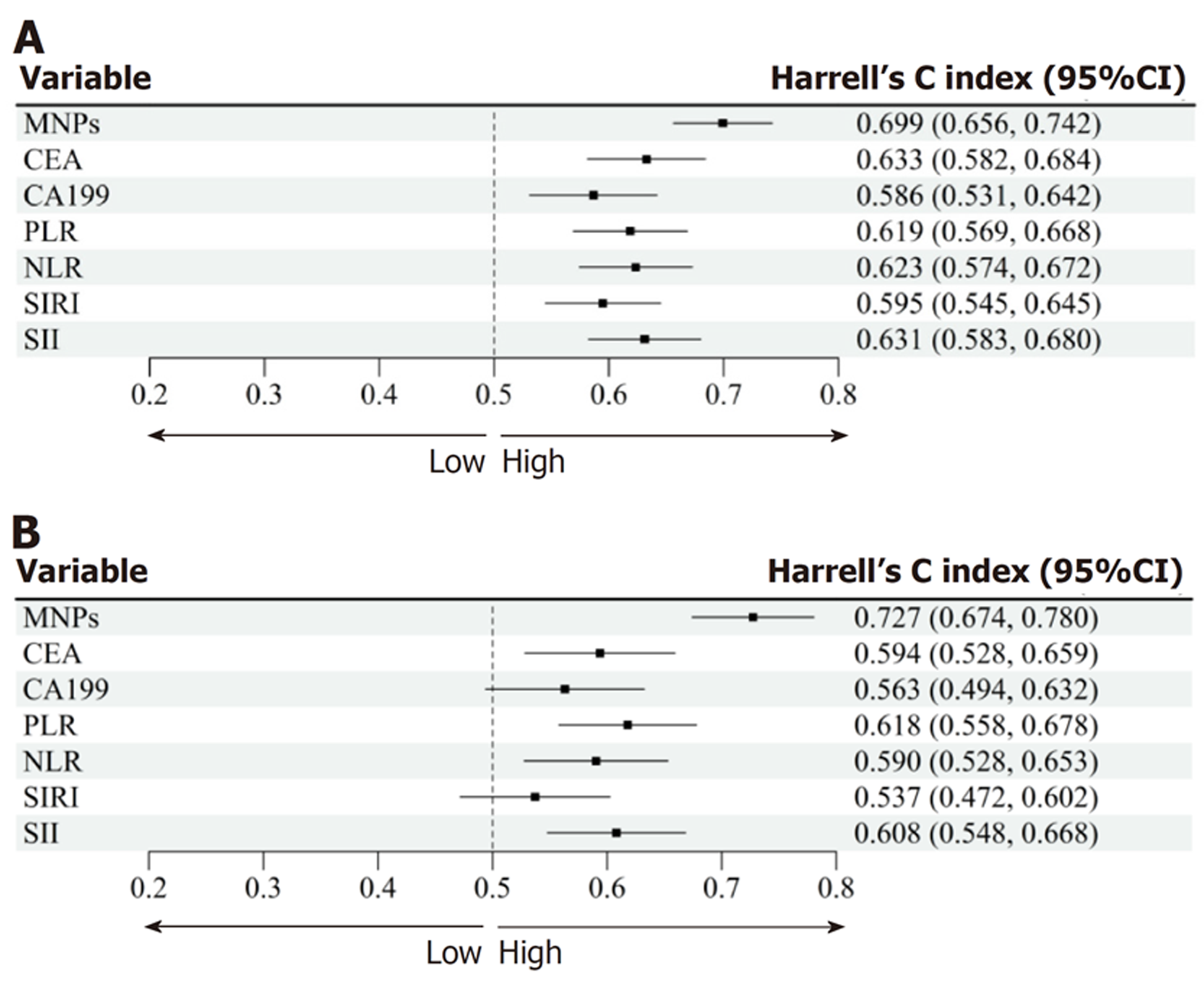
2.5.1 MNPs与其他指标预测OS的C指数对比: 对MNPs评分以及CEA、CA199、PLR、NLR、SIRI、SII预测OS的C指数进行评估, 结果显示: MNPs评分的C指数为0.699, 明显高于其他指标, 见图3A, 提示MNPs具有更好的区分能力.
2.5.2 MNPs与其他指标预测RFS的C指数对比: 对MNPs评分以及CEA、CA199、PLR、NLR、SIRI、SII预测RFS的C指数进行评估, 结果显示: MNPs评分的C指数为0.727, 明显优于其他指标, 见图3B, 提示MNPs具有更好的区分RFS的能力.
炎症反应在肿瘤的发生、发展过程中发挥着重要作用[10]. 持续的损伤和感染会增加患者的患癌风险, 促进癌前病变向癌症的转变[11]. 炎症细胞释放促炎因子、趋化因子和生长因子, 形成肿瘤微环境(tumor microenvironment, TME). TME中的炎症反应可促进癌细胞的生存、增殖、转移、血管生成以及免疫逃避等, 进一步推动恶性肿瘤的进展[12]. 我们已经发现术前生物标志物可预测恶性肿瘤患者的生存期, 包括胃癌[7,13-17]、CRC[18-21]、食管癌[22]、胰腺癌[23]和肝内胆管癌[24]等. 炎症是恶性肿瘤进展的关键因素[25]. 大量研究证据表明各种新的生物标志物已经在CRC的预测方面发挥着重要的价值. Copija等[26]研究发现高NPS患者在转移性疾病中更常见. 类似的, Hasirci等[27]发现NLR和SII可作为粪便潜血检测阳性患者早期诊断CRC重要生物标志物等; Miyatani等[28]发现术后LCR可精确预测胃癌患者的预后, 这可能提示MNPs在CRC中可能有类似的规律. 本研究首次探索了术前MNPs在CRC患者预后中的临床价值. 我们的研究结果表明, 术前MNPs是CRC患者的独立预后因素, 术前高MNPs与可切除CRC患者低OS和低RFS相关. 术前MNPs较NLR、PLR、SIR来说, 具有较高的临床预测价值.
TME中的免疫细胞与肿瘤细胞相互作用, 从而诱导血管生成、免疫抑制等生物学行为[29]. 既往研究已经证明, 中性粒细胞和血小板通过各种途径促进癌症的增殖扩散[6,30]. 血小板表达P-选择素和中性粒细胞表达P-选择素糖蛋白配体-1介导中性粒细胞在炎症或受损内皮细胞上的滚动和沉积, 形成中性粒细胞血小板聚集体. 中性粒细胞血小板聚集体不仅是血栓形成的前体, 更是促进循环肿瘤细胞粘附血管内皮、外渗和转移定植的关键效应单元. 它们还能抑制抗肿瘤免疫, 营造免疫抑制微环境. 此外血小板还能通过释放趋化因子进一步激活中性粒细胞, 增强肿瘤微环境中的炎症反应[31]. 激活的血小板还分泌高迁移率族蛋白B1, 高迁移率族蛋白B1可以激活中性粒细胞上的RAGE和TLR4受体, 从而启动中性粒细胞胞外陷阱形成. 中性粒细胞胞外诱捕网也可以引发或促进持续的血栓形成. 中性粒细胞胞外陷阱形成已经作为癌症介导的血栓形成的潜在机制[32]. 血小板被C型凝集素样受体2-podoplanin和TLR4-HMGB1激活后, 释放生长因子并上调白细胞、内皮细胞和潜在肿瘤细胞的细胞因子, 增加IL-8、CCL2和CXCL12水平, 最终导致肿瘤增殖和血管生成[33]. 在全身炎症反应(systemic inflammatory response, SIR)早期, 中性粒细胞会导致血小板快速增加. 因此, 中性粒细胞数量增加和血小板激活都反映了SIR的状态[8]. MNPs升高是机体持续放大的中性粒细胞血小板轴活化状态和系统性炎症负荷的血液学体现. 若术后持续升高, 可能提示残存微转移或抑制微环境持续存在. 临床上已经有很多替代生物标志物用于预测肿瘤患者的预后. 但MNPs直接反映了SIR状态, 这种状态预示着更强的促肿瘤炎症、血管生成、侵袭转移潜能和免疫抑制, 与恶性肿瘤患者更差的预后相关.
本研究对503例接受CRC根治术患者进行回顾性分析. 首先评估术前MNPs与全身炎症反应指数水平和临床病理特征的关系, 根据MNPs评分分为三组(0分: n = 275; 1分: n = 156; 2分: n = 72). 结果显示, 三组性别、年龄、身体质量指数、肿瘤部位、临床分期、N、M等资料差异无统计学意义. 生存分析显示, 术前MNPs评分越高, 患者的OS和RFS越差, 三组的生存曲线分离明显. 不同风险组别分析显示, 无论是结肠癌还是直肠癌随着风险组别的增加, 患者的OS和RFS均呈显著缩短的趋势. 单因素Cox回归分析表明, 术前MNPs评分是OS的危险因素, 评分越高死亡风险越大. 同样, 术前MNPs评分也与RFS显著相关, 评分越高复发风险越高. 在多因素Cox回归分析中(校正单因素分析中P<0.05的混杂因素), 术前MNPs仍是OS和RFS的独立预测因子. 进一步评估术前MNPs及其他指标(包括CEA、CA199、PLR、NLR、SIRI、SII)对OS和RFS的预测效能, 结果显示, 术前MNPs评分预测OS的C指数为0.699, 预测RFS的C指数为0.727, 均显著高于其他指标. 这表明术前MNPs评分相较于其他生物标志物具有更优的区分能力. 但本研究存在一定的局限性. 首先本研究是一项回顾性分析, 患者的选择和患者信息存在偏倚. 我们已经努力通过严格的纳入和排除标准来确保数据质量, 但潜在的遗失资料(如某些实验室指标或详细的合并症信息)仍可能影响结果的完整性. 其次, 我们排除了术前存在远处转移且不可切除的患者, 这意味着我们的研究样本预后整体较好. 因此, 本研究主要适用于接受根治性手术且无远处转移(M0)的患者, 其外推性需谨慎, 并应在未来的前瞻性或外部验证或包括更广泛分期患者的研究中进一步验证. 此外, 术前MNPs临界值最初源于胃癌研究, 并非专门针对CRC人群特性得出的最优值. 未来有必要探索更精确的、CRC特异性的术前MNPs临界值, 以进一步提升其预测能力和临床适用性. 术前MNPs在预测OS和RFS方面的C指数约为0.7. 虽然术前MNPs显著高于同时比较的其他常用生物标志物, 但C指数在0.7左右通常被认为是中等预测水平. 术前MNPs可作为单一预测因子, 但它的预测能力尚有提升空间. 未来可以结合已确立的强预后指标(如CEA、CA199、PLR、NLR、SIRI、SII)进行整合或进行外部验证, 增强预测模型的效能和推广性. 尽管我们通过综合评估排除了术前存在明确活动性感染的患者, 但极少数潜在的、无症状的亚临床炎症状态可能未被完全识别. 此外, 本研究未校正糖尿病、高血压等基础疾病对全身炎症状态的潜在影响. 尽管对术前MNPs的干扰可能较弱, 但残存混杂的可能性仍存在. 因回顾性数据中术后规律血常规记录不完整, 我们无法分析MNPs术后变化对预后的影响. 未来研究应前瞻性收集这些数据以完善模型.
综上所述, 本研究首次证实了术前MNPs在评估CRC患者OS和RFS方面具有显著的临床预测能力, 为指导恶性肿瘤患者的预后提供了可靠的证据, 有助于临床工作者制定个性化、精准的治疗方案, 进而改善患者的预后.
越来越多的证据表明, 肿瘤相关的炎症反应在癌症的发生、发展和转移中扮演着关键角色. 中性粒细胞与淋巴细胞比值(neutrophil-to-lymphocyte ratio, NLR)、淋巴细胞与单核细胞比值(monocyte-to-lymphocyte ratio, LMR)和血小板与淋巴细胞比值(platelet-lymphocyte ratio, PLR)等, 已被广泛研究并证实对结直肠癌(colorectal cancer, CRC)患者预后具有一定的预测价值. 然而, 这些指标在预测效能和临床应用方面存在一定的局限性. 改良中性粒细胞血小板评分(modified neutrophil-platelet score, MNPs)作为一种整合了中性粒细胞和血小板计数的新型炎症指标, 理论上可能更全面地反映肿瘤相关炎症状态及其对预后的影响. 本研究旨在深入探索术前MNPs水平与CRC患者术后总生存期(overall survival, OS)和无复发生存期(recurrence free survival, RFS)的关联, 评估其作为独立预后预测因子的价值.
现有血液炎症指标(如NLR/LMR/PLR)对CRC预后的预测效能仍有待提高. 本研究旨在评估术前MNPs对CRC患者术后生存的预测价值, 重点解决: (1)术前MNPs是否独立关联OS和RFS?(2)术前MNPs预测效能是否优于现有指标?其意义在于: 揭示中性粒细胞-血小板协同机制, 深化系统性炎症在CRC进展中的作用认知; 提供基于术前血常规的便捷预后工具, 精准识别高风险患者, 指导个体化治疗及随访. 本研究为术前MNPs作为CRC新型预后标志物提供关键证据.
(1)验证术前MNPs与CRC患者OS和RFS的关联性; (2)明确MNPs是否为OS和RFS的独立预测因子; (3)比较MNPs与传统炎症指标对CRC患者预后的预测效能差异.通过对503例CRC患者5年随访数据的回顾性分析, 所有目标均得到充分实现: MNPs升高显著增加死亡风险和复发风险; MNPs是OS与RFS的独立预测因子; MNPs的预后能力优于传统炎症指标. 首次证实了MNPs作为新型复合炎症标志物的独立预后价值, 将进一步丰富对系统性炎症反应在CRC进展和转归中作用机制的理解, 并可能揭示中性粒细胞与血小板协同作用的潜在生理学意义. 此外, MNPs仅依赖术前常规血检即可获取, 临床医生可据此在治疗前精准识别高危患者, 优化辅助治疗强度及随访策略.
本研究采用回顾性队列分析, 探究了术前MNPs对CRC患者预后的预测价值. 通过系统回顾患者的电子病历和临床数据库, 收集其术前的详细临床资料和实验室检查结果. 对所有纳入患者进行了完整的5年生存随访. 对于不同分组下的OS/RFS差异, 绘制KM曲线进行分析, 并进行Logrank检验比较组间差异. 并通过单变量和多变量Cox回归探索MNPs评分与OS/RFS之间的关联. 并计算C指数评估MNPs与其他炎症指标的预测效能差异. 特征: 研究不仅评估了MNPs自身的预测能力, 还将其与现有常用炎症指标进行直接比较, 这是其方法学上的重要环节, 旨在证明新指标的相对优势. 研究方法的独创性, 研究MNPs这种复合指标可能更综合地反映了肿瘤相关的全身炎症反应状态. 这为临床进行个体化预后评估和风险分层提供了新的、有前景的工具.
本研究根据术前MNPs分为三组(0分: n = 275; 1分: n = 156; 2分: n = 72). 三组基线特征(性别/年龄/分期等)无统计学差异. 生存分析显示MNPs评分越高, OS和RFS越差; 结肠癌/直肠癌亚组中, 高风险组OS/RFS均显著缩短. Cox回归证实MNPs为OS/RFS独立预测因子. MNPs预测OS和RFS的C指数显著高于现有指标. MNPs作为新型凝血-炎症标志物: 首此被验证其独立预后价值; 预测效能优于主流炎症指标; 为个体化治疗提供客观依据; 揭示中性粒细胞-血小板协同机制.
首次证实术前MNPs是CRC患者OS和RFS的独立预测因子, 其预测效能显著优于传统炎症指标(C指数: OS = 0.699, RFS = 0.727). 术前MNPs整合中性粒细胞与血小板, 全面反映肿瘤炎症微环境对预后的影响, 突破现有标志物局限.关键价值包括; 相同分期下可识别隐匿性高危患者; 术前MNPs越高, 生存曲线下降越陡峭; 可提前5年预测生存与复发风险; 未来有望纳入常规评估指导个体化辅助治疗强度, 实现早诊早治.
本研究为回顾性分析, 存在患者选择和资料偏倚, 样本限于无远处转移(M0)患者, 导致结果外推性受限; 术前MNPs临界值非CRC特异, 预测能力中等, 且未完全排除亚临床炎症或基础疾病(如糖尿病)的干扰. 未来有望探索CRC特异性术前MNPs临界值以提升预测能力; 结合其他生物标志物构建整合模型; 分析MNPs动态变化对预后的影响; 在更广泛分期患者中验证结果. 我们应采用前瞻性设计, 进行外部验证队列研究, 纳入多样化患者群体以增强推广性.
学科分类: 胃肠病学和肝病学
手稿来源地: 黑龙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B, B
C级 (良好): 0
D级 (一般): D, D
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁
| 1. | Zhang X, Yang L, Liu S, Cao LL, Wang N, Li HC, Ji JF. [Interpretation on the report of global cancer statistics 2022]. Zhonghua Zhong Liu Za Zhi. 2024;46:710-721. [PubMed] [DOI] |
| 2. | Kajiwara Y, Ueno H. Essential updates 2022-2023: Surgical and adjuvant therapies for locally advanced colorectal cancer. Ann Gastroenterol Surg. 2024;8:977-986. [PubMed] [DOI] |
| 3. | Wolf AMD, Fontham ETH, Church TR, Flowers CR, Guerra CE, LaMonte SJ, Etzioni R, McKenna MT, Oeffinger KC, Shih YT, Walter LC, Andrews KS, Brawley OW, Brooks D, Fedewa SA, Manassaram-Baptiste D, Siegel RL, Wender RC, Smith RA. Colorectal cancer screening for average-risk adults: 2018 guideline update from the American Cancer Society. CA Cancer J Clin. 2018;68:250-281. [PubMed] [DOI] |
| 4. | Nunes L, Li F, Wu M, Luo T, Hammarström K, Torell E, Ljuslinder I, Mezheyeuski A, Edqvist PH, Löfgren-Burström A, Zingmark C, Edin S, Larsson C, Mathot L, Osterman E, Osterlund E, Ljungström V, Neves I, Yacoub N, Guðnadóttir U, Birgisson H, Enblad M, Ponten F, Palmqvist R, Xu X, Uhlén M, Wu K, Glimelius B, Lin C, Sjöblom T. Prognostic genome and transcriptome signatures in colorectal cancers. Nature. 2024;633:137-146. [PubMed] [DOI] |
| 5. | Misiewicz A, Dymicka-Piekarska V. Fashionable, but What is Their Real Clinical Usefulness? NLR, LMR, and PLR as a Promising Indicator in Colorectal Cancer Prognosis: A Systematic Review. J Inflamm Res. 2023;16:69-81. [PubMed] [DOI] |
| 6. | Menyhart O, Fekete JT, Győrffy B. Inflammation and Colorectal Cancer: A Meta-Analysis of the Prognostic Significance of the Systemic Immune-Inflammation Index (SII) and the Systemic Inflammation Response Index (SIRI). Int J Mol Sci. 2024;25:8441. [PubMed] [DOI] |
| 7. | Jing Y, Ren M, Li X, Sun X, Xiao Y, Xue J, Liu Z. The Effect of Systemic Immune-Inflammatory Index (SII) and Prognostic Nutritional Index (PNI) in Early Gastric Cancer. J Inflamm Res. 2024;17:10273-10287. [PubMed] [DOI] |
| 8. | Otani K, Aoyama T, Maezawa Y, Hashimoto I, Kamiya N, Kato A, Numata M, Kawahara S, Tamagawa A, Nakazono M, Tamagawa H, Segami K, Kazama K, Sawazaki S, Yukawa N, Saito A, Rino Y. The Clinical Benefit of the Modified Neutrophil-Platelet Score as a Surrogate Prognostic Marker in Patients With Resectable Gastric Cancer. In Vivo. 2024;38:897-903. [PubMed] [DOI] |
| 9. | Okugawa Y, Toiyama Y, Yamamoto A, Omura Y, Kusunoki K, Yin C, Ide S, Kitajima T, Koike Y, Fujikawa H, Yasuda H, Okita Y, Hiro J, Yoshiyama S, Ohi M, Araki T, Kusunoki M. Modified neutrophil-platelet score as a promising marker for stratified surgical and oncological outcomes of patients with gastric cancer. Surg Today. 2020;50:223-231. [PubMed] [DOI] |
| 10. | Sui Q, Zhang X, Chen C, Tang J, Yu J, Li W, Han K, Jiang W, Liao L, Kong L, Li Y, Hou Z, Zhou C, Zhang C, Zhang L, Xiao B, Mei W, Xu Y, Qin J, Zheng J, Pan Z, Ding PR. Inflammation promotes resistance to immune checkpoint inhibitors in high microsatellite instability colorectal cancer. Nat Commun. 2022;13:7316. [PubMed] [DOI] |
| 11. | Antonucci L, Karin M. The Past and Future of Inflammation as a Target to Cancer Prevention. Cancer Prev Res (Phila). 2024;17:141-155. [PubMed] [DOI] |
| 12. | Shahgoli VK, Noorolyai S, Ahmadpour Youshanlui M, Saeidi H, Nasiri H, Mansoori B, Holmskov U, Baradaran B. Inflammatory bowel disease, colitis, and cancer: unmasking the chronic inflammation link. Int J Colorectal Dis. 2024;39:173. [PubMed] [DOI] |
| 13. | Liu Z, Dou Y, Lu C, Han R, He Y. Neutrophil extracellular traps in tumor metabolism and microenvironment. Biomark Res. 2025;13:12. [PubMed] [DOI] |
| 14. | Ding P, Wu H, Li T, Wu J, Yang L, Yang J, Guo H, Tian Y, Yang P, Meng L, Zhao Q. Impact of preoperative sarcopenia on postoperative complications and prognosis in patients undergoing robotic gastric cancer surgery: A propensity score matching study. Nutrition. 2024;123:112408. [PubMed] [DOI] |
| 15. | Fu M, Zhang X, Shen F, Ma J, Li Z. Prognostic value of peripheral blood neutrophil/lymphocyte ratio, platelet/lymphocyte ratio, pan-immune-inflammation value and systemic immune-inflammation index for the efficacy of immunotherapy in patients with advanced gastric cancer. Immunotherapy. 2024. [PubMed] [DOI] |
| 16. | Xu M, Liu D, Wang L, Sun S, Liu S, Zhou Z. Clinical implications of CT-detected ascites in gastric cancer: association with peritoneal metastasis and systemic inflammatory response. Insights Imaging. 2024;15:237. [PubMed] [DOI] |
| 17. | Nechita VI, Al-Hajjar N, Moiş E, Furcea L, Nechita MA, Graur F. Inflammatory Ratios as Predictors for Tumor Invasiveness, Metastasis, Resectability and Early Postoperative Evolution in Gastric Cancer. Curr Oncol. 2022;29:9242-9254. [PubMed] [DOI] |
| 18. | Verter E, Berger Y, Perl G, Peretz I, Tovar A, Morgenstern S, Brenner B, Benchimol D, Kashtan H, Sadot E. Neutrophil-to-Lymphocyte Ratio Predicts Recurrence Pattern in Patients with Resectable Colorectal Liver Metastases. Ann Surg Oncol. 2021;28:4320-4329. [PubMed] [DOI] |
| 19. | Aktan M, Yavuz BB, Kanyilmaz G, Oltulu P. Factors affecting pathological response and survival following neoadjuvant chemoradiotherapy in rectal cancer patients. Indian J Cancer. 2021;58:553-560. [PubMed] [DOI] |
| 20. | Wu H, Wang Y, Deng M, Zhai Z, Xue D, Luo F, Li H. Preoperative inflammatory markers and tumor markers in predicting lymphatic metastasis and postoperative complications in colorectal cancer: a retrospective study. BMC Surg. 2025;25:71. [PubMed] [DOI] |
| 21. | Nøst TH, Alcala K, Urbarova I, Byrne KS, Guida F, Sandanger TM, Johansson M. Systemic inflammation markers and cancer incidence in the UK Biobank. Eur J Epidemiol. 2021;36:841-848. [PubMed] [DOI] |
| 22. | Jiang Y, Xu D, Song H, Qiu B, Tian D, Li Z, Ji Y, Wang J. Inflammation and nutrition-based biomarkers in the prognosis of oesophageal cancer: a systematic review and meta-analysis. BMJ Open. 2021;11:e048324. [PubMed] [DOI] |
| 23. | Han R, Tian Z, Jiang Y, Guan G, Wang X, Sun X, Yu Y, Jing X. Prognostic significance of the systemic immune inflammation index in patients with metastatic and unresectable pancreatic cancer. Front Surg. 2022;9:915599. [PubMed] [DOI] |
| 24. | Li Q, Zhang R, Fu JL, Zhang J, Su JB, Jin ZC, Chen C, Zhang D, Geng ZM. [The prognostic value of preoperative peripheral blood inflammatory biomarkers for intrahepatic cholangiocarcinoma after radical resection]. Zhonghua Zhong Liu Za Zhi. 2022;44:1194-1201. [PubMed] [DOI] |
| 25. | Kim ES, Kim SY, Moon A. C-Reactive Protein Signaling Pathways in Tumor Progression. Biomol Ther (Seoul). 2023;31:473-483. [PubMed] [DOI] |
| 26. | Copija A, Nowakowska-Zajdel E, Janion K, Walkiewicz K. Clinical Characteristics of Colorectal Cancer Patients in terms of Selected Platelet Indices. Dis Markers. 2020;2020:6145604. [PubMed] [DOI] |
| 27. | Hasirci I, Şahin A. Importance of the neutrophil-lymphocyte ratio and systemic immune-inflammation index in predicting colorectal pathologies in fecal occult blood-positive patients. J Clin Lab Anal. 2023;37:e24878. [PubMed] [DOI] |
| 28. | Miyatani K, Sawata S, Makinoya M, Miyauchi W, Shimizu S, Shishido Y, Matsunaga T, Yamamoto M, Tokuyasu N, Takano S, Sakamoto T, Hasegawa T, Saito H, Fujiwara Y. Combined analysis of preoperative and postoperative lymphocyte-C-reactive protein ratio precisely predicts outcomes of patients with gastric cancer. BMC Cancer. 2022;22:641. [PubMed] [DOI] |
| 29. | Nishida A, Andoh A. The Role of Inflammation in Cancer: Mechanisms of Tumor Initiation, Progression, and Metastasis. Cells. 2025;14:488. [PubMed] [DOI] |
| 30. | Yamamoto T, Kawada K, Obama K. Inflammation-Related Biomarkers for the Prediction of Prognosis in Colorectal Cancer Patients. Int J Mol Sci. 2021;22:8002. [PubMed] [DOI] |
| 31. | Li Y, Wang H, Zhao Z, Yang Y, Meng Z, Qin L. Effects of the interactions between platelets with other cells in tumor growth and progression. Front Immunol. 2023;14:1165989. [PubMed] [DOI] |
| 32. | Mandel J, Casari M, Stepanyan M, Martyanov A, Deppermann C. Beyond Hemostasis: Platelet Innate Immune Interactions and Thromboinflammation. Int J Mol Sci. 2022;23:3868. [PubMed] [DOI] |