修回日期: 2025-06-25
接受日期: 2025-08-18
在线出版日期: 2025-08-28
老年人群身体机能降低, 肺部感染后更易出现胃食管反流(gastroesophageal reflux, GER), 会诱发气道炎症, 加重感染程度, 甚至危及患者生命安全. 因此, 本研究尝试探索老年肺部感染继发胃食管反流的风险因素, 以期提前预测风险、改善患者预后.
观察老年肺部感染合并GER的临床特征, 并分析其影响因素.
选取2021-01/2024-08就诊于义乌中西医结合医院的159例老年肺部感染患者为研究对象, 观察老年肺部感染合并GER患者的临床特征, 并统计发生率, 依据是否合并GER分为研究组、对照组, 对比两组临床资料, 采用Logistic回归分析老年肺部感染合并GER的影响因素.
159例老年肺部感染中有63例(39.62%)细菌感染, 51例(32.08%)病毒感染, 31例(19.50%)支原体感染, 另有14例(8.81%)为混合感染. 159例老年肺部感染患者中, GER发生率39.62%(63/159). 老年肺部感染合并GER患者均存在呼吸急促、发热及双肺干湿啰音, 多数患者出现剧烈咳嗽(90.48%)、反酸(95.24%)、烧心(93.65%)症状, 同时白细胞计数升高患者占比96.83%, C反应蛋白升高占比95.24%; 影像学检查提示, 病变以中下肺野区为主, 可见双肺多发斑片影(61.90%)、单侧肺不张(41.27%). 两组年龄、睡眠障碍、肺部感染严重程度、焦虑情绪、服用镇静药、机械通气、糖尿病病史、既往GER疾病史方面对比, 差异有统计学意义(P<0.05). Logistic回归分析显示, 肺部感染严重程度、年龄、焦虑情绪、肺部感染严重程度、既往GER疾病史、糖尿病病史是老年肺部感染患者合并GER的独立影响因素(P<0.05).
老年肺部感染合并GER患者临床症状及体征具有一定特异性, 患者合并GER的独立危险因素包括肺部感染严重程度、焦虑情绪、年龄、既往GER疾病史、睡眠障碍、糖尿病病史, 临床工作者可加强对高危患者的针对性干预以减少GER的发生.
核心提要: 目前临床已有学者对肺部感染、胃食管反流(gastroesophageal reflux, GER)单一病种的特征及影响因素进行分析, 但缺乏老年肺部感染合并GER患者的相关报告, 此类患者在风险防控上是否具备特异性尚待研究予以论证. 为填补这一空白, 本研究初次尝试分析老年肺部感染合并GER的影响因素, 并对其临床特征进行分析, 以期为完善干预路径提供支持.
引文著录: 黄智一. 老年肺部感染合并胃食管反流的临床现况及影响因素分析. 世界华人消化杂志 2025; 33(8): 640-648
Revised: June 25, 2025
Accepted: August 18, 2025
Published online: August 28, 2025
Since elderly people have declined physical function, and gastroesophageal reflux (GER) is more likely to occur after lung infection in this population, which will induce airway inflammation, aggravate the degree of infection, and even endanger the life of patients. Therefore, this study attempts to explore the risk factors for GER secondary to lung infection in the elderly, in order to predict the risk in advance and improve the prognosis of patients.
To observe the clinical characteristics of elderly patients with pulmonary infection complicated by GER disease, and analyze their influencing factors.
A total of 159 elderly patients with pulmonary infection who visited Yiwu Integrated Traditional Chinese and Western Medicine Hospital from January 2021 to August 2024 were selected as the study subjects. The clinical characteristics of elderly patients with pulmonary infection complicated by GER were observed, and the incidence rate of GER was calculated. Patients were categorized into a study group and a control group based on whether they had GER. The clinical data of the two groups were compared, and Logistic regression analysis was used to analyze the influencing factors of pulmonary infection complicated by GER in the elderly.
Among 159 elderly patients with pulmonary infections, 63 (39.62%) had bacterial infections, 51 (32.08%) had viral infections, 31 (19.50%) had mycoplasmal infections, and 14 (8.81%) had mixed infections. The incidence of GER was 39.62% (63/159). Elderly patients with pulmonary infections complicated by GER all presented with shortness of breath, fever, and bilateral lung rales, with most patients experiencing severe cough (90.48%), acid reflux (95.24%), and heartburn (93.65%). At the same time, 96.83% of patients had elevated white blood cell count, and 95.24% had elevated C-reactive protein. Imaging studies indicated that the lesions were located mainly in the middle and lower lung fields, with multiple patchy shadows (61.90%) and unilateral atelectasis (41.27%) visible in both lungs. There were significant differences in age, sleep disorders, severity of pulmonary infection, anxiety, use of sedatives, mechanical ventilation, history of diabetes, and previous history of GER disease between the two groups (P < 0.05). Logistic regression analysis showed that the severity of pulmonary infection, age, anxiety, previous history of GER disease, and history of diabetes were independent influencing factors for GER in elderly patients with pulmonary infection (P < 0.05).
The clinical symptoms and signs of elderly patients with pulmonary infection combined with GER exhibit certain specificity. The independent risk factors for GER in patients with pulmonary infection include the severity of pulmonary infection, anxiety, age, previous history of GER disease, sleep disorders, and diabetes history. Clinicians should strengthen targeted intervention for high-risk patients to reduce the incidence of GER.
- Citation: Huang ZY. Clinical characteristics and their influencing factors in elderly patients with pulmonary infection complicated by gastroesophageal reflux disease. Shijie Huaren Xiaohua Zazhi 2025; 33(8): 640-648
- URL: https://www.wjgnet.com/1009-3079/full/v33/i8/640.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v33.i8.640
老年人群生理功能呈退行性变化、抵抗力降低, 肺部感染风险较高, 加之多数老年患者多病共病、胃肠蠕动功能降低, 肺部感染后更易出现胃食管反流(gastroesophageal reflux, GER)[1,2]. GER是胃内容物或(和)十二指肠内容物等反复流入食管引起的临床综合征[3]. 目前GER与呼吸系统疾病的相关性已得到充足证据支持[4,5]. 尤其老年患者身体抵抗力降低, 肺部感染继发GER后, 因反流物进入气道, 微量吸入即可能损伤呼吸黏膜, 破坏纤毛清除功能, 诱发气道炎症, 且食管反流会刺激迷走神经, 引起气管痉挛, 进一步加重感染程度, 导致不良转归, 甚至危及患者生命安全[6]. 因此, 及时识别肺部感染后出现GER的风险对临床循证实施个体化干预措施具有重要指导价值. 目前临床已有学者[7,8]对肺部感染、GER单一病种的特征及影响因素进行分析[7,8], 但缺乏老年肺部感染合并GER患者的相关报告, 此类患者在风险防控上是否具备特异性尚待研究予以论证. 为填补这一空白, 本研究初次尝试分析老年肺部感染合并GER的影响因素, 并对其临床特征进行分析, 以期为完善干预路径提供支持.
本研究为前瞻性研究, 已获得伦理委员会审批(审批号: 2021-5-3), 选取2021-01/2024-08义乌中西医结合医院收治的159例老年肺部感染住院患者为研究对象. 纳入标准: 临床诊断为肺部感染[9], 均为原发疾病; 均可耐受动态监测仪监测; 年龄≥60岁; 患者及家属知情研究方案, 自愿签署同意书. 排除标准: 因脑卒中、手术等其他明确原因引起的继发性肺部感染者; 合并恶性肿瘤者; 合并精神类疾病者; 合并免疫缺陷型疾病者; 合并甲肝、乙肝等严重传染性疾病者; 治疗期间病亡者.
样本量估算: 根据影响因素样本量估算方法, 样本量应为结局变量的10-15倍, 本研究查阅既往相关文献[10]并结合临床观察预计筛选出6个变量, 并预估肺部感染后出现GER发生率57.9%, 同时考虑10%样本无效率, 计算最小样本量n = 10×5÷(1-0.1)÷57.9% ≈ 116, 即最小样本量为116例. 本研究依据本院情况纳入研究对象159例, 符合样本量要求.
采用本院自制一般资料问卷, 收集患者临床资料, 包括性别、体质量指数[体重(kg)/身高2(m2)]、吸烟史、年龄、饮酒史、高血压病史、GER发生情况、既往GER疾病史、幽门螺杆菌感染、服用镇静药、肺部感染严重程度、糖尿病病史、睡眠障碍、焦虑情绪、补充钾剂、鼻饲管喂养、感染类型、机械通气及生化指标[白细胞计数(white blood cell count, WBC)、中性粒细胞、C反应蛋白(C-reactive protein, CRP)、红细胞沉降率(erythrocyte sedimentation rate, ESR)、降钙素原(procalcitonin, PCT)].
1.3.1 评估方法: GER评估标准[11]: 出现反酸、烧心等典型症状; 或出现胸痛、上腹烧灼感、上腹胀、上腹痛、嗳气等不典型症状; 或出现咳嗽、哮喘、咽喉症状及牙蚀症等食管外症状; 出现前述任一项症状的患者, 需接受美国Sandhill公司的BioSTAR的动态监测仪对其24 h食道下段pH值进行监测, 食管下段pH值<4的时间占比≥4.2%, 或Demeester评分(总酸暴露时间、反流次数、持续>5分钟的反流次数、立位/卧位酸暴露时间、最长反流时间)>14.72分, 则确诊为GER. 观察并记录患者住院期间出现GER的情况.
肺部感染病情严重程度: 患者入院24 h内完成CURB-65量表[12], 包括5个方面: 意识错乱、尿素>7 mmol/L、年龄≥65岁、低舒张压(≤60 mmHg)或收缩压(<90 mmHg)、呼吸频率≥30次/min, 各项症状存在记为1分, 不存在记为0分, 评分越高表示病情越严重, 0-1分为轻度, 2分为中度, ≥3分为重度.
饮酒史: 每日饮酒≥1次, 且持续时间≥1年, 包括截止入组时戒酒时间<3年.
吸烟史: 每日吸烟≥1支, 且持续时间≥1年, 包括截止入组时戒烟时间<3年.
高血压病史: 正在服用降压药, 或既往诊断为高血压, 或参照《中国高血压健康管理规范(2019)》[13]确诊为高血压.
糖尿病病史: 正在服用降糖药, 或既往诊断为糖尿病, 或参照《糖尿病的实验室诊断管理专家共识》[14]确诊为糖尿病.
睡眠质量: 于患者病情稳定时采用匹兹堡睡眠质量量表(Pittsburgh Sleep Quality Index, PSQI)[15]评估患者睡眠质量, 量表包括7个问题: 入睡时间、睡眠障碍、睡眠质量、睡眠时间、睡眠效率、日间功能、催眠药物, 均采用0-3分评估法最高分21分, 评分越高表示睡眠质量越差, PSQI评分≥8分表示存在睡眠障碍.
焦虑情绪: 于患者病情稳定时采用焦虑自评量表(Self-Absorption Scale, SAS)[16]评估患者情绪状态, 量表包括20个条目, 均采用四级评分法, 获取总分后转化为百分制评分, 评分越高提示焦虑情绪越严重, SAS评分≥50分表示存在焦虑情绪.
1.3.2 检测方法: 生化指标: 患者入院2 h内分管采集肘静脉血, 取乙二胺四乙酸抗凝管(紫色管帽)采集血液2 mL, 全血上血细胞分析仪(日本sys-mex XE2100型)测定WBC、中性粒细胞; 取枸橼酸钠抗凝管(黑色管帽)采集血液2 mL, 2 h内以Westergren法测定ESR; 取无抗凝剂采血管(红色管帽)采集血液2 mL, 离心(转速3000 r/min, 半径12 cm, 时间10 min)后取血清, 选择全自动免疫分析仪(MaGlumi-X8型)以电化学发光免疫分析法测定血清PCT, 以免疫比浊法测定血清CRP. 血清PCT正常值参考范围0-0.05 mg/mL, 血清CRP正常值参考范围(0-10.0) mg/L, 外周血WBC正常值参考范围(4-10)×109/L; 中性粒细胞正常值参考范围40%-75%; 血清ESR正常值参考范围: 女性(0-20) mm/h, 男性(0-15) mm/h.
病原体检测: 患者入院后依据其临床症状, 初步评估感染类型, 疑似细菌感染, 2 h内采集痰液标本, 痰液标本经生理盐水洗涤, 分别接种于麦康凯琼脂、血琼脂及巧克力琼脂平板(购自Oxoid公司), 孵育(18-24) h, 在显微镜下观察菌落形态、染色, 可疑菌落应用VITEK2-Compact(生物梅里埃)及其配套试剂卡进行细菌鉴定, 采用纸片扩散法进行药敏试验. 疑似非典型肺炎, 鼻咽拭子取样, 应用实时荧光定量PCR仪检测病毒(A型流感病毒、腺病毒、甲型流感病毒、人呼吸道合胞病毒、柯萨奇病毒、B型流感病毒等), 采用胶体金试纸条测定病毒蛋白, 读取病毒类型. 同时采集血液样本3 mL, 3000 r/min转速离心10 min(12 cm半径), 取血清采用酶联免疫吸附法测定检测IgM/IgG抗体, 同步进行痰液取样, 提取核酸, 采用多重PCR法扩增支原体P1蛋白基因/衣原体ompA基因, 熔解曲线分析结果. 所有过程参照《全国临床检验操作规程》[17]严格遵循质控规范.
由接受统一培训并通过考核的研究人员在患者出院前完成资料采集工作. 收集资料前需先向患者说明本次研究的目的及意义, 获取患者知情同意后, 通过查阅患者病历档案及面对面访谈获取相关资料, 资料收集完成后, 安排双人录入数据, 经逻辑审核识别异常数据, 二次纠正无误后, 建立数据库. 本次收集资料159份, 有效回收率100%.
(1)观察并记录老年肺部感染患者出现GER的情况; (2)观察并记录老年肺部感染合并GER患者的临床特征; (3)以是否合并GER为依据将患者分为研究组、对照组, 对比两组临床资料; (4)采用Logistic回归方程分析老年肺部感染合并GER的影响因素.
统计学处理 应用SPSS 26.0统计学软件分析数据. 计数资料以n(%)表示, 组间比较采用χ2检验; 计量资料以均数±标准差(mean±SD)表示, 组间比较采用t检验; 采用Logistic分析老年肺部感染合并GER的相关因素. 以P<0.05为差异有统计学意义.
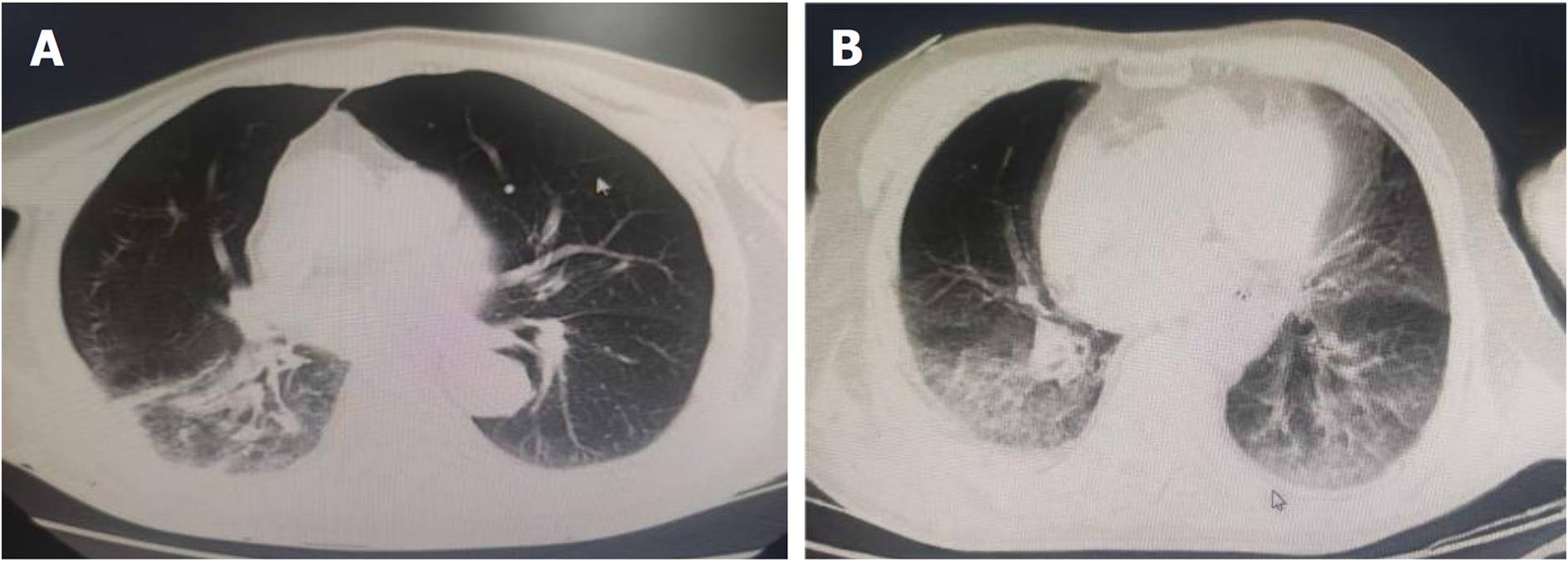
159例老年肺部感染患者, 63例出现GER, 发生率39.62%. 63例肺部感染合并GER患者临床均表现出发热、呼吸急促及双肺干湿啰音, 多数患者出现剧烈咳嗽、反酸、烧心, 部分患者伴有发绀、胸痛、咳痰伴痰中带血、低氧血症. 且96.83%患者WBC升高, 95.24% CRP升高, 36.51% ESR升高. 影像学检查显示, 26例(41.27%)单侧肺不张, 39例(61.90%)双肺多发斑片影, 以中下肺野区为主. 见表1. 典型病例见图1. 同时病原菌分布中, 159例老年肺部感染中细菌感染63例(39.62%)(以革兰氏阴性菌62.20%为主), 病毒感染51例(32.08%), 支原体感染31例(19.50%), 另有14例为混合感染(8.81%).
| 临床特征 | 例数 | 构成比(%) |
| 临床表现 | ||
| 呼吸急促 | 63 | 100.00 |
| 发热 | 63 | 100.00 |
| 双肺干湿啰音 | 63 | 100.00 |
| 反酸 | 60 | 95.24 |
| 烧心 | 59 | 93.65 |
| 发绀 | 26 | 41.27 |
| 剧烈咳嗽 | 57 | 90.48 |
| 胸痛 | 7 | 11.11 |
| 咳痰伴痰中带血 | 23 | 36.51 |
| 低氧血症 | 14 | 22.22 |
| 实验室检查 | ||
| WBC升高 | 61 | 96.83 |
| CRP升高 | 60 | 95.24 |
| ESR升高 | 23 | 36.51 |
| 影像学检查结果 | ||
| 单侧肺不张 | 26 | 41.27 |
| 双肺多发斑片影 | 39 | 61.90 |
两组在年龄、肺部感染严重程度、糖尿病病史、睡眠障碍、焦虑情绪、机械通气、既往GER疾病史、服用镇静药方面对比, 差异有统计学意义(P<0.05). 见表2.
| 资料 | 研究组(n = 63) | 对照组(n = 96) | t/χ2 | P值 |
| 性别 | 0.118 | 0.731 | ||
| 男 | 26(41.27) | 37(38.54) | ||
| 女 | 37(58.73) | 59(61.46) | ||
| 年龄 | 75.15±4.59 | 72.14±5.03 | 3.819 | <0.001 |
| 肺部感染严重程度 | 6.323 | 0.013 | ||
| 中度 | 24(38.10) | 56(58.33) | ||
| 重度 | 39(61.90) | 40(41.67) | ||
| BMI | 21.05±1.61 | 20.89±1.55 | 0.627 | 0.532 |
| 吸烟史 | 1.146 | 0.284 | ||
| 有 | 29(46.03) | 36(37.50) | ||
| 无 | 34(53.97) | 60(62.50) | ||
| 饮酒史 | 0.229 | 0.633 | ||
| 有 | 20(31.75) | 34(35.42) | ||
| 无 | 43(68.25) | 62(64.58) | ||
| 高血压病史 | 0.321 | 0.571 | ||
| 有 | 26(41.27) | 44(45.83) | ||
| 无 | 37(58.73) | 52(54.17) | ||
| 糖尿病病史 | 8.669 | 0.003 | ||
| 有 | 33(52.38) | 28(28.17) | ||
| 无 | 30(47.62) | 68(70.83) | ||
| H. pylori感染 | 0.233 | 0.629 | ||
| 有 | 22(34.92) | 30(31.25) | ||
| 无 | 41(65.08) | 66(68.75) | ||
| 睡眠障碍 | 7.395 | 0.007 | ||
| 有 | 34(53.97) | 31(32.29) | ||
| 无 | 29(46.03) | 65(67.71) | ||
| 焦虑情绪 | 4.069 | 0.044 | ||
| 有 | 23(36.51) | 21(21.88) | ||
| 无 | 40(63.49) | 75(78.13) | ||
| 服用镇静药 | 4.049 | 0.044 | ||
| 有 | 26(41.27) | 25(26.04) | ||
| 无 | 37(58.73) | 71(73.96) | ||
| 机械通气 | 4.243 | 0.039 | ||
| 有 | 32(50.79) | 33(34.38) | ||
| 无 | 31(49.21) | 63(65.63) | ||
| 鼻饲管喂养 | 2.122 | 0.145 | ||
| 有 | 33(52.38) | 39(40.63) | ||
| 无 | 30(47.62) | 57(59.38) | ||
| 既往GER疾病史 | 14.143 | <0.001 | ||
| 有 | 38(60.32) | 29(30.21) | ||
| 无 | 25(39.68) | 67(69.79) | ||
| 感染类型 | 2.363 | 0.501 | ||
| 细菌感染 | 27(42.86) | 36(37.50) | ||
| 病毒感染 | 20(31.75) | 31(32.29) | ||
| 混合感染 | 7(11.11) | 7(7.29) | ||
| 支原体感染 | 9(14.29) | 22(22.92) | ||
| 实验室指标 | ||||
| WBC(×109/L) | 18.15±3.26 | 17.44±2.95 | 1.424 | 0.157 |
| 中性粒细胞(%) | 86.15±6.15 | 84.98±6.51 | 1.133 | 0.259 |
| CRP(mg/L) | 20.15±5.48 | 18.91±6.01 | 1.317 | 0.190 |
| PCT(mg/ml) | 0.82±0.11 | 0.79±0.14 | 1.434 | 0.153 |
| ESR(mm/h) | 24.15±3.45 | 23.94±4.01 | 0.341 | 0.734 |
以老年肺部感染患者是否合并GER为因变量(是 = 1, 否 = 0), 以表2中差异有统计学意义的指标(8个)作为自变量, 赋值见表3, 进入Logistic回归分析, 结果显示, 年龄、肺部感染严重程度、糖尿病病史、睡眠障碍、焦虑情绪、既往GER疾病史是老年肺部感染患者合并GER的独立影响因素(P<0.05), 见表4.
| 变量 | 序号 | 变量赋值 |
| 年龄 | X1 | 原值代入 |
| 肺部感染严重程度 | X2 | 中度 = 1, 重度 = 2 |
| 糖尿病病史 | X3 | 有 = 1, 无 = 0 |
| 睡眠障碍 | X4 | 有 = 1, 无 = 0 |
| 焦虑情绪 | X5 | 有 = 1, 无 = 0 |
| 机械通气 | X6 | 有 = 1, 无 = 0 |
| 服用镇静药 | X7 | 有 = 1, 无 = 0 |
| 既往GER疾病史 | X8 | 有 = 1, 无 = 0 |
| 影响因素 | β | SE | Wald/χ2值 | P值 | OR值 | 95%CI | |
| 下限 | 上限 | ||||||
| 年龄 | 0.077 | 0.608 | 0.016 | 0.023 | 1.080 | 1.005 | 1.160 |
| 肺部感染严重程度 | 1.020 | 0.558 | 3.343 | <0.001 | 2.774 | 1.445 | 5.325 |
| 糖尿病病史 | 0.586 | 0.620 | 0.894 | <0.001 | 1.797 | 1.036 | 3.118 |
| 睡眠障碍 | 0.570 | 0.489 | 1.360 | <0.001 | 1.769 | 1.02 | 3.067 |
| 焦虑情绪 | 0.435 | 0.581 | 0.560 | 0.011 | 1.544 | 1.201 | 1.986 |
| 机械通气 | 0.970 | 0.519 | 3.491 | 0.082 | 2.637 | 0.856 | 8.125 |
| 服用镇静药 | 0.374 | 0.489 | 0.584 | 0.193 | 1.453 | 0.689 | 3.064 |
| 既往GER疾病史 | 1.738 | 0.660 | 6.932 | <0.001 | 5.684 | 3.159 | 10.228 |
| Logit(P) | -8.456 | 0.541 | 6.459 | <0.001 | |||
目前GER与呼吸道疾病的关系受到临床关注, 老年肺部感染患者因生理机能降低, 病情多较为严重, 一旦出现GER, 不仅伴随烧心、胸骨后疼痛及上腹疼痛等症状, 极大影响患者躯体舒适度, 严重者还可能引发上消化道出血, 加重肺部感染, 造成不良预后[18]. 如何有效识别老年肺部感染合并GER的危险因素仍待大量研究予以探索.
本研究结果显示, 159例老年肺部感染患者中有63例出现GER, 发生率39.62%, 低于苑丽双等[10]关于小儿肺炎合并GER的调查数据(57.90%). 研究对象不同, 可能造成结果差异, 但仍能发现老年肺部感染患者出现GER的风险较高. 本研究中病原体感染以细菌感染为主, 其次为病毒性感染、支原体感染, 另有14例混合感染, 其中细菌感染主要以革兰氏阴性菌感染为主, 与既往调查结果[19,20]相似. 且单因素分析显示, 研究组、对照组感染类型对比, 差异无统计学意义(P>0.05), 提示, 不同病原体感染不会对GER的发生造成明显影响. 同时63例老年肺部感染合并GER患者临床均出现呼吸急促、发热及双肺干湿啰音的症状, 此外反酸、烧心、剧烈咳嗽发生率较高, 分别为95.24%、93.65%、90.48%, 实验室数据分析显示, 多数患者出现WBC、CRP升高, 且影像学检查显示患者存在不同程度的肺组织损伤. 可见, 老年肺部感染合并GER的临床症状具有一定特异性, 医护工作者需及时观察以发现相关症状, 做好风险管控.
经Logistic回归分析显示, 年龄、糖尿病病史、睡眠障碍、肺部感染严重程度、焦虑情绪、既往GER疾病史是老年肺部感染患者合并GER的影响因素(P<0.05). (1)随着老年肺部感染患者年龄增加, 其出现GER的风险升高. 王伟等[21]研究也表示, 年龄越高, 出现GER病风险越高. 老年患者生理机能呈退行性减退, 因食管下括约肌、膈肌功能减弱, 抗反流防御功能降低, 同时存在胃肠蠕动能力下降, 消化吸收功能减退的情况[22]. 加之肺部感染, 非自主性的咳嗽、呼吸急促等症状会增加腹内压, 影响食管下括约肌的闭合功能, 增加反流风险[23]; (2)目前糖尿病与GER的关系存在一定争议, 尚缺乏糖尿病患者发生GER的大规模流行病学调查数据. 一项国外的孟德尔随机化研究[24]指出, 2型糖尿病的遗传易感性与多种胃肠疾病有关, 每增加一个自然对数单位, GER病的OR值增加6%. Yuan等[25]学者在相关研究中明确指出, 糖尿病与GER病有关. 本研究也发现, 糖尿病病史是老年肺部感染患者合并GER的独立影响因素. 分析原因可能是, 长期高血糖环境会引起微血管病变, 其中迷走神经损伤是常见自主神经病变, 会影响食管运动及感觉功能, 导致胃排空延迟, 延长内容物滞留时间, 增加反流风险[26]. 且高血糖环境更利于病原菌增殖, 会加重肺部感染严重程度, 可能诱发机会性感染, 其与胃食管功能障碍协同破坏胃肠道屏现异常反流的风险是无睡眠障碍患者的1.223倍. 另有学者[27]在研究中表示夜间入睡晚、夜间睡眠时间短与GER病风险升高相关. 本研究在肺部感染合并GER患者中发现相似结论. 存在睡眠障碍的老年肺部感染患者一方面存在呼吸系统症状, 频繁的咳嗽或排痰等会增大胃肠压力, 另一方面睡眠质量差可能伴随着失眠、睡眠呼吸暂停等症状, 昼夜节律紊乱, 影响食管功能, 引起感知异常, 增加GER发生概率[28]; (3)钱栋等[29]研究表示, 睡眠障碍患者出, 阻碍机体功能恢复, 继而削弱胃食管黏膜防御, 若患者睡眠呼吸暂停症状较严重, 不定时用力吸气, 更易诱发胃内容物反流[30,31]; (4)GER引起烧心、胸痛等症状, 会降低患者躯体舒适度, 引发不良情绪, 已有研究证实[32], GER病与患者精神心理因素相关. 本研究中存在焦虑情绪的肺部感染老年患者出现GER的风险是无焦虑情绪患者的1.544倍. 焦虑状态下患者交感神经兴奋抑制迷走神经活性, 影响食管蠕动功能, 还可能通过脑-肠轴介导神经递质分泌路径继而诱发食管内脏高敏感性, 降低胃肠道功能, 增加GER风险[33]; (5)既往存在GER病史的老年肺部感染患者往往存在食管防御机制障碍, 本身存在较高的反流易感性, 在肺部感染的特殊情况下, 更易诱发食管下括约肌松弛, 引起GER[34]. 且此类患者因频繁的胃内容物反流, 造成食管黏膜损伤, 肺部感染、食管损伤多重不良因素相互交织增加病危风险; (6)本研究中患者病情严重程度与GER相关. 严重肺部感染引起剧烈咳嗽导致胸腹内压急剧升高, 可能压迫胃肠内容物逆向流入食管, 且重度肺部感染患者卧床时间更长, 长期平卧位减弱了重力抗反流作用, 后增加反流风险[35,36]. 有研究发现[37], 俯卧位通气持续时长为≥12 h且不足16 h的重症肺炎患者反流发生率低于时长≥16 h的患者. 同时食物反流会刺激迷走神经, 迷走神经负责调控食管下段及支气管功能, 受到胃部内容物刺激后会引发气管痉挛, 加重呼吸困难症状, 会延缓患者病情恢复. 可见GER与肺部感染存在密切相互作用相关. 临床需警惕存在危险因素的老年肺部感染患者出现反流的情况, 可通过体位调整、药物干预等降低反流发生率.
综上所述, 老年肺部感染患者合并GER患者的临床特征存在一定特异性, 合并GER的影响因素有焦虑情绪、年龄、睡眠障碍、糖尿病病史、肺部感染严重程度、既往GER疾病史, 提示临床不仅需不断精进个体化治疗方案以控制基础病情, 帮助患者度过危险期, 同时还需关注患者睡眠及情绪状态等, 以通过全方位干预措施降低GER的发生. 本研究初次对老年肺部感染合并GER的影响因素进行分析, 纳入指标较为全面, 包括病情资料、生活习惯、实验室指标等, 为本文的创新之处, 但本次研究单中心选例、样本量较少, 未来还需大量开展大样本量、多中心研究以验证本文结论.
目前胃食管反流(gastroesophageal reflux, GER)与呼吸系统疾病的相关性已得到充足证据支持. 尤其老年患者身体抵抗力降低, 肺部感染继发GER后, 因反流物进入气道, 微量吸入即可能损伤呼吸黏膜, 破坏纤毛清除功能, 诱发气道炎症, 且食管反流会刺激迷走神经, 引起气管痉挛, 进一步加重感染程度, 导致不良转归, 甚至危及患者生命安全.
及时识别肺部感染后出现GER的风险对临床循证实施个体化干预措施具有重要指导价值. 目前临床已有学者对肺部感染、GER单一病种的特征及影响因素进行分析, 但缺乏老年肺部感染合并GER患者的相关报告, 此类患者在风险防控上是否具备特异性尚待研究予以论证.
观察老年肺部感染合并GER的临床特征, 并分析其影响因素.
选取2021-01/2024-08就诊于义乌中西医结合医院的159例老年肺部感染患者为研究对象, 观察老年肺部感染合并GER患者的临床特征, 并统计发生率, 依据是否合并GER分为研究组、对照组, 对比两组临床资料, 采用Logistic回归分析老年肺部感染合并GER的影响因素.
老年肺部感染合并GER的影响因素, 并对其临床特征进行分析, 为完善干预路径提供支持.
老年肺部感染合并GER患者临床症状及体征具有一定特异性, 患者合并GER的独立危险因素包括肺部感染严重程度、焦虑情绪、年龄、既往GER疾病史、睡眠障碍、糖尿病病史, 临床工作者可加强对高危患者的针对性干预以减少GER的发生.
本研究初次对老年肺部感染合并GER的影响因素进行分析, 纳入指标较为全面, 包括病情资料、生活习惯、实验室指标等, 为本文的创新之处, 但本次研究单中心选例、样本量较少, 未来还需大量开展大样本量、多中心研究以验证本文结论.
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C, C, C
D级 (一般): D
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁
| 1. | Cutajar J, Gkrania-Klotsas E, Sander C, Floto A, Chandra A, Manson A, Kumararatne D. Respiratory infectious burden in a cohort of antibody deficiency patients treated with immunoglobulin replacement therapy: The impact of lung pathology and gastroesophageal reflux disease. J Allergy Clin Immunol Glob. 2023;2:100133. [PubMed] [DOI] |
| 2. | Won EJ, Lee YJ, Kim MJ, Kim TJ, Shin HJ, Kim TO, Kwon YS. Lower respiratory tract microbiota in patients with clinically suspected nontuberculous mycobacterial pulmonary disease according to the presence of gastroesophageal reflux. PLoS One. 2024;19:e0309446. [PubMed] [DOI] |
| 4. | Dong R, Zhang Q, Peng H. Gastroesophageal reflux disease and the risk of respiratory diseases: a Mendelian randomization study. J Transl Med. 2024;22:60. [PubMed] [DOI] |
| 5. | Zhang L, Aierken A, Zhang M, Qiu Z. Pathogenesis and management of gastroesophageal reflux disease-associated cough: a narrative review. J Thorac Dis. 2023;15:2314-2323. [PubMed] [DOI] |
| 6. | Kim Y, Yoon JH, Ryu J, Yang B, Chung SJ, Kang HK, Park DW, Park TS, Moon JY, Kim TH, Kim SH, Sohn JW, Yoon HJ, Lee H, Choi H. Gastroesophageal Reflux Disease Increases Susceptibility to Nontuberculous Mycobacterial Pulmonary Disease. Chest. 2023;163:270-280. [DOI] |
| 9. | 中华医学会; 中华医学会杂志社; 中华医学会全科医学分会; 中华医学会呼吸病学分会肺部感染学组; 中华医学会《中华全科医师杂志》编辑委员会; 呼吸系统疾病基层诊疗指南编写专家组. 成人社区获得性肺炎基层诊疗指南(2018年). 中华全科医师杂志. 2019;18:117-126. [DOI] |
| 11. | 中国医疗保健国际交流促进会胃食管反流多学科分会. 中国胃食管反流病多学科诊疗共识. 中华胃食管反流病电子杂志. 2020;7:1-28. [DOI] |
| 12. | Gelaidan A, Almaimani M, Alorfi YA, Alqahtani A, Alaklabi NG, Alshamrani SM, Rambo R, Mujahed JA, Alsulami RY, Namenkani M. Comparative Effectiveness of CURB-65 and qSOFA Scores in Predicting Pneumonia Outcomes: A Systematic Review. Cureus. 2024;16:e71394. [PubMed] [DOI] |
| 13. | 国家卫生健康委员会疾病预防控制局; 国家心血管病中心; 中国医学科学院阜外医院; 中国疾病预防控制中心; 中华医学会心血管病学分会; 中国医师协会高血压专业委员会; 中国体育科学学会; 中国营养学会; 中国卒中学会; 中华心血管病杂志编辑委员会. 中国高血压健康管理规范(2019). 中华心血管病杂志. 2020;48:10-46. [DOI] |
| 15. | Bellofatto M, Gentile L, Bertini A, Tramacere I, Manganelli F, Fabrizi GM, Schenone A, Santoro L, Cavallaro T, Grandis M, Previtali SC, Scarlato M, Allegri I, Padua L, Pazzaglia C, Villani F, Cavalca E, Saveri P, Quattrone A, Valentino P, Tozza S, Russo M, Mazzeo A, Vita G, Piacentini S, Didato G, Pisciotta C, Pareyson D, Italian C. M. T. Network. Daytime sleepiness and sleep quality in Charcot-Marie-Tooth disease. J Neurol. 2023;270:5561-5568. [PubMed] [DOI] |
| 16. | Tiksnadi BB, Triani N, Fihaya FY, Turu' Allo IJ, Iskandar S, Putri DAE. Validation of Hospital Anxiety and Depression Scale in an Indonesian population: a scale adaptation study. Fam Med Community Health. 2023;11:e001775. [PubMed] [DOI] |
| 17. | 尚 红, 王 毓三, 申 子瑜. 全国临床检验操作规程. 4版. 北京: 人民卫生出版社 2015: 171-172. |
| 18. | 张 利, 张 梦茹, 阿丽米热· 艾尔肯, 邱 忠民. 咽喉反流性疾病在常见呼吸道疾病中的作用. 山东大学耳鼻喉眼学报. 2024;38:23-29. [DOI] |
| 21. | 王 伟刚, 赵 福坤, 朱 祥, 董 鹤翔, 蒋 维荣, 刘 芸, 张 晓贝, 任 程晖, 曹 栋, 俞 永江. 甘肃省胃食管反流病流行病学调查及其危险因素分析. 中国预防医学杂志. 2024;25:349-356. [DOI] |
| 22. | Radaelli A, Mancia G, Balestri G, Bonfanti D, Castiglioni P. Respiratory patterns and baroreflex function in heart failure. Sci Rep. 2023;13:2220. [PubMed] [DOI] |
| 23. | Kang J, Lee R, Lee SW. Effects of gastroesophageal reflux disease treatment with proton pump inhibitors on the risk of acute exacerbation and pneumonia in patients with COPD. Respir Res. 2023;24:75. [PubMed] [DOI] |
| 24. | Chen J, Yuan S, Fu T, Ruan X, Qiao J, Wang X, Li X, Gill D, Burgess S, Giovannucci EL, Larsson SC. Gastrointestinal Consequences of Type 2 Diabetes Mellitus and Impaired Glycemic Homeostasis: A Mendelian Randomization Study. Diabetes Care. 2023;46:828-835. [PubMed] [DOI] |
| 25. | Yuan S, Larsson SC. Adiposity, diabetes, lifestyle factors and risk of gastroesophageal reflux disease: a Mendelian randomization study. Eur J Epidemiol. 2022;37:747-754. [PubMed] [DOI] |
| 26. | Kuznetsov KO, Mikheeva AJ, Ishmukhametova AA, Tolstykh TA, Gallyametdinova AR, Botirova ZU, Zabirova AA, Sharipova AS, Shaikhlislamova AB, Abdrakhmanova DR. [Diabetic gastroenteropathy: modern methods of diagnosis and treatment]. Probl Endokrinol (Mosk). 2022;68:67-78. [PubMed] [DOI] |
| 28. | Hsu WH, Geng JH, Wu PY, Huang JC, Kuo CH, Chen SC. Metabolic syndrome is associated with gastroesophageal reflux disease in a large Taiwanese population study. Int J Med Sci. 2025;22:1555-1561. [PubMed] [DOI] |
| 30. | Tan X, Wang S, Wu F, Zhu J. Bidirectional correlation between gastroesophageal reflux disease and sleep problems: a systematic review and meta-analysis. Peer J. 2024;12:e17202. [PubMed] [DOI] |
| 31. | Thomas DC, Colonna A, Manfredini D. Obstructive sleep apnoea, sleep bruxism and gastroesophageal reflux - mutually interacting conditions? A literature review. Aust Dent J. 2024;69 Suppl 1:S38-S44. [PubMed] [DOI] |
| 35. | Uraguchi K, Matsumoto N, Mitsuhashi T, Takao S, Makihara S, Ando M, Yorifuji T. Association Between Dinner-to-Bed Time and Gastroesophageal Reflux-Related Diseases in Children. Cureus. 2025;17:e77709. [PubMed] [DOI] |
| 36. | You D, Wu Y, Lu M, Shao F, Tang Y, Liu S, Liu L, Zhou Z, Zhang R, Shen S, Lange T, Xu H, Ma H, Yin Y, Shen H, Chen F, Christiani DC, Jin G, Zhao Y. A genome-wide cross-trait analysis characterizes the shared genetic architecture between lung and gastrointestinal diseases. Nat Commun. 2025;16:3032. [PubMed] [DOI] |