修回日期: 2022-02-28
接受日期: 2022-03-26
在线出版日期: 2022-04-08
阿仑膦酸钠引起的食管炎是一种临床少见的药物性食管炎疾病, 随着该药的广泛应用, 食管不良反应事件有所增多, 部分内镜医师对该病的认识相对不足, 无法及时明确病因.
本文报道了1例因胸痛就诊的患者, 通过结合病史及典型内镜下表现确诊了阿仑膦酸钠相关药物性食管炎, 去除病因, 避免了进一步食管损伤.
该病重在预防和及时诊断, 详尽的病史、典型的内镜下表现和病理学特征有助于及早确诊.
核心提要: 阿仑膦酸钠相关药物性食管炎疾病, 具有独特的内镜下表现和病理学特征, 重在预防和及时诊断. 本病例典型的内镜下表现和病理学特征可加强临床医师对该病的认识, 减少漏诊和误诊.
引文著录: 王安华, 郇通, 范震. 阿仑膦酸钠相关药物性食管炎1例. 世界华人消化杂志 2022; 30(7): 336-340
Revised: February 28, 2022
Accepted: March 26, 2022
Published online: April 8, 2022
Alendronate-induced esophagitis is a rare form of pill esophagitis. With the wide application of alendronate, the incidence of adverse events affecting the esophagus has increased; however, some endoscopists have a relatively insufficient understanding of the disease and cannot identify the cause in time.
A woman presented with chest pain and she was diagnosed with alendronate-associated pill esophagitis by the medical history and typical endoscopic findings, thus removing the cause and avoiding further esophageal injury.
Alendronate-associated pill esophagitis relies on prevention and timely diagnosis. A detailed medical history, typical endoscopic manifestations, and pathological features are helpful for early diagnosis.
- Citation: Wang AH, Xun T, Fan Z. Alendronate-induced pill esophagitis: A case report. Shijie Huaren Xiaohua Zazhi 2022; 30(7): 336-340
- URL: https://www.wjgnet.com/1009-3079/full/v30/i7/336.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v30.i7.336
阿仑膦酸钠自1995年在美国上市以来, 已被广泛用于治疗佩吉特骨病、糖皮质激素诱发的骨质疏松症和绝经后骨质疏松症[1], 它是首个获得美国食品与药物管理局批准用于治疗绝经后骨质疏松症的双膦酸盐类药物, 其可直接抑制破骨细胞, 促进破骨细胞凋亡, 进而降低骨转换, 明显增加绝经后骨质疏松症患者的骨密度, 减少骨折发生[2]. 虽然已显示其预防和治疗疾病的功效, 但国外有病例报告描述了使用该药物对上消化道的损害, 特别是糜烂性或溃疡性食管炎.近年来随着我国步入老龄化社会, 阿仑膦酸钠的应用日益广泛, 由此引发的药物性食管炎有所增多, 部分内镜医师对该病的认识不足, 现结合国内外文献将我院收治的1例阿仑膦酸钠相关药物性食管炎患者的诊疗过程并文献复习报道如下.
患者, 女, 62岁. 患者因"胸骨后疼痛不适3天"就诊, 自述3天前开始出现持续性下段胸骨后胀痛不适, 进食时加重, 有哽咽感, 无反酸嗳气、呕血黑便、咳嗽咳痰、呼吸困难等不适症状, 起病前无腐蚀性物质、异物吞咽史, 近期无体重下降. 既往史: 6年前因甲状腺部分切除术后继发性甲状腺功能减退, 长期口服左甲状腺素钠125 ug qd补充治疗.1周前外院诊断为"骨质疏松症", 予以口服阿仑膦酸钠1片qw治疗.体格检查: 体温38.1 ℃, 余无特殊.
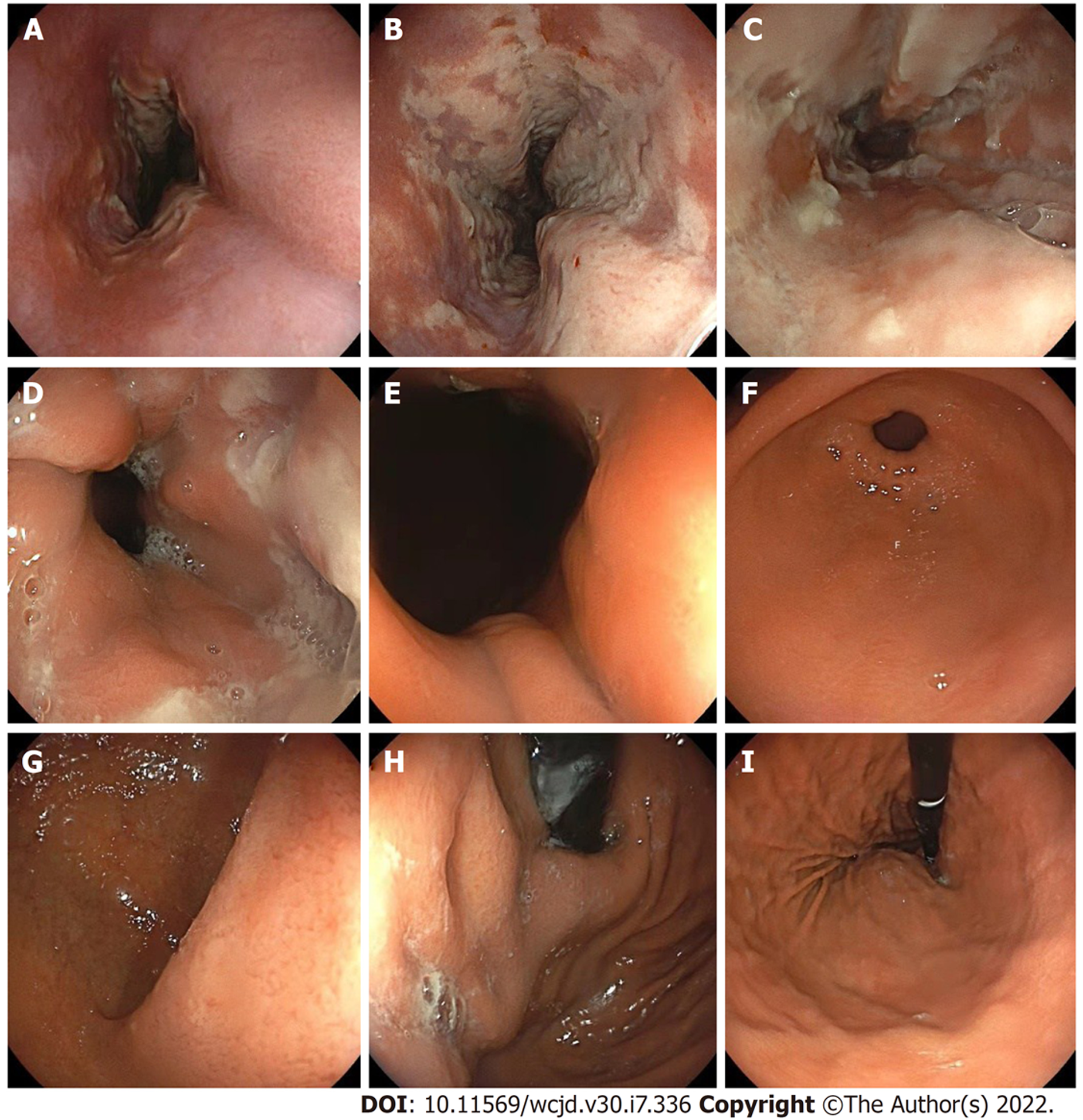
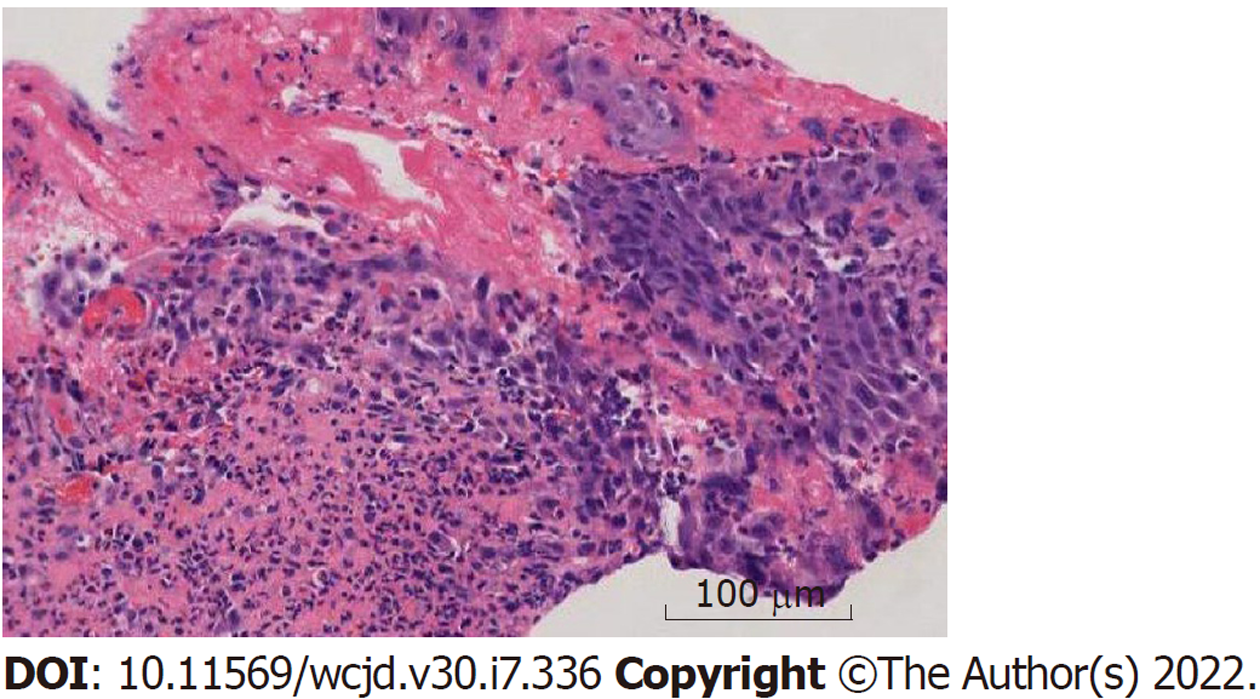
(1)血常规WBC 13.1×109/L, N% 77.7%, Hb 146 g/L, CRP 25 mg/L; 血生化、心肌酶、TNI、凝血功能、肿瘤标记物均未见异常; 常规心电图及胸部CT平扫未见异常; (2)无痛电子胃镜检查(图1A-I): 食管上段黏膜未见异常, 距门齿23 cm-40 cm可见黏膜广泛发红、糜烂、伴深浅不一的溃疡形成, 呈全周性, 表面有厚薄不均的白色渗出液松散粘附, 具有伪膜样外观, 节段性病变与正常黏膜界限清晰.病变节段内可见散布小片状正常黏膜. 食管内腔轻度相对狭窄, 溃疡段内镜通过顺畅, 予多处活检. 胃部及十二指肠未见明显异常. 组织病理结果(图2): 炎性坏死组织伴肉芽组织增生, 少许肿大、深染的多核鳞状上皮巨细胞伴中性粒细胞浸润.
(1)阿仑膦酸钠相关药物性食管炎; (2)骨质疏松症; (3)甲状腺切除术后.
患者入院后予以禁食、抑酸、头孢他啶抗感染及营养支持等治疗. 次日行内镜检查, 发现后食管黏膜损伤呈节段性病变, 并呈全周性, 与正常部位界限清晰, 追问病史, 得知患者口服阿仑膦酸钠时饮水不足50 mL. 明确诊断后, 嘱其停服阿仑膦酸钠, 开放流质饮食, 加用硫糖铝口服混悬液保护食管黏膜.
第4天患者体温及血象均回复正常, 可进食半流质饮食, 予以出院. 出院1个月后患者门诊随访未有胸痛、吞咽困难等症状.
阿仑膦酸钠引起的食管炎是一种临床少见的药物性食管炎, 可见于服用双膦酸盐治疗绝经后骨质疏松症的女性. 国外一项对阿仑膦酸盐全球上市后监测数据进行的大型回顾表明, 0.04%(199/475000)的治疗者出现了与食道相关的不良反应[3]. 但另一方面, 多项随机双盲对照试验表明[4,5], 若遵嘱规范服用, 接受阿仑膦酸盐治疗的患者其上消化道不良反应的总体发生率与接受安慰剂的患者相似.这些结果表明食道不良反应只发生在很小的范围内且多与不恰当的服用方法密切相关.
食管损伤的临床症状包括吞咽疼痛、吞咽困难、胸骨后胸痛、上腹痛和呕血等.根据既往的病例报道, 症状通常在服药开始后的数天至数周内被发现, 大多数病例在半月内即可痊愈, 亦有个例报道[10]口服药物长达10个月才发现食管损伤, 并最终因为食管狭窄而行外科手术治疗. 本病例为初次口服阿仑膦酸钠即出现明显吞咽疼痛症状就诊, 及时停服药物后, 门诊复诊未出现食管狭窄等相关后遗症.因此, 该病诊疗最重要的便是及时发现真正的病因, 避免药物引起再次损伤, 如有可能应停用口服药物, 所以消化内科医师应深化对该食管炎的认识.
目前其发病机制被认为主要是由于食管黏膜长期接触药物溶解时产生的高浓度腐蚀性物质, 引起化学性损伤. Abraham等[6]和Ribeiro等[7]报道的案例中, 绝大多数组织病理学发现溃疡部位有肉芽组织和炎性渗出物, 这与本病例的结果一致. Abraham等[6]发现, 60%的活检组织中含有可极化异物, 这些异物具有清晰、折射、结晶状的外观, 并与炎性渗出物混合在一起, 提示药物与黏膜之间的接触时间延长. Ribeiro等[7]则进一步证实该双折射结晶物质确为药物碎屑, 从而提出大多数阿仑膦酸盐引起的食管粘膜损伤是由于长时间接触药物造成的. 本病例中患者不规范的药物服用史及被正常黏膜包围的节段性食管炎侧面证实了该机制.
另一种可能引起食管损伤的机制与胃食管反流病有关. 当pH高于3.5时, 阿仑膦酸盐以单钠盐形式存在; 然而, 当pH低于2时, 它主要以游离酸的形式存在, 对黏膜更具刺激性[8]. 因此, 尤其是在服用片剂后没有保持直立状态30 min的患者中, 被胃酸溶解的阿仑膦酸钠可能会通过反流对食管远端造成特定的毒性. 这解释了为什么部分病例报告中活检染色未发现片状结晶物质. 近年还有学者研究[9]提出发病机制可能与T细胞介导的迟发型超敏反应有关, 但需进一步研究证实.
该药物性食管炎通常具有独特的内镜表现, 呈节段性的广泛的糜烂、溃疡和表面覆有致密的炎性渗出物组成的松散粘连的假膜. 由本病例图片可见, 食管节段性的黏膜广泛发红、糜烂、伴深浅不一的溃疡形成, 呈全周性, 沿食管壁环形分布或对吻分布, 大小不等, 部分溃疡有融合, 溃疡边界清楚, 整体呈花斑样改变(图1B)和表面覆盖着一种突出的、稠密厚实的白色伪膜样渗出物松散粘连(图1C). 病变黏膜两端存在正常黏膜, 界限清晰(图1A和1D). 病变节段内可见散布小片状正常黏膜(图1C)及程度不一的黏膜损伤进一步证实了药物长期接触是该病的主要致病机制. 食管损伤通常位于食管中下端, 自食管第二生理狭窄食物易滞留处起始, 这与上文提到的发病机制有关. 阿仑膦酸盐相关性食管炎的渗出液在内镜下的表现与反流性食管炎显著不同, 结合黏膜完整的远端食管可以排除胃食管反流病引起的食管炎.
已报道的阿仑膦酸钠相关药物性食管炎的病理特征多为非特异性炎性改变, 显微镜下可见肉芽组织, 纤维素性炎性渗出物和病变部位附近肿大、深染的多核鳞状上皮巨细胞[2]. 部分活检标本中存在折光结晶物质. Gómez等[2]对1例病例的报道发现, 除上述病理特征外该病还具有独特的组织病理学改变: 散在的角化异常细胞(特征为散在的嗜酸性包涵体或凋亡小体)和其靠近黏膜的基底层(而非管腔侧)可见巨大的、奇异的鳞状上皮细胞, 但需更多案例加以证实.
详细的病史和上消化道镜检是诊断的关键. 而组织病理活检可明确食管非特异性炎症改变和结晶样物质的存在, 以及排除病毒、真菌和细菌感染, 都有助于确诊阿仑膦酸钠相关性食管炎. 明确诊断后, 立即停用阿仑膦酸钠, 必要时加用抑酸剂和黏膜保护剂等治疗, 多数患者可于1月内痊愈, 长期服用导致损伤者可能会遗留有不同程度的食管狭窄.为减少可能存在的食管损伤风险, 贲门失弛缓症和其他食管动力障碍、食管狭窄或已有重度反流性食管炎患者应避免服用双膦酸盐类药物. 同时, 应用非甾体抗炎药的患者需谨慎使用双膦酸盐类口服药物. 有研究表明[11], 这两种药物对溃疡形成具有协同作用. 为尽量减少食管损伤, 我们建议患者应于早餐前半小时服用双膦酸盐片剂, 并用至少180 mL-240 mL的水送服, 在吞咽片剂后保持直立姿势至少30 min[12].
总之, 阿仑膦酸钠相关药物性食管炎重在预防和及时诊断, 国内未见相似报道, 本病例典型的内镜下表现和病理学特征可加强临床医师对该病的认识, 减少漏诊和误诊.
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C
D级 (一般): D, D
E级 (差): 0
科学编辑: 张砚梁 制作编辑:张砚梁
| 1. | Liberman UA, Weiss SR, Bröll J, Minne HW, Quan H, Bell NH, Rodriguez-Portales J, Downs RW, Dequeker J, Favus M. Effect of oral alendronate on bone mineral density and the incidence of fractures in postmenopausal osteoporosis. The Alendronate Phase III Osteoporosis Treatment Study Group. N Engl J Med. 1995;333:1437-1443. [PubMed] [DOI] |
| 2. | Gómez V, Xiao SY. Alendronate-induced esophagitis in an elderly woman. Int J Clin Exp Pathol. 2009;2:200-203. [PubMed] |
| 3. | de Groen PC, Lubbe DF, Hirsch LJ, Daifotis A, Stephenson W, Freedholm D, Pryor-Tillotson S, Seleznick MJ, Pinkas H, Wang KK. Esophagitis associated with the use of alendronate. N Engl J Med. 1996;335:1016-1021. [PubMed] [DOI] |
| 4. | Lanza F, Sahba B, Schwartz H, Winograd S, Torosis J, Quan H, Reyes R, Musliner T, Daifotis A, Leung A. The upper GI safety and tolerability of oral alendronate at a dose of 70 milligrams once weekly: a placebo-controlled endoscopy study. Am J Gastroenterol. 2002;97:58-64. [PubMed] [DOI] |
| 5. | Lowe CE, Depew WT, Vanner SJ, Paterson WG, Meddings JB. Upper gastrointestinal toxicity of alendronate. Am J Gastroenterol. 2000;95:634-640. [PubMed] [DOI] |
| 6. | Abraham SC, Cruz-Correa M, Lee LA, Yardley JH, Wu TT. Alendronate-associated esophageal injury: pathologic and endoscopic features. Mod Pathol. 1999;12:1152-1157. [PubMed] |
| 7. | Ribeiro A, DeVault KR, Wolfe JT, Stark ME. Alendronate-associated esophagitis: endoscopic and pathologic features. Gastrointest Endosc. 1998;47:525-528. [PubMed] [DOI] |
| 8. | Dobrucali A, Tobey NA, Awayda MS, Argote C, Abdulnour-Nakhoul S, Shao W, Orlando RC. Physiological and morphological effects of alendronate on rabbit esophageal epithelium. Am J Physiol Gastrointest Liver Physiol. 2002;283:G576-G586. [PubMed] [DOI] |
| 9. | Naniwa T, Maeda T, Mizoshita T, Hayami Y, Watanabe M, Banno S, Ito R. Alendronate-induced esophagitis: possible pathogenic role of hypersensitivity to alendronate. Intern Med. 2008;47:2083-2085. [PubMed] [DOI] |
| 10. | Ryan JM, Kelsey P, Ryan BM, Mueller PR. Alendronate-induced esophagitis: case report of a recently recognized form of severe esophagitis with esophageal stricture--radiographic features. Radiology. 1998;206:389-391. [PubMed] [DOI] |
| 11. | Graham DY, Malaty HM. Alendronate and naproxen are synergistic for development of gastric ulcers. Arch Intern Med. 2001;161:107-110. [PubMed] [DOI] |