修回日期: 2020-11-11
接受日期: 2020-11-26
在线出版日期: 2021-01-08
目前内镜治疗已成为治疗食管胃静脉曲张(gastroesophageal variceal, GOV)的重要手段, 尤其是内镜下精准食管胃静脉曲张断流术(endoscopic selective varices devascularition, ESVD)在临床中得到较广泛应用. 该技术要求术前精准判断GOV的来源及去路血管, 内镜治疗术中精准封堵靶血管, 要求最大程度地止血并预防术后出血. 但是如何术前寻找封堵的GOV的来源血管即靶血管, 目前尚缺乏临床指南指导也没有统一的标准, 对于内镜医生是个需要解决的难题.
观察CT门静脉成像(CT portography, CTP)指导内镜胃底曲张静脉组织胶血管内注射治疗, 精准断流的临床疗效.
单中心回顾性分析68例肝硬化食管胃底静脉曲张患者, 其中38例病人内镜治疗前进行了CTP, 为CTP指导治疗组; 同期治疗前未行CTP的对照组病人30例. 比较2组治疗后的改善率, 用胶量, 以及再出血率.
38例CTP指导治疗组患者和对照组患者治疗前后肝功能均无差异; CTP指导治疗组患者治疗前后Child-Pugh分级无差异, 对照组治疗前后 Child-Pugh有显著差异(P<0.001); CTP组用胶量1.2 mL±0.4 mL较对照组2.0±0.6 mL明显减少(P<0.001); CTP组套扎环数7.2±2.7环比对照组8.7±2.7环减少(P<0.05); CTP组3 mo内再出血率5.3% (2/38)较对照组23.3% (7/30)减少(P<0.05); CPT组改善率65.8% (25/38), 优于对照组为53.3% (16/30) (P<0.001).
CTP指导内镜胃底曲张静脉组织胶血管内注射治疗胃底静脉曲张疗效及安全性较好, 有较好的指导作用.
核心提要: 观察CT门静脉成像(CT portography, CTP)指导内镜精准断流治疗疗效. CTP可以缩小治疗范围, 聚焦靶静脉, 减少用胶量, 减少食管静脉套扎环数, 并且减少再出血率, 是内镜胃底曲张静脉精准断流治疗的参照和保障.
引文著录: 宋明全, 孙学国, 李倩, 单体栋, 沈剑华, 刘福国, 江月萍. CT门静脉成像指导内镜治疗胃底静脉曲张疗效. 世界华人消化杂志 2021; 29(1): 41-47
Revised: November 11, 2020
Accepted: November 26, 2020
Published online: January 8, 2021
Endoscopic therapy is undoubtedly beneficial in the management of esophageal and gastric varices (GOV), especially the recently widely performed endoscopic selective varices devascularization (ESVD). ESVD requires accurate determination of the source and destination of varices in pre-endoscopic therapy planning, as well as accurate blockade of variceal flow during endoscopic therapy. ESVD is now advocated as a safe procedure for prevention of variceal rebleeding and achieving adequate hemostasis. However, finding the source vessel or target vessel before operation is a difficult problem for each endoscopist, and there is still a lack of clinical guidance and unified standard in administering this therapy.
To evaluate the clinical efficacy of endoscopic injection of cyanoacrylate into gastric varices guided by CT portography (CTP), which could narrow down to exact vessels to be devasculated.
In a single-center study, a retrospective cohort of 68 cirrhosis patients with esophagogastric varices undergoing endoscopic treatment were analyzed. The patients were divided into either a CTP group with 38 cases who underwent CTP before treatment by selective varices devascularization using the sandwich method, or a control group with 30 cases who were treated by sandwich method without CTP beforehand. The main outcomes assessed were rates of improvement, efficiency, overall rebleeding, and adverse events.
There was no difference in liver function between the two groups before and after treatment; there was no difference in Child-Pugh grade in the CTP group before and after treatment, but there was a significant difference in the control group (P < 0.001). The amount of glue used in the CTP group was 1.2 ± 0.4 mL, which was significantly lower than that of the control group (2.0 ± 0.6 mL; P < 0.001). The number of ligation rings in the CTP group was less than that of the control group (7.2 ± 2.7 vs 8.7 ± 2.7, P < 0.05). The rate of rebleeding was significantly lower in the CTP group than in the control group [5.3% (2/38) vs 23.3% (7/30), P < 0.05]. The improvement rate in the CPT group was 65.8% (25/38), which was better than that of the control group [53.3% (16/30); P < 0.001).
CTP guided endoscopic injection of cyanoacrylate appears to be the preferred strategy for treatment of esophagogastric varices.
- Citation: Song MQ, Sun XG, Li Q, Shan TD, Shen JH, Liu FG, Jiang YP. CT portography guided endoscopic injection of cyanoacrylate into gastric varices. Shijie Huaren Xiaohua Zazhi 2021; 29(1): 41-47
- URL: https://www.wjgnet.com/1009-3079/full/v29/i1/41.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v29.i1.41
食管胃底静脉曲张破裂出血(esophageal gastric varices bleeding, EVB)是肝硬化严重并发症, 在临床上有较高的致残率和致死率[1,2]. 根据目前内镜精准治疗的要求, 应用最少的组织胶精准栓塞胃底曲张静脉起始血管, 既要有效阻断食管胃底血管曲张, 达到静脉曲张消失, 又要避免异位栓塞和脱胶出血等并发症. 提前预判起始血管精准栓塞, 是每位内镜医师所要解决的临床难题.
CT门静脉成像(CT portography, CTP)可以给门静脉及其分支的血管进行三维重建, 进一步明确胃底曲张静脉的起源支, 可以为内镜胃底曲张静脉硬化栓塞提供有利的指导. 本研究旨在通过对肝硬化食管胃底静脉曲张患者在内镜治疗前行CTP, 初步评估组织胶的注射部位, 以求减少注射曲张静脉的部位及组织胶用量.
回顾性总结收集2015-12/2018-07在青岛大学附属医院消化内科因肝硬化行胃镜治疗或"呕血和(或)黑便"收入院的肝硬化失代偿期合并中重度胃底静脉曲张的患者为研究对象68例, 均符合2015年中国《肝硬化门静脉高压食管胃静脉曲张出血防治指南》[3], GOV型(GOV1、GOV2)食管胃静脉曲张.根据胃底静脉直径分为Ⅰ、Ⅱ度两型, Ⅰ度为静脉直径<5 mm, Ⅱ度静脉直径≥5 mm. 患者签订了胃镜检查及治疗知情同意书, 本研究通过了青岛大学附属医院医学伦理委员会同意. 排除标准为: (1)存在常规内镜检查绝对禁忌症; (2)合并肝癌和门脉癌栓; (3)患者有其他肝脏疾病; (4)以前接受过内镜硬化套扎治疗; (5)螺旋CT门脉血管成像显示曲张静脉存在胃肾、脾肾分流; (6)孤立的胃静脉曲张(isolated gastric varicose type, IGV型); (7)未签署知情同意书者. CTP指导治疗组病人38例: 胃镜治疗前进行CTP检查, 缩小治疗的范围至胃小弯近贲门处靶血管; 同期对照组病人30例: 胃镜治疗前未行CTP检查.
仪器和设备: 电子胃镜(Olympus 290, 日本), Olympus 23G注射针, 注射针头直径 0.5 mm, 针头长度4 mm, 总长度1650 mm; α-氰基丙烯酸正丁酯, 组织胶:北京康派特医疗器械有限公司0.5 mL/支, 国械注准201736545764; 碘化油注射液: 10 mL/支, 国药准字H37022398; COOK六连发套扎器 规格型号MBL-6-F, 国械注进20163225031.
CTP应用Siemens 64层螺旋CT扫描仪, 扫描参数: 管电压120kV, 管电流250 mA, 层厚5 mm, 螺距0.983. 上腹部的扫描范围为膈顶至双侧髂嵴水平. 所检查的患者都在完成上腹部CT平扫的基础上, 应用双筒高压注射器以3.0 mL/s的速率经前臂静脉留置针注入总量为80-100 mL (1.5 mL/kg)的非离子型造影剂碘海醇(300 mgI/mL), 行动脉期(20 s)、门静脉期(60 s)和平衡期(120 s)动态增强扫描.通过软件的三维重建系统观察肝门静脉主干、胃左静脉、胃短/胃后静脉等.
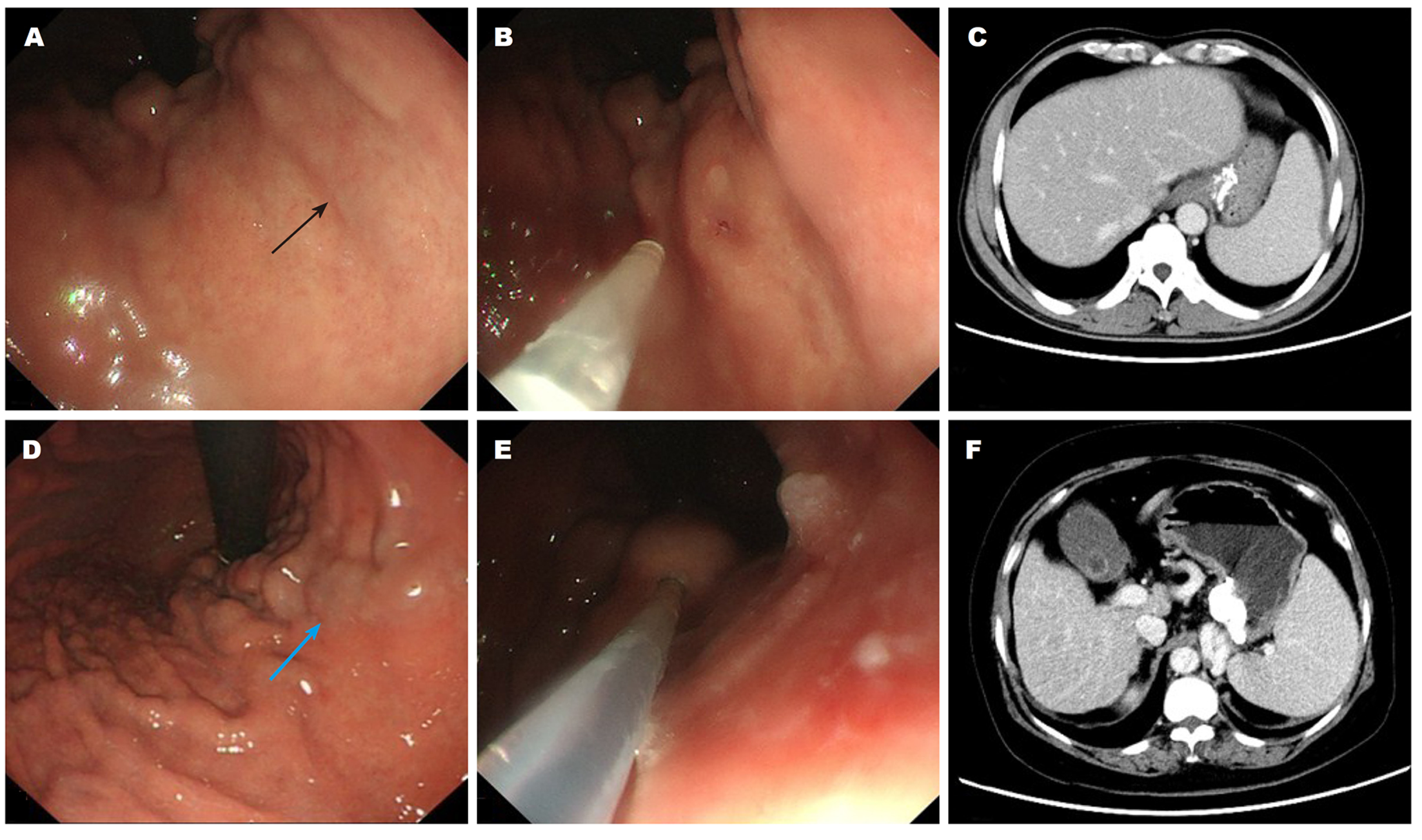
内镜治疗前给予常规支持对症治疗, 贫血较重者予输血治疗. 过生化检查、影像学检查、Child-Pugh评估肝脏功能. 内镜检查与治疗前, 常规使用血管活性药物(生长抑素或特利加压素)和抗生素等. 应用"三明治夹心法"碘化油(1.0 mL)+组织胶混合物(1.0 mL)+碘化油(1.0 mL), 曲张静脉血管内注射, 触碰注射处血管变硬变白后退针, 若注射针孔有渗血, 用注射针管头端压迫止血10余秒, 无渗血后停止压迫. 判断胃底静脉断流效果, 可退镜到食管, 若曲张的静脉完全消失或者明显萎缩, 认为胃底血管充分阻断; 如果食管静脉仍曲张明显, 说明胃底断流不完全, 可重复上述步骤进行第2点的组织胶注射. 一般每次注射1-4点. 胃底曲张静脉硬化注射后, 应用COOK六连发套扎器自食管下段至食管中上段, 螺旋密集套扎食管曲张静脉, 至食管上段曲张静脉消失. CTP指导治疗组: 根据CTP结果, 选择胃底小弯近贲门处, 曲张静脉上源迂曲不明显, 略有隐伏的较细小静脉为靶静脉; 对照组: 根据传统夹心三明治治疗方法, 选择胃底小弯及大弯处迂曲静脉较明显的曲张静脉(图1).
疗效评估: 随访1-3 mo, 随访截点为曲张静脉消失或第2次内镜下治疗. 内镜治疗后2 wk内观察近期再发出血情况, 治疗后1 mo复查胃镜观察曲张静脉改善情况, 3 mo内观察再发出血情况. 再出血: 术后2 wk-3 mo内出现呕血或黑便, 经胃镜证实食管胃底静脉曲张破裂再出血. 不良反应: 包括术后发热、胸腹部疼痛、吞咽困难、败血症、异位栓塞、穿孔等.
术后1 mo复查胃镜观察疗效, 内镜下曲张静脉特征的评估指定由2名高年医师进行, 评估方法如下[4]: (1)显效, 食管曲张静脉减轻为中度以下红色征消失, 且胃底曲张静脉缩小超过50%; (2)有效, 食管曲张静脉减轻中度以下但红色征未消失或仅有红色征消失, 且胃底曲张静脉团块缩小25%-50%; (3)无效, 除显效和有效外均视为无效; (4)改善, 将显效和有效视为改善, 即改善例数=显效例数+有效例数.
统计学处理 数据分析使用SPSS 26.0统计学软件, 正态分布的计量资料以mean±SD表示, 组间比较采用成组t检验; 计数资料以n(%)表示, 组间比较采用χ2检验, 检验水准α = 0.05, P<0.05为差异有统计学意义.
CTP指导治疗组38例, 男31例, 女7例, 平均年龄51岁±11.1岁. 同期对照组患者30例, 男25例, 女5例, 平均年龄49.0岁±10.3岁, 两组年龄性别无差异; 两组肝功能Child-pugh分级、肝硬化病因以及胃底静脉曲张分级均无差异(表1).
| CTP组 | 对照组 | χ2 | P值 | ||
| 性别 | 男 | 31 | 25 | 0.060 | 1.000 |
| 女 | 7 | 5 | |||
| Child-Pugh分级 | A | 17 | 13 | 4.041 | 0.133 |
| B | 16 | 14 | |||
| C | 5 | 3 | |||
| Sarin分型 | GOV1 | 31 | 25 | 0.036 | 0.851 |
| GOV2 | 7 | 5 | |||
| 肝硬化病因 | 乙型肝炎 | 26 | 22 | 2.933 | 0.402 |
| 丙型肝炎 | 1 | 2 | |||
| 酒精性 | 8 | 4 | |||
| 其他 | 3 | 2 | |||
| 胃底静脉曲张分度 | Ⅰ度 | 28 | 25 | 0.352 | 0.635 |
| Ⅱ度 | 8 | 5 |
通过内镜观察两组病人食管胃静脉曲张LDRf分型, 应用中华消化内镜学会新消化道静脉曲张记录标准[5], 分为食管静脉曲张(Le)、食管胃静脉曲张(Le, g)和胃静脉曲张(Lg). CTP指导治疗组中Le 3例, Le, g 35例; 其中静脉曲张位于食管下段(Lei)18例, 静脉曲张位于食管中下段(Lemi)12例, 静脉曲张位于全食管(Lemis)8例; 对照组患者中 Le 3例, Le, g 27例; 两组食管胃底曲张静脉所占位置比较无差异(P>0.05). 曲张静脉直径(D): CTP指导治疗组中D1.0 cm 18例, D 1.5 cm 11例, D 2.0 cm 6例, D 3.0 cm 3例; 同期对照组患者30例; 对照组中D 1.0 cm 12例, D 1.5 cm 10例, D 2.0 cm 5例, D 3.0 cm 3例. 两组曲张静脉直径分布比较无差异(P>0.05).
CTP组治疗前后Child-Pugh分级无差异(P>0.05); CTP组治疗前ALB 33.5 g/L±6.6 g/L 治疗后33.9 g/L±5.9 g/L (P>0.05); 治疗前TBil 26.1 mmol/L±13.7 mmol/L治疗后24.4 mmol/L±12.9 mmol/L (P>0.05); 治疗前ALT 27.7 mmol/L±14.3 mmol/L; 治疗后23.7 mmol/L±11.7 mmol/L P>0.05); 治疗前AST 34.8 mmol/L±22.7 mmol/L; 治疗后31.2 mmol/L±18.5 mmol/L (P>0.05); 治疗前GGT 49.8 mmol/L±49.2 mmol/L; 治疗后51.6 mmol/L±52.1 mmol/L (P>0.05).
对照组治疗前后Child-Pugh分级有显著差异(P<0.001); 对照组治疗前ALB 34.5 g/L±7.3 g/L; 治疗后34.9 g/L±6.9 g/L (P>0.05); 治疗前TBil 26.4 mmol/L±13.8 mmol/L; 治疗后25.0 mmol/L±12.9 mmol/L (P>0.05); 治疗前ALT 29.3 mmol/L±15.2 mmol/L; 治疗后24.2 mmol/L±9.7 mmol/L (P>0.05); 治疗前AST 35.6 mmol/L±24.3 mmol/L; 治疗后29.9 mmol/L±15.9 mmol/L (P>0.05); 治疗前GGT 65.5 mmol/L±84.6 mmol/L; 治疗后54.0 mmol/L±59.4 mmol/L (P>0.05).
两组用胶量比较, CTP组1.2±0.4 mL对照组2.0 mL±0.6 mL (P<0.001); 两组套扎环数比较, CTP组7.2±2.7环, 对照组8.7±2.7环(P<0.05). 3 mo内再出血率, CTP组5.3% (2/38)较对照组23.3% (7/30)减少(P<0.05, 表2).
| CTP组 | 对照组 | t值或χ2 | P值 | |
| 用胶量(mL) | 1.2±0.4 | 2.0±0.6 | -8.975 | 0.000 |
| 套扎环数 | 7.2±2.7 | 8.7±2.7 | -2.376 | 0.019 |
| 3 mo内出血人数 | 2/38 | 7/30 | 4.767 | 0.037 |
CPT组显效19例(50.0%)、有效13例(34.2%)、无效10例, 改善率为65.8% (25/38); 对照组显效8例(26.7%)、有8效例(26.7%)、无效14例, 改善率为53.3% (16/30).两组食管胃静脉曲张改善率比较, 经卡方检验发现差异有统计学意义(χ2 = 13.152, P<0.001; 两组病人食管胃静脉曲张显效率、有效率的比较, 经秩和检验发现差异有统计学意义(rs = 462.0, P<0.05).
EVB是肝硬化失代偿期最严重并发症之一, 若不经过有效治疗, 反复出血的发生率甚至可以高达70%以上[6], 早期有效的控制曲张血管破裂出血至关重要. 内镜精准曲张静脉断流术[7,8], 按照Sarin分类法适用于食管胃连通型曲张静脉即GOV1和GOV2. 内镜精准治疗方法需要内镜下准确判断胃底曲张静脉的起始静脉和末端静脉, 准确把组织胶注射到血管内. 但是起始静脉和末端静脉有多种变化, 不易单纯通过内镜判断. 精准的食管胃底静脉曲张的内镜血管栓塞不但可以减少组织胶用量, 减少脱胶溃疡出血的发生, 减少内镜治疗后并发症, 还可以减少治疗费用和住院时间.
CTP能充分进行三维重建, 显示门静脉血管血管及其周围血管的解剖结构, 并且有快速、无创、禁忌症少等优点. CTP对肝硬化引起的食管胃静脉曲张分型、分级上的判断与胃镜检查有较好的一致性, 辅助内镜治疗聚焦靶向血管, CTP甚至可以精确测量曲张静脉直径[9]. 在GOV1型, 胃底曲张静脉多为胃左静脉为主来供应. GOV2型, 胃左静脉、胃短静脉和(或)胃后静脉均参与胃底曲张静脉的供血, 但大部分由胃短/胃后静脉为主供血, 少部分病例伴胃/脾-肾分流[10]. CTP上曲张的胃左静脉表现为胃小弯侧点状、条状迂曲扩张的血管影, 失去其正常的解剖形态, 严重时血管可扭曲呈团状. 根据CTP的显示, 多数GOV1型胃底曲张静脉是来自贲门旁小弯侧内镜下直径较小的非显著曲张的静脉, 而胃底较大的静脉团多数是迂曲扭曲的血管球; 而GOV2型除了小弯侧曲张静脉外, 由胃短胃后参与形成的胃大弯侧迂曲静脉. 根据门静脉CTP和胃镜下曲张静脉走形, 对于存在胃/脾-肾分流的GOV2型, 可以辅助金属夹. 本研究CTP指导治疗组选择了贲门旁小弯侧起始静脉注射, 多数病人应用1 mL的碘化油组织胶混合剂单点注射就能达到较好的效果, 个别病人通过CTP评估, 曲张静脉直径较粗, 单点注射后有拔针有明显出血, 再次追加一针碘化油组织胶混合剂就可达到较好的止血效果.本研究结果显示, CTP组在用胶量明显小于对照组, 并且食管曲张静脉套扎的环数也明显减少. 对照组由于没有选择起始静脉, 多数是对明显曲张的静脉直接做血管内组织胶注射, 往往需要多点注射用胶量自然就增加了. 虽然两组治疗后均没有发生异位栓塞, 但是对照组较多的组织胶增加了脱胶出血的可能. 研究结果也显示对照组3 mo内再出血发生率(23.3%)明显超过CTP组(5.3%).
经典的黏合剂注射疗法采用碘油-组织胶-碘油的三明治夹心法, 本研究中采用改良三明治夹心法, 治疗前把等量组织胶和碘化油混合, 可以减少组织胶用量, 降低治疗费用. 我院对于食管胃底静脉曲张的治疗, 从八十年代末应用碘化油组织胶, 也逐步过渡到近年应用聚桂醇组织胶的"新三明治法", 目前严格限制"传统三明治法"在GOV1、GOV2型病人, 对于IGV1型病人存在显著的脾肾分流或胃肾分流等情况, 更应用金属夹辅助多点组织胶血管内注射治疗. 本研究严格选择GOV1、GOV2型食管胃底静脉曲张病人, 治疗后均没有出现异位栓塞的并发症. 我们在临床中发现, 改良的碘化油组织胶混合治疗胃底静脉曲张, 可以作为造影剂明确显示栓塞血管的位置, 为再次治疗提供清晰的影像依据(图1), 可以直观的显示硬化封堵的曲张静脉血管.
近期一项超声内镜引导下细针穿刺注射组织胶血管内硬化治疗结果, 与内镜直视下血管注射相比较, 用胶量明显减少, 并发症两种治疗方法基本相似[11]. 由于内镜组织胶血管注射治疗存在组织胶外溢堵塞内镜工作通道的可能, 我院超声内镜配备数量很少, 在临床工作中, 组织胶注射过程中一旦有操作不慎, 就会出现组织胶堵塞内镜工作通道的可能, 而被组织胶堵塞的内镜很难短时间被清洗干净, 会严重影响其他超声内镜的治疗, 所以通过超声内镜实时引导组织胶血管硬化注射治疗目前还是有较大的难度的.
本研究中CTP组应用较少组织胶治疗后对病人的肝功能影响较小, 治疗前后Child-Pugh分级、ALB、TBil、ALT、AST、GGT等结果均无明显差异; 而对照组病人治疗前后Child-Pugh分级有明显的加重.组织胶硬化治疗加重肝功能损伤的原因能否排除消化道出血肝细胞灌注不足导致的缺血性肝损伤, 具体机理仍需对更多的临床病例进行观察总结.
通过CTP指导选择胃底曲张静脉精准治疗, 可以缩小曲张静脉起始血管的选择范围, 为提前预测组织胶血管内注射剂量提供参考, 减少组织胶用量, 减少术后肝功能进一步损伤, 在临床精准治疗胃底食管曲张静脉有较好的参考价值.
通过CTP指导聚焦胃底曲张静脉精准治疗的靶血管范围, 并提前预测组织胶血管内注射剂量提供影像学参考依据, 减少术中组织胶用量, 并减少术后肝功能进一步损伤, 为临床内镜下精准治疗胃底食管曲张静脉提供参考. 目前内镜下精准食管胃静脉曲张断流术要求术前精准判断曲张静脉的来源及去路血管, 要求术中精准封堵靶血管, 最大程度地止血并预防术后出血. 但是如何术前寻找判断封堵的靶血管, 目前尚没有临床指南和统一标准作指导.
探索一种胃底静脉曲张内镜治疗术前精准判断曲张静脉的方法, 以便在术中指导精确封堵靶血管.
通过CT门静脉成像(CT portography, CTP)技术, 指导内镜治疗术前评估组织胶的注射部位, 以求减少注射曲张静脉的部位及组织胶用量.
回顾性分析68例肝硬化食管胃底静脉曲张患者, 分成内镜治疗前行CTP的指导治疗组和未行CTP的对照组, 比较2组治疗后用胶量, 改善率以及再出血率等指标.
CTP指导治疗组患者和对照组患者治疗前后肝功能及Child-Pugh分级无差异; CTP组患者的用胶量和套扎环数比较对照组患者明显减少; CTP组患者3 mo内再出血率较对照组患明显减少; CPT组患者病情改善率也优于对照组.
CTP指导内镜胃底曲张静脉组织胶血管内注射安全性较好, 可以提高疗效, 有一定临床参考价值.
随着3D技术的发展, CT门静脉成像技术将会更加清晰生动, CD与3D-DSA融合技术已经在临床应用, 多种图像融合的3D技术, 将会更加清晰明确地指导和评估临床医生内镜下对治疗静脉曲张的治疗.
学科分类: 胃肠病学和肝病学
手稿来源地: 山东省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C
D级 (一般): D
E级 (差): 0
科学编辑: 刘继红 制作编辑:张砚梁
| 1. | Kockerling D, Nathwani R, Forlano R, Manousou P, Mullish BH, Dhar A. Current and future pharmacological therapies for managing cirrhosis and its complications. World J Gastroenterol. 2019;25:888-908. [PubMed] [DOI] |
| 2. | 刘 艳萍, 李 国庆, 谢 娟, 陈 宏辉, 王 正根, 朱 理辉, 封 英娟. 内镜下组织胶注射治疗肝硬化胃底静脉曲张出血的临床观察. 中南医学科学杂志. 2015;53-55+77. [DOI] |
| 6. | Seo YS. Prevention and management of gastroesophageal varices. Clin Mol Hepatol. 2018;24:20-42. [PubMed] [DOI] |
| 10. | Bandali MF, Mirakhur A, Lee EW, Ferris MC, Sadler DJ, Gray RR, Wong JK. Portal hypertension: Imaging of portosystemic collateral pathways and associated image-guided therapy. World J Gastroenterol. 2017;23:1735-1746. [PubMed] [DOI] |
| 11. | Bick BL, Al-Haddad M, Liangpunsakul S, Ghabril MS, DeWitt JM. EUS-guided fine needle injection is superior to direct endoscopic injection of 2-octyl cyanoacrylate for the treatment of gastric variceal bleeding. Surg Endosc. 2019;33:1837-1845. [PubMed] [DOI] |