修回日期: 2019-12-09
接受日期: 2019-12-29
在线出版日期: 2020-01-08
目前国内外较多研究发现阿柏西普联合FOLFOX4/FOLFIRI方案治疗转移性结肠癌(metastatic colorectal cancer, mCRC)具有比较好的疗效, 本研究在国内外多项研究的基础上, 对于其疗效和安全性进行Meta分析, 进而提供循证医学相关的依据.
运用Meta分析系统性研究和评价阿柏西普在治疗mCRC中的治疗效果和安全性.
检索从2009-01/2019-01阿柏西普联合FOLFOX4/FOLFIRI方案治疗mCRC的对照试验, 包括: 中国知网数据库、维普数据库、万方数据库、中国生物医学文献数据库、PubMed、The Cochrane Library和EMBASE, 以Cochrane系统评价手册为文献评价标准对于文献进行评价, 对于所筛选的文献用Revman 5.3软件进行Meta分析, 95%可信区间估计.
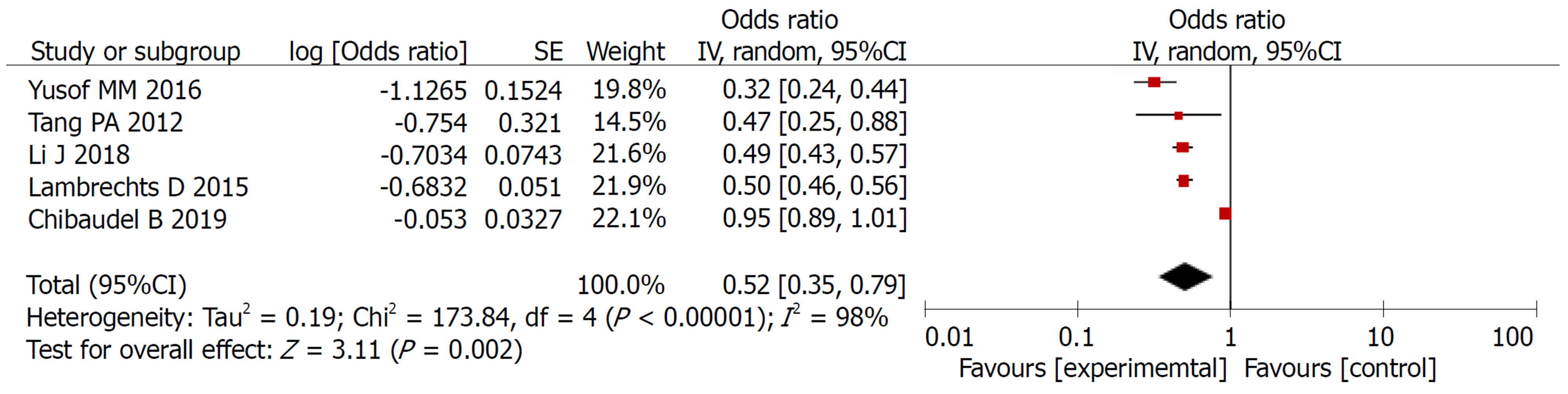
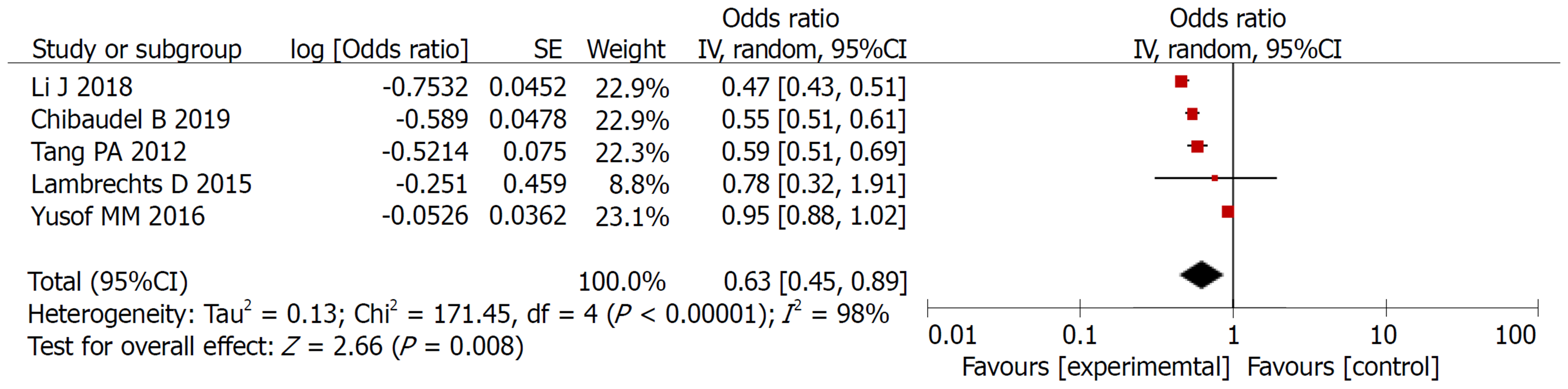
本研究共纳入5篇文献, Meta分析结果表明: 实验组患者在3年总生存率和3年无进展生存率方面的生存率高于对照组, 差异有统计学意义(OR = 0.52, 95%CI: 0.35-0.79, P = 0.002; OR = 0.63, 95%CI: 0.45-0.89, P = 0.008). 实验组患者在总不良反应方面的发生率低于对照组患者, 二者差异有统计学意义(OR = 0.58, 95%CI: 0.40-0.84, P = 0.004), 在腹泻、白细胞减少、食欲减退、恶心呕吐发生率均低于对照组, 二者差异有统计学意义(P<0.05).
阿柏西普联合FOLFOX4/FOLFIRI方案治疗mCRC较FOLFOX4/FOLFIRI治疗mCRC的效果好且安全性较高.
核心提要: 目前国内外较多研究发现阿柏西普联合FOLFOX4/FOLFIRI方案治疗转移性结肠癌具有比较好的疗效, 但此类研究样本量太少且无国内对于此类研究的系统性评价报道也相对较少, 本研究在国内外多项研究的基础上, 对于其疗效和安全性进行Meta分析, 进而提供循证医学相关的依据.
引文著录: 童秀萍, 雷鑫明, 何刘. 抗血管生成药物阿柏西普治疗转移性结肠癌疗效与安全性的Meta分析. 世界华人消化杂志 2020; 28(1): 18-25
Revised: December 9, 2019
Accepted: December 29, 2019
Published online: January 8, 2020
Numerous studies have reported that the combination of arbacicept and FOLFOX4/FOLFIRI regimen can more effectively treat metastatic colon cancer (mCRC). In the preset study, we performed a meta-analysis to assess the efficacy and safety of arbacicept for mCRC to provide an evidence-based medicine related basis for the application of this drug.
To systematically assess the clinical efficacy and safety of aflibercept for patients with metastatic colorectal cancer (mCRC) by meta-analysis.
Controlled trials that involved aflibercept with FOLFOX4/FOLFIRI regimen for treating mCRC from January 2009 to January 2019 were searched, covering China HowNet database, Weipu database, Wanfang database, China Biomedical Literature database, PubMed, as well as The Cochrane Library and EMBASE. The retrieved studies were evaluated according to the Cochrane Systematic Evaluation Manual. A meta-analysis was performed with RevMan5.3 software and 95% confidence interval (CI) estimation.
Five studies were included. The results of the meta-analysis showed that the 3-year overall survival rate and 3-year recurrence-free survival rate were significantly higher in the study group than in the control group (OR [odds ratio] = 0.52, 95%CI: 0.35-0.79, P = 0.002; OR = 0.63, 95%CI: 0.45-0.89, P = 0.008). Compared with the control group, the study group had fewer adverse events (OR = 0.58, 95%CI: 0.40-0.84, P = 0.004). Furthermore, the study group had a significantly lower incidence of diarrhea, leukopenia, loss of appetite, and nausea and vomiting than the control group (P < 0.05).
Aflibercept with FOLFOX4/FOLFIRI regimen has better efficacy and adverse event profile for treatment of refractory mCRC than FOLFOX4/FOLFIRI alone.
- Citation: Tong XP, Lei XM, He L. Meta-analysis of safety and efficacy of antiangiogenic drug aflibercept for metastatic colorectal cancer. Shijie Huaren Xiaohua Zazhi 2020; 28(1): 18-25
- URL: https://www.wjgnet.com/1009-3079/full/v28/i1/18.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v28.i1.18
结肠癌(colorectal cancer, CRC)在全世界非常常见, 其发生率仅次于肺癌和肝癌, 每年全世界范围内新增的CRC的病例在100万以上, 且大约有一半以上的CRC患者在确诊时已经存在远处转移的情况, 故全世界每年CRC患者的死亡率有逐渐上升的趋势[1]. 现随着人们的保健意识提高, 且伴随着世界医疗、卫生技术的发展, 我国针对CRC的诊疗水平较前有了明显的提升[2]. 然而, 由于目前人们还缺乏体检意识, 且早期CRC并无明显特征性表现, 故众多患者在确诊CRC后已经处于晚期, 且伴多处转移, 此类患者已无法通过手术根治CRC[3]. 对于CRC的患者来说, 以往多采用单纯化疗, 主要以FOLFOX4/FOLFIRI方案为代表, 然而疗效往往不尽如人意[4], 近年来, 已有众多研究发现, 靶向药物能明显提高转移性结肠癌(metastatic colorectal cancer, mCRC)患者的预后, 其主要包括抗血管内皮生长因子(anti-vascular endothelial growth factor, VEGF)抗体及抗表皮生长因子受体抗体[5]. 目前国内外较多研究发现阿柏西普联合FOLFOX4/FOLFIRI方案治疗mCRC具有比较好的疗效, 但此类研究样本量太少且无国内对于此类研究的系统性评价报道也相对较少, 本研究在国内外多项研究的基础上, 对于其疗效和安全性进行Meta分析, 进而提供循证医学相关的依据.
1.1.1 检索方法: 检索国内外公开数据库, 检索时间范围为2009-01/2019-01. 检索词主要为: "aflibercept"、"metastatic colorectal cancer"和"阿柏西普"、"结肠癌". 检索员至少为2人, 检索的数据库主要包括: 中文数据库中国知网数据库、维普数据库、万方数据库、中国生物医学文献数据库、国外数据库PubMed、The Cochrane Library和EMBASE. 检索语种主要为英文和中文并从中多次选择直至选出最佳的文献.
1.1.2 纳入及排除标准: 纳入标准: (1)所选择的研究对象必须通过手术病理标本, 肠镜病理标本, 或者影像学确诊为CRC; (2)所选择的研究对象必须无法手术, 且伴有远处转移; (3)所选择对象需排除其它治疗方式. 排除标准: (1)确诊对象非初诊或者不符合CRC诊断标准的患者; (2)动物实验; (3)不存在远处转移、且以往接受过手术治疗方式的研究对象; (4)样本量过小, 随访时间过短, 失访率过高且观察指标过少的研究对象.
1.2.1 干预方法: 阿柏西普联合FOLFOX4/FOLFIRI为试验组; FOLFOX4/FOLFIRI组为对照组; 两组患者在一般资料方面如: 年龄、性别、病理类型等方面差异无统计学意义(P>0.05), 试验组和对照组具有可比性.
1.2.2 结局指标: 3年总生存率, 3年无进展生存率, 不良反应: 腹泻、白细胞减少、食欲减退、恶心呕吐等发生率.
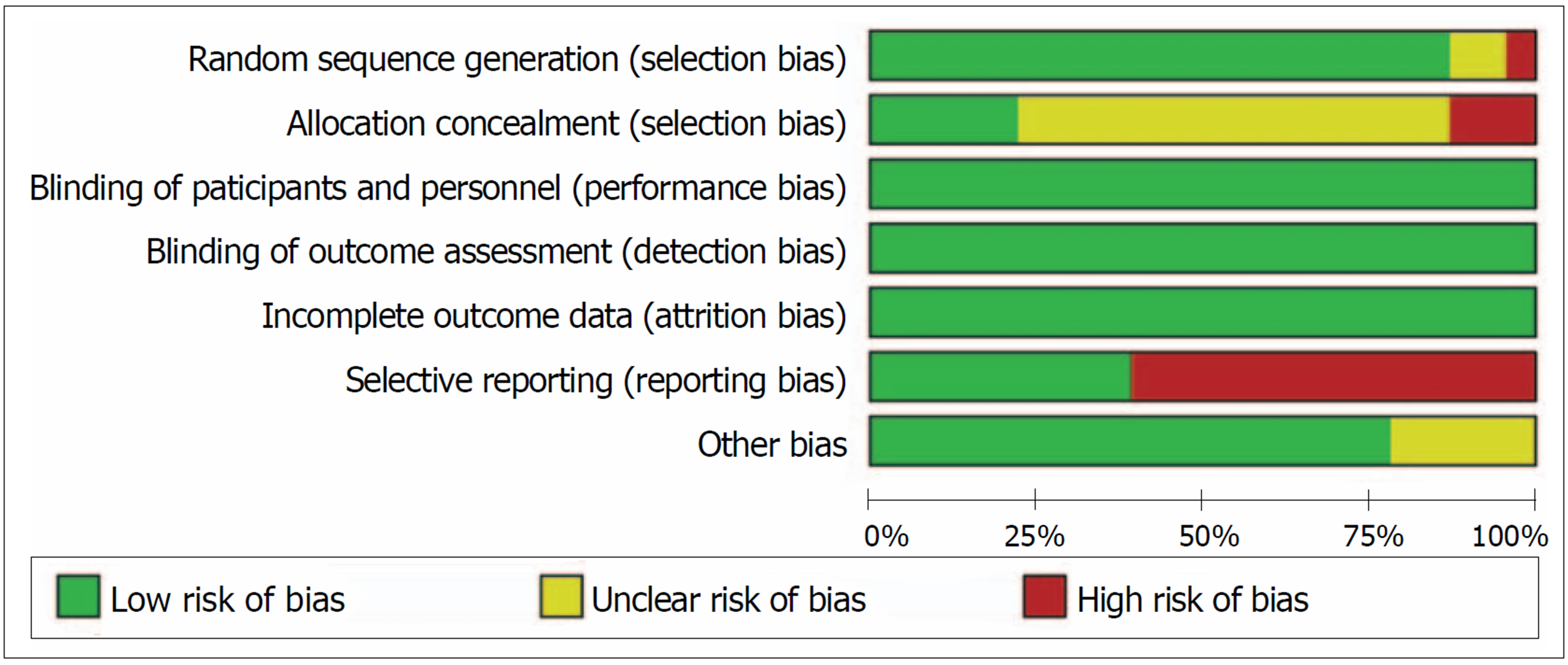
1.2.3 相关文献评价: 以Cochrane系统评价手册为文献评价标准[6], 由2名研究者对选中的文献进行筛选和评价并相互核对, 对于结论不一致的文献, 通过征求第三方、文献作者的意见的方式得出最终结论. 评价标准主要包括6个方面: (1)实验类型; (2)对于失访患者的描述情况; (3)对研究对象、治疗方案实施者、研究结果测量者采用盲法; (4)随机分配方法; (5)分配方案隐藏.
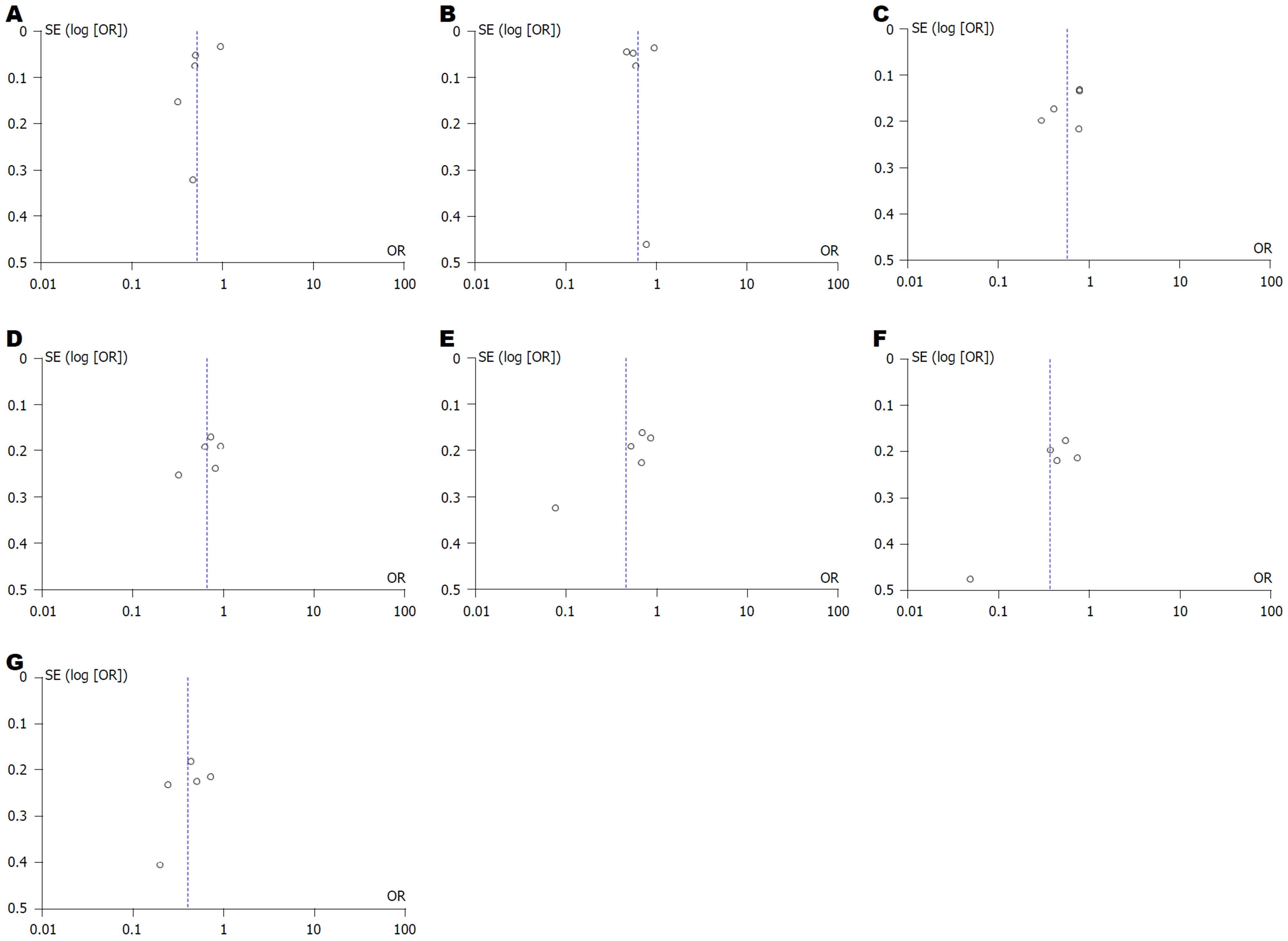
统计学处理 用RevMan 5.3进行Meta分析. 采用OR值及其95%CI描述, 采用χ2检验各研究间异质性, 并主要用I2来评价异质性大小. 当I2<50%, P>0.1时, 则提示各研究之间异质性较低或者异质性不存在, 此时Meta分析采用固定效应模型. 然而当I2≥50%, P≤0.1时, 则提示异质性较高, 此时Meta分析采用随机效应模型, 最终运用漏斗图进行偏倚评价.
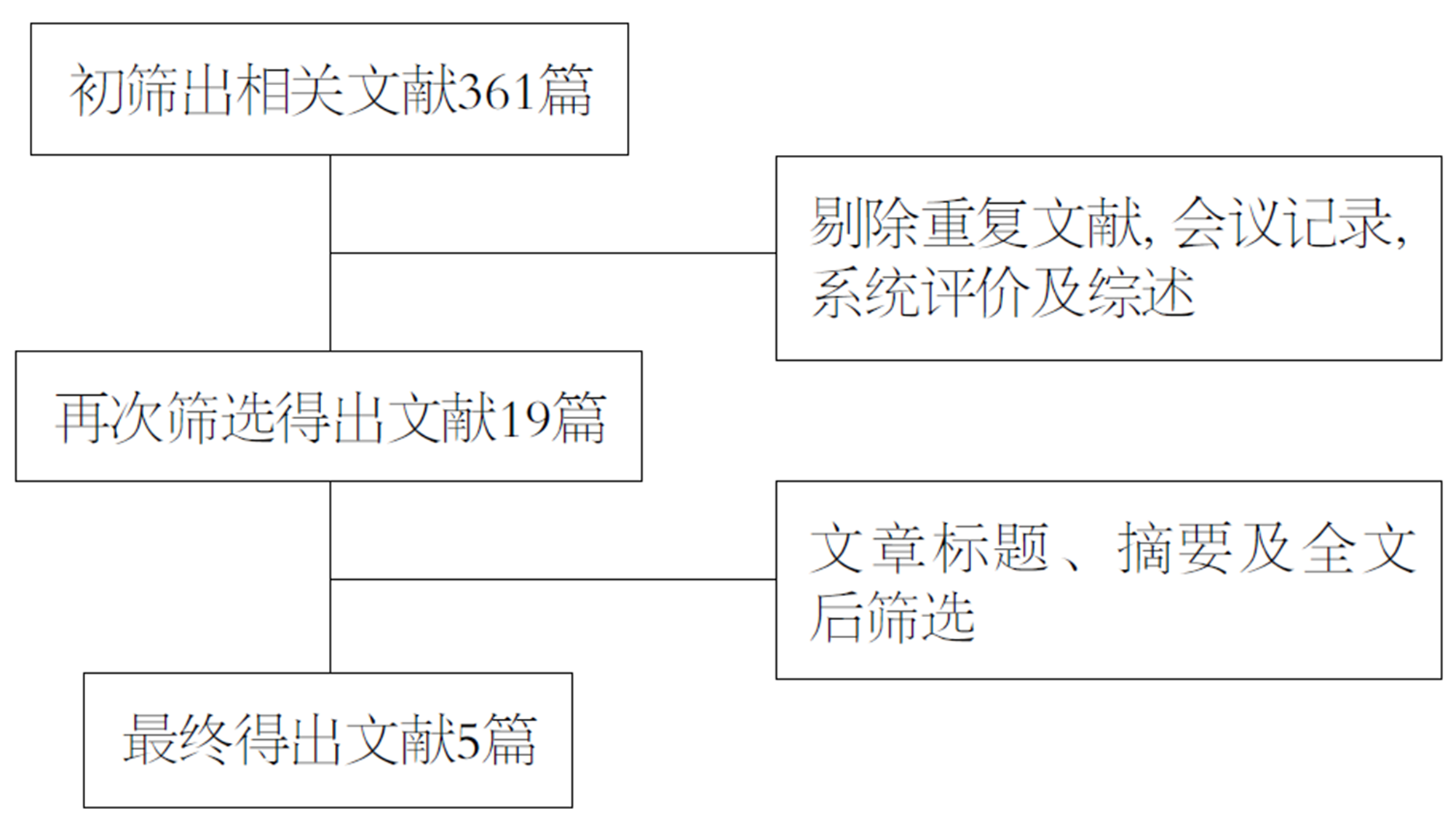
按照以上关键词搜索各个数据库, 得出总文献361篇, 将所有的重复文献, 会议记录, 系统评价及综述剔除后得到文献19篇, 再通过文章标题、摘要及全文后最终得到5篇文献[7-11]. 实验组共1362例, 对照组共741例, 4篇文献实验方法为随机对照实验, 其余1篇为非随机对照实验. 其中3篇文献质量评价为B级, 其余2篇文献分别为A、C级, 各文献、患者基本情况分别见表1和表2, 文献评价见图1, 具体搜索过程详见图2.
| 作者 | 治疗方法 | 每组人数 (人) | 平均年龄(岁) | 随访时间(月) | 并发症人数(人) | 3年总生存率(%) | 3年总生存人数(人) | 3年无进展生存率(%) | 3年无进展生存人数(人) |
| Chibaudel等[7] | 实验组 | 522 | 52(35-75) | 52 | 152 | 51 | 267 | 30 | 154 |
| 对照组 | 522 | 62(33-85) | 37 | 178 | 42 | 218 | 14 | 72 | |
| Yusof等[8] | 实验组 | 285 | 54.5±13.2 | 36±12 | 123 | 57 | 148 | 44 | 125 |
| 对照组 | 285 | 49.1±11.3 | 42±11 | 185 | 44 | 125 | 22 | 63 | |
| Li等[9] | 实验组 | 175 | 55(27-63) | 58±6 | 92 | 59 | 103 | 55 | 96 |
| 对照组 | 175 | 52.5(35-75) | 45±18 | 103 | 55 | 97 | 32 | 56 | |
| Tang等[10] | 实验组 | 320 | 52.5 | 39 | 52 | 75 | 239 | 55 | 175 |
| 对照组 | 253 | 52 | 41 | 100 | 44 | 112 | 34 | 86 | |
| Lambrechts等[11] | 实验组 | 510 | 56.5±13.5 | 46.1 | 175 | 57 | 291 | 49 | 254 |
| 对照组 | 498 | 57.5±14.5 | 45.3 | 198 | 25 | 123 | 13 | 63 |
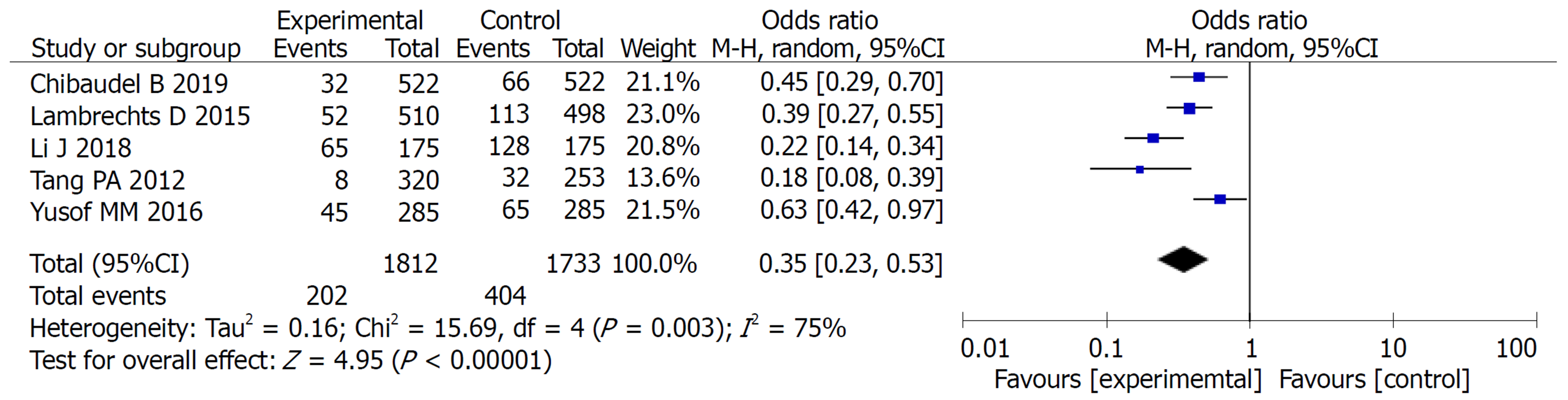
2.2.1 3年总生存率: 对实验组和对照组组间异质性检测得出P<0.00001, I2 = 98%, 存在异质性, 则用随机效应模型进行Meta分析, 结果显示OR = 0.52, 95%CI: 0.35-0.79, P = 0.002, 两组差异有统计学意义(P<0.05)(图3).
2.2.2 3年无进展生存率: 对实验组和对照组组间异质性检测得出P<0.00001, I2 = 98%, 存在异质性, 则用随机效应模型进行Meta分析, 结果显示OR = 0.63, 95%CI: 0.45-0.89, P = 0.008, 两组差异有统计学意义(P<0.05)(图4).
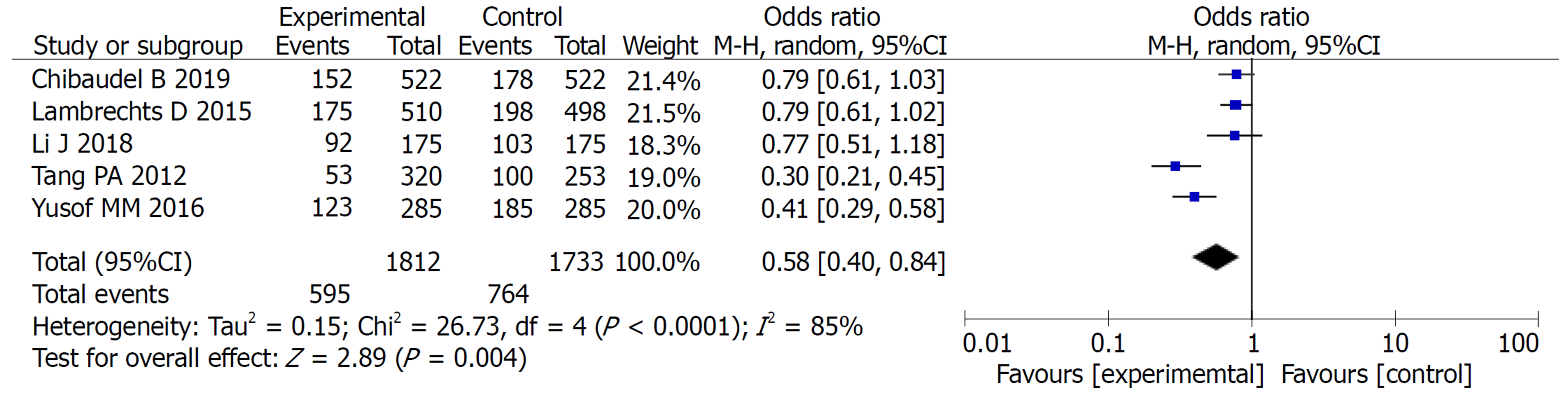
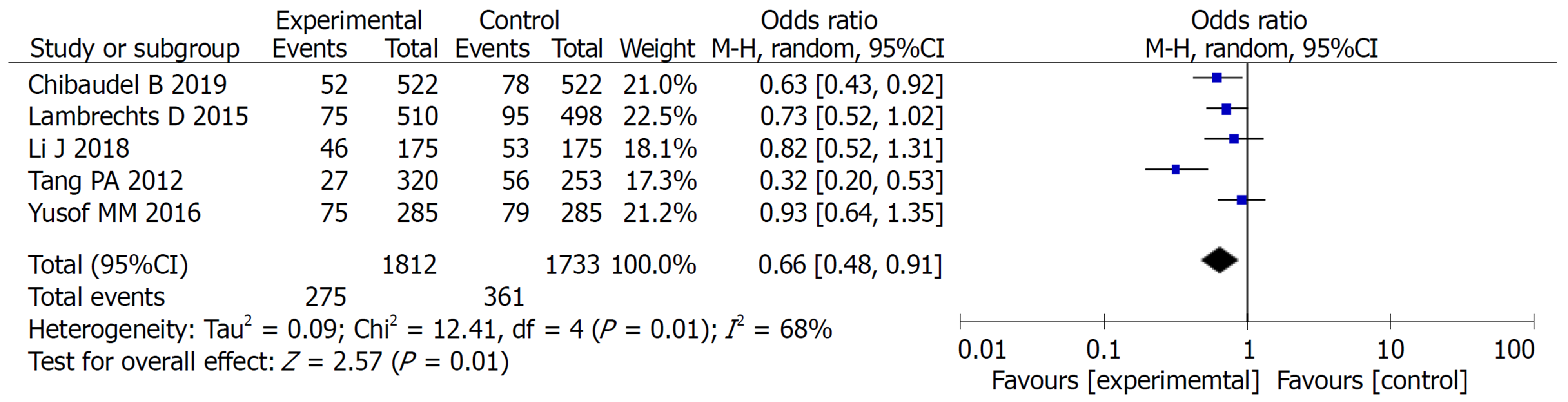
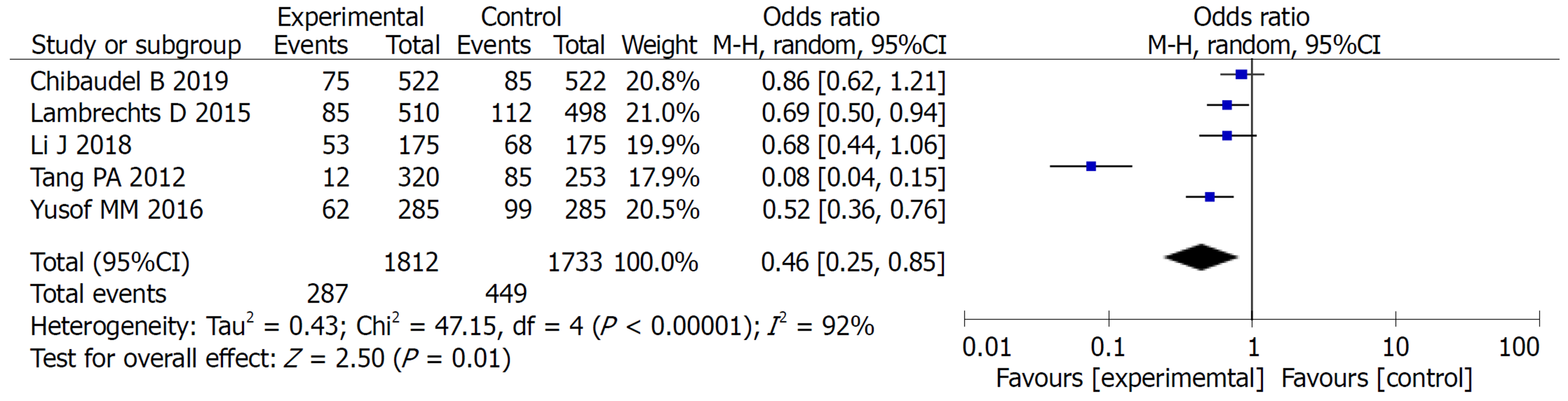
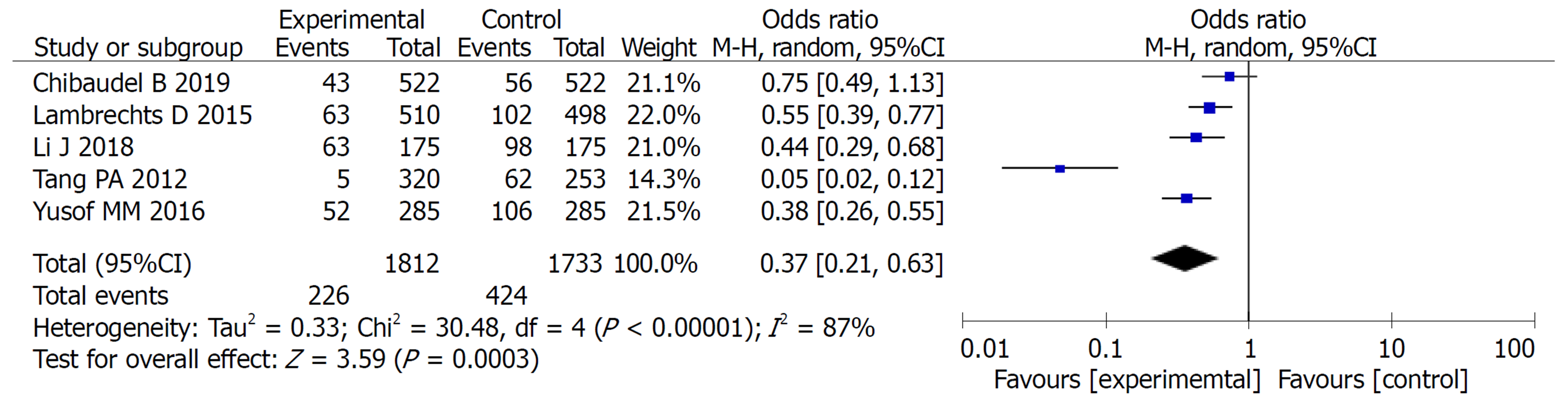
2.2.3 不良反应比较: 对实验组和对照组组间异质性检测得出P<0.00001, I2 = 85%, 存在异质性, 则用随机效应模型进行Meta分析, 结果显示OR = 0.58, 95%CI: 0.40-0.84, P = 0.004, 两组差异有统计学意义(P<0.05). 常见的不良反应主要包括: 腹泻、白细胞减少、食欲减退、恶心呕吐. Meta分析提示: 实验组中以上不良反应的发生率均低于对照组, 两组差异均有统计学意义(P<0.05)(图5-9).
2.2.4 发表偏倚评价: 各个研究漏斗图显示散点基本对称并且呈倒漏斗状分布, 故漏斗图提示无偏倚(图10).
CRC发病率仅次于肺癌及肝癌, 在全世界非常常见, 目前全球每年新增的确诊CRC的人数在120万左右, 然而由于国内人们体检意识不强, 且CRC早期并无明显特异性临床表现, 仅仅表现为排便习惯改变, 故很多患者在确诊为CRC时已经处于晚期[12]. 以往晚期CRC的治疗方案以化疗为主, 其一线治疗方案主要为FOLFOX4及FOLFIRI化疗方案, 但其疗效往往不佳且副作用大, 现越来越多研究发现, 肿瘤的生长, 转移与肿瘤内新生血管的形成有着密切的关系, 且抗血管生成药物的广泛应用给众多CRC的患者带来福音[13].
阿柏西普作为抗肿瘤血管生成药物的代表药物之一, 是一种基因重组的、可溶的、完全性人源化VEGF受体(VEGF receptor, VEGFR)融合蛋白. 目前阿柏西普在国外应用非常广泛, 主要应用于眼科和CRC两大领域, 美国FDA和EMA于2012年批准阿柏西普联合FOLFIRI治疗对于奥沙利铂耐药的mCRC患者的治疗, 目前仍有大量的相关研究正在进展当中.
阿柏西普具有较强的抗肿瘤作用. 由IgG1的Fc段和VEGFR的胞外结构域融合形成的一种基因重组的可溶性VEGFR融合蛋白, Khayat等[14]进行的Ⅰ期临床研究发现, 阿柏西普联合FOLFIRI方案治疗转移性结直肠癌具有良好的安全性和疗效, 其中接受阿柏西普联合FOLFIRI方案治疗的患者中位治疗疾病控制率为13%, 周期数为12, 明显好于FOLFIRI组. Van Cutsem等[12]进行了有关一项阿柏西普联Ⅰ期研究, 此研究实验组用阿柏西普联合FOLFIRI方案治疗, 对照组用单纯FOLFIRI治疗, 发现实验组患者的疾病控制率为75%, 实验组患者的中位治疗周期为10, 实验组患者中位无进展生存时间为7.59 mo(95%CI: 2.33-9.59), 而中位无进展生存期明显长于单纯FOLFIRI治疗晚期结直肠癌的患者(2.5-5.1 mo)[15-17]. 在Yoshino等[15]研究的一项有关阿柏西普的Ⅲ期临床试验中共1226例转移性结直肠癌患者入组. 将所有入组患者按1:1随机分配到阿柏西普联合FOLFIRI组和安慰剂联合FOLFIRI组, 研究结果发现, 实验组较对照组中位总生存、无进展生存时间明显延长(13.50 mo:12.06 mo; HR = 0.817, 95%CI: 0.713-0.937, P = 0.0032; 6.90 mo:4.67 mo; HR = 0.758, 95%CI: 0.661-0.869, P<0.0001). 实验组的肿瘤总缓解率较对照组明显提高(19.8%:11.1%, P<0.001). 此项研究结果为阿柏西普应用于mCRC患者提供了有力的临床证据. 但目前国内关于此药物的疗效及安全性研究仍然较少, 本研究在国内外研究的基础上进行Meta分析, 进而提供循证医学相关的依据[18].
本研究共纳入5篇文献, 实验组共1812例研究对象, 对照组共1733例研究对象, Meta分析结果表明: 在3年总生存率和3年无瘤生存率方面, 实验组患者的生存率高于对照组, 差异有统计学意义(P<0.05). 在不良反应方面, 实验组患者发生率低于对照组患者, 二者差异有统计学意义(P<0.05). 笔者认为阿伯西普疗效高的原因主要有以下方面, 有研究认为, 阿伯西普主要通过抑制肿瘤血管细胞的生成进而抑制肿瘤细胞的复制, 进而促进其凋亡, 从而提高患者的总生存率和无进展生存率. 另一种研究认为可能与药物的剂量相关, 较单纯使用FOLFOX4/FOLFIRI方案的剂量更佳, 故治疗效果较好, 但具体的机制仍然需要进一步的研究.
综上所述, 阿柏西普对于难治性mCRC的治疗具有良好的疗效和较高的安全性. 但由于此次研究文献数目少, 大部分研究的质量为B级或C级, 且无法对每一篇文献进行进一步的亚组分析, 因此希望将来有更多的多中心、双盲、大样本、随访时间长、随机的对照实验的出现为临床医师提供重要指导[19].
目前国内外较多研究发现阿柏西普联合FOLFOX4/FOLFIRI方案治疗转移性结肠癌(metastatic colorectal cancer, mCRC)具有比较好的疗效, 本研究在国内外多项研究的基础上, 对于其疗效和安全性进行Meta分析, 进而提供循证医学相关的依据.
本研究旨在运用Meta分析的研究方法系统性评价阿柏西普治疗mCRC中的治疗效果和安全性, 进而提供循证医学相关的依据.
本研究主要的目标在于通过搜集国内外大量文献, 评价阿柏西普在治疗mCRC中的治疗效果和安全性比较进行Meta分析, 进而提供循证医学相关的依据. 进而对于临床医师在治疗CRC的患者上提供重要的参考.
检索2009-01/2019-01阿柏西普联合FOLFOX4/FOLFIRI方案治疗mCRC的对照试验, 包括: 中国知网数据库、维普数据库、万方数据库、中国生物医学文献数据库、PubMed、The Cochrane Library和EMBASE, 以Cochrane系统评价手册为文献评价标准对于文献进行评价, 对于所筛选的文献用Revman 5.3软件进行Meta分析, 95%可信区间估计.
本研究共纳入5篇文献, Meta分析结果表明: 实验组患者在3年总生存率和3年无进展生存率方面的生存率高于对照组, 差异有统计学意义(OR = 0.52, 95%CI: 0.35-0.79, P = 0.002; OR = 0.63, 95%CI: 0.45-0.89, P = 0.008). 实验组患者在总不良反应方面的发生率低于对照组患者, 二者差异有统计学意义(OR = 0.58, 95%CI: 0.40-0.84, P = 0.004), 腹泻、白细胞减少、食欲减退、恶心呕吐发生率均低于对照组, 二者差异有统计学意义(P<0.05).
阿柏西普联合FOLFOX4/FOLFIRI方案治疗mCRC较FOLFOX4/FOLFIRI治疗mCRC的效果好且安全性较高.
希望将来有更多的多中心、双盲、大样本、随访时间长、随机的对照实验的出现, 为临床医师提供重要指导.
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): 0
D级 (一般): D
E级 (差): 0
编辑: 王禹乔 电编:刘继红
| 1. | Li L, Ma BB. Colorectal cancer in Chinese patients: current and emerging treatment options. Onco Targets Ther. 2014;7:1817-1828. [PubMed] [DOI] |
| 2. | Eveno C, Pocard M. VEGF levels and the angiogenic potential of the microenvironment can affect surgical strategy for colorectal liver metastasis. Cell Adh Migr. 2012;6:569-573. [PubMed] [DOI] |
| 4. | Martinelli E, Troiani T, Morgillo F, Orditura M, De Vita F, Belli G, Ciardiello F. Emerging VEGF-receptor inhibitors for colorectal cancer. Expert Opin Emerg Drugs. 2013;18:25-37. [PubMed] [DOI] |
| 5. | Allegra CJ, Lakomy R, Tabernero J, Prausová J, Ruff P, Hazel GV, Moiseyenko VM, Ferry DR, McKendrick JJ, Cutsem EV. Effects of prior bevacizumab (B) use on outcomes from the VELOUR study: A phase III study of aflibercept (Afl) and FOLFIRI in patients (pts) with metastatic colorectal cancer (mCRC) after failure of an oxaliplatin regimen. J Clin Oncol. 2012;30:3505. [DOI] |
| 7. | Chibaudel B, Bachet JB, André T, Auby D, Desramé J, Deplanque G, Lecaille C, Louvet C, Tournigand C, Lebrun-Ly V, Dauba J, Lledo G, Garcia ML, Dubreuil O, Hamed NB, Meurisse A, Larsen AK, Tijeras-Raballand A, Bonnetain F, De Gramont A. Efficacy of aflibercept with FOLFOX and maintenance with fluoropyrimidine as firstline therapy for metastatic colorectal cancer: GERCOR VELVET phase II study. Int J Oncol. 2019;54:1433-1445. [PubMed] [DOI] |
| 8. | Yusof MM, Abdullah NM, Sharial MM, Zaatar A. Safety and Management of Toxicity Related to Aflibercept in Combination with Fluorouracil, Leucovorin and Irinotecan in Malaysian Patients with Metastatic Colorectal Cancer. Asian Pac J Cancer Prev. 2016;17:973-978. [PubMed] [DOI] |
| 9. | Li J, Xu R, Qin S, Liu T, Pan H, Xu J, Bi F, Lim R, Zhang S, Ba Y, Bai Y, Fan N, Tsuji A, Yeh KH, Ma B, Wei V, Shi D, Magherini E, Shen L. Aflibercept plus FOLFIRI in Asian patients with pretreated metastatic colorectal cancer: a randomized Phase III study. Future Oncol. 2018;14:2031-2044. [PubMed] [DOI] |
| 10. | Tang PA, Cohen SJ, Kollmannsberger C, Bjarnason G, Virik K, MacKenzie MJ, Lourenco L, Wang L, Chen A, Moore MJ. Phase II clinical and pharmacokinetic study of aflibercept in patients with previously treated metastatic colorectal cancer. Clin Cancer Res. 2012;18:6023-6031. [PubMed] [DOI] |
| 11. | Lambrechts D, Thienpont B, Thuillier V, Sagaert X, Moisse M, Peuteman G, Pericay C, Folprecht G, Zalcberg J, Zilocchi C, Margherini E, Chiron M, Van Cutsem E. Evaluation of efficacy and safety markers in a phase II study of metastatic colorectal cancer treated with aflibercept in the first-line setting. Br J Cancer. 2015;113:1027-1034. [PubMed] [DOI] |
| 12. | Van Cutsem E, Tabernero J, Lakomy R, Prenen H, Prausová J, Macarulla T, Ruff P, van Hazel GA, Moiseyenko V, Ferry D, McKendrick J, Polikoff J, Tellier A, Castan R, Allegra C. Addition of aflibercept to fluorouracil, leucovorin, and irinotecan improves survival in a phase III randomized trial in patients with metastatic colorectal cancer previously treated with an oxaliplatin-based regimen. J Clin Oncol. 2012;30:3499-3506. [PubMed] [DOI] |
| 13. | Van Cutsem E, Joulain F, Hoff PM, Mitchell E, Ruff P, Lakomý R, Prausová J, Moiseyenko VM, van Hazel G, Cunningham D, Arnold D, Schmoll HJ, Ten Tije AJ, McKendrick J, Kröning H, Humblet Y, Grávalos C, Le-Guennec S, Andria M, Dochy E, Vishwanath RL, Macarulla T, Tabernero J. Aflibercept Plus FOLFIRI vs. Placebo Plus FOLFIRI in Second-Line Metastatic Colorectal Cancer: a Post Hoc Analysis of Survival from the Phase III VELOUR Study Subsequent to Exclusion of Patients who had Recurrence During or Within 6 Months of Completing Adjuvant Oxaliplatin-Based Therapy. Target Oncol. 2016;11:383-400. [PubMed] [DOI] |
| 14. | Khayat D, Tejpar S, Spano JP, Verslype C, Bloch J, Vandecaveye V, Assadourian S, Soussan-Lazard K, Cartot-Coton S, Van Cutsem E. Intravenous aflibercept administered in combination with irinotecan, 5-fluorouracil and leucovorin in patients with advanced solid tumours: results from the expansion cohort of a phase I study. Eur J Cancer. 2013;49:790-797. [PubMed] [DOI] |
| 15. | Yoshino T, Yamazaki K, Yamaguchi K, Doi T, Boku N, Machida N, Onozawa Y, Asayama M, Fujino T, Ohtsu A. A phase I study of intravenous aflibercept with FOLFIRI in Japanese patients with previously treated metastatic colorectal cancer. Invest New Drugs. 2013;31:910-917. [PubMed] [DOI] |
| 16. | Pastorino A, Di Bartolomeo M, Maiello E, Iaffaioli V, Ciuffreda L, Fasola G, Di Costanzo F, Frassineti GL, Marchetti P, Antoniotti C, Leone F, Zaniboni A, Aprile G, Zilocchi C, Sobrero A, Bordonaro R. Aflibercept Plus FOLFIRI in the Real-life Setting: Safety and Quality of Life Data From the Italian Patient Cohort of the Aflibercept Safety and Quality-of-Life Program Study. Clin Colorectal Cancer. 2018;17:e457-e470. [PubMed] [DOI] |
| 17. | Ruff P, Van Cutsem E, Lakomy R, Prausova J, van Hazel GA, Moiseyenko VM, Soussan-Lazard K, Dochy E, Magherini E, Macarulla T, Papamichael D. Observed benefit and safety of aflibercept in elderly patients with metastatic colorectal cancer: An age-based analysis from the randomized placebo-controlled phase III VELOUR trial. J Geriatr Oncol. 2018;9:32-39. [PubMed] [DOI] |
| 18. | Tabernero J, Van Cutsem E, Lakomý R, Prausová J, Ruff P, van Hazel GA, Moiseyenko VM, Ferry DR, McKendrick JJ, Soussan-Lazard K, Chevalier S, Allegra CJ. Aflibercept versus placebo in combination with fluorouracil, leucovorin and irinotecan in the treatment of previously treated metastatic colorectal cancer: prespecified subgroup analyses from the VELOUR trial. Eur J Cancer. 2014;50:320-331. [PubMed] [DOI] |
| 19. | FDA approves regorafenib (Stivarga) for GIST. Oncology (Williston Park). 2013;27:164. [PubMed] |