修回日期: 2019-09-09
接受日期: 2019-09-18
在线出版日期: 2019-10-08
经肝动脉化疗栓塞术(transcatheter arterial chemoembolization, TACE)和微波消融术(microwave ablation, MWA)是国内外肝癌治疗的主要手段, TACE术可阻断肝癌供血血管, 并可清晰显示肿瘤所在区域, 序贯应用MWA可以将实体瘤完全消融. 但无论哪种术式, 肝癌术后复发问题都难以解决.
分析经肝动脉化疗栓塞联合微波消融治疗巴萨罗那临床肝癌分期(barcelona clinic liver cancer, BCLC)早期肝癌的效果及影响复发的因素.
回顾性分析了2016-02/2017-11在昆明市第三人民医院行TACE联合MWA治疗的乙肝病毒(hepatitis B virus, HBV)感染后的BCLC早期肝癌患者42例, 术后即刻评价疗效, 记录并发症, 所有患者完成WMA后1 mo、2 mo、3 mo、6 mo、12 mo、18 mo复查增强CT、甲胎蛋白(alpha-fetoprotein, AFP)、肝功和或肝动脉造影, 记录复发时间.
截至随访时, 手术总有效率为61.5%, 病灶控制率为84.2%. 中位无进展生存期 (progression-free-survival, PFS)为7.3 mo(范围2.3-34 mo). 单因素分析中, 女性患者的PFS为14 mo, 男性的PFS为11 mo. ≥60岁的患者PFS为3.8 mo, <60岁患者的PFS为8.9 mo. <3 cm的肿瘤PFS为14 mo, 3-5 cm为10.7 mo, 5-10 cm以上的肿瘤PFS为11.2 mo. 单个肿瘤的PFS为13.6 mo, ≥2个肿瘤的PFS为4 mo. Child A级的PFS为20.8 mo, Child B级的PFS为11.2 mo, Child A级患者的PFS高于Child B级的患者. BCLC 0期的患者PFS为15.5 mo, BCLC A期的患者PFS为11.2 mo, BCLC 0期患者的PFS明显高于BCLC A期. 术前HBV-DNA阳性的患者PFS为11.2 mo, HBV-DNA阴性的患者PFS为13.3 mo. HBeAg阳性的中位PFS为11.2 mo, HBeAg阴性的PFS为13.3 mo. 单因素分析显示, 性别、年龄、Child分级、肿瘤数目、BCLC分期有统计学差异, 肿瘤大小、术前HBV-DNA、HBeAg阳性无统计学差异. 在多因素分析中, Child分级、BCLC A期、性别为影响TACE序贯MWA的HBV感染后的的BCLC早期肝癌的PFS的独立危险因素(P<0.05).
TACE序贯MWA治疗BCLC早期肝癌是安全有效的, Child分级、BCLC分期、性别可能影响术后复发.
核心提要: 对于乙肝病毒感染引发的巴萨罗那临床肝癌分期(barcelona clinic liver cancer, BCLC)早期肝癌, 经肝动脉化疗栓塞术序贯微波消融术治疗是安全可行的, 术后管理和随访至关重要, 除规范抗病毒外, 应定期随访监测复发. Child分级、BCLC分期和性别可能是影响无进展生存期的重要因素, 随访时需加强关注.
引文著录: 罗煜, 付海艳, 黄红丽, 李红娟, 张洁, 周宇君, 徐斌, 王洁. 经肝动脉化疗栓塞联合微波消融治疗BCLC早期肝癌的效果及无进展生存期的影响预后因素分析. 世界华人消化杂志 2019; 27(19): 1201-1208
Revised: September 9, 2019
Accepted: September 18, 2019
Published online: October 8, 2019
Transcatheter arterial chemoembolization (TACE) and microwave ablation (MWA) are the main methods for the treatment of liver cancer worldwide. TACE can block the blood vessels of liver cancer and clearly show the area where the tumor is located. The solid tumor can be completely ablated by MWA. However, postoperative recurrence is still a difficult problem to solve.
To assess the efficacy of TACE combined with MWA in the treatment of liver cancer at early Barcelona clinic liver cancer (BCLC) stage and identify the factors affecting recurrence.
A retrospective analysis was performed on 42 patients with post-hepatitis B virus (HBV) liver cancer at early BCLC stage who underwent TACE combined with MWA at our hospital from February 2016 to November 2017. After surgery, the efficacy was evaluated and complications were recorded. The patients were followed at 1 mo, 2 mo, 3, mo 6 mo, 12 mo, and 18 mo after WMA for CT, alpha fetoprotein (AFP), liver function, or hepatic angiography, and the time to recurrence was recorded.
By the last follow-up, the total effective rate was 61.5% and the lesion control rate was 84.2%. The median progression-free-survival (PFS) was 7.3 mo (range, 2.3-34). Univariate analysis showed that female patients had a PFS of 14 mo and male patients had a PFS of 11 mo. Patients ≥ 60 years of age had a PFS of 3.8 mo, and patients < 60 years of age had a PFS of 8.9 mo. The PFS of patients with tumor < 3 cm, 3 to 5 cm, and 5-10 cm was 14, 10.5, and 11.2 mo, respectively. The PFS of patients with single tumor and multiple tumors was 13.6 and 4 mo, respectively. The PFS of patients with Child A and Child B disease was 20.8 mo vs 11.2 mo. The PFS of BCLC stage 0 patients and BCLC stage A patients was 15.5 mo vs 11.2 mo. HBV-DNA positive patients had a PFS of 11.2 mo, and HBV-DNA negative patients had a PFS of 13.3 mo. The median PFS of HBeAg-positive cases was 11.2 mo, and that of HBeAg-negative cases was 13.3 mo. Univariate analysis showed that gender, age, Child grade, number of tumors, and BCLC stage were significantly correlated with PFS, but tumor size, preoperative HBV-DNA, and HBeAg status did not. In multivariate analysis, Child grade, BCLC stage, and gender were identified to be independent risk factors for PFS in early BCLC stage liver cancer patients undergoing sequential treatment of TACE and MWA (P < 0.05).
TACE combined with MWA is safe and effective in the treatment of early BCLC stage liver cancer. Child grade, BCLC stage, and gender may affect postoperative recurrence.
- Citation: Luo Y, Fu HY, Huang HL, Li HJ, Zhang J, Zhou YJ, Xu B, Wang J. Transcatheter arterial chemoembolization combined with microwave ablation for treatment of early liver cancer: Efficacy and prognostic factors for progression-free survival. Shijie Huaren Xiaohua Zazhi 2019; 27(19): 1201-1208
- URL: https://www.wjgnet.com/1009-3079/full/v27/i19/1201.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v27.i19.1201
国际癌症机构发布了来自185个国家36种癌症的发病率和死亡率, 2018年肝癌新发病例数841080人, 占总数的4.7%, 死亡人数781631人, 占总死亡人数的8.2%[1]. 来自中国癌症中心的数据显示, 2003-2015年城市中肝癌的总体生存率下降[2], 我国肝癌的发病率和死亡率均高于全球. 在我国, 肝癌公认的诱因是乙肝病毒(hepatitis B virus, HBV)感染. 肝癌的早诊早治对于提高生存率至关重要. 巴塞罗那临床肝癌分期(barcelona clinic liver cancer, BCLC)包括0期到D期5个阶段, 是目前国内外肝癌分期管理的最常用方法, 其中0期的极早期和A期的早期都可归为早期, BCLC指南认为早期肝癌切除、移植、消融都是可以选择的策略[3]. 然而, 中国以HBV诱因的肝癌多发, 由于乙肝病毒的复制等问题, 术后复发率相对较高需反复手术限制了外科应用, 肝移植成功率低、术后风险高, 且由于供肝选择困难以及HBV再感染问题, 可以优先考虑介入治疗. 本研究回顾性分析了2016-02/2017-11在昆明市第三人民医院行经肝动脉化疗栓塞术(transcatheter arterial chemoembolization, TACE)联合微波消融术(microwave ablation, MWA)治疗的HBV感染后的BCLC早期肝癌患者42例的临床资料, 观察治疗效果及安全性.
本研究经昆明市第三人民医院伦理委员会批准, 所有病例均获得了患者的书面知情同意书, 仅用于治疗和用于临床研究的数据. 根据2018年中国临床肿瘤学会的建议, 肝细胞癌(hepatocellular carcinoma, HCC)的诊断基于非侵入性标准. 根据BCLC分期系统, BCLC 0期定义为单个肿瘤<2 cm、无门脉高压; BCLC A期定义为单个肿瘤任何大小或者3个以内肿瘤, 但单个肿瘤大小均<3 cm, Child分级为A-B. 美国东部肿瘤协作组(eastern cooperative oncology group, ECOG)体力状况(performance status, PS)评分标准定义为, 0级定义为活动能力完全正常, 与起病前活动能力无任何差异, 1级定义为能自由走动及从事轻体力活动, 包括一般家务或者办公室工作, 但不能从事较重的体力活动. 纳入标准: (1)在TACE和MWA之前没有相关的肝癌治疗; (2)HBsAg阳性; (3)BCLC 0期和A期; (4)无严重的心肺肾功能异常, 无合并其他肿瘤; (5)血小板≥50×109/L; (6)ECOG PS评分0分或1分.
TACE采用Seldinger插管技术, 经右股动脉插管, 肝固有动脉进行造影, 明确肿瘤大小、位置及供血血管, 采用微导管超选择至肿瘤供血动脉. 根据患者肿瘤大小行肝动脉灌注化疗栓塞术, 予罂粟乙碘油(3-13 mL)及化疗药物混悬乳剂联合明胶海绵颗粒明胶海绵颗粒(350-560 μm, 江苏恒瑞)栓塞肿瘤供血动脉. TACE术后平均8 d, MWA采用CT扫描定位, 明确肿瘤位置, 常规消毒麻醉后, 使用抽吸式组织活检针为引导针, 经皮穿刺至肿瘤病灶中心处, CT扫描后确定消融针位置(一次性水冷微波消融针由南京维京九洲器械提供, 型号: MTC-3CA-II18, 规格: 1.8 mm×150 mm, 1.8 mm×180 mm), 微波功率20 W, 6 s试针成功后, 沿引导针路径穿刺至肿瘤中心, CT确认消融针位置正确, 80 W消融6 min, 根据患者耐受程度调整功率, 但不低于50 W, 调整消融针位置, 消融直径超过肿瘤边缘1 cm. 术后即可复查CT观察有无出血等并发症. WMA术后即刻疗效评价: 肿瘤所在区域动脉期未见强化定义为完全消融(complete response, CR), 肿瘤病灶所在区域内局部动脉期有强化者, 定义为不完全消融(incomplete response, ICR). 对于ICR给与再次消融. 随访使用mRECIST指南评估治疗反应[4]. 完全反应(complete reaction, CR)定义为所有靶病变中任何肿瘤内动脉期未见强化(最多两个可测量的肝脏病变); 部分反应(partial reaction, PR)定义为可见肿瘤内动脉期部分强化, 但可测量的肿瘤直径总和至少减少30%; 稳定(stable disease, SD)定义为PR和PD之间; 进展(progressive disease, PD)被定义为病变直径总和至少增加20%或出现新发病灶. 总有效率RR = (CR+PR)/总例数×100%; 病灶控制率 = (CR+PR+SD)/总例数×100%. 随访开始时间为患入院后进行TACE当日, 截止时间为其出现疾病进展或死亡当日. 无进展生存期(progression-free-survival, PFS)定义为从TACE术开始至疾病进展或死亡当日. 所有患者完成WMA后1 mo、2 mo、3 mo、6 mo、12 mo、18 mo复查增强CT、AFP、肝功和HBV-DNA, 根据变化确定是否需要行肝动脉造影, 随访终点为2019-04-01.
统计学处理 采用SPSS 20.0软件对数据进行统计分析. 计数资料以例或率表示, 组间比较采用χ2检验; 对于符合正态分布的计量资料以mean±SD表示, 不符合正态分布的计量资料采用中位数(四分位间距)表示, 符合正态分布的组间比较采用t检验或方差分析, 不符合正态分布的采用秩和检验; 将单因素分析中P<0.2的指标纳入多因素分析中, 生存曲线采用Kaplan-Meier生存分析法, 组间生存曲线比较采用Log-rank检验. P<0.05为差异有统计学意义. 对随访期间失访的病例, 统计学分析时按删失数据处理; 对末次随访仍未出现进展的病例, 统计学分析时按截尾数据处理.
在研究期间, 将42名患者中符合纳入标准的40名患者作为研究对象纳入本研究. 其中男性患者34例(89.4%), 女性患者6例(10.6%). 中位年龄为54岁(38, 68). 所有患者均为HBsAg阳性, 有12例患者(30%)为HBeAg阳性. 40例患者均口服核苷类似物抗病毒治疗, 抗病毒药物包括恩替卡韦、替诺福韦及阿德福韦酯. 肝功能Child A级32例(80%), Child B级8例(20%), HBV-DNA低于检测下限16例(参考范围为<1.00E+02 IU/mL), 其余HBV-DNA中位数为1.42E+107(219-1.35E+108) IU/mL. 27例患者肿瘤直径<3 cm(67.5%), 均值为1.9 cm(1.3, 2.8), 8例患者3 cm≤肿瘤直径<5 cm(20%), 5例患者肿瘤直径≥5 cm, 最大肿瘤直径为10 cm(12.5%), 其中4例患者有2个肿瘤, 其余均为单个肿瘤. 所有患者甲胎蛋白(alpha-fetoprotein, AFP)均升高, 范围在40-3100 μg/LT. TACE术后平均8 d(范围5-14 d)实施WMA, 2例因肿瘤直径较大实施2次MWA.
所有病人均未观察到严重的并发症. 主要并发症为栓塞后综合征, 栓塞后综合症包括发热(15%), 腹痛(20%)、转氨酶和黄胆红素轻度升高. 股动脉穿刺部位出血(n = 1, 2.5%). 所有并发症均在对症治疗后5 d内得到解决, 没有治疗相关的死亡.
中位随访时间为23 mo(范围18-34 mo). 到随访时, 40例全部存活, 未出现失访. 在随访第18 mo时, 手术总有效率为61.5%, 病灶控制率为84.2%. 中位PFS为7.3 mo(范围2.3-34 mo). 单因素分析显示, 女性患者的PFS为14 mo, 男性的PFS为11 mo; ≥60岁的患者PFS为3.8 mo, <60岁患者的PFS为8.9 mo; <3 cm的肿瘤PFS为14 mo, 3-5 cm为10.7 mo, 5-10 cm为11.2 mo; 单个肿瘤的PFS为13.6 mo, ≥2个肿瘤的PFS为4 mo; Child A级的PFS为20.8 mo, Child B级的PFS为11.2 mo, Child A级患者的PFS高于Child B级的患者; BCLC 0期的患者PFS为15.5 mo, BCLC A期的患者PFS为11.2 mo, BCLC 0期患者的PFS明显高于BCLC A期; 术前HBV-DNA阳性的患者PFS为11.2 mo, HBV-DNA阴性的患者PFS为13.3 mo; HBeAg阳性的中位PFS为11.2 mo, HBeAg阴性的PFS为13.3 mo. 单因素分析显示, 性别、年龄、Child分级、肿瘤数目、BCLC分期有统计学差异, 肿瘤大小、术前HBV-DNA、HBeAg阳性无统计学差异. 具体结果详见表1.
| 因素 | PFS[中位数(四分位数间距)] | Z/χ2值 | P值 |
| 性别 | -2.376 | 0.016 | |
| 男 | 11.34 (9.80) | ||
| 女 | 14.04 (11.92) | ||
| 年龄 | -2.003 | 0.045 | |
| ≥60 | 3.75 (10.88) | ||
| <60 | 8.96 (10.46) | ||
| 肿瘤大小 | 4.706 | 0.095 | |
| <3 cm | 14.02 (9.71) | ||
| 3 cm | 10.71 (10.28) | ||
| 5 cm | 11.27 (12.95) | ||
| 肿瘤数目 | -2.673 | 0.008 | |
| 1个 | 13.58 (10.78) | ||
| ≥2个 | 3.94 (1.44) | ||
| Child分级 | -2.485 | 0.013 | |
| A | 20.79 (10.81) | ||
| B | 11.17 (10.03) | ||
| BCLC分期 | -2.095 | 0.036 | |
| 0 | 15.45 (9.73) | ||
| A | 11.19 (10.90) | ||
| 术前HBV-DNA | -0.75 | 0.453 | |
| 阴性 | 13.30 (10.69) | ||
| 阳性 | 12.16 (10.73) | ||
| HbeAg | -0.291 | 0.771 | |
| 阴性 | 13.32 (11.67) | ||
| 阳性 | 11.21 (8.29) |
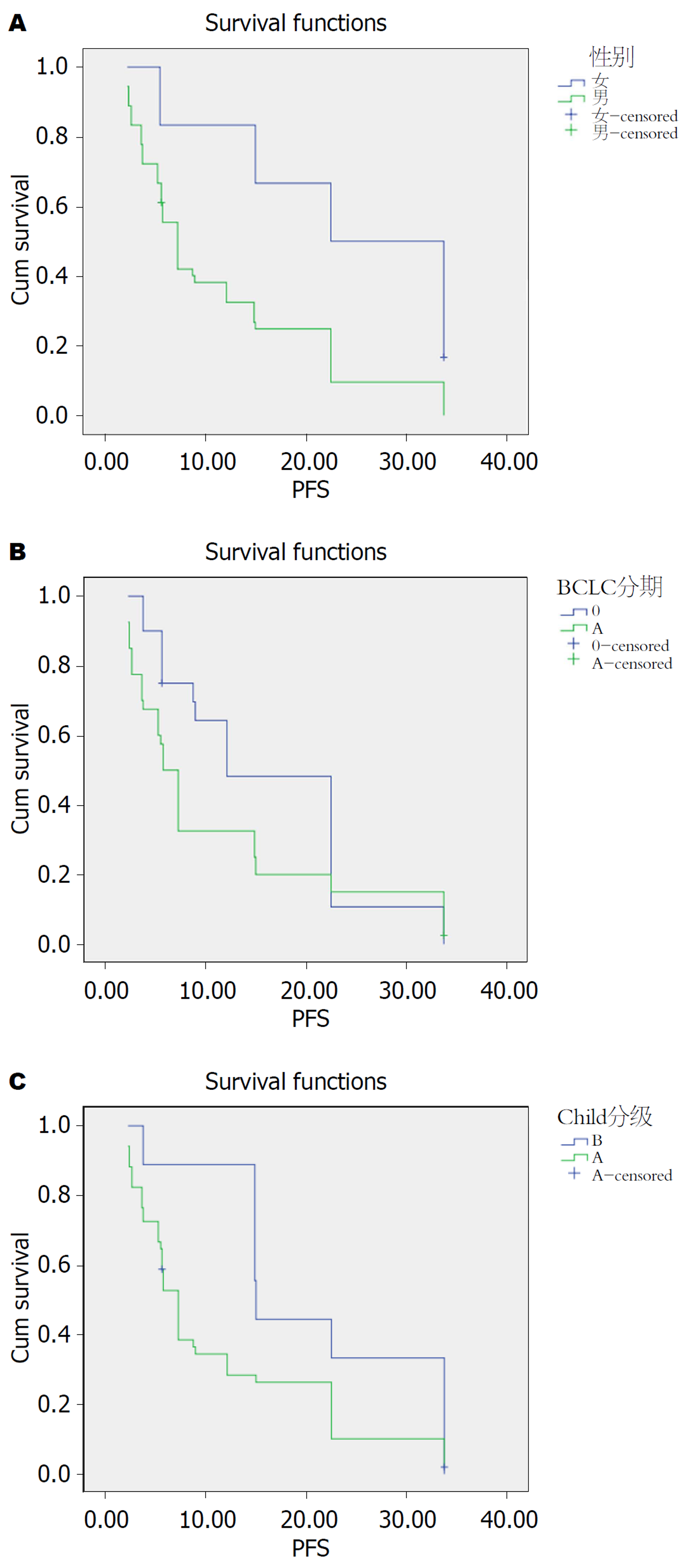
根据相关研究, 并结合单因素分析结果, 选取性别、年龄、肿瘤大小、肿瘤数目、Child分级、BCLC 0期和A期、术前HBV-DNA、HBeAg八个因素作为可能影响PFS的因素进行多重线性回归分析, 结果显示, 女性、BCLC 0期、Child A级患者PFS更高(图1A、图1B、图1C), 性别、BCLC 0期和A期、Child分级为影响TACE序贯MWA治疗HBV感染后的BCLC早期肝癌的PFS的独立危险因素(P<0.05)(表2).
| 变量 | 偏回归系数 | 标准误 | 标准化偏回归系数 | t值 | P值 |
| 性别 | -20.86 | 5.00 | -0.59 | -4.17 | <0.001 |
| 年龄 | 0.10 | 0.15 | 0.08 | 0.65 | 0.518 |
| 肿瘤大小 | 0.18 | 1.10 | 0.04 | 0.16 | 0.871 |
| 肿瘤数目 | 1.62 | 4.79 | 0.05 | 0.34 | 0.737 |
| Child分级 | -18.42 | 4.00 | -0.62 | -4.60 | <0.001 |
| BCLC分期 | -12.85 | 4.90 | -0.57 | -2.62 | 0.012 |
| 术前HBV-DNA | 3.86 | 2.74 | 0.18 | 1.41 | 0.165 |
| HbeAg | 0.02 | 3.17 | 0.00 | 0.01 | 0.994 |
一直以来, 国内外多数研究只关注肝癌术后生存率, 少有研究关注术后复发的影响因素. 与欧洲国家的肝癌发病诱因不同, 我国肝癌的诱因多为HBV感染, 由于乙肝表面抗原难以完全清除, 不论何种手术方式, 术后复发是长期以来亟待解决的问题. 2018年欧洲肝脏病学会指南建议, 对于BCLC A期肝癌, 早期的孤立肿瘤是外科切除的合适候选者[5]. 来自一项全球的肝癌中心的回顾性研究显示, 肝脏功能正常, BCLC 0-A原发性肝癌(hepatocellular carcinoma, HCC)的患者明显具有更好的无病生存率, 如果与慢性肝炎或肝硬化相关则不是这种情况. HBV感染引起的肝癌术后复发, 即使再次接受手术治疗效果也极差, 复发是影响肝癌术后生存时间的重要因素, 故研究术后复发影响因素意义重大.
已有研究指出, 慢性乙型肝炎患者肝癌根治性肝切除术后监测HCC与长期总体无复发率和无复发生存率有关[6], 早期诊断在延长HCC术后生存期上可能起到了最重要的作用. 多数肝癌发现已至晚期, 在本研究中, 所有确诊的早期肝癌患者均来自于我院肝病内科, 并长期接受规范的核苷类似物抗病毒治疗, 多数患者在定期随访过程中发现了肝癌, 截止到随访时间点, 未出现死亡或者失访, 说明肝癌早期诊断和HBV感染后肝癌术后管理至关重要.
TACE是选择性地将细胞毒性药物递送到肿瘤部位, 通过动脉栓塞导致肿瘤缺血性坏死[7]. 其优点是它可以保留肝脏功能[8,9]. 现有研究中TACE最常使用的抗癌药物是多柔比星(36%), 其次是顺铂(31%), 表阿霉素(12%), 米托蒽醌(8%), 丝裂霉素(8%)[10]. 经导管血管闭塞可通过各种栓塞剂实现, 包括可降解的明胶海绵和不可降解的产品, 如聚乙烯醇栓塞微球. 有研究显示, 在TACE/多柔比星治疗BCLC A期和B期乙肝和或丙肝后性肝癌时, 聚苯F涂层水凝胶微球的栓塞效果优于聚丙烯微球[11]. 在本研究中, 考虑到术后复发可能多次手术的问题, TACE术基本选用明胶海绵, 原因在于明胶海绵可以再通, 尽量将对肝功的影响降至最低. 在TACE术后, 最大限度的保留了肝脏功能, 无一例患者因为术后并发症影响序贯的MWA.
研究显示, Child A级[12,13]是肝癌患者局部消融后影响预后的因素, 与我们研究结论一致, 在术后复发时间上, Child A级的PFS明显长于Chlid B级的患者, 也有报道指出肿瘤大小和对治疗的反应[14]也是影响预后的原因之一. 与射频消融(radiofrequency ablation, RFA)相比, MWA可提供比射频消融更好的肿瘤反映[15]. 一项来自亚洲的Meta分析显示, MWA在3年生存率上略显优势, 但二者统计学上无显著性差异; 在复发上, MWA明显优于RFA, 尤其对肿瘤体积大的肝癌优势更显著, 二者具有统计学差异[16]. 在TACE联合RFA和MWA治疗大、中型HCC的回顾性研究中发现, TACE联合RFA组1年, 2年和3年累积生存率分别为68.30%, 36.60%和14.60%, 而TACE+MWA组分别为79.40%, 53.00%和38.20%. TACE联合RFA组无瘤生存率分别为53.70%, 29.30%和12.20%, TACE联合MWA组无瘤生存率分别为58.80%, 38.20%和29.40%. 两组存活率的差异以及术后不良反应的差异均无无统计学意义[17]. 在本研究中, 全部病例采用TCAE序贯MWA, 结果显示肿瘤大小并不是影响PFS的主要因素. 截止到随访之日, 所有病人全部存活, 故术后整体存活率需要进一步观察研究.
在孤立大肝癌和多发肝癌的治疗中, 与单独TACE相比, TACE+MWA在延长总生存期(overall survival, OS)方面具有更多优势, 疾病进展时间延长[18]. TACE+MWA组的进展时间和OS中位数分别为12.5 mo和26.6 mo, TACE组分别为6.7 mo和17.1 mo. TACE+MWA组的1年, 2年和3年OS率分别为85.9%, 59.8%和32.6%, TACE+MWA组的相应复发率分别为47.8%, 78.3%和94.6%, TACE组的复发率分别为74.7%, 96.4%和97.6%. 该研究的术后复发时间明显长于我们的研究, 但是我们发现, 该研究中, 应用了50 mg的洛铂灌注化疗栓塞, 术后出现了发热(77.2%), 腹痛(68.5%), 呕吐(39.1%), Ⅰ-Ⅱ级骨髓抑制(3.2%)等并发症, 术后并发症发生率高于我们的研究, 尽管我们的研究显示复发时间相对较短, 但是到随访时, 患者1年的OS达到100%. 在TACE术中应用化疗药物可能推后复发的时间, 但是是否对OS产生有益影响, 还需要临床大样本、随机、多中心的头对头的比较研究. 据报道, 肿瘤的数量预测了肝内扩散的程度[19], 肿瘤个数越多复发的机会越高. 在本研究中, 纳入的患者均为1-2个肿瘤, 且多数患者为单发肿瘤, 所以肿瘤个数并未为对PFS产生影响. HBV肝癌的患者中, 女性和较低的PS评分是TACE术后乙肝病毒再激活的重要原因[20]. 女性也较男性患者更容易出现TACE术后呕吐[21], 在本研究中, 并未采用化疗药物, 故出现呕吐并发症的比率大大降低, 结果显示女性比男性有更长的PFS, 考虑是因为本研究的女性患者仅有6例, 比率较低造成, 而且所有患者均持续应用核苷类似物抗病毒治疗, 并未出现术后HBV再激活. 鉴于男性患者有更高的吸烟、饮酒的比率[22], 故通常肝癌术后男性的OS低于女性患者. 在本研究中, 尚需继续观察.
本研究尚有不足之处, 研究为单臂研究, 未设置对照组, 如手术切除或TACE序贯RAF治疗组, 在以后的研究中, 可完善补充相关数据, 对比不同治疗方法的疗效及安全性等.
通过本研究, 对于HBV感染后的BCLC早期肝癌患者, TACE序贯MWA是有效的方法之一, 且不良反应少, 性别、BCLC分级和Child分期是影响术后复发的重要因素, 抗病毒的全程管理和术后监测对于管理HBV感染后的早期肝癌至关重要.
经肝动脉化疗栓塞术(transcatheter arterial chemoembolization, TACE)和微波消融术(microwave ablation, MWA)是目前各大肝癌指南均推荐的肝癌治疗方法, 因不同国家和地区肝癌发生的诱因不完全相同, 加之肿瘤异质性等问题, 术后复发率高, 影响患者的总生存期和生活质量.
为了探讨TACE序贯MWA治疗巴萨罗那临床肝癌分期(barcelona clinic liver cancer, BCLC)早期肝癌的效果, 以及哪些因素可能影响术后无进展生存期(progression-free-survival, PFS), 为临床肝癌治疗选择和术后监测提供一定的理论依据.
找出影响TACE序贯MWA治疗BCLC早期肝癌术后的PFS因素, 包括单因素与多因素分析的结果, 作为以后临床相同或相似手术后监测复发的根据之一.
采用前瞻性研究方法, 通过长期随访调查, 记录数据. 分析数据采用单因素及多因素分析, 生存曲线采用Kaplan-Meier生存分析法.
本研究已达到实验目的, TACE序贯MWA治疗BCLC早期肝癌手术总有效率为61.5%, 病灶控制率为84.2%. 中位PFS为7.3 mo(范围2.3-34 mo), 说明TACE序贯MWA治疗BCLC早期肝癌有效率尚可, 病灶控制率较高. 在影响术后PFS的单因素分析中, 性别、年龄、肿瘤数目, Child分级和BCLC分期均有统计学差异. 而在影响术后PFS的多因素分析结果中, Child分级、BCLC分期、性别显示有统计学差异. 提示在TACE序贯MWA治疗早期肝癌后, 要注意监测Child分级、BCLC分期和性别, 三者可能影响PFS.
本研究认为, TACE序贯MWA治疗BCLC早期肝癌是临床优先考虑的治疗策略之一, Child分级、BCLC分期、性别是影响术后PFS的重要因素.
本组病例将继续观察研究, 选择OS为观察终点, 研究PFS和OS的关系, 以及BCLC早期肝癌的整体OS究竟如何.
学科分类: 胃肠病学和肝病学
手稿来源地: 云南省
同行评议报告分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C, C, C, C
D级 (一般): 0
E级 (差): 0
编辑: 王禹乔 电编:刘继红
| 1. | Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68:394-424. [PubMed] [DOI] |
| 2. | Zeng H, Chen W, Zheng R, Zhang S, Ji JS, Zou X, Xia C, Sun K, Yang Z, Li H, Wang N, Han R, Liu S, Li H, Mu H, He Y, Xu Y, Fu Z, Zhou Y, Jiang J, Yang Y, Chen J, Wei K, Fan D, Wang J, Fu F, Zhao D, Song G, Chen J, Jiang C, Zhou X, Gu X, Jin F, Li Q, Li Y, Wu T, Yan C, Dong J, Hua Z, Baade P, Bray F, Jemal A, Yu XQ, He J. Changing cancer survival in China during 2003-15: a pooled analysis of 17 population-based cancer registries. Lancet Glob Health. 2018;6:e555-e567. [PubMed] [DOI] |
| 3. | Bruix J, Sherman M; American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma: an update. Hepatology. 2011;53:1020-1022. [PubMed] [DOI] |
| 4. | Lencioni R, Llovet JM. Modified RECIST (mRECIST) assessment for hepatocellular carcinoma. Semin Liver Dis. 2010;30:52-60. [PubMed] [DOI] |
| 5. | European Association for the Study of the Liver. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol. 2018;69:182-236. [PubMed] [DOI] |
| 6. | Li ZL, Wu H, Wei YP, Zhong Q, Song JC, Yu JJ, Li C, Wang MD, Xu XF, Li JD, Han J, Xing H, Lau WY, Wu MC, Shen F, Yang T. Impact of Surveillance in Chronic Hepatitis B Patients on Long-Term Outcomes After Curative Liver Resection for Hepatocellular Carcinoma. J Gastrointest Surg. 2019;. [PubMed] [DOI] |
| 7. | Wáng YX, De Baere T, Idée JM, Ballet S. Transcatheter embolization therapy in liver cancer: an update of clinical evidences. Chin J Cancer Res. 2015;27:96-121. [PubMed] [DOI] |
| 8. | Bruix J, Sherman M; Practice Guidelines Committee, American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma. Hepatology. 2005;42:1208-1236. [PubMed] [DOI] |
| 9. | Llovet JM, Di Bisceglie AM, Bruix J, Kramer BS, Lencioni R, Zhu AX, Sherman M, Schwartz M, Lotze M, Talwalkar J, Gores GJ; Panel of Experts in HCC-Design Clinical Trials. Design and endpoints of clinical trials in hepatocellular carcinoma. J Natl Cancer Inst. 2008;100:698-711. [PubMed] [DOI] |
| 10. | Marelli L, Stigliano R, Triantos C, Senzolo M, Cholongitas E, Davies N, Tibballs J, Meyer T, Patch DW, Burroughs AK. Transarterial therapy for hepatocellular carcinoma: which technique is more effective? A systematic review of cohort and randomized studies. Cardiovasc Intervent Radiol. 2007;30:6-25. [PubMed] [DOI] |
| 11. | Lee SH, Lin CY, Hsu YC, Liu YS, Chuang MT, Ou MC. Comparison of the Efficacy of Two Microsphere Embolic Agents for Transcatheter Arterial Chemoembolization in Hepatocellular Carcinoma Patients. Cancer Res Treat. 2019;. [PubMed] [DOI] |
| 12. | Hasegawa K, Kokudo N, Makuuchi M, Izumi N, Ichida T, Kudo M, Ku Y, Sakamoto M, Nakashima O, Matsui O, Matsuyama Y. Comparison of resection and ablation for hepatocellular carcinoma: a cohort study based on a Japanese nationwide survey. J Hepatol. 2013;58:724-729. [PubMed] [DOI] |
| 13. | Choi D, Lim HK, Rhim H, Kim YS, Lee WJ, Paik SW, Koh KC, Lee JH, Choi MS, Yoo BC. Percutaneous radiofrequency ablation for early-stage hepatocellular carcinoma as a first-line treatment: long-term results and prognostic factors in a large single-institution series. Eur Radiol. 2007;17:684-692. [PubMed] [DOI] |
| 14. | Sala M, Llovet JM, Vilana R, Bianchi L, Solé M, Ayuso C, Brú C, Bruix J; Barcelona Clínic Liver Cancer Group. Initial response to percutaneous ablation predicts survival in patients with hepatocellular carcinoma. Hepatology. 2004;40:1352-1360. [PubMed] [DOI] |
| 15. | Marrero JA, Kulik LM, Sirlin CB, Zhu AX, Finn RS, Abecassis MM, Roberts LR, Heimbach JK. Diagnosis, Staging, and Management of Hepatocellular Carcinoma: 2018 Practice Guidance by the American Association for the Study of Liver Diseases. Hepatology. 2018;68:723-750. [PubMed] [DOI] |
| 16. | Huang Q, Yang H, Lin QN, Qin X. 'Microwave ablation versus radiofrequency ablation for the treatment of hepatocellular carcinoma: a systematic review and meta-analysis': Two issues should be noted. Int J Hyperthermia. 2016;32:345. [PubMed] [DOI] |
| 17. | Cotofana S, Lachman N. The Superficial Face Dissection as an Example for Integrating Clinical Approaches, Authentic Learning, and Changing Perspectives in Anatomy Dissection. Anat Sci Educ. 2019;. [PubMed] [DOI] |
| 18. | Zheng L, Li HL, Guo CY, Luo SX. Comparison of the Efficacy and Prognostic Factors of Transarterial Chemoembolization Plus Microwave Ablation versus Transarterial Chemoembolization Alone in Patients with a Large Solitary or Multinodular Hepatocellular Carcinomas. Korean J Radiol. 2018;19:237-246. [PubMed] [DOI] |
| 19. | Zhong JH, Rodríguez AC, Ke Y, Wang YY, Wang L, Li LQ. Hepatic resection as a safe and effective treatment for hepatocellular carcinoma involving a single large tumor, multiple tumors, or macrovascular invasion. Medicine (Baltimore). 2015;94:e396. [PubMed] [DOI] |
| 20. | Li X, Zhong X, Chen ZH, Wang TT, Ma XK, Xing YF, Wu DH, Dong M, Chen J, Ruan DY, Lin ZX, Wen JY, Wei L, Wu XY, Lin Q. Efficacy of Prophylactic Entecavir for Hepatitis B Virus-Related Hepatocellular Carcinoma Receiving Transcatheter Arterial Chemoembolization. Asian Pac J Cancer Prev. 2015;16:8665-8670. [PubMed] [DOI] |
| 21. | Wang SY, Zhu WH, Vargulick S, Lin SB, Meng ZQ. Nausea and vomiting after transcatheter arterial chemoembolization for hepatocellular carcinoma: incidence and risk factor analysis. Asian Pac J Cancer Prev. 2013;14:5995-6000. [PubMed] [DOI] |
| 22. | Wu EM, Wong LL, Hernandez BY, Ji JF, Jia W, Kwee SA, Kalathil S. Gender differences in hepatocellular cancer: disparities in nonalcoholic fatty liver disease/steatohepatitis and liver transplantation. Hepatoma Res. 2018;4. [PubMed] [DOI] |