修回日期: 2019-04-15
接受日期: 2019-05-15
在线出版日期: 2019-06-28
炎症性肠病(inflammatory bowel disease, IBD)是一种慢性、炎症性、自身免疫性疾病, 其发病机制尚未明确, 目前认为是由宿主易感基因、环境、肠道菌群等因素综合作用引发机体异常免疫炎症应答所致. 研究证明, 情绪障碍与IBD的发生发展关系密切, 其可通过改变下丘脑-垂体-肾上腺轴或影响肠道菌群进而影响肠动力、肠道激素分泌、免疫等加重IBD患者的临床症状并增加复发可能性. 在临床治疗中必要时予以心理干预改善情绪障碍有利于提高IBD患者的生存质量. 本文就IBD与情绪障碍之间的关系进行了梳理和总结.
核心提要: 近年来, 情绪在炎症性肠病(inflammatory bowel disease, IBD)中的作用越来越受到重视. 不良情绪可加重临床症状, 增加复发率, 降低治疗依从性等, 一定的心理干预可提高患者的生存质量. 本文梳理了情绪与IBD的关系, 为IBD发病及治疗提供线索.
引文著录: 李思慧, 吴巧凤. 炎症性肠病与情绪障碍. 世界华人消化杂志 2019; 27(12): 727-733
Revised: April 15, 2019
Accepted: May 15, 2019
Published online: June 28, 2019
Inflammatory bowel disease (IBD) is a group of inflammatory conditions which arise as a result of the interactions of susceptible genetic factors, environment, and intestinal microbiota, which lead to abnormal immunological responses and inflammation in the colon and small intestine. The exact pathogenesis of IBD is still unclear. Studies have shown that the existence of emotional dysfunction such as depression or anxiety contributes to the onset and development of IBD. It has been proposed that emotional changes may mediate or influence the gut microbiota-brain axis, thereby influencing intestinal motility, hormone secretion, and immunity, aggravating the intestinal immune inflammatory response, and increasing the clinical symptoms and recurrent risk of IBD. Giving psychological treatments when necessary will be beneficial to patients with IBD. In this paper, we discuss the relationship between emotional dysfunction and IBD.
- Citation: Li SH, Wu QF. Emotional dysfunction and inflammatory bowel disease. Shijie Huaren Xiaohua Zazhi 2019; 27(12): 727-733
- URL: https://www.wjgnet.com/1009-3079/full/v27/i12/727.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v27.i12.727
炎症性肠病(inflammatory bowel disease, IBD)是一种慢性、复发性、非特异性肠道疾病, 包括克罗恩病(crohn's disease, CD)和溃疡性结肠炎(ulcerative colitis, UC). 近年来IBD发病有明显上升趋势, 除欧美等高发地区外, 原本低发病率地区如东欧、亚洲等, 其患病率也呈持续上升趋势. 中国UC和CD的患病率分别为(120-200)/10万和(50-200)/10万[1], 严重地影响着患者的生活质量和社会经济发展. 目前IBD发病原因未知, 可能与遗传、环境、异常的免疫应答及情绪等多种因素相关. 其中, 情绪障碍与IBD的关系逐渐引起人们的重视. 研究发现, IBD患者较健康人群普遍存在不同程度的情绪紊乱[2], 如焦虑、抑郁、敏感、内向、悲观、失望等, 反之, 长期处于情绪障碍中, 不但会加重患者的病情, 降低患者的生活质量, 同时还会增加IBD复发的风险[3,4]. 故本文就情绪障碍与IBD的关系进行梳理及总结.
IBD患者易伴有抑郁、焦虑情绪, 据报道其抑郁症发生率是全球平均抑郁症发生率的2-4倍[5], 焦虑症发生率是全球平均焦虑症发生率的2-5倍[6], 且其严重程度与疾病活动度、生活质量等密切相关. Bhamre等[7]对170名IBD患者的观察性研究表明, 抑郁发生率为34.3%, 焦虑发生率为18.6%, 二者与疾病活动度呈正相关. Iglesiasrey等[8]对875名患者的横断面调查显示, 抑郁发生率为20.1%, 焦虑发生率为10.5%. Bennebroek Evertsz等[9]的临床调查显示, 231名IBD患者中抑郁、焦虑的发生率为43%. 国内胡兰等[10]通过临床调查发现在231名IBD患者中, 抑郁发生率为59.90%, 焦虑发生率为66.18%. 胡义亭等[11]发现, 60名患者中60%有抑郁情绪, 45%有焦虑情绪, 且严重影响患者生活质量. 陈晨等[12]纳入101名患者的临床调查提示, 抑郁发生率为44.5%, 焦虑发生率为48.5%. 李雪娇等[13]的临床调查显示, 102名患者中, 抑郁发生率为65.69%, 焦虑发生率为47.06%. 李晓婷等[14]发现, 115名IBD患者中48.6%有抑郁症状, 42.6%有焦虑症状. 张茂琛等[15]针对CD的临床调查表明, 128名患者中, 抑郁发生率为61.7%, 焦虑发生率为83.5%. 一项前瞻性研究显示有55%的IBD患者会产生抑郁、焦虑情绪[16]. Vegni等[17]的队列研究提示约40.9%的IBD患者认为抑郁或焦虑症状是引发IBD的原因之一. Bannaga等[18]报道IBD疾病缓解期约有35%合并有抑郁或焦虑情绪, 活动期合并有抑郁情绪的患者高达60%, 焦虑情绪更高达80%. 上述流行病学调查显示IBD患者存在广泛的焦虑与抑郁情绪障碍. 系统评价的证据则更具说服力, Neuendorf等[19]对所纳入的171篇文章、158371名患者的系统评价研究表明, IBD患者焦虑的发生率约为20%, 抑郁的发生率约为15%. 在这158371名患者中, 与疾病的缓解期相比, 处于疾病活动期的IBD患者焦虑发生率更高, 为75.6%, 抑郁症状的发生率为21.6%. Mikocka-Walus等[20]的系统评价也显示, 处于活动期的IBD患者抑郁发生率为66.4%, 焦虑发生率为34.7%, 提示IBD患者较正常人更易产生抑郁、焦虑症状, 且疾病活动期负面情绪产生率更高.
IBD患者可具有神经质、内向、敏感、易激惹、易怒等心理障碍及对外界刺激反应强烈, 环境适应能力较差等特点. Neuendorf等[19]的系统评价提示, 除抑郁焦虑外, IBD患者强迫症的发生率为9.4%, 高于世界平均强迫症患病率2%. Sewitch等[21]的横断面研究显示, 处于疾病活动期的IBD患者约有50%伴有悲伤情绪. 此外, Carrozzino等[22]的系统评价提示约有33%的IBD患者有述情障碍, 即以"病人不能识别、描述情感, 不能与他人交流情感"为特点[23], 这是一种独立于抑郁、焦虑的情绪障碍. 但在伴有抑郁及焦虑的IBD患者中, 述情障碍发生率更高, 可分别达33.3%及42%[24]. 无论是哪种情绪改变, 均能严重地影响IBD患者的康复.
消化系统是情绪的反应板, 据报道有45%-75%的消化疾病伴有心身因素[25]. 针对IBD疾病, 不良情绪会影响肠动力及肠道促炎因子与抑炎因子的平衡, 破坏肠道黏膜屏障, 从而加重临床症状、疾病活动度、增加远期复发率、影响患者生活质量、睡眠质量等. Mawdsley等[26]发现, 焦虑或抑郁会导致异常的结肠运动形式, 结肠运动次数及幅度会增加; 同时会抑制机体免疫力, 损伤肠道黏膜屏障功能, 使肠上皮通透性增加, 细菌抗原及毒物更易渗透至肠道黏膜下层. Chen等[27]发现抑郁或焦虑会导致部分肠道菌群移位及肠道微生物丰富度和数量的改变. Cámara等[28]发现处于不良情绪状态下, 被激活的肥大细胞会脱颗粒释放相应促炎因子如IL-1、IL-8、IL-23等, 从而加重肠道炎症反应. Yongwen等[29]及张淑艳等[30]的临床调查发现情绪障碍会增加自主神经的兴奋性, 通过调节内脏核团加重疼痛感, 使IBD患者腹痛程度升高.
此外, 情绪紊乱的程度也与疾病的严重程度密切相关, 有效的情绪管理对IBD疾病的康复与治疗具有重要价值. Castillo等[31]的研究发现, 与没有或者轻度抑郁症的CD患者相比, 中度至重度抑郁症的CD患者出现中重度IBD疾病活动的可能性增加2.165倍(OR = 2.165, P = 0.022); 此外, 与没有或轻度抑郁症相比, 中度至重度抑郁症的UC患者出现中度至重度IBD疾病活动的可能性为3.151倍(OR = 3.151, P = 0.008). 一项纳入763449例UC患者的大样本研究[32]发现, 从1994年至2009年间, 在UC发病前后出现的情绪障碍均对UC的进展有一定影响, 提示情绪障碍可能为导致UC的病因之一. Narula等[33]的前瞻性纵向随访研究提示, 从2008-2016年间, 在纳入研究时已具有不同程度焦虑症状的125名IBD患者较剩下289名患者更易产生不良结局, 如高疾病活动度, 高复发率, 高住院率等. Mikocka-Walus等[20]的一项大样本、前瞻性、纳入2007例IBD患者的队列研究发现, 随着病程推移, 抑郁症、焦虑症和临床复发症状之间存在显著联系(P = 0.000001). Ghosh等[34]的前瞻性队列研究(n = 2007), 提示抑郁症的存在会增加IBD的复发率(P<0.001). Izaguirre等[35]在关于青少年IBD患者的自我效能量表的评分结果中发现, IBD患者的情绪障碍程度及临床症状严重程度与自我效能得分呈负相关, 即情绪障碍程度越低, 临床症状越轻, 患者自我效能得分越高, 生活质量水平越高.
《IBD诊断与治疗的共识意见(2018年, 北京)》[36]中强调, 在临床治疗中要加强患者的情绪管理以降低疾病严重程度、复发频率, 预防并发症, 减少住院和手术切除率, 提高生活质量. 研究显示从情绪管理方面着手, 确可有效地改善患者的情绪障碍[37], 并能一定程度缓解患者的临床症状及提高其生活质量. 首先, 抗焦虑抑郁药的作用不容忽视, 已有研究[38]证明抗抑郁药可有效地降低IBD的活动性, 缓解患者胃肠道的症状. 例如, Daghaghzadeh等[39]将抗抑郁药物度洛西汀应用于IBD患者的治疗过程中, 12 wk后完成试验的35名患者的抑郁、焦虑状态得以改善(P = 0.041, P = 0.049), 生存质量得以提高(P = 0.015), 并且改善程度远大于安慰剂组. 一项纳入了14例经低剂量三环类抗抑郁药治疗的UC患者的回顾性研究提示[40], 与治疗前相比, 患者在抗抑郁治疗一年内UC的复发率(P = 0.002)和类固醇类药物的使用率(P<0.001)均显著降低. 张炜等[41]发现加用氟哌噻吨美利曲辛的黛力新组IBD患者较采用常规疗法的对照组, 临床症状改善更为明显, 溃疡愈合率更高(χ2 = 11.99, P<0.05). 胡义亭等[42]将60名IBD患者分为黛力新组(n = 30)及对照组(n = 30), 进行抗抑郁焦虑治疗后, 黛力新组患者抑郁自评量表(self-rating depression scale, SDS)及焦虑自评量表(self-rating anxiety scale, SAS)较前均有明显下降(P<0.05), 且评分水平明显低于对照组(P<0.05). 研究显示抗焦虑或抗抑郁治疗可提高患者的生活质量, 同时降低肠道的炎症水平. 其次, 认知行为疗法也对缓解IBD症状有益. 刘春霞等[43]采用认知行为干预疗法辅助治疗IBD, 10 wk后, 研究组的患者SAS、SDS评分较干预前明显下降(47.11±8.82, 38.25±9.33), (48.13±9.33, 41.28±7.13), (P<0.01); 研究组评分水平明显低于对照组(P<0.01), 患者的心理状态明显改善, 生活质量也得到显著提升. Schoultz等[44]的多中心临床试验也提示认知行为疗法可改善IBD患者的抑郁、焦虑等(P = 0.083, P = 0.027), 情绪管理后即可提高患者的生活质量. Lores等[45]在为期一年的综合心理疗法干预后, 患者的抑郁(M1 = 8.38 vs M2 = 6.42, P<0.001)、焦虑(M1 = 12.11 vs M2 = 9.59, P<0.001)、整体压力水平(M1 = 17.99 vs M2 = 13.96, P<0.001)、生活质量(M1 = 57.60 vs M2 = 64.10, P<0.001)均有不同程度改善. Gracie等[46]的系统评价证实在短期内心理疗法及认知行为疗法可改善患者的抑郁症状、提升患者生活质量, 其纳入从1947-2016年间的发表的临床对照试验共1196人, 抑郁评分(P = 0.04; I2 = 0%)与生活质量(P = 0.01; I2 = 42%)对比对照组均有较大改善. 此外, Wynne等[47]为期8 wk的临床对照试验表明接受与实现疗法也能明显改善压力(P = 0.036)、抑郁(P = 0.010)及整体生活质量水平(P = 0.009).
肠道菌群及相关神经-内分泌-免疫网络是目前认为广泛参与IBD和情绪障碍的重要原因. 菌群可以通过自身代谢及产物影响机体, 而机体也可通过神经、免疫、内分泌系统网络调节肠道菌群的变化, 但具体机制目前尚不清楚, 相关研究亟待深入.
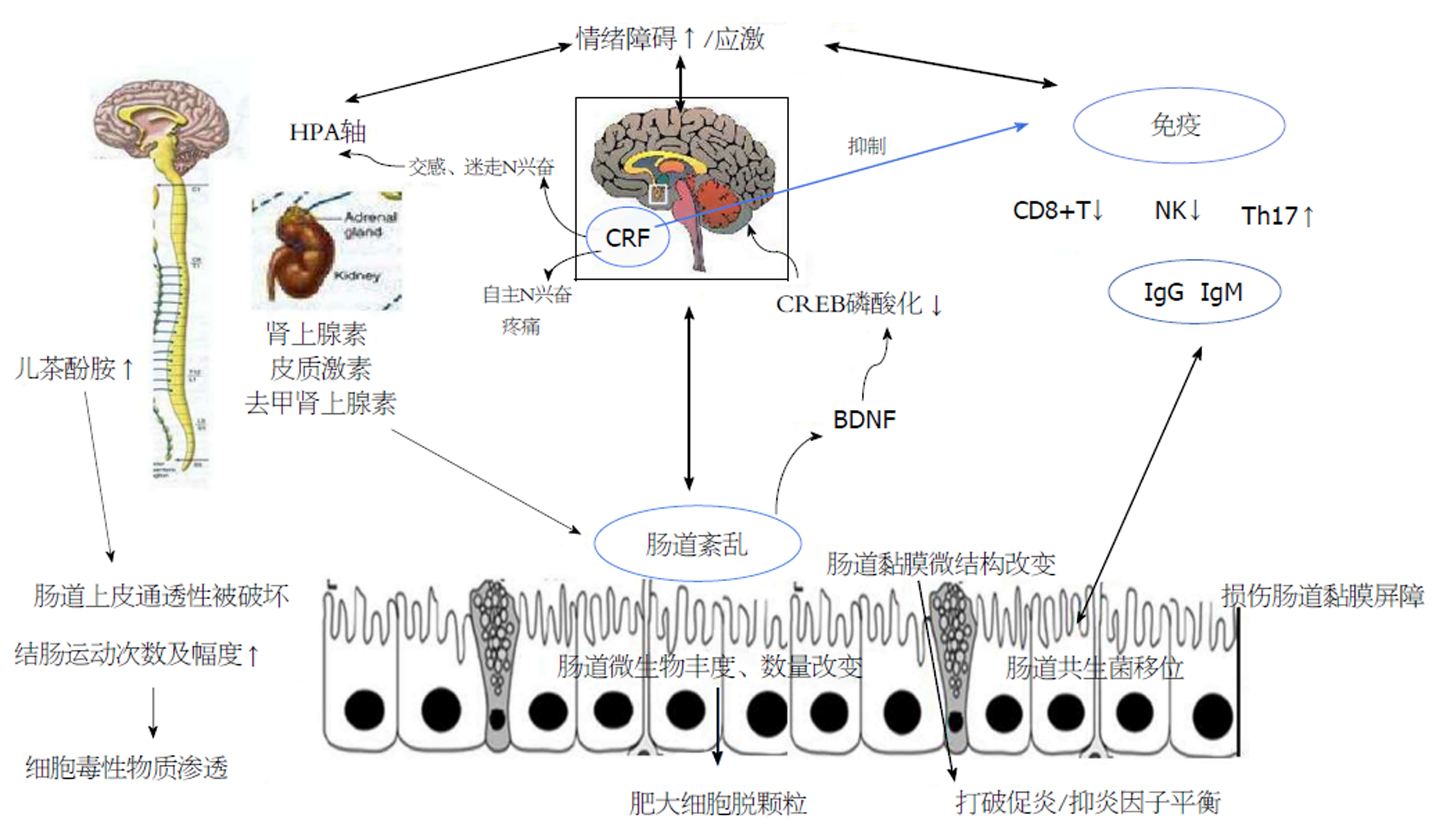
作为神经内分泌系统重要的组成部分, 下丘脑-垂体-肾上腺轴(the hypothalamic-pituitary-adrenal axis, HPA)的异常与抑郁、焦虑、双相障碍等密切相关[48]. 在长期的情绪障碍如抑郁、焦虑等应激状态下, HPA轴被激活, 介由下丘脑及外周肾上腺释放的促肾上腺皮质激素释放因子(corticotropin releasing factor, CRF)一方面直接影响中枢神经系统的兴奋性, 另一方面可作用于肠道, 使其发生相应物理改变或导致肠道菌群紊乱(图1).
不良情绪可首先兴奋大脑皮质, 其次通过边缘系统皮质-纹状体-苍白球-下丘脑环路兴奋下丘脑, 使其释放CRF. CRF的存在可使肾上腺皮质释放糖皮质激素, 抑制免疫功能, 损伤肠道黏膜屏障功能[26], 使细胞毒性物质渗透, 加重肠道炎症. 其次, CRF可导致交感神经功能亢进, 儿茶酚胺和肾上腺髓质释放增加, 结肠运动次数和幅度增强, 产生异常的结肠运动形式, 加重IBD患者的临床症状[26]. CRF还可使肠道肥大细胞的数量增多[27], 活性增强, 削弱肠道黏膜的屏障作用, 通过肥大细胞脱颗粒的方式及促炎因子的释放加重局部肠道炎症. 同时, CRF能导致自主神经中枢核团对内脏感觉及疼痛反应的调控等改变, 引发对胃肠道功能状态的感知反应和调控偏差, 导致相应运动感觉异常. CRF还可降低食欲, 使人体摄入肠道营养不足, 增加肠黏膜上皮的损伤概率. 此外, 精神心理因素还可使患者血清中的CD8+T细胞、NK细胞减少、T细胞功能异常[49], 导致机体免疫功能的异常.
此外, 不良情绪的刺激可通过中枢激活交感神经系统, 进而破坏肠道通透性、改变肠道微生物的构成、增加免疫刺激剂中细菌细胞壁免疫成分的循环水平, 进而增加细胞毒物的成分及促炎因子的释放. 研究证明, 持续4 mo慢性间断性的注射脂多糖(lipopolysaccharide, LPS)可造成小鼠的抑郁状态[50], 急性的LPS紊乱也可导致抑郁样行为的出现. LPS紊乱会产生炎性、氧化性及硝化性(inflammatory, oxidative and nitrosative, IO and NS)过程及Toll样受体, 升高中枢及外周的相关促炎细胞因子水平如TNF-α, IL-1β等, 并通过改变胶质细胞活性导致中枢炎症及抑郁样行为.
情绪障碍还可激活免疫细胞, 诱发IgM和IgM的免疫应答, 使肠道共生菌移位, 加重肠道炎症. 外源性刺激可激活肠道的肥大细胞, 使其脱颗粒释放出促炎细胞因子如IL-1、IL-2、IL-6、IL-8、IFN-γ、TNF-α等, 增加肠道上皮通透性, 细菌抗原及毒物渗入肠道黏膜下层加重肠道炎症. 研究证明[49], 长期暴露于应激状态下(如情绪障碍及负性生活事件等)可改变肠道黏膜超微结构, 并增加促炎因子如IL-1β、IL-6、TNF-α的产生, 加重炎症状态及肠道代谢的异常. 异常的肠道炎症状态及肠道代谢异常反过来加重情绪障碍, 形成恶性循环. 研究证明, 不平衡的人犬尿氨酸(Kyn)与色氨酸(tryptophan)的比值及5-HT水平可能造成抑郁状态. 中枢神经系统中, 5-HT参与了情绪的调节过程、行为及认知功能. 在炎症状态下可促进人犬尿氨酸的产生酶生成, 进而加速色氨酸介由人犬尿氨酸途径的代谢频率, 使5-HT水平降低[51], 又可通过调节脑内海马组织BDNF的水平及其mRNA表达降低环磷腺苷效应元件结合蛋白的磷酸化, 加重情绪障碍[52]. 此外, Kyn还可通过分解代谢的喹啉酸[51], 一种神经毒性剂, 抑制N-甲基-D-天冬氨酸受体(N-methyl-D-aspartic acid receptor, NMDA)参与抑郁症状的产生过程.
随着医学模式从"生物-医学"模式向"生物-心理-社会"模式转变, 情绪对疾病的影响日益受到关注. IBD作为一种心身疾病, 很有必要全面梳理情绪障碍在IBD中的作用, 深入研究情绪与IBD之间相互作用的机制. 目前, 在临床工作中, 针对情绪障碍的诊断及监管仍有一定问题. Lewis等[53]的研究表明, 在被调查的242名IBD患者中, 33%拥有抑郁症状及67%拥有焦虑症状的患者均被漏诊. 其中男性被漏诊抑郁症的概率更高(OR = 3.36; 95%CI: 1.28-8.85). Janmohamed等[54]的研究表明仅有32%及42%的焦虑、抑郁症状被临床诊断, 剩余患者的情绪问题在临床治疗过程中可能因量表评估工具使用不当等原因造成漏诊. 除漏诊外, Moulton等[55]的最新研究提出, 当前应用于诊断抑郁的医院焦虑抑郁评分(hospital anxiety and depression scale, HADS)仅有38%的诊断敏感性, 即被诊断的部分IBD患者中可能存在误诊. 在临床中, 应用于抑郁的常用量表目前有HADS、患者健康问卷(patient health questionnaire, PHQ-8/9)及SDS等. 应用于焦虑的常用量表为HADS及SAS. 在针对IBD疾病中产生的抑郁、焦虑情绪, 不同量表有各自的不足. HADS为综合量表, 适用范围广, 信度好, 内部一致性高, 但在评判IBD过程中并未囊括其特有的躯体症状如疲倦、睡眠障碍等而显得效度较低, 在评判过程中可能会受到躯体症状影响而产生偏倚. Bernstein等[2]针对以上量表的信效度分析表明, HADS的临界值(cut-point)较其他量表敏感性更低. 相比之下, PHQ-9量表更适合应用于IBD患者情绪障碍的评价因其纳入了躯体症状及自杀倾向等多种问题. SAS及SDS为自评量表, 虽具有耗时较短, 评定速度快, 便于随访等优势, 但SAS与其他焦虑量表相较其评定一致性仅为轻到中等程度[56], SDS则特异性较低. 目前临床治疗过程中针对不良情绪的监管力度仍显不足, Bennebroek等的[9]研究提示, 伴有不良情绪的IBD患者中仅17.9%接受精神心理干预治疗, 10.5%服用抗抑郁药, 7.4%服用抗焦虑药, 3%同时服用抗抑郁和抗焦虑药, 证明除明确诊断外, 施行相应管理措施也尤为重要.
此外, 究竟是什么原因引发了抑郁、焦虑等情绪仍不清楚, 可能与躯体症状、性别、年龄、疾病活动度、手术、社会支持度等相关. Jonefjäll等[57]的纳入288名IBD患者的横断面研究及Chavarría等[58]的纳入544名IBD患者的前瞻性多中心研究(n = 22)均表明, 其中有41%有疲倦症状, 其严重程度与抑郁、焦虑等情绪障碍的严重程度密切相关. Hood等[59]的临床调查显示, 睡眠障碍与情绪关系密切, 可能成为引发不良情绪的高危因素之一. 即不良情绪极有可能由躯体症状而诱发, 故在临床治疗中, 有针对性的缓解躯体症状可能会降低不良情绪的发生率.
临床针对IBD情绪紊乱治疗方面已有一些针对性的措施, 但在众多的精神心理疗法中, 究竟哪一种疗法能达到最好的疗效仍有待进一步研究. 此外, 情绪状态究竟改善到何种程度才能将对IBD患者的影响降到最低, 从而更好地缓解IBD患者的临床症状及降低远期复发率, 我们又将如何将情绪改善程度进一步量化, 这些问题也是目前研究的热点. 总之, IBD是生物、心理和社会共同作用的结果, 随着生活方式的改变, 生活节奏的加快, 应激源的增加, 情绪、应激等极易诱发IBD, 而针对性地情绪管理将具有重要的缓冲作用. 因此, 对于IBD患者, 临床上在应用药物治疗的同时, 还应注意给予心理治疗, 使患者尽快康复.
学科分类: 胃肠病学和肝病学
手稿来源地: 四川省
同行评议报告分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C
D级 (一般): D
E级 (差): E
编辑: 崔丽君 电编:刘继红
| 1. | Ng WK, Wong SH, Ng SC. Changing epidemiological trends of inflammatory bowel disease in Asia. Intest Res. 2016;14:111-119. [PubMed] [DOI] |
| 2. | Bernstein CN, Hitchon CA, Walld R, Bolton JM, Sareen J, Walker JR, Graff LA, Patten SB, Singer A, Lix LM, El-Gabalawy R, Katz A, Fisk JD, Marrie RA; CIHR Team in Defining the Burden and Managing the Effects of Psychiatric Comorbidity in Chronic Immunoinflammatory Disease. Increased Burden of Psychiatric Disorders in Inflammatory Bowel Disease. Inflamm Bowel Dis. 2019;25:360-368. [PubMed] [DOI] |
| 3. | Hauser W, Moser G, Klose P, Mikocka-Walus A. Psychosocial issues in evidence-based guidelines on inflammatory bowel diseases: a review. World J Gastroenterol. 2014;20:3663-3671. [PubMed] [DOI] |
| 4. | Tabibian A, Tabibian JH, Beckman LJ, Raffals LL, Papadakis KA, Kane SV. Predictors of health-related quality of life and adherence in Crohn¡¯s disease and ulcerative colitis: implications for clinical management. Dig Dis Sci. 2015;60:1366-1374. [PubMed] [DOI] |
| 5. | Ferrari AJ, Charlson FJ, Norman RE, Patten SB, Freedman G, Murray CJ, Vos T, Whiteford HA. Burden of depressive disorders by country, sex, age, and year: findings from the global burden of disease study 2010. PLoS Med. 2013;10:e1001547. [PubMed] [DOI] |
| 6. | Baxter AJ, Scott KM, Vos T, Whiteford HA. Global prevalence of anxiety disorders: a systematic review and meta-regression. Psychol Med. 2013;43:897-910. [PubMed] [DOI] |
| 7. | Bhamre R, Sawrav S, Adarkar S, Sakaria R, J Bhatia S. Psychiatric comorbidities in patients with inflammatory bowel disease. Indian J Gastroenterol. 2018;37:307-312. [PubMed] [DOI] |
| 8. | Iglesias-Rey M, Barreiro-de Acosta M, Caamano-Isorna F, Rodriguez IV, Ferreiro R, Lindkvist B, Gonzalez AL, Dominguez-Munoz JE. Psychological factors are associated with changes in the health-related quality of life in inflammatory bowel disease. Inflamm Bowel Dis. 2014;20:92-102. [PubMed] [DOI] |
| 9. | Bennebroek Evertsz F, Thijssens NA, Stokkers PC, Grootenhuis MA, Bockting CL, Nieuwkerk PT, Sprangers MA. Do Inflammatory Bowel Disease patients with anxiety and depressive symptoms receive the care they need? J Crohns Colitis. 2012;6:68-76. [PubMed] [DOI] |
| 15. | 张 茂琛, 洪 理文, 张 天宇, 林 筠, 胡 淑榕, 程 朦朦, 郑 思畅, 范 嵘, 王 正廷, 钟 捷. 克罗恩病患者健康状况、疾病认知、应对方式与心理状况之间的关系. 内科理论与实践. 2016;11:37-41. |
| 16. | Brooks AJ, Norman P, Peach EJ, Ryder AH, Scott AJ, Narula P, Corfe BM, Lobo AJ, Rowse G. Prospective Study of Psychological Morbidity and Illness Perceptions in Young People with Inflammatory Bowel Disease. J Crohns Colitis. 2019;. [PubMed] [DOI] |
| 17. | Vegni E, Gilardi D, Bonovas S, Corro BE, Menichetti J, Leone D, Mariangela A, Furfaro F, Danese S, Fiorino G. Illness Perception in Inflammatory Bowel Disease Patients is Different Between Patients With Active Disease or in Remission: A Prospective Cohort Study. J Crohns Colitis. 2019;13:417-423. [PubMed] [DOI] |
| 18. | Bannaga AS, Selinger CP. Inflammatory bowel disease and anxiety: links, risks, and challenges faced. Clin Exp Gastroenterol. 2015;8:111-117. [PubMed] [DOI] |
| 19. | Neuendorf R, Harding A, Stello N, Hanes D, Wahbeh H. Depression and anxiety in patients with Inflammatory Bowel Disease: A systematic review. J Psychosom Res. 2016;87:70-80. [PubMed] [DOI] |
| 20. | Mikocka-Walus A, Pittet V, Rossel JB, von Kanel R; Swiss IBD Cohort Study Group. Symptoms of Depression and Anxiety Are Independently Associated With Clinical Recurrence of Inflammatory Bowel Disease. Clin Gastroenterol Hepatol. 2016;14:829-835.e1. [PubMed] [DOI] |
| 21. | Sewitch MJ, Abrahamowicz M, Bitton A, Daly D, Wild GE, Cohen A, Katz S, Szego PL, Dobkin PL. Psychological distress, social support, and disease activity in patients with inflammatory bowel disease. Am J Gastroenterol. 2001;96:1470-1479. [PubMed] [DOI] |
| 22. | Carrozzino D, Porcelli P. Alexithymia in Gastroenterology and Hepatology: A Systematic Review. Front Psychol. 2018;9:470. [PubMed] [DOI] |
| 23. | Vigano CA, Beltrami MM, Bosi MF, Zanello R, Valtorta M, Maconi G. Alexithymia and Psychopathology in Patients Suffering From Inflammatory Bowel Disease: Arising Differences and Correlations to Tailoring Therapeutic Strategies. Front Psychiatry. 2018;9:324. [PubMed] [DOI] |
| 24. | Son SH, Jo H, Rim HD, Kim JH, Kim HW, Bae GY, Lee SJ. A Comparative Study on Alexithymia in Depressive, Somatoform, Anxiety, and Psychotic Disorders among Koreans. Psychiatry Investig. 2012;9:325-331. [PubMed] [DOI] |
| 26. | Mawdsley JE, Rampton DS. Psychological stress in IBD: new insights into pathogenic and therapeutic implications. Gut. 2005;54:1481-1491. [PubMed] [DOI] |
| 27. | Chen C, Brown DR, Xie Y, Green BT, Lyte M. Catecholamines modulate Escherichia coli O157:H7 adherence to murine cecal mucosa. Shock. 2003;20:183-188. [PubMed] [DOI] |
| 28. | Camara RJ, Lukas PS, Begre S, Pittet V, von Kanel R; Swiss Inflammatory Bowel Disease Cohort Study Group. Effects of social support on the clinical course of Crohn’s disease. Inflamm Bowel Dis. 2011;17:1277-1286. [PubMed] [DOI] |
| 29. | Yongwen Ng J, Chauhan U, Armstrong D, Marshall J, Tse F, Moayyedi P, Reinisch W, Halder S. A Comparison of the Prevalence of Anxiety and Depression Between Uncomplicated and Complex IBD Patient Groups. Gastroenterol Nurs. 2018;41:427-435. [PubMed] [DOI] |
| 31. | Castillo A, Fasihuddin F, Saliaj M, Nolan A, Reyes P, Rodriguez MC, Cruz KS, Aly S. Tu2015 The impact of depression on disease activity in inflammatory bowel disease (IBD) patients. Gastroenterology. 2016;150:S1006. [DOI] |
| 32. | Cawthorpe D, Davidson M. Temporal comorbidity of mental disorder and ulcerative colitis. Perm J. 2015;19:52-57. [PubMed] [DOI] |
| 33. | Narula N, Pinto-Sanchez MI, Calo NC, Ford AC, Bercik P, Reinisch W, Moayyedi P. Anxiety But Not Depression Predicts Poor Outcomes in Inflammatory Bowel Disease. Inflamm Bowel Dis. 2019;. [PubMed] [DOI] |
| 34. | Ghosh S, Mitchell R. Impact of inflammatory bowel disease on quality of life: Results of the European Federation of Crohn’s and Ulcerative Colitis Associations (EFCCA) patient survey. J Crohns Colitis. 2007;1:10-20. [PubMed] [DOI] |
| 35. | Izaguirre MR, Taft T, Keefer L. Validation of a Self-efficacy Scale for Adolescents and Young Adults With Inflammatory Bowel Disease. J Pediatr Gastroenterol Nutr. 2017;65:546-550. [PubMed] [DOI] |
| 37. | McCombie AM, Mulder RT, Gearry RB. Psychotherapy for inflammatory bowel disease: a review and update. J Crohns Colitis. 2013;7:935-949. [PubMed] [DOI] |
| 38. | Tarricone I, Regazzi MG, Bonucci G, Rizzello F, Carini G, Muratori R, Poggioli G, Campieri M, EspriMici Study Group Ω. Prevalence and effectiveness of psychiatric treatments for patients with IBD: A systematic literature review. J Psychosom Res. 2017;101:68-95. [PubMed] [DOI] |
| 39. | Daghaghzadeh H, Naji F, Afshar H, Sharbafchi MR, Feizi A, Maroufi M, Tabatabaeeyan M, Adibi P, Tavakoli H. Efficacy of duloxetine add on in treatment of inflammatory bowel disease patients: A double-blind controlled study. J Res Med Sci. 2015;20:595-601. [PubMed] [DOI] |
| 40. | Goodhand JR, Greig FI, Koodun Y, McDermott A, Wahed M, Langmead L, Rampton DS. Do antidepressants influence the disease course in inflammatory bowel disease? A retrospective case-matched observational study. Inflamm Bowel Dis. 2012;18:1232-1239. [PubMed] [DOI] |
| 44. | Schoultz M, Atherton I, Watson A. Mindfulness-based cognitive therapy for inflammatory bowel disease patients: findings from an exploratory pilot randomised controlled trial. Trials. 2015;16:379. [PubMed] [DOI] |
| 45. | Lores T, Goess C, Mikocka-Walus A, Collins KL, Burke ALJ, Chur-Hansen A, Delfabbro P, Andrews JM. Integrated psychological care is needed, welcomed and effective in ambulatory Inflammatory Bowel Disease management: Evaluation of a new initiative. J Crohns Colitis. 2019;. [PubMed] [DOI] |
| 46. | Gracie DJ, Irvine AJ, Sood R, Mikocka-Walus A, Hamlin PJ, Ford AC. Effect of psychological therapy on disease activity, psychological comorbidity, and quality of life in inflammatory bowel disease: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol. 2017;2:189-199. [PubMed] [DOI] |
| 47. | Wynne B, McHugh L, Gao W, Keegan D, Byrne K, Rowan C, Hartery K, Kirschbaum C, Doherty G, Cullen G, Dooley B, Mulcahy HE. Acceptance and Commitment Therapy Reduces Psychological Stress in Patients With Inflammatory Bowel Diseases. Gastroenterology. 2019;156:935-945.e1. [PubMed] [DOI] |
| 48. | Abautret-Daly A, Dempsey E, Parra-Blanco A, Medina C, Harkin A. Gut-brain actions underlying comorbid anxiety and depression associated with inflammatory bowel disease. Acta Neuropsychiatr. 2018;30:275-296. [PubMed] [DOI] |
| 49. | 刘 萍, 罗 本燕. 肠道微生态与中枢神经系统疾病的相关性. 中国神经精神疾病杂志. 2016;42:251-254. [DOI] |
| 50. | Martin-Subero M, Anderson G, Kanchanatawan B, Berk M, Maes M. Comorbidity between depression and inflammatory bowel disease explained by immune-inflammatory, oxidative, and nitrosative stress; tryptophan catabolite; and gut-brain pathways. CNS Spectr. 2016;21:184-198. [PubMed] [DOI] |
| 51. | Baj A, Moro E, Bistoletti M, Orlandi V, Crema F, Giaroni C. Glutamatergic Signaling Along The Microbiota-Gut-Brain Axis. Int J Mol Sci. 2019;20. [PubMed] [DOI] |
| 53. | Lewis K, Marrie RA, Bernstein CN, Graff LA, Patten SB, Sareen J, Fisk JD, Bolton JM; CIHR Team in Defining the Burden and Managing the Effects of Immune-Mediated Inflammatory Disease. The Prevalence and Risk Factors of Undiagnosed Depression and Anxiety Disorders Among Patients With Inflammatory Bowel Disease. Inflamm Bowel Dis. 2019;. [PubMed] [DOI] |
| 54. | Janmohamed N, Steinhart AH. Measuring Severity of Anxiety and Depression in Patients with Inflammatory Bowel Disease: Low Concordance Between Patients and Male Gastroenterologists. Inflamm Bowel Dis. 2017;23:1168-1173. [PubMed] [DOI] |
| 55. | Moulton CD, Hopkins CWP, Mohamedali Z, Powell N. Out of Sight, Out of Mind: The Limitations of the Hospital Anxiety and Depression Scale in Inflammatory Bowel Disease. Inflamm Bowel Dis. 2019;. [PubMed] [DOI] |
| 56. | 叶 瑞繁, 耿 庆山, 陈 剑, 区 丽明, 张 美兰, 董 春玲, 朱 春燕, 李 河. 3种焦虑评定表量在综合医院门诊患者中的应用比较. 中华行为医学与脑科学杂志. 2013;22:271-273. [DOI] |
| 57. | Jonefjall B, Simren M, Lasson A, Ohman L, Strid H. Psychological distress, iron deficiency, active disease and female gender are independent risk factors for fatigue in patients with ulcerative colitis. United European Gastroenterol J. 2018;6:148-158. [PubMed] [DOI] |
| 58. | Chavarria C, Casanova MJ, Chaparro M, Barreiro-de Acosta M, Ezquiaga E, Bujanda L, Rivero M, Arg¨¹elles-Arias F, Martin-Arranz MD, Martinez-Montiel MP, Valls M, Ferreiro-Iglesias R, Llao J, Moraleja-Yudego I, Casellas F, Antolin-Melero B, Cortes X, Plaza R, Pineda JR, Navarro-Llavat M, Garcia-Lopez S, Robledo-Andres P, Marin-Jimenez I, Garcia-Sanchez V, Merino O, Algaba A, Arribas-Lopez MR, Banales JM, Castro B, Castro-Laria L, Honrubia R, Almela P, Gisbert JP. Prevalence and Factors Associated with Fatigue in Patients with Inflammatory Bowel Disease: A Multicenter Study. J Crohns Colitis. 2019;. [PubMed] [DOI] |
| 59. | Hood MM, Wilson R, Gorenz A, Jedel S, Raeisi S, Hobfoll S, Keshavarzian A. Sleep Quality in Ulcerative Colitis: Associations with Inflammation, Psychological Distress, and Quality of Life. Int J Behav Med. 2018;25:517-525. [PubMed] [DOI] |