修回日期: 2017-03-28
接受日期: 2017-04-05
在线出版日期: 2017-05-18
杯状细胞(goblet cell, GC)由肠黏膜基底干细胞分化而来, 形似高脚杯, 内含黏液颗粒, 黏液颗粒的组成成分主要为黏蛋白. MUC2是一种重要的拥有特殊网状结构的黏蛋白. GC分泌黏液到肠上皮细胞形成黏液层填补细胞间隙. 黏液层使得GC能在肠黏膜抵御内外源侵袭时发挥重要作用, 尤其是将上皮与肠道菌分离, 从而能维持肠道微生态平衡. 除此之外, GC还能接受和参与免疫调节. 更重要的是GC及其分泌黏蛋白的缺陷与肠道多种疾病密切相关. 总之, GC对肠道健康的作用不容小视.
核心提要: 肠杯状细胞(goblet cell, GC)是散分布于肠黏膜上皮中的黏液分泌细胞, 其主要功能是分泌黏蛋白, 在肠道的固有屏障中发挥重要作用. 黏蛋白的分泌受到多种因素、多途径调节. 除了黏液分泌之外, GC还以多种方式参与机体的免疫调节, GC数量、结构、功能的缺陷及其分泌的黏蛋白的缺陷都会对肠道微生态及免疫的平衡产生不利影响, 与机体多种疾病发病机制相关. 于机体而言, GC扮演了一个强有力的"保护者"角色.
引文著录: 刘玥宏, 丁悦, 徐敬东. 肠道杯状细胞及其功能研究进展. 世界华人消化杂志 2017; 25(14): 1279-1286
Revised: March 28, 2017
Accepted: April 5, 2017
Published online: May 18, 2017
Intestinal goblet cells originate from intestinal basal stem cells, and they acquired their name for their typical goblet-like appearance. A goblet cell contains numerous mucus vesicles, which are composed of mucins. MUC2 is a kind of important mucin with a special net-like structure. Goblet cells secrete mucus to fill intercellular spaces. The mucus layer makes goblet cells play an important role in resisting the invasion of internal and external pathogens into the intestinal mucosa, especially separating the epithelium from intestinal bacteria so that commensal bacteria can friendly coexist with the host. In addition, goblet cells can participate in immune regulation. What's more, the defect of goblet cells and mucin secretion is closely related to many kinds of intestinal diseases.
- Citation: Liu YH, Ding Y, Xu JD. Goblet cells and their functions. Shijie Huaren Xiaohua Zazhi 2017; 25(14): 1279-1286
- URL: https://www.wjgnet.com/1009-3079/full/v25/i14/1279.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v25.i14.1279
杯状细胞(goblet cell, GC)作为单细胞腺在人体扮演了重要的保护者的角色. 肠GC分泌黏蛋白, 建立肠黏膜上皮屏障, 分离肠道菌与黏膜上皮细胞, 使数以亿计的肠道共生菌能与正常宿主互利共生, 在肠道微生态平衡中发挥了不可替代的作用, 除此之外, GC还调节肠道免疫. 本文基于近年对GC结构和功能的研究进展, 对GC的角色重要性予以综述.
迄今为止发现肠上皮基底多能干细胞可分化为吸收细胞, GC, 潘氏细胞, 肠内分泌细胞和丛细胞, 并且每3-7天更新一次. GC出现得最早(可在人类9-10 wk妊娠的胎儿小肠中发现[1,2]). 有研究[1,3]表明结肠GC的分化与转录因子Hath1、KLF4等及Notch、Wnt/β-catenin、成骨蛋白、PI3-激酶/Akt信号肽介导的信号转导通路的相互作用有关, 尤其重要的是Notch通路, 其激活了Heth1基因转录因子. Notch通路的抑制导致肠上皮细胞向分泌细胞族系的细胞快速而完全的转化如GC、潘氏细胞、肠内分泌细胞, 并伴随Math1的活化(人类为Hath1). 除此之外, Klf4和Elf3与GC的终末分化相关(KLF4突变的小鼠其结肠GC的数目较正常小鼠减少约90%). 但遗憾的是这些具体的分化机制尚未在人体得到充分明确的证明[4].
肠道GC散在分布于吸收细胞之间, 形似高脚杯(小鼠GC因缺少MUC2基因而缺乏典型GC形态). GC从十二指肠至回肠末端逐渐增多, 结肠近端数目少于远端[5], 而肠道内的细菌数量在不同部位为: 十二指肠约为102 cfu/mL, 空肠约为102 cfu/mL, 近端回肠约为103 cfu/mL, 远端回肠约为107-108 cfu/mL, 结肠约为1011-1012 cfu/mL[6], 可见GC的数量分布与肠道菌保持一致. GC顶部膨大, 胞质底部细窄, 位于基膜上, 核较小, 位基底, 呈三角形或扁圆形, 着色较深. 电镜观察GC游离面有少量微绒毛, 基部含有丰富的粗面内质网和游离核糖体. GC为单分泌腺, 分泌高度加工的黏蛋白至细胞外与水结合成黏液, 作为肠道黏膜上皮屏障, 在上皮细胞表面起着润滑和保护上皮的作用[7].
GC的特征性结构为细胞顶部的黏蛋白颗粒. 黏蛋白由黏蛋白基因转录翻译而来, 在GC内质网和高尔基体进行聚合, 修饰, 糖基化和折叠, 再分泌到细胞外, 与水及肠腔内一些物质混合形成黏液凝胶. 迄今共发现21种黏蛋白基因, 以发现的先后顺序予以命名[8], 而根据黏蛋白的结构和定位将黏蛋白分为两类: 分泌型和膜结合型, 形成黏液凝胶的分泌型黏蛋白由5种寡聚体黏蛋白(MUC2、MUC5AC、MUC5B[9]、MUC6、MUC19)及一种非寡聚体黏蛋白(MUC7)组成[4,10].膜结合性蛋白主要包括: MUC1、MUC3A、MUC3B、MUC4、MUC12、MUC13、MUC16、MUC17、MUC20[4]. 除黏蛋白之外, GC分泌颗粒内还包括其他黏液组分[11].
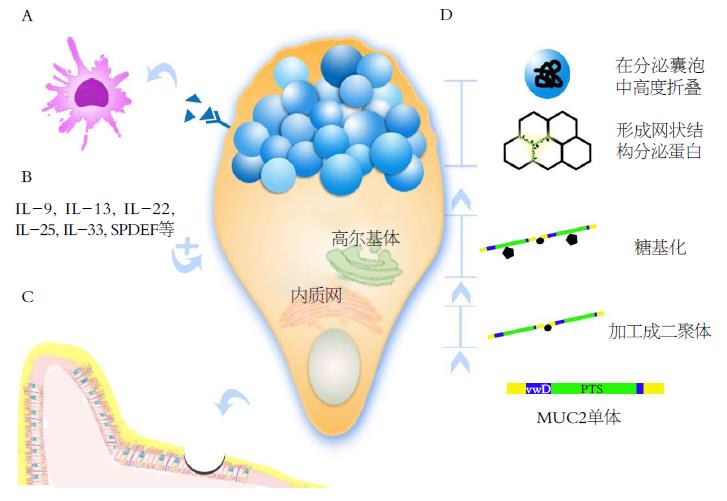
MUC2黏蛋白为高度糖基化的蛋白, 蛋白骨架与多种O-型寡糖侧链结合. MUC2单体主要由两个PTS区域和一些vwD区域(von Willebrand D domain)组成. 单体形成之后, 在内质网通过C-末端远端的CK区域的分子内二硫键两两连接形成二聚体[12-15]. 在内质网加工完成的蛋白产物抵达高尔基体进行糖基化. 定位于高尔基体内的半乳糖胺类调控着O-型糖基化蛋白生物合成, PTS区域与O-型寡糖侧链结合, 高尔基体内多肽α-N-乙酰半乳糖胺转移酶家族转移尿苷二磷酸半乳糖胺(UDP-GalNAc)中α-GalNAc至丝氨酸、苏氨酸残基多肽受体合成半乳糖胺α1-O型丝氨酸/苏氨酸(GalNacα1-O-Ser/Thr)[4,16]. 此后, 在GC的分泌囊泡中, 可视化电镜显示MUC2黏蛋白二聚体进一步形成三聚体, 并自发的以延长的蛋白结构域形成铰链般的环状结构, 通过C-末端尾对尾的连接其他MUC2蛋白分子. 近期, 对MUC2黏蛋白N-末端D3结构域的研究[17]表明: 每秒MUC2蛋白环旋转180度使环状结构的N-末端得以相遇, 从而形成复杂网状结构[11]. 在GC的分泌颗粒中, 由于低pH环境和高钙离子浓度[18], MUC2黏蛋白被包装的相当紧密, 当黏蛋白从分泌颗粒中排出后, 迅速展开空间骨架, 体积可扩大千倍[11,19].
3.1.1 黏液分泌过程: 在GC在临近分泌之时, 被紧密包装的黏蛋白扩展千倍以上, 成为一张"巨网". 一种蛋白质水解酶--甲基氨脂β(meprin β)使MUC2分开, 助MUC2黏蛋白从GC顶端释放[20], 这个过程依赖pH的上升和N-末端移动来联结游离钙离子[18]. 黏液的分泌需要高碳酸氢盐的转运[21], 实验表明IL-4能提高钙离子和cAMP活化的氯化物或碳酸氢盐的分泌, 使碳酸氢盐浓度提高并升高上皮表面pH, 这一机制在对气道GC的研究中较为清晰[22]. 理论上黏蛋白扩展的过程快速而有序, 但GC黏蛋白包装模型表示: 这一过程缺乏秩序, 并且该模型发现钙离子的作用犹如一个盾牌, 以抵抗大多数黏蛋白所带负电荷糖基的静电排斥. 这一模型并未观察到上述迅速而高度有序的黏蛋白伸展过程[11].
GC分泌时, 胞内高钙离子浓度和钙离子动员媒介如乙酰胆碱和新斯的明等能触发GC黏蛋白分泌, 乙酰胆碱被证明为鼠、兔的小肠和大肠及人类结肠[23]黏蛋白的促分泌剂, 实验表明乙酰胆碱、卡巴胆碱等胆碱能物质能提高黏蛋白分泌率, 但分泌率会在30 min内回到基线水平. 小肠较结肠对卡巴胆碱更为敏感. 乙酰胆碱的作用靶点在小肠隐窝的GC, 但小肠绒毛和结肠表面GC对胆碱能促分泌剂反应不佳[24]. 研究[25]表明前列腺素E2(prostaglandin E2, PGE2)也能促进鼠小肠和兔结肠的黏蛋白分泌, 但在人类结肠只能促进液体分泌, 这种不同物种对PGE2反应的差异可能取决于在依赖环磷酸腺苷和钙离子的信号通路中不同受体的表达.
黏蛋白的分泌至少有两种方式: 普通的囊泡分泌和复合胞吐. 普通囊泡分泌过程与气道黏膜的GC分泌机制相似[26]: 典型囊泡胞吐相关蛋白如突触融合蛋白(Syntaxins)、Munc18蛋白、突触小泡缔合性膜蛋白和突触小体相关蛋白介导的膜融合. 还有一些研究表明GC黏蛋白颗粒的胞吐与内吞、自噬、活性氧的产生及免疫祖细胞的聚集和活化有关. 而复合胞吐迄今没有清晰地分子学研究, 但形态学研究发现了细胞在复合胞吐时的"爆炸", 从而推测复合胞吐应该是GC的更为剧烈的内容物排空过程[11], 并且Grootjans等[27]研究表明结肠隐窝GC复合胞吐的触发在肠道黏膜屏障维持中非常重要.
3.1.2 内黏液层的结构、性质和功能: 在胃肠上皮细胞表面覆盖有板层状的黏液层, 小肠只有一层黏液层[24], 而胃和结肠黏液层分内外两层, 结肠GC分泌的MUC2黏蛋白网状结构展开, 与水和其他GC产物如小肠三叶因子、抵抗素样分子β[28,29]、Fcγ免疫球蛋白IgG结合蛋白抗体、抗菌肽以及分泌性IgA等混合, 如胶冻般平铺在肠黏膜上皮细胞表面, 形成内黏液层. GC持续分泌黏液, 在体研究[1,15]显示: 大鼠结肠末端的黏液层每1-2个小时更新一次, 随着黏液持续分泌, 内黏液层向外黏液层移动, 形成板层状结构. 大鼠结肠末端内黏液层厚约50 μm, 人类的约厚200 μm[11,25], 并且胃、回肠和结肠的黏液层厚于空肠[30], 这可能与各部位肠道抵御肠道中外源刺激, 尤其是抵御肠道细菌侵袭的能力相关.
MUC2黏蛋白的网状结构赋予其选择透过的性质, 其以分子大小作为选择透过的机制[25], 像大分子的细菌和细菌产物便无法透过结构完整的内黏液层从而接触肠黏膜上皮细胞. 而外黏液层由于蛋白微孔的扩大, 可使一些细菌及其产物轻易透过, 由于有这样的性质, 内黏液层成为肠黏膜上皮的"护盾", 除此之外, 还为肠道黏膜上皮细胞"站岗放哨", 在受到肠道菌的刺激之后, 可激活相应信号转导通路, 募集邻近的GC并触发MUC2黏蛋白的共同分泌, 有力地将入侵的细菌冲回到肠腔[31], 并且结构和功能完整的内黏液层将上皮与细菌分离[11,15,32,33], 从而不至于引起肠道过度免疫反应, 实现宿主与肠道共生菌的和平共处.
3.2.1 GC的抗原呈递功能: 研究[34]表明GC另一个重要功能是能将小肠腔的抗原呈递给小肠固有层CD103+的树突状细胞. 在常规喂养的鼠中, 只在小肠观察到自发的抗原呈递, 结肠却没有发现, 但将该鼠置于无菌环境中并且经口饲喂抗生素后, 便在结肠中发现了抗原呈递过程. 这表明, 结肠的抗原呈递可能被结肠共生菌群所抑制. 而与黏液分泌类似, 小肠GC抗原呈递也能被胆碱能激动剂诱发, 其抗原呈递性在小肠比大肠敏感, 其固有的和激动剂诱导的抗原呈递都能被毒覃碱样受体4(muscarinic receptor 4, MR4)介导. 肠GC能捕获肠腔内抗原的能力与MR4等受体表达程度相关[35,36], MR4在小肠的表达高于结肠, 并且抗生素能上调受体表达, 这或许就能进一步解释在常规喂养的鼠结肠中没有发现抗原呈递过程的原因.
3.2.2 GC参与免疫调节: 研究[37,38]表明, 多种免疫调节因子能促进GC的分化和成熟以及黏蛋白的分泌. IL-13能促进GC的增殖[39-41]. 外源促IL-9和IL-25过表达能诱导GC的增殖并通过IL-13依赖的通路提高黏蛋白的表达[11]. SPDEF(SAM pointed domain ETS factor)与气道及小肠GC的成熟相关, 其能调节GC的增殖[42-44]. Th17和IL-22一样在GC分化成熟和黏蛋白表达中起到重要作用, IL-22缺陷的小鼠出现MUC2异常表达, GC增殖度降低, 从而比野生型小鼠更易感染巴西钩虫和鼠鞭虫[45]. IL-33被证实在鼻黏膜能促进GC增殖[46].
在失血性休克达一定程度时, 肠道黏膜遭受较重损害, 但仍然能够在短期内大部分恢复其黏膜细胞的连续性. 形态学观察表明: 损伤后的肠黏膜表面GC数量增多, 在休克复苏后3 h就非常明显, 12 h时发现因为部分绒毛脱落形成的缺损面上几乎完全由GC所替代, 实验表明GC的强黏附力和黏蛋白分泌的增加在肠黏膜损伤重建中起到着关键作用[47].
炎症性肠病(inflammatory bowel disease, IBD)是一种原因不明的累及肠道的慢性炎症性疾病. 溃疡性结肠炎(ulcerative colitis, UC)是IBD的一种, 病理特点为结肠黏膜炎症, 直肠大多受累, 炎症以不同程度连续性向近端扩展(无跳跃区域); 组织学特征包括上皮损害、炎症、隐窝脓肿、GC减少或消失和异形增生[48], UC患者隐窝上1/3减少最为明显[49], GC的减少消失与hath1基因的表达受抑相关[50].而同样属于IBD的克罗恩病(Crohn's disease, CD)却有所不同[51], 相同水平的炎症促进CD患者肠GC的分化, 这可能与CD的炎症诱导Hath1及KLF4表达有关[52].在对MUC2黏蛋白缺陷[53]的小鼠的研究[19,54]中发现, 这些小鼠表现出类似UC的便血、体质量下降、脱肛等症状, 由GC分泌的黏蛋白MUC2结构和功能的缺陷与UC发病密切相关: MUC2黏蛋白糖基和网状结构的破坏会导致肠黏膜上皮在细菌环境下的广泛暴露, 长期如此便会触发机体强烈的免疫反应而致病. MUC2的折叠与其分子伴侣ERN2(又称IRE1b)密切相关, ERN2是MUC2黏蛋白折叠的专用蛋白[55]. 几个错误折叠的蛋白能触发一个非折叠蛋白(unfolded protein response, UPR), 反过来与炎症相关联. MUC2基因的单一突变可以导致内质网积聚, 从而触发UPR反应, 使免疫调节因子水平上调. 当大量细菌侵袭上皮, MUC2的需求量大大增加, 将会进一步对内质网的折叠加工系统形成挑战, 触发UPR反应而加重炎症[55-57]. 然而研究[58]发现IL-22和IL-10能够限制这种对机体有害的过程. 除此之外, 一些膜结合蛋白(如MUC1、MUC13、MUC17)的表达异常也会增加IBD的易感性[4].
另有研究[59]表明炎性体作为一种潜在的因子调控GC的分泌. 炎性体是细胞内的一类多蛋白复合物, 由一种NOD样受体(NOD-like receptor, NLR)[60]家族成员通过与一种受体蛋白ASC(apoptosis-associated speck-like protein containing a CARD)相互作用联结半胱天冬酶, 能在感受刺激信号后激活半胱天冬酶-1, 活化的半胱天冬酶-1能调控IL-1β、IL-18、IL-33的加工分泌. NLRPs被认为是多种内源性损伤和病原相关分子以及各种危险信号的感受器, NLRPs对维持肠道微生态的平衡作用明显, NLRP6[31,61]缺乏的小鼠对葡糖硫酸盐和柠檬酸杆菌属[19]诱导的结肠炎易感性增加[62].
新近研究表明异常表达的黏蛋白与机体多种肠道癌症相关. MUC系列黏蛋白影响肿瘤细胞的黏附力、免疫识别、转移和预后. MUC2黏蛋白异常表达的小鼠极易发展为结肠腺癌, 特别是MUC2缺陷的小鼠可自发发展为结肠炎、结肠腺癌甚至是侵袭性腺癌, MUC2分子表面的Sialyl-Lewsx和Sialyl-Lewsa是黏附分子选择素的配体, 故可参与细胞与血管内皮的黏附还参与癌细胞的转移[52]; IL-6和膜结合蛋白MUC1的表达促进癌细胞转移; MUC1的过度表达可致小鼠肠道IBD样炎症恶化, 甚至导致结肠炎相关结肠癌; 膜结合蛋白MUC3A和MUC4异常表达与癌组织中, 可提示预后不良[4].
总之, GC并不是一个简单的单分泌腺, 其分泌多种黏蛋白, 尤其是拥有特殊网状结构的分泌蛋白MUC2, 在肠黏膜上皮细胞表面凭借其"分子筛"样的作用使细菌与上皮分离, 加上GC的免疫调节机制, 通过多种免疫调节因子如IL-13、IL-22、SPDEF、IL-10等与其他免疫机制协同将机体的肠道免疫功能调整得恰到好处[65], 使机体能够与数以亿计的肠道共生菌和平共处, 当遇到有害物质侵袭时, 正常结构和功能的GC的作用也不容小觑(图1). 反之, GC数量、结构、功能的缺陷及其分泌的黏蛋白的缺陷都会对肠道微生态及免疫的平衡产生不利影响[66]. 由此可见, GC为人体肠道名副其实的有力"保护者". 然而, GC分泌黏蛋白的过程尤其是黏蛋白的伸展过程及免疫调节功能当中的更多细节问题还有待发现、研究和探讨.
杯状细胞(goblet cell, GC)作为一种单分泌腺分布于人体呼吸道、消化道、生殖道等部位, 肠GC由肠上皮基底多能干细胞分化而来, 分泌高度加工的黏蛋白至细胞外与水和其他物质结合形成黏液, 黏液在肠道黏膜上皮表面形成黏液屏障, 起着润滑和保护上皮的作用. GC无疑是机体的"保护者", 其结构、功能以及与炎性肠病等多种肠道疾患的关系一直以来都是众多生命科学研究者的探索方向.
大量研究证实肠道黏液层是防止肠道细菌入侵的第一道防线. 这一发现很大程度上改变了人们对于肠道黏液层生物学作用的看法, 开创了一个全新的研究领域. 此后有关黏液的生成、分泌、破坏等各个过程的研究, 深化了生命科学研究者们对于肠道菌群与机体互动机制的认识, 而这些过程的异常变化与炎性肠病的相关性成为目前的研究热点, 其中的细节问题包括分子机制, 及其能为炎性肠病尤其是溃疡性结肠炎的发病机制和治疗方法带来的突破性思路还亟待研究.
肠道的GC分泌的黏液形成的黏液层在维持肠道上皮的完整性具有不可替代的作用. 当黏液减少时, 出现黏膜受损、细菌感染, 诱发肠道炎性反应. 由此可见GC在肠道保护和免疫调节中扮演重要的角色. 一旦有细菌穿过黏液层, 这种类型的GC便会立即感知并通知周围的GC, 使其迅速"喷"出大量的黏液, 将细菌冲出黏液层. 这一重要发现发表于2017年的Gut Microbes期刊上, 这些研究揭示了GC与肠道细菌易位后诱发疾病的机制, 从而有望为这些疾病的研究和治疗带来新的思路.
本文从GC分化、功能及对某些肠道疾病的影响等方面作出逻辑上较为完整的叙述; 配图并重点阐述了GC作为单分泌腺的黏液分泌功能; 对该领域上最新进的研究结果包括肠道黏膜上皮GC上的TLR感知肠道微生物的刺激, 并激活相应信号转导通路, 募集邻近的GC共同分泌大量黏液, 有力地将入侵的细菌冲回到肠腔的过程, 以及GC参与机体免疫调节的研究进展进行了总结.
肠道共生的细菌易位归因于"泄漏", 或肠道上皮细胞的屏障破坏, 允许活细菌渗透入肠黏膜屏障. 大量研究显示GC通过抗原呈递的作用将信息传递给树突状细胞, 引发肠道固有免疫和获得性免疫反应. 肠道共生的细菌的易位导致轻度炎症反应, 以应对并发的上皮损伤和黏膜损害. 结肠黏液在结肠共生细菌的生长和相关疾病的发生中越来越引起科学家的关注, 同时也有望成为肠道疾病的研究和治疗新靶点.
杯状细胞: 分散在黏膜中孤立的细胞, 但具有显著的分泌机能, 所以也把这种细胞称为单细胞腺. 胞质内充满粗大的嗜碱性颗粒, 颗粒中含有黏蛋白, 黏蛋白分泌入肠腔后, 与水及多种物质结合形成黏液, 润滑肠腔和参与肠道免疫.
耿明, 主任医师, 济南军区总医院医技楼10楼病理科
本文作者阅读大量文献复习回顾了肠GC形态及其功能研究进展, 具有一定的创新性, 语言流畅.
手稿来源: 自由投稿
学科分类: 胃肠病学和肝病学
手稿来源地: 北京市
同行评议报告分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C
D级 (一般): 0
E级 (差): 0
编辑: 马亚娟 电编:李瑞芳
| 1. | Kim YS, Ho SB. Intestinal goblet cells and mucins in health and disease: recent insights and progress. Curr Gastroenterol Rep. 2010;12:319-330. [PubMed] [DOI] |
| 2. | Agawa S, Muto T, Sawada T, Saito Y, Adachi M, Kubota Y, Sugihara K, Konishi F, Kamiya J, Morioka Y. [A histochemical study of goblet cell mucin in ulcerative colitis with special reference to time sequence]. Nihon Shokakibyo Gakkai Zasshi. 1985;82:58-64. [PubMed] |
| 3. | Clevers H. The intestinal crypt, a prototype stem cell compartment. Cell. 2013;154:274-284. [PubMed] [DOI] |
| 4. | 胡 艳艳, 刘 小伟. 肠道杯状细胞结构和功能的研究进展. 国际病理科学与临床杂志. 2013;33:424-430. |
| 6. | Sartor RB. Microbial influences in inflammatory bowel diseases. Gastroenterology. 2008;134:577-594. [PubMed] [DOI] |
| 8. | Dekker J, Rossen JW, Büller HA, Einerhand AW. The MUC family: an obituary. Trends Biochem Sci. 2002;27:126-131. [PubMed] [DOI] |
| 9. | Ridley C, Kouvatsos N, Raynal BD, Howard M, Collins RF, Desseyn JL, Jowitt TA, Baldock C, Davis CW, Hardingham TE. Assembly of the respiratory mucin MUC5B: a new model for a gel-forming mucin. J Biol Chem. 2014;289:16409-16420. [PubMed] [DOI] |
| 10. | 马 卉, 董 蕾, 赵 平. 杯状细胞在溃疡性结肠炎中的研究进展. 世界核心医学期刊文摘·胃肠病学. 2005;1:1-5. |
| 11. | Birchenough GM, Johansson ME, Gustafsson JK, Bergström JH, Hansson GC. New developments in goblet cell mucus secretion and function. Mucosal Immunol. 2015;8:712-719. [PubMed] [DOI] |
| 12. | Lang T, Hansson GC, Samuelsson T. Gel-forming mucins appeared early in metazoan evolution. Proc Natl Acad Sci USA. 2007;104:16209-16214. [PubMed] [DOI] |
| 13. | Godl K, Johansson ME, Lidell ME, Mörgelin M, Karlsson H, Olson FJ, Gum JR, Kim YS, Hansson GC. The N terminus of the MUC2 mucin forms trimers that are held together within a trypsin-resistant core fragment. J Biol Chem. 2002;277:47248-47256. [PubMed] [DOI] |
| 14. | Hansson GC, Johansson ME. The inner of the two Muc2 mucin-dependent mucus layers in colon is devoid of bacteria. Gut Microbes. 2010;1:51-54. [PubMed] [DOI] |
| 15. | Johansson ME, Phillipson M, Petersson J, Velcich A, Holm L, Hansson GC. The inner of the two Muc2 mucin-dependent mucus layers in colon is devoid of bacteria. Proc Natl Acad Sci USA. 2008;105:15064-15069. [PubMed] [DOI] |
| 16. | Bennett EP, Mandel U, Clausen H, Gerken TA, Fritz TA, Tabak LA. Control of mucin-type O-glycosylation: a classification of the polypeptide GalNAc-transferase gene family. Glycobiology. 2012;22:736-756. [PubMed] [DOI] |
| 17. | Nilsson HE, Ambort D, Bäckström M, Thomsson E, Koeck PJ, Hansson GC, Hebert H. Intestinal MUC2 mucin supramolecular topology by packing and release resting on D3 domain assembly. J Mol Biol. 2014;426:2567-2579. [PubMed] [DOI] |
| 18. | Ambort D, Johansson ME, Gustafsson JK, Nilsson HE, Ermund A, Johansson BR, Koeck PJ, Hebert H, Hansson GC. Calcium and pH-dependent packing and release of the gel-forming MUC2 mucin. Proc Natl Acad Sci USA. 2012;109:5645-5650. [PubMed] [DOI] |
| 20. | Schütte A, Ermund A, Becker-Pauly C, Johansson ME, Rodriguez-Pineiro AM, Bäckhed F, Müller S, Lottaz D, Bond JS, Hansson GC. Microbial-induced meprin β cleavage in MUC2 mucin and a functional CFTR channel are required to release anchored small intestinal mucus. Proc Natl Acad Sci USA. 2014;111:12396-12401. [PubMed] [DOI] |
| 21. | Gorrieri G, Scudieri P, Caci E, Schiavon M, Tomati V, Sirci F, Napolitano F, Carrella D, Gianotti A, Musante I. Goblet Cell Hyperplasia Requires High Bicarbonate Transport To Support Mucin Release. Sci Rep. 2016;6:36016. [PubMed] [DOI] |
| 22. | Gustafsson JK, Ermund A, Ambort D, Johansson ME, Nilsson HE, Thorell K, Hebert H, Sjövall H, Hansson GC. Bicarbonate and functional CFTR channel are required for proper mucin secretion and link cystic fibrosis with its mucus phenotype. J Exp Med. 2012;209:1263-1272. [PubMed] [DOI] |
| 23. | Ermund A, Gustafsson JK, Hansson GC, Keita AV. Mucus properties and goblet cell quantification in mouse, rat and human ileal Peyer's patches. PLoS One. 2013;8:e83688. [PubMed] [DOI] |
| 24. | Ermund A, Schütte A, Johansson ME, Gustafsson JK, Hansson GC. Studies of mucus in mouse stomach, small intestine, and colon. I. Gastrointestinal mucus layers have different properties depending on location as well as over the Peyer's patches. Am J Physiol Gastrointest Liver Physiol. 2013;305:G341-G347. [PubMed] [DOI] |
| 25. | Gustafsson JK, Ermund A, Johansson ME, Schütte A, Hansson GC, Sjövall H. An ex vivo method for studying mucus formation, properties, and thickness in human colonic biopsies and mouse small and large intestinal explants. Am J Physiol Gastrointest Liver Physiol. 2012;302:G430-G438. [PubMed] [DOI] |
| 26. | Adler KB, Tuvim MJ, Dickey BF. Regulated mucin secretion from airway epithelial cells. Front Endocrinol (Lausanne). 2013;4:129. [PubMed] [DOI] |
| 27. | Grootjans J, Hundscheid IH, Lenaerts K, Boonen B, Renes IB, Verheyen FK, Dejong CH, von Meyenfeldt MF, Beets GL, Buurman WA. Ischaemia-induced mucus barrier loss and bacterial penetration are rapidly counteracted by increased goblet cell secretory activity in human and rat colon. Gut. 2013;62:250-258. [PubMed] [DOI] |
| 28. | Bergstrom KS, Morampudi V, Chan JM, Bhinder G, Lau J, Yang H, Ma C, Huang T, Ryz N, Sham HP. Goblet Cell Derived RELM-β Recruits CD4+ T Cells during Infectious Colitis to Promote Protective Intestinal Epithelial Cell Proliferation. PLoS Pathog. 2015;11:e1005108. [PubMed] [DOI] |
| 29. | Busch RA, Heneghan AF, Pierre JF, Neuman JC, Reimer CA, Wang X, Kimple ME, Kudsk KA. Bombesin Preserves Goblet Cell Resistin-Like Molecule β During Parenteral Nutrition but Not Other Goblet Cell Products. JPEN J Parenter Enteral Nutr. 2016;40:1042-1049. [PubMed] [DOI] |
| 30. | Atuma C, Strugala V, Allen A, Holm L. The adherent gastrointestinal mucus gel layer: thickness and physical state in vivo. Am J Physiol Gastrointest Liver Physiol. 2001;280:G922-G929. [PubMed] |
| 31. | Birchenough GM, Nyström EE, Johansson ME, Hansson GC. A sentinel goblet cell guards the colonic crypt by triggering Nlrp6-dependent Muc2 secretion. Science. 2016;352:1535-1542. [PubMed] [DOI] |
| 32. | Arumugam M, Raes J, Pelletier E, Le Paslier D, Yamada T, Mende DR, Fernandes GR, Tap J, Bruls T, Batto JM. Enterotypes of the human gut microbiome. Nature. 2011;473:174-180. [PubMed] [DOI] |
| 33. | McGuckin MA, Lindén SK, Sutton P, Florin TH. Mucin dynamics and enteric pathogens. Nat Rev Microbiol. 2011;9:265-278. [PubMed] [DOI] |
| 34. | McDole JR, Wheeler LW, McDonald KG, Wang B, Konjufca V, Knoop KA, Newberry RD, Miller MJ. Goblet cells deliver luminal antigen to CD103+ dendritic cells in the small intestine. Nature. 2012;483:345-349. [PubMed] [DOI] |
| 35. | Howe SE, Lickteig DJ, Plunkett KN, Ryerse JS, Konjufca V. The uptake of soluble and particulate antigens by epithelial cells in the mouse small intestine. PLoS One. 2014;9:e86656. [PubMed] [DOI] |
| 36. | Knoop KA, McDonald KG, McCrate S, McDole JR, Newberry RD. Microbial sensing by goblet cells controls immune surveillance of luminal antigens in the colon. Mucosal Immunol. 2015;8:198-210. [PubMed] [DOI] |
| 37. | Xia W, Bai J, Wu X, Wei Y, Feng S, Li L, Zhang J, Xiong G, Fan Y, Shi J. Interleukin-17A promotes MUC5AC expression and goblet cell hyperplasia in nasal polyps via the Act1-mediated pathway. PLoS One. 2014;9:e98915. [PubMed] [DOI] |
| 38. | Lan A, Andriamihaja M, Blouin JM, Liu X, Descatoire V, Desclée de Maredsous C, Davila AM, Walker F, Tomé D, Blachier F. High-protein diet differently modifies intestinal goblet cell characteristics and mucosal cytokine expression in ileum and colon. J Nutr Biochem. 2015;26:91-98. [PubMed] [DOI] |
| 39. | Marillier RG, Michels C, Smith EM, Fick LC, Leeto M, Dewals B, Horsnell WG, Brombacher F. IL-4/IL-13 independent goblet cell hyperplasia in experimental helminth infections. BMC Immunol. 2008;9:11. [PubMed] [DOI] |
| 40. | Oeser K, Schwartz C, Voehringer D. Conditional IL-4/IL-13-deficient mice reveal a critical role of innate immune cells for protective immunity against gastrointestinal helminths. Mucosal Immunol. 2015;8:672-682. [PubMed] [DOI] |
| 41. | Lee JJ, Kim D, Pyo KH, Kim MK, Kim HJ, Chai JY, Shin EH. STAT6 expression and IL-13 production in association with goblet cell hyperplasia and worm expulsion of Gymnophalloides seoi from C57BL/6 mice. Korean J Parasitol. 2013;51:589-594. [PubMed] [DOI] |
| 42. | Park KS, Korfhagen TR, Bruno MD, Kitzmiller JA, Wan H, Wert SE, Khurana Hershey GK, Chen G, Whitsett JA. SPDEF regulates goblet cell hyperplasia in the airway epithelium. J Clin Invest. 2007;117:978-988. [PubMed] [DOI] |
| 43. | McCauley HA, Liu CY, Attia AC, Wikenheiser-Brokamp KA, Zhang Y, Whitsett JA, Guasch G. TGFβ signaling inhibits goblet cell differentiation via SPDEF in conjunctival epithelium. Development. 2014;141:4628-4639. [PubMed] [DOI] |
| 44. | Liu Z, Chen X, Wu Q, Song J, Wang L, Li G. miR-125b inhibits goblet cell differentiation in allergic airway inflammation by targeting SPDEF. Eur J Pharmacol. 2016;782:14-20. [PubMed] [DOI] |
| 45. | Turner JE, Stockinger B, Helmby H. IL-22 mediates goblet cell hyperplasia and worm expulsion in intestinal helminth infection. PLoS Pathog. 2013;9:e1003698. [PubMed] [DOI] |
| 46. | Ishinaga H, Kitano M, Toda M, D'Alessandro-Gabazza CN, Gabazza EC, Shah SA, Takeuchi K. Interleukin-33 induces mucin gene expression and goblet cell hyperplasia in human nasal epithelial cells. Cytokine. 2017;90:60-65. [PubMed] [DOI] |
| 48. | Harrison TR, Longo DL. Harrison's manual of medicine. New York: McGraw-Hill Medical 2013; 1003-1004. |
| 49. | Heazlewood CK, Cook MC, Eri R, Price GR, Tauro SB, Taupin D, Thornton DJ, Png CW, Crockford TL, Cornall RJ. Aberrant mucin assembly in mice causes endoplasmic reticulum stress and spontaneous inflammation resembling ulcerative colitis. PLoS Med. 2008;5:e54. [PubMed] [DOI] |
| 50. | Zheng X, Tsuchiya K, Okamoto R, Iwasaki M, Kano Y, Sakamoto N, Nakamura T, Watanabe M. Suppression of hath1 gene expression directly regulated by hes1 via notch signaling is associated with goblet cell depletion in ulcerative colitis. Inflamm Bowel Dis. 2011;17:2251-2260. [PubMed] [DOI] |
| 51. | Gersemann M, Becker S, Kübler I, Koslowski M, Wang G, Herrlinger KR, Griger J, Fritz P, Fellermann K, Schwab M. Differences in goblet cell differentiation between Crohn's disease and ulcerative colitis. Differentiation. 2009;77:84-94. [PubMed] [DOI] |
| 53. | Boland CR, Lance P, Levin B, Riddell RH, Kim YS. Abnormal goblet cell glycoconjugates in rectal biopsies associated with an increased risk of neoplasia in patients with ulcerative colitis: early results of a prospective study. Gut. 1984;25:1364-1371. [PubMed] [DOI] |
| 54. | Vaiphei K, Saha M, Sharma BC, Bhasin DK, Singh K. Goblet cell status in idiopathic ulcerative colitis--implication in surveillance program. Indian J Pathol Microbiol. 2004;47:16-21. [PubMed] |
| 55. | Martino MB, Jones L, Brighton B, Ehre C, Abdulah L, Davis CW, Ron D, O'Neal WK, Ribeiro CM. The ER stress transducer IRE1β is required for airway epithelial mucin production. Mucosal Immunol. 2013;6:639-654. [PubMed] [DOI] |
| 56. | Eri RD, Adams RJ, Tran TV, Tong H, Das I, Roche DK, Oancea I, Png CW, Jeffery PL, Radford-Smith GL. An intestinal epithelial defect conferring ER stress results in inflammation involving both innate and adaptive immunity. Mucosal Immunol. 2011;4:354-364. [PubMed] [DOI] |
| 57. | Hetz C. The unfolded protein response: controlling cell fate decisions under ER stress and beyond. Nat Rev Mol Cell Biol. 2012;13:89-102. [PubMed] [DOI] |
| 58. | Begue B, Verdier J, Rieux-Laucat F, Goulet O, Morali A, Canioni D, Hugot JP, Daussy C, Verkarre V, Pigneur B. Defective IL10 signaling defining a subgroup of patients with inflammatory bowel disease. Am J Gastroenterol. 2011;106:1544-1555. [PubMed] [DOI] |
| 59. | Johansson ME, Hansson GC. Is the intestinal goblet cell a major immune cell? Cell Host Microbe. 2014;15:251-252. [PubMed] [DOI] |
| 60. | Wang H, Kim JJ, Denou E, Gallagher A, Thornton DJ, Shajib MS, Xia L, Schertzer JD, Grencis RK, Philpott DJ. New Role of Nod Proteins in Regulation of Intestinal Goblet Cell Response in the Context of Innate Host Defense in an Enteric Parasite Infection. Infect Immun. 2015;84:275-285. [PubMed] [DOI] |
| 61. | Wlodarska M, Thaiss CA, Nowarski R, Henao-Mejia J, Zhang JP, Brown EM, Frankel G, Levy M, Katz MN, Philbrick WM. NLRP6 inflammasome orchestrates the colonic host-microbial interface by regulating goblet cell mucus secretion. Cell. 2014;156:1045-1059. [PubMed] [DOI] |
| 62. | Chen GY, Liu M, Wang F, Bertin J, Núñez G. A functional role for Nlrp6 in intestinal inflammation and tumorigenesis. J Immunol. 2011;186:7187-7194. [PubMed] [DOI] |
| 63. | Grainger JR, Wohlfert EA, Fuss IJ, Bouladoux N, Askenase MH, Legrand F, Koo LY, Brenchley JM, Fraser ID, Belkaid Y. Inflammatory monocytes regulate pathologic responses to commensals during acute gastrointestinal infection. Nat Med. 2013;19:713-721. [PubMed] [DOI] |
| 64. | Gerbe F, Sidot E, Smyth DJ, Ohmoto M, Matsumoto I, Dardalhon V, Cesses P, Garnier L, Pouzolles M, Brulin B. Intestinal epithelial tuft cells initiate type 2 mucosal immunity to helminth parasites. Nature. 2016;529:226-230. [PubMed] [DOI] |
| 65. | Kurashima Y, Kiyono H. Mucosal Ecological Network of Epithelium and Immune Cells for Gut Homeostasis and Tissue Healing. Annu Rev Immunol. 2017; [Epub ahead of print]. [PubMed] [DOI] |