修回日期: 2016-08-16
接受日期: 2016-08-23
在线出版日期: 2016-10-08
炎症性肠病(inflammatory bowel diseases, IBD)在青年女性中发病率高, 与生育年龄重叠. 病情活动会增加患者的不孕率、导致不良妊娠结局等, 因此建议应在病情缓解后再妊娠. 此外妊娠过程中如何维持缓解及复发后的治疗等问题受到广泛的关注. 本文旨在探讨IBD与妊娠间的相互影响作用, 并就妊娠中IBD缓解期的维持、活动期的治疗等问题作一综述, 指导患者安全度过整个妊娠过程, 为准备受孕及已经怀孕的IBD患者提供参考.
核心提要: 炎症性肠病(inflammatory bowel diseases, IBD)多发于中青年, 恰与生育年龄重叠, 病情的变化严重影响母婴的健康, 因此受到广泛的关注. 妊娠期间的用药也十分特殊, 目前国内缺乏有关与妊娠期间IBD管理的相关文献. 本文系统地介绍了IBD与妊娠间的相互影响、常见治疗药物安全性、缓解期的维持及复发的治疗等问题, 为临床IBD患者妊娠期间的管理提供参考.
引文著录: 管丽芳, 胡博文, 孙琳, 廉方, 刘同亭. 妊娠期炎症性肠病的治疗策略与动态管理. 世界华人消化杂志 2016; 24(28): 3978-3984
Revised: August 16, 2016
Accepted: August 23, 2016
Published online: October 8, 2016
Inflammatory bowel disease (IBD) is frequently diagnosed during female reproductive years. Active disease may increase the risk of infertility and adverse outcomes. Therefore, we suggest delaying conception until the disease becomes inactive. It has attracted much attention on how to maintain and induce remission in pregnancy. This review discusses the interplay between pregnancy and IBD, the treatment of active IBD, and the maintenance of remission during pregnancy, with an aim to provide reference for woman who are pregnant or may become pregnant.
- Citation: Guan LF, Hu BW, Sun L, Lian F, Liu TT. Dynamic management and therapeutic strategy for inflammatory bowel disease in pregnancy. Shijie Huaren Xiaohua Zazhi 2016; 24(28): 3978-3984
- URL: https://www.wjgnet.com/1009-3079/full/v24/i28/3978.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v24.i28.3978
炎症性肠病(inflammatory bowel diseases, IBD)主要包括溃疡性结肠炎(ulcerative colitis, UC)、克罗恩病(Crohn's disease, CD). IBD好发于20-40岁, 与生育时期重叠[1]. IBD与妊娠相互影响, 尤其疾病活动状态对妊娠的期胎儿与孕妇的不良影响更为显著, 规范妊娠期IBD的治疗对于降低IBD患者妊娠的风险有重要意义.
大多研究[2]表明IBD缓解期患者生育能力与正常人无明显差别, 疾病活动期生育能力下降. 文献报道CD与UC缓解期女性患者怀孕的概率并不会降低. 早在1986年Miller等[3]进行了一项荟萃分析, 研究纳入了1300多例UC和700例CD女性患者, 研究发现两组患者正常妊娠率分别为83%、85%, 与健康者并无差别. 但另有研究[4]却发现CD患者的子女数只有正常人的一半. 分析原因主要来自两方面, 一方面是担心妊娠加重病情、遗传后代、压力等问题而恐于妊娠; 另外, 外科手术也会对生育率产生影响, 尤其接受回肠肛门吻合(ileal pouch anal anastomosis, IPAA)治疗后, IBD女性患者的生育能力明显下降. 文献报道[5]接受IPAA治疗后, 生育率从手术前的48.0%降到14.6%. Wikland等[6]通过一项回顾研究也发现结直肠切除并行回肠造口的IBD患者的生育率从术前72%下降到37%.
IBD导致不良分娩结果, 疾病活动期产生不良妊娠的风险更高. 一项纳入2377例CD患者的研究[7,8]发现, CD患者妊娠期出现早产、低体质量儿、剖腹产分娩等问题. 同样一项纳入2637例UC患者的研究发现UC患者妊娠出现早产、低体质量儿、及剖腹分娩等情况的可能性较健康人高. 近些年的一项荟萃分析[9]表明IBD患者可出现早产(OR = 1.85, 95%CI: 1.67-2.05), 生长迟缓(OR = 1.36, 95%CI: 1.16-1.60), 先天畸形(OR = 1.29, 95%CI: 1.05-1.58), 死胎(OR = 1.57, 95%CI: 1.03-2.38)等不良妊娠结局. 研究[1]发现无论受孕前还是妊娠期间, 疾病的活动状态对分娩结局都有影响. 其中疾病活动状态面临风险更高. Bröms等[10]对2006-2010年间瑞典的1833例UC及1220例CD女性患者进行了回顾性研究, 发现IBD患者妊娠期间病情复发是导致死产、早产、生长迟缓等不良妊娠的危险因素, 其中UC患者早产(OR = 1.78, 95%CI: 1.49-2.13), CD早产(OR = 1.65, 95%CI: 1.33-2.06), 活动期CD死产(OR = 4.48, 95%CI: 1.67-11.90). 此外大量研究[11]表明CD患者出现不良妊娠的风险高于UC患者.
研究[12]表明妊娠对IBD患者病情的影响主要与疾病缓解还是活动密切相关. 缓解期妊娠的IBD患者与一般正常女性面临的妊娠风险无明显差异, 而病情活动期妊娠的患者更容易出现早产、低体质量儿等不良结果[13-16]. 研究[12]发现疾病缓解期怀孕, 将有2/3患者在整个妊娠期都将处于缓解期; 妊娠发生在疾病活动期间时, 2/3的患者会保持活动的状态, 这些患者中的2/3甚至病情会加重甚至爆发[12,17]. Ujihara[18] 等同样发现怀孕时处于疾病活动状态的UC患者中48.3%妊娠期间处于中重度活动, 孕前病情缓解的患者, 妊娠期间只有14%患者出现病情复发.
妊娠期间, UC女性患者比CD女性患者更容易复发[9,19]. 对患者妊娠期间及产后6 mo进行随访, 发现妊娠并未改变CD的病程, 而UC妊娠患者妊娠期、产后复发率明显增高[1], 其中妊娠1-3 mo复发(RR = 8.80, 95%CI: 2.05-79.3, P<0.0004), 4-6 mo复发(RR = 2.84, 95%CI: 1.2-7.45, P = 0.0098), 产后6 mo内复发(RR = 6.22, 95%CI: 2.05-79.3, P = 0.0004). 同样Pedersen等[9]进一步发现UC患者妊娠1-3 mo复发的危险性最大(RR = 8.80, 95%CI: 2.05-79.3, P<0.0098), 4-6 mo复发可能为(RR = 2.84, 95%CI: 1.2-7.45, P = 0.0098), 产后3 mo内的复发率也很高. 但其主要机制仍不清楚, 需要进一步研究.
对于妊娠期IBD患者而言, 延长缓解时间至关重要. 根据2015年多伦多妊娠期炎症性肠病管理共识意见[20], 分析临床IBD常见维持缓解药物及其药物安全等级划分如表1.
| 药物 | 药物安全等级 | 建议 |
| 5-氨基水杨酸 | B级 | 低风险, 建议使用 |
| 糖皮质激素 | C级 | 建议使用 |
| 免疫抑制剂 | ||
| 硫唑嘌呤 | D级 | 建议使用 |
| 6-巯基嘌呤 | D级 | 建议使用 |
| 甲氨蝶呤 | X级 | 禁用 |
| 生物制剂 | ||
| 英夫利昔 | B级 | 建议使用 |
| 阿达木 | B级 | 建议使用 |
5-氨基水杨酸类药物(5-aminosalicylic acid, 5-ASA)在妊娠安全用药中属于B级, 应用剂量不超过3 g/d时, 相对安全[21]. 其中柳氮磺胺吡啶能通过胎盘, 并且抑制叶酸的合成和吸收, 因此妊娠期使用的安全性备受质疑[22]. 但也有多数研究[23-26]证实了妊娠期间使用柳氮磺胺吡啶的安全性. 5-ASA临床最常应用于维持妊娠期IBD缓解, 尤其对于妊娠期UC患者是个不错的选择.
有研究[27-29]表明5-ASA维持UC缓解与对安慰剂组1年内复发率为30% vs 62%(P<0.01). 含有邻苯二甲酸二丁酯(dibutyl phthalate, DBP)成分的5-ASA药物禁止用于妊娠期. 因为DBP对女性生殖系统造成不良影响[30]并导致性早熟[31]. 因此建议孕前若使用的含有DBP的5-ASA药物的患者换成不含有DBP的5-ASA. 激素在妊娠安全用药中属于C级, 常用于中重度IBD急性期临床诱导缓解, 不作为维持治疗. 研究[32]发现器官移植术后及风湿免疫患者妊娠期间使用糖皮质激素, 并未增加胎儿出现先天畸形的风险. Bay Bjørn等[33]也指出妊娠期间使用糖皮质激素的妇女并不会导致唇腭裂和先天畸形. 然而仍有一些研究[11,34-36]表明激素会导致低体质量儿、早产、胎儿生长迟缓、唇腭裂等问题, 但由于研究样本量较小, 且患者病情严重程度不同以及其他药物的应用, 仍需进一步研究.
此外还发现激素中强的松、强的松龙、甲强龙比长效的地塞米松、倍他米松更安全[20]. 6-巯基嘌呤和硫唑嘌呤都是嘌呤类似物, 在妊娠安全用药中属于D级, 临床常应用于IBD的诱导缓解另一类常见药物. 2015年通过对312例妊娠IBD患者研究[37], 发现妊娠期间服用巯基嘌呤的患者胎儿畸形率是对照组2.95倍(95%CI: 1.03-8.43). Akbari等[38]2013年使用巯基嘌呤治疗的IBD患者出现低体质量儿(OR = 1.01, 95%CI: 0.96-1.06)、早产(OR = 1.67, 95%CI: 1.26-2.20)、先天畸形的(OR = 1.45, 95%CI: 0.99-2.13). Bröms等[10]也发现巯基嘌呤不会导致胎儿畸形, 但是会导致早产. 巯基嘌呤用于稳定期与活动期出现的不良妊娠结局的风险也不同, 其中稳定期患者(OR = 2.41, 95%CI: 1.05-5-51), 疾病活动期(OR = 4.90, 95%CI: 2.76-8.69), 由此可见使用巯基嘌呤不良反应的增加主要与IBD本身病情相关[20]. 由于病情反复会对增加妊娠风险、不良妊分娩结果等诸多问题, 所以建议妊娠的全过程仍继续使用巯基嘌呤. 甲氨蝶呤在妊娠安全用药中属于X级, 禁止用于妊娠期间IBD的治疗. 由于甲氨蝶呤可以长时间内存在体内, 因此建议至少停药3-6 mo以上再考虑妊娠[13,20]. 服用甲氨蝶呤过程中出现妊娠的患者, 应立即停止继续用药, 并立即补充叶酸制剂, 叶酸可以降低甲氨蝶呤的不良反应[39]. 对于应用甲氨蝶呤过程中妊娠的患者, 不建议强制终止妊娠, 而应该向产科医师咨询[20].
生物制剂在妊娠安全用药中属于B级. 应用英夫利昔组与未使用组对照研究[40]发现, 两组CD患者流产率10.0% vs 6.7%, 新生儿并发症发生率6.9% vs 10.0%, 未见明显差异. 对妊娠期间维持英夫利昔治疗的患者进行随访, 发现所有患者生产的新生儿均未出现先天畸形[41]. 2011年研究[42]纳入了212例IBD患者与56例健康者, 研究发现应用生物制剂组与健康人组妊娠结果并无差异. 欧洲克罗恩病和结肠炎组织也建议英夫利昔和阿达木均可以用于孕前及妊娠过程[43]. 正在使用生物制剂的妊娠期IBD女性, 建议使用该方案继续治疗, 必须在评估患者复发低风险的情况下才能停用生物制剂治疗方案[20,44]. 为减少巯基嘌呤的特异性不良反应[45-47], 建议未使用过巯基嘌呤而直接开始采用生物制剂方案治疗的妊娠期 IBD 患者, 应采用生物制剂单药治疗而非联合应用生物制剂和巯基嘌呤类药物[20].
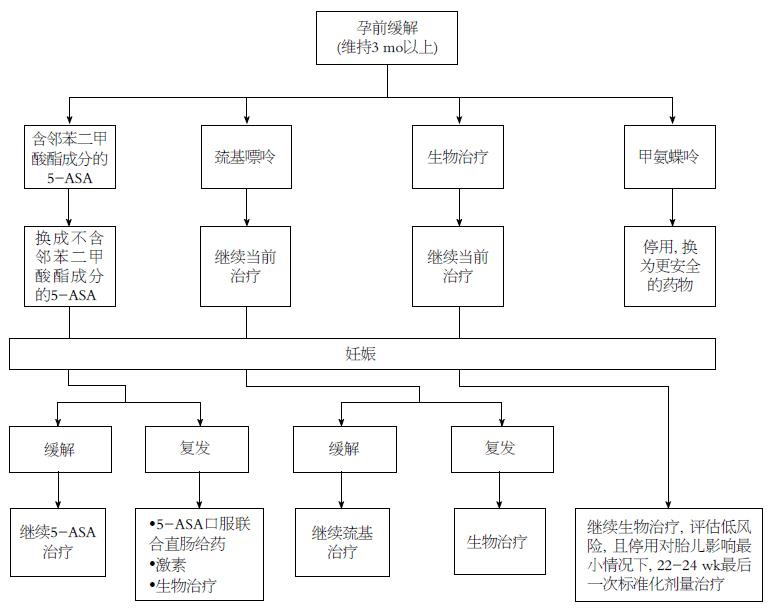
患者使用5-ASA维持治疗过程若出现轻中度的疾病复发, 建议采用5-ASA口服联合直肠给药尽快诱导症状缓解[20]. 研究[48]发现口服联合直肠给药诱导缓解较单独口服5-ASA诱导缓解相比, 无效(RR = 0.65, 95%CI: 0.47-0.91), 且联合使用并未增加药物不良反应. 虽然有研究[49]指出5-ASA较大剂量使用(≥3 g)时, 出现早产的风险也增加, 但考虑到疾病活动状态对孕妇及胎儿的影响, 仍建议口服联合直肠给药. 应用5-ASA或巯基嘌呤维持治疗过程中, 若出现疾病复发, 建议全身应用糖皮质激素诱导缓解或开始使用生物制剂[20]. 妊娠期IBD患者, 出现糖皮质激素抵抗性复发时, 建议开始生物治疗以尽快诱导症状缓解, 但若此时妊娠已超过37 wk, 分娩是更好的选择[20]. 权衡胎儿与孕妇的, 多伦多炎症性肠病共识意见[20]为临床IBD者妊娠期的管理制定方案, 详情如图1.
IBD具有反复发作、迁延难愈、好发于生育期等特点, 而受到广泛的关注. 由于疾病活动期会增加患者不孕率, 增加不良妊娠的风险, 降低药物安全性、增加妊娠期间疾病复发的可能, 因此孕前及整个妊娠期间维持病情缓解十分必要. 所有治疗IBD的药物除甲氨蝶呤外均可用于妊娠期间IBD的治疗, 此外对于妊娠期女性而言药物治疗时, 最大的威胁并不是药物的不良反应, 而是疾病的复发. 因此为维持或尽快诱导缓解, 多数药物必要时均可用于治疗. 具体用药选择是个复杂的问题, 需要结合患者病情、权衡胎儿与孕妇的安全, 制定治疗方案.
炎症性肠病(inflammatory bowel diseases, IBD)发病年龄与妊娠年龄有重叠, 而国内有关妊娠期间IBD系统管理的相关资料较少, 结合2015年多伦多关于妊娠期间IBD管理的共识指南, 系统介绍特殊时期IBD的管理.
靖大道, 教授, 主任医师, 上海交通大学附属第一人民医院消化科; 钦丹萍, 教授, 浙江中医药大学附属第一医院消化内科
IBD缓解期的患者的生育能力并不受影响, 而且缓解期妊娠出现不良妊娠结局的风险也相对较低. 临床常用药物中除氨甲蝶呤外, 其他常见药物均可以应用. 对于IBD患者而言, 疾病复发所带来的风险远远高于药物的不良反应. 生物制剂相对安全, 对于胎儿的免疫等是否有影响, 仍需要进一步研究.
大量文献报道了巯基嘌呤和激素导致不良妊娠的风险, 但是由于样本量较少, 而且病情复发所带来的风险较药物的不良反应更大. 作者建议必要时, 巯基嘌呤和激素也是可以应用的.
本文较为系统的讲述了患者妊娠期间不同时期药物的选择及治疗, 为患者及临床医生提供指导. 但是关于孕后母乳喂养的安全性问题并未涉及.
2015年欧洲《多伦多妊娠期炎症性肠病(IBD)管理共识意见》发布, 本文在此共识意见的基础上, 就IBD对妊娠期及妊娠结果影响、妊娠期对IBD的影响以及妊娠期IBD患者活动期、缓解期的治疗策略进行了综述, 这对临床工作中, 针对妊娠期IBD患者的治疗管理、妊娠及妊娠结果的风险评估具有一定的指导意义.
手稿来源: 自由投稿
学科分类: 胃肠病学和肝病学
手稿来源地: 山东省
同行评议报告分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C, C
D级 (一般): 0
E级 (差): 0
编辑: 马亚娟 电编:胡珊
| 1. | Salari P, Nikfar S, Abdollahi M. Current opinion on treatment of inflammatory bowel disease in pregnant women. Arch Med Sci. 2012;8:983-986. [PubMed] [DOI] |
| 2. | Winter R, Nørgård BM, Friedman S. Treatment of the Pregnant Patient with Inflammatory Bowel Disease. Inflamm Bowel Dis. 2016;22:733-744. [PubMed] [DOI] |
| 3. | Miller JP. Inflammatory bowel disease in pregnancy: a review. J R Soc Med. 1986;79:221-225. [PubMed] |
| 4. | Tavernier N, Fumery M, Peyrin-Biroulet L, Colombel JF, Gower-Rousseau C. Systematic review: fertility in non-surgically treated inflammatory bowel disease. Aliment Pharmacol Ther. 2013;38:847-853. [PubMed] [DOI] |
| 5. | Waljee A, Waljee J, Morris AM, Higgins PD. Threefold increased risk of infertility: a meta-analysis of infertility after ileal pouch anal anastomosis in ulcerative colitis. Gut. 2006;55:1575-1580. [PubMed] [DOI] |
| 6. | Rajaratnam SG, Eglinton TW, Hider P, Fearnhead NS. Impact of ileal pouch-anal anastomosis on female fertility: meta-analysis and systematic review. Int J Colorectal Dis. 2011;26:1365-1374. [PubMed] [DOI] |
| 7. | Stephansson O, Larsson H, Pedersen L, Kieler H, Granath F, Ludvigsson JF, Falconer H, Ekbom A, Sørensen HT, Nørgaard M. Crohn's disease is a risk factor for preterm birth. Clin Gastroenterol Hepatol. 2010;8:509-515. [PubMed] [DOI] |
| 8. | Cornish J, Tan E, Teare J, Teoh TG, Rai R, Clark SK, Tekkis PP. A meta-analysis on the influence of inflammatory bowel disease on pregnancy. Gut. 2007;56:830-837. [PubMed] [DOI] |
| 9. | Pedersen N, Bortoli A, Duricova D, D Inca R, Panelli MR, Gisbert JP, Zoli G, López-Sanromán A, Castiglione F, Riegler G. The course of inflammatory bowel disease during pregnancy and postpartum: a prospective European ECCO-EpiCom Study of 209 pregnant women. Aliment Pharmacol Ther. 2013;38:501-512. [PubMed] [DOI] |
| 10. | Bröms G, Granath F, Linder M, Stephansson O, Elmberg M, Kieler H. Birth outcomes in women with inflammatory bowel disease: effects of disease activity and drug exposure. Inflamm Bowel Dis. 2014;20:1091-1098. [PubMed] [DOI] |
| 11. | Hashash JG, Kane S. Pregnancy and Inflammatory Bowel Disease. Gastroenterol Hepatol (N Y). 2015;11:96-102. [PubMed] |
| 12. | Hosseini-Carroll P, Mutyala M, Seth A, Nageeb S, Soliman D, Boktor M, Sheth A, Chapman J, Morris J, Jordan P. Pregnancy and inflammatory bowel diseases: Current perspectives, risks and patient management. World J Gastrointest Pharmacol Ther. 2015;6:156-171. [PubMed] [DOI] |
| 13. | Dubinsky M, Abraham B, Mahadevan U. Management of the pregnant IBD patient. Inflamm Bowel Dis. 2008;14:1736-1750. [PubMed] [DOI] |
| 14. | Kwan LY, Mahadevan U. Inflammatory bowel disease and pregnancy: an update. Expert Rev Clin Immunol. 2010;6:643-657. [PubMed] [DOI] |
| 15. | Kornfeld D, Cnattingius S, Ekbom A. Pregnancy outcomes in women with inflammatory bowel disease--a population-based cohort study. Am J Obstet Gynecol. 1997;177:942-946. [PubMed] |
| 16. | Fonager K, Sørensen HT, Olsen J, Dahlerup JF, Rasmussen SN. Pregnancy outcome for women with Crohn's disease: a follow-up study based on linkage between national registries. Am J Gastroenterol. 1998;93:2426-2430. [PubMed] [DOI] |
| 17. | Alstead EM. Inflammatory bowel disease in pregnancy. Postgrad Med J. 2002;78:23-26. [PubMed] |
| 18. | Ujihara M, Ando T, Ishiguro K, Maeda O, Watanabe O, Hibi S, Kamiya T, Mimura S, Hirayama Y, Morise K. Sa1240 Appropriate pharmaceutical management is crucial for pregnant women complicated by ulcer ative colitis. colitis. Gastroenterology. 2012;142:251-252. [DOI] |
| 19. | Mahadevan U, Martin CF, Sandler RS, Kane SV, Dubinsky M, Lewis JD, Sandborn WJ, Sands BE. PIANO: a 1000 patient prospective registry of pregnancy outcomes in women with IBD exposed to immunomodulators and bio-logic therapy. Gastroenterology. 2012;142:S149. [DOI] |
| 20. | Nguyen GC, Seow CH, Maxwell C, Huang V, Leung Y, Jones J, Leontiadis GI, Tse F, Mahadevan U, van der Woude CJ. The Toronto Consensus Statements for the Management of Inflammatory Bowel Disease in Pregnancy. Gastroenterology. 2016;150:734-757.e1. [PubMed] [DOI] |
| 21. | Cury DB, Moss AC. Treatment of Crohn's disease in pregnant women: Drug and multidisciplinary approaches. World J Gastroenterol. 2014;20:8790-8795. [PubMed] [DOI] |
| 22. | Baggott JE, Morgan SL, Ha T, Vaughn WH, Hine RJ. Inhibition of folate-dependent enzymes by non-steroidal anti-inflammatory drugs. Biochem J. 1992;282:197-202. [PubMed] |
| 23. | Khosla R, Willoughby CP, Jewell DP. Crohn's disease and pregnancy. Gut. 1984;25:52-56. [PubMed] [DOI] |
| 24. | Nørgård B, Hundborg HH, Jacobsen BA, Nielsen GL, Fonager K. Disease activity in pregnant women with Crohn's disease and birth outcomes: a regional Danish cohort study. Am J Gastroenterol. 2007;102:1947-1954. [PubMed] [DOI] |
| 25. | Van Assche G, Dignass A, Reinisch W, van der Woude CJ, Sturm A, De Vos M, Guslandi M, Oldenburg B, Dotan I, Marteau P. The second European evidence-based Consensus on the diagnosis and management of Crohn's disease: Special situations. J Crohns Colitis. 2010;4:63-101. [PubMed] [DOI] |
| 26. | Mogadam M, Dobbins WO, Korelitz BI, Ahmed SW. Pregnancy in inflammatory bowel disease: effect of sulfasalazine and corticosteroids on fetal outcome. Gastroenterology. 1981;80:72-76. [PubMed] |
| 27. | Marshall JK, Thabane M, Steinhart AH, Newman JR, Anand A, Irvine EJ. Rectal 5-aminosalicylic acid for maintenance of remission in ulcerative colitis. Cochrane Database Syst Rev. 2012;11:CD004118. [PubMed] [DOI] |
| 28. | Rahimi R, Nikfar S, Rezaie A, Abdollahi M. Pregnancy outcome in women with inflammatory bowel disease following exposure to 5-aminosalicylic acid drugs: a meta-analysis. Reprod Toxicol. 2008;25:271-275. [PubMed] [DOI] |
| 29. | Ford AC, Kane SV, Khan KJ, Achkar JP, Talley NJ, Marshall JK, Moayyedi P. Efficacy of 5-aminosalicylates in Crohn's disease: systematic review and meta-analysis. Am J Gastroenterol. 2011;106:617-629. [PubMed] [DOI] |
| 30. | Asacol (mesalamine), package insert. OH, USA: Warner Chilcott Pharmaceuticals Inc. 2010; . |
| 31. | Hernández-Díaz S, Mitchell AA, Kelley KE, Calafat AM, Hauser R. Medications as a potential source of exposure to phthalates in the U.S. population. Environ Health Perspect. 2009;117:185-189. [PubMed] [DOI] |
| 32. | Bar Oz B, Hackman R, Einarson T, Koren G. Pregnancy outcome after cyclosporine therapy during pregnancy: a meta-analysis. Transplantation. 2001;71:1051-1055. [PubMed] |
| 33. | Bay Bjørn AM, Ehrenstein V, Hundborg HH, Nohr EA, Sørensen HT, Nørgaard M. Use of corticosteroids in early pregnancy is not associated with risk of oral clefts and other congenital malformations in offspring. Am J Ther. 2014;21:73-80. [PubMed] [DOI] |
| 34. | Carmichael SL, Shaw GM. Maternal corticosteroid use and risk of selected congenital anomalies. Am J Med Genet. 1999;86:242-244. [PubMed] |
| 35. | Park-Wyllie L, Mazzotta P, Pastuszak A, Moretti ME, Beique L, Hunnisett L, Friesen MH, Jacobson S, Kasapinovic S, Chang D. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology. 2000;62:385-392. [PubMed] [DOI] |
| 36. | Plauborg AV, Hansen AV, Garne E. Use of azathioprine and corticosteroids during pregnancy and birth outcome in women diagnosed with inflammatory bowel disease. Birth Defects Res A Clin Mol Teratol. 2016;106:494-499. [PubMed] [DOI] |
| 37. | Coelho J, Beaugerie L, Colombel JF, Hébuterne X, Lerebours E, Lémann M, Baumer P, Cosnes J, Bourreille A, Gendre JP. Pregnancy outcome in patients with inflammatory bowel disease treated with thiopurines: cohort from the CESAME Study. Gut. 2011;60:198-203. [PubMed] [DOI] |
| 38. | Akbari M, Shah S, Velayos FS, Mahadevan U, Cheifetz AS. Systematic review and meta-analysis on the effects of thiopurines on birth outcomes from female and male patients with inflammatory bowel disease. Inflamm Bowel Dis. 2013;19:15-22. [PubMed] [DOI] |
| 39. | Hernández-Díaz S, Werler MM, Walker AM, Mitchell AA. Folic acid antagonists during pregnancy and the risk of birth defects. N Engl J Med. 2000;343:1608-1614. [PubMed] [DOI] |
| 40. | Katz JA, Antoni C, Keenan GF, Smith DE, Jacobs SJ, Lichtenstein GR. Outcome of pregnancy in women receiving infliximab for the treatment of Crohn's disease and rheumatoid arthritis. Am J Gastroenterol. 2004;99:2385-2392. [PubMed] [DOI] |
| 41. | Mahadevan U, Kane S, Sandborn WJ, Cohen RD, Hanson K, Terdiman JP, Binion DG. Intentional infliximab use during pregnancy for induction or maintenance of remission in Crohn's disease. Aliment Pharmacol Ther. 2005;21:733-738. [PubMed] [DOI] |
| 42. | Schnitzler F, Fidder H, Ferrante M, Ballet V, Noman M, Van Assche G, Spitz B, Hoffman I, Van Steen K, Vermeire S. Outcome of pregnancy in women with inflammatory bowel disease treated with antitumor necrosis factor therapy. Inflamm Bowel Dis. 2011;17:1846-1854. [PubMed] [DOI] |
| 44. | Torres J, Boyapati RK, Kennedy NA, Louis E, Colombel JF, Satsangi J. Systematic Review of Effects of Withdrawal of Immunomodulators or Biologic Agents From Patients With Inflammatory Bowel Disease. Gastroenterology. 2015;149:1716-1730. [PubMed] [DOI] |
| 45. | Timmer A, Patton PH, Chande N, McDonald JW, MacDonald JK. Azathioprine and 6-mercaptopurine for maintenance of remission in ulcerative colitis. Cochrane Database Syst Rev. 2016;CD000478. [PubMed] [DOI] |
| 46. | Dignass A, Lindsay JO, Sturm A, Windsor A, Colombel JF, Allez M, D'Haens G, D'Hoore A, Mantzaris G, Novacek G. Second European evidence-based consensus on the diagnosis and management of ulcerative colitis part 2: current management. J Crohns Colitis. 2012;6:991-1030. [PubMed] [DOI] |
| 47. | Kornbluth A, Sachar DB. Ulcerative colitis practice guidelines in adults: American College Of Gastroenterology, Practice Parameters Committee. Am J Gastroenterol. 2010;105:501-523; quiz 524. [PubMed] [DOI] |
| 48. | Ford AC, Khan KJ, Achkar JP, Moayyedi P. Efficacy of oral vs. topical, or combined oral and topical 5-aminosalicylates, in Ulcerative Colitis: systematic review and meta-analysis. Am J Gastroenterol. 2012;107:167-176; author reply 177. [PubMed] [DOI] |
| 49. | Marteau P, Tennenbaum R, Elefant E, Lémann M, Cosnes J. Foetal outcome in women with inflammatory bowel disease treated during pregnancy with oral mesalazine microgranules. Aliment Pharmacol Ther. 1998;12:1101-1108. [PubMed] |