修回日期: 2015-07-23
接受日期: 2015-07-30
在线出版日期: 2015-09-08
目的: 探讨姜黄素对非酒精性脂肪性肝病(non-alcoholic fatty liver disease, NAFLD)大鼠内脏脂肪素(Visfatin)、锌-α2糖蛋白(Zinc-α2-glycoprotein, ZAG)影响.
方法: 将56只♂大鼠, 随机分为正常组(16只)和模型组Ⅰ(40只), 分别予以普通饲料和高脂饲料喂养. 8 wk末处死两组大鼠各8只, 取肝脏病理学检查. 证实NAFLD造模成功后, 将模型组Ⅰ大鼠随机分为低剂量组、中剂量组、高剂量组、模型组Ⅱ, 每组8只, 分别予以姜黄素50、100、200 mg/(kg•d)、等体积羧甲基纤维素钠溶液(caboxymethylcellulose, CMC)灌胃, 连续4 wk; 正常组予以等体积CMC灌胃, 连续4 wk. 12 wk末处死所有大鼠, 取肝组织, 称质量, 并作HE染色光镜检查. 检测血清谷丙转氨酶(alanine aminotransferase, ALT)、谷草转氨酶(aspartate aminotransferase, AST)、甘油三酯(triglycerides, TG)、总胆固醇(total cholesterol, TC)、空腹血糖(fasting blood glucose, FBG)及空腹血胰岛素(fasting serum insulin, FINS)水平, 并估计稳态模式评估法胰岛素抵抗(the homeostasis model assessment of insulin resistance, HOMA-IR). 采用免疫组织化学测肝脏Visfatin、ZAG表达, 采用RT-PCR测Visfatin mRNA表达.
结果: 与正常组相比, 模型组肝指数、血清ALT、AST、TG、TC、FINS、FBG和HOMA-IR升高(P<0.01). 低、中、高剂量组较模型组Ⅱ肝指数、血清ALT、AST、TG、TC、FINS、FBG和HOMA-IR降低(P<0.05), 但高于正常组(P<0.05), 除肝指数、TG、FINS、FBG, 低、中、高剂量组间有明显差异(P<0.05). 与正常组相比, 模型组肝组织Visfatin表达增加(P<0.01), ZAG表达降低(P<0.01). 低、中、高剂量组较模型组Ⅱ肝组织Visfatin表达下降(P<0.01), ZAG表达增加(P<0.05), 但没有恢复正常(P<0.05), 且低、中、高剂量组间有明显差异(P<0.05).
结论: Visfatin和ZAG可能参与非酒精性脂肪性肝病的发病; 姜黄素治疗NAFLD大鼠可能是通过调节肝Visfatin水平降低, ZAG水平升高发挥作用.
核心提示: 本实验发现非酒精性脂肪性肝病(non-alcoholic fatty liver disease, NAFLD)大鼠肝组织内脏脂肪素(Visfatin)蛋白表达增加和锌-α2糖蛋白(Zinc-α2-glycoprotein)表达减少促进了NAFLD发展, 可能是NAFLD发病机制之一. 姜黄素治疗NAFLD大鼠, 脂质代谢紊乱、胰岛素抵抗及肝组织病变程度均有所改善, 肝功、血脂、血糖等各项指标均有明显下降.
引文著录: 陈韵, 李珏宏, 李昌平, 钟晓琳, 康敏. 姜黄素对NAFLD大鼠Visfatin、锌-α2糖蛋白的影响. 世界华人消化杂志 2015; 23(25): 4005-4014
Revised: July 23, 2015
Accepted: July 30, 2015
Published online: September 8, 2015
AIM: To investigate the effect of curcumin on Visfatin and Zinc-α2-glycoprotein (ZAG) expression in non-alcoholic fatty liver disease (NAFLD) in rats.
METHODS: Fifty-six male rats were randomly divided into a normal group (n = 16) and a model group Ⅰ (n = 40). The normal group was fed a normal diet, and the model group Ⅰ was fed a high fat diet for 8 wk. After that, 8 rats from each group were sacrificed for liver pathology examination. After confirming NAFLD was successfully developed, the model group Ⅰ was further divided into four groups: a model group Ⅱ and low-, medium- and high-dose curcumin groups. The low-, medium- and high-dose curcumin groups were administrated 50, 100 and 200 mg/kg curcumin by gavage daily for 4 wk. The model group Ⅱ and normal group were administrated equal volume of CMC and normal saline, respectively. Rats were then sacrificed to collect liver tissue samples for pathological observation by HE staining. Serum levels of alanine aminotransferase (ALT), aspartate aminotransferase (AST), triglycerides (TG), total cholesterol (TC), fasting blood glucose (FBG) and fasting serum insulin (FINS) were assayed, and the homeostasis model assessment of insulin resistance (HOMA-IR) was calculated. The protein levels of Visfatin and ZAG were tested by immunohistochemical determination, and the mRNA expression of Visfatin was quantified by RT-PCR.
RESULTS: Compared with the normal group, the levels of liver index, ALT, AST, TG, TC, FINS, FBG and HOMA-IR in the model groups were significantly increased (P < 0.01). The levels of liver index, ALT, AST, TG, TC, FINS, FBG and HOMA-IR in the low-, medium- and high-dose curcumin groups were significantly lower than those in the model group Ⅱ, but significantly higher than those in the normal group (P < 0.05). There were significant differences between the low-, medium- and high-dose curcumin groups (P < 0.05) in the above parameters except liver index, TG, FINS, and FBG. Compared with the normal group, the protein level of Visfatin in the model groups significantly increased (P < 0.01), and the protein level of ZAG in the model groups significantly decreased (P < 0.01). Compared with the model group Ⅱ, the protein levels of Visfatin in the low-, medium- and high-dose curcumin groups significantly decreased (P < 0.01), and the protein levels of ZAG significantly increased (P < 0.05), but both did not return to normal (P < 0.05). There were significant differences in the protein levels of Visfatin and ZAG between the low-, medium- and high-dose curcumin groups (P < 0.05).
CONCLUSION: Visfatin and ZAG may participate in the pathogenesis of NAFLD. The efficacy of curcumin for treating NAFLD rats may be through decreasing the expression of Visfatin protein and increasing the expression of ZAG protein.
- Citation: Chen Y, Li JH, Li CP, Zhong XL, Kang M. Effect of curcumin on Visfatin and Zinc-α2-glycoprotein expression in NAFLD in rats. Shijie Huaren Xiaohua Zazhi 2015; 23(25): 4005-4014
- URL: https://www.wjgnet.com/1009-3079/full/v23/i25/4005.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i25.4005
非酒精性脂肪性肝病(non-alcoholic fatty liver disease, NAFLD)是组临床病理综合征, 疾病谱包括单纯性脂肪肝病、非酒精性脂肪性肝炎(non-alcoholic steatohepatitis, NASH)及相关肝硬化[1]. NAFLD发病机制尚不清楚, 研究[2,3]发现内脏脂肪素(Visfatin)在NAFLD发病过程中作用尚有争议, 其可能使肝细胞脂肪变性, 促进NAFLD的发生. 锌-α2糖蛋白(Zinc-α2-glycoprotein, ZAG)可能通过调节脂类代谢酶活性, 维持脂质代谢的平衡, 从而在NAFLD发病过程中起到保护作用[4]. NAFLD目前尚无满意的治疗方案, 临床上多采用综合疗法. NAFLD有多种治疗药物, 其疗效和安全性尚存争议. 最近研究[5]姜黄有抗氧化、清除氧自由基、抗炎等作用. 姜黄素是姜黄最重要的活性成分, 研究[6]显示其对NAFLD有一定的治疗作用, 但其作用机制尚不清楚. 本文通过建立NAFLD模型来检测肝组织中Visfatin、ZAG表达, 探讨姜黄素对NAFLD大鼠影响及其机制, 以期为NAFLD治疗提供新的思路和策略.
56只健康♂SD大鼠, 体质量210 g±30 g, 由四川医科大学实验动物中心提供. 大鼠饲养温度约15 ℃-25 ℃, 明暗各12 h, 大鼠自由进食、饮水. 胆固醇、胆酸钠(上海蓝季科技发展有限公司), 姜黄素(成都曼思特生物科技有限公司, 浓度98%), Visfatin兔抗大鼠多克隆抗体(Proteintech生物科技有限公司), ZAG兔抗大鼠多克隆抗体(Bioworld生物科技有限公司), RT-PCR试剂盒(博瑞克公司). 高脂饲料配制: 82.5%普通饲料+10%猪油+2%胆固醇+0.5%胆酸钠+5%蔗糖.
1.2.1 NAFLD大鼠模型建立: 大鼠随机分为正常组16只及模型组Ⅰ40只, 分别予以普通饲料、高脂饲料喂养, 于8 wk末处死两组大鼠各8只, 取肝脏予以病理学检查, 观察肝脏脂肪变, 以证实模型组造模成功.
1.2.2 药物干预: 8 wk末将模型组Ⅰ其余大鼠随机分为低剂量组、中剂量组、高剂量组和模型组Ⅱ, 每组8只, 分别予以姜黄素50、100、200 mg/(kg•d)及等体积羧甲基纤维素钠溶液(caboxymethylcellulose, CMC)溶液灌胃, 连续4 wk. 正常组予以等体积CMC溶液灌胃, 连续4 wk.
1.2.3 肝脏肉眼观察: 分别于8、12 wk处死大鼠(每次每组8只), 处死大鼠后观察肝脏形态体积、质地弹性等以及称肝质量、计算肝指数(肝质量/体质量×100%).
1.2.4 肝功能测定及肝组织HE染色: 血清测谷丙转氨酶(alanine aminotransferase, ALT)、谷草转氨酶(aspartate aminotransferase, AST)、甘油三酯(triglycerides, TG)、总胆固醇(total cholesterol, TC)、空腹血糖(fasting blood glucose, FBG)及空腹血胰岛素(fasting serum insulin, FINS)水平, 并估计稳态模式评估法胰岛素抵抗(the homeostasis model assessment of insulin resistance, HOMA-IR). 取肝组织约1 cm×l cm×0.5 cm, 置入4%的多聚甲醛. 固定24 h后, 清水冲洗, 脱水, 透明, 浸蜡, 包埋, 5 μm切片, HE染色.
1.2.5 免疫组织化学测Visfatin和ZAG蛋白表达情况: 石蜡切片脱蜡至水, 柠檬酸缓冲液(pH 6.0)高压抗原修复, 3%甲醇H2O2浸泡10 min(避光)以消除内源性过氧化氢酶活性, 滴加Visfatin兔抗大鼠多克隆抗体、ZAG兔抗大鼠多克隆抗体(1:100), 27 ℃孵育60 min, 滴加二抗, 27 ℃孵育30 min, DAB显色5-10 min, 光镜下掌控, 流水冲洗终止显色, 苏木素复染2 min, 0.1%稀盐酸分化, 饱和碳酸锂反兰, 脱水, 透明, 封片. 采集图像, 使用image-pro plus(IPP)进行图像分析, 测积分光密度值(integrated optical density, IOD).
1.2.6 RT-PCR半定量法检测Visfatin mRNA表达: 肝组织置于液氮研碎, 取约100 mg研碎组织加入1 mL TRIzol, 参照试剂盒提取RNA. 取5 μL RNA样品加入1 μL 6×Loading Buffer混匀, 电泳(100 V, 30 min). 用氯仿-异丙醇-750 mL/L乙醇法常规操作提取RNA, 按逆转录试剂盒说明书操作, 配制成20 μL逆转录反应体系逆转录. Visfatin上游引物为: 5'-CCTACTTTGAATGCCGTGAA-3', 下游引物为: 5'-CAATCCAGTTGTGAGCC-3'. PCR反应: 取cDNA产物1 μL, 上下游引物(10 μmol/L)各1 μL、2×Master Mix 12.5 μL, ddH2O 9.5 μL至总体积25 μL进行PCR, PCR反应后, 取PCR产物5 μL, 用1.5%琼脂糖凝胶电泳(100 V, 15-30 min), 采集图像, 予以灰度扫描, 计算Visfatin/GAPDH的灰度比值.
统计学处理 应用SPSS19.0软件进行数据统计, 实验数据以mean±SD表示. 组间比较采用单因素方差分析法, P<0.05为差异有统计学意义.
模型组Ⅱ大鼠(0.0390±0.0024)较于正常组12 wk肝指数(0.0271±0.0037)明显增加(P<0.01). 随着造模时间延长, 肝指数增加(P<0.05). 低、中、高剂量组(0.0339±0.0025、0.0334±0.0022、0.0318±0.0027)姜黄素均能降低大鼠肝指数(与模型组Ⅱ相比, P<0.01). 且随着姜黄素浓度增高, 肝指数下降, 但低、中、高剂量组间无明显差异(P>0.05), 姜黄素干预肝指数未降至正常(P<0.05).
模型组大鼠较同时期正常组血清ALT、AST、TC、TG增加(P<0.01), 随着造模时间延长, 血清ALT、AST、TC、TG增加(P<0.05). 姜黄素能降低大鼠血清ALT、AST、TC、TG水平(与模型组Ⅱ相比, P<0.05). 且随着姜黄素浓度增高, ALT、AST、TC、TG水平下降, 低、中、高剂量组血清ALT、AST、TC水平有明显差异(P<0.05), 但血清TG低、中、高剂量组无明显差异(P>0.05), 姜黄素干预血清ALT、AST、TC、TG水平未降至正常(P<0.05)(表1).
| 分组 | ALT(U/L) | AST(U/L) | TC(mmol/L) | TG(mmol/L) |
| 正常组8 wk | 37.48±2.51 | 101.35±6.39 | 1.18±0.21 | 0.48±0.08 |
| 模型组Ⅰ | 45.48±4.29a | 163.03±18.54a | 1.73±0.25a | 0.73±0.12a |
| 正常组12 wk | 40.80±3.65 | 129.10±14.46 | 1.29±0.10 | 0.40±0.12 |
| 模型组Ⅱ | 69.33±4.37c | 259.98±13.77c | 3.02±0.21c | 1.24±0.23c |
| 低剂量组 | 58.25±1.84cei | 208.57±20.53cei | 1.97±0.08cei | 0.95±0.24ce |
| 中剂量组 | 49.87±2.44ceh | 178.75±10.03ceh | 1.78±0.08ceh | 0.88±0.19ce |
| 高剂量组 | 44.63±3.74cehi | 161.72±8.44cehi | 1.50±0.06cehi | 0.78±0.13ce |
模型组大鼠较同时期正常组血清FBG、FINS及HOMA-IR增加(P<0.01). 随着造模时间延长, 血清FBG、FINS及HOMA-IR水平升高(P<0.05). 姜黄素能降低大鼠血清FBG、FINS及HOMA-IR水平(与模型组Ⅱ相比, P<0.05). 且随着姜黄素浓度增高, FBG、FINS及HOMA-IR下降, HOMA-IR低、中、高剂量组间有明显差异(P<0.05), 但血清FBG低、中剂量组无明显差异(P>0.05), 血清FINS中、高剂量组无明显差异(P>0.05). 姜黄素干预血清FBG、FINS及HOMA-IR未降至正常(P<0.05)(表2).
| 分组 | FBG(mmol/L) | FINS(mIU/L) | HOMA-IR |
| 正常组8 wk | 4.34±0.49 | 11.82±2.03 | 2.62±0.76 |
| 模型组Ⅰ | 9.339±1.04a | 42.94±3.33a | 18.25±2.86a |
| 正常组12 wk | 4.32±0.85 | 11.85±3.71 | 2.37±1.00 |
| 模型组Ⅱ | 11.27±1.70c | 53.50±7.98c | 24.89±3.42c |
| 低剂量组 | 8.73±1.47cf | 35.79±4.04cfi | 14.09±4.00cfi |
| 中剂量组 | 7.58±1.11cf | 27.73±3.52cfg | 9.47±2.54cfg |
| 高剂量组 | 5.90±0.76cfgi | 22.59±3.69cfg | 6.03±1.84cfgi |
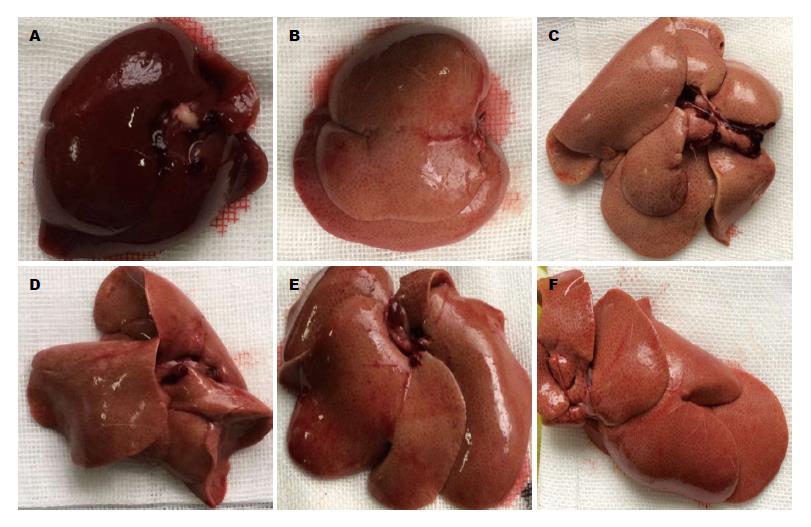
2.4.1 肝脏肉眼观察: 正常组大鼠肝脏组织色鲜红, 质软光滑, 有弹性, 边缘锐利, 与周围组织无黏连(图1A); 模型组大鼠肝脏组织淡黄色, 体积较正常组明显增大, 被膜紧张, 边缘饱满圆钝, 质脆油腻, 弹性差, 与周围组织黏连不易分离(图1B, C); 低、中、高剂量组介于正常组与模型组之间, 随着姜黄素剂量增加, 接近正常组(图1D-F).
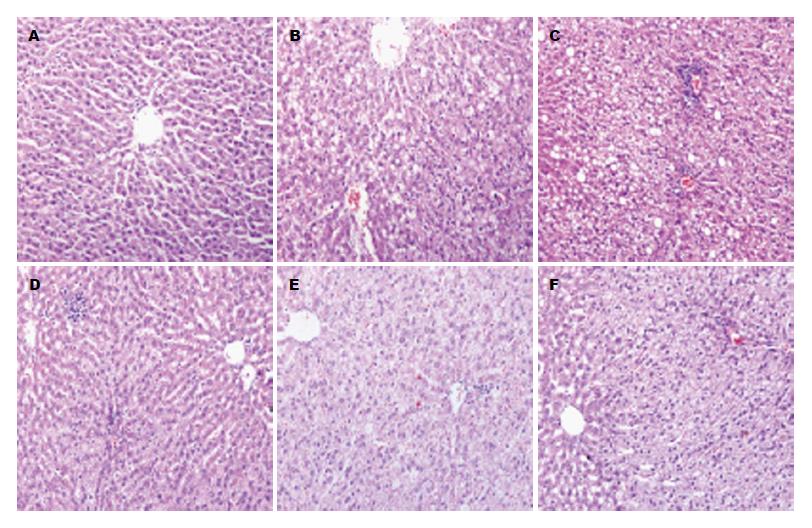
2.4.2 肝组织病理学改变: 正常组可见肝小叶结构完整, 肝索呈放射状, 中央静脉及门管区清晰, 未见肝细胞脂肪变、气球样变及炎细胞浸润(图2A).
模型组Ⅰ可见肝细胞中可见大小不一空泡, 气球样变明显, 少量炎细胞浸润(图2B). 模型组Ⅱ肝小叶结构紊乱, 肝细胞内大量脂滴, 可见程度不等的炎症, 点状或碎片状坏死, 坏死灶较模型组Ⅰ多, 明显气球样变(图2C).
姜黄素治疗后(低、中、高剂量组)可见肝小叶结构紊乱, 肝细胞内可见脂滴, 小叶内、门管区可见程度不等的炎症, 较模型组Ⅱ稍轻, 可见点状或碎片状坏死, 较模型组Ⅱ少, 肝细胞气球样变(图2D-F).
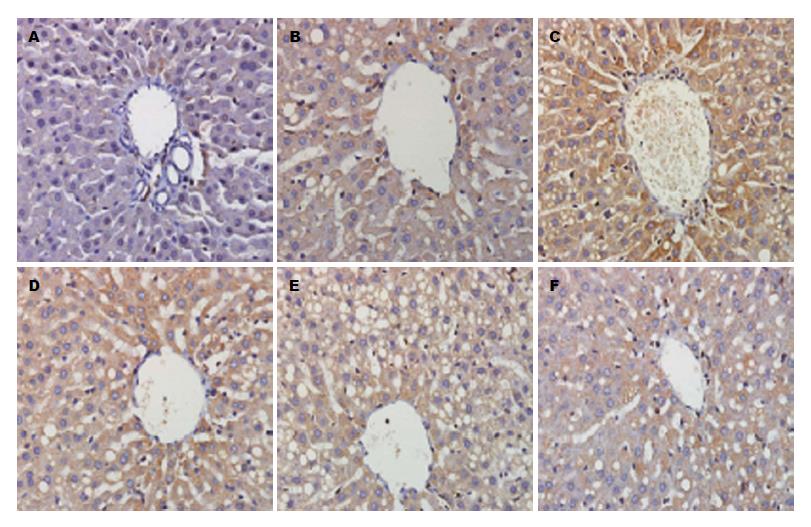
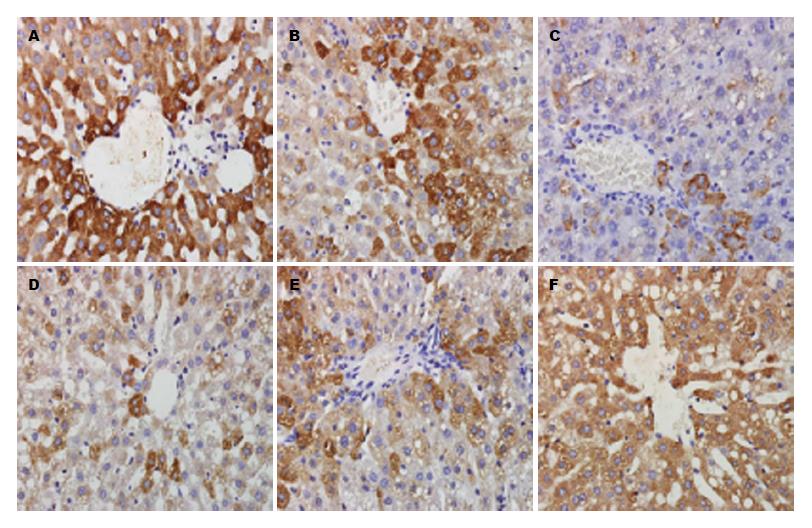
模型组大鼠较同时期正常组肝组织Visfatin水平升高、ZAG水平降低(P<0.01), 随着造模时间延长, 大鼠肝组织Visfatin水平升高、ZAG水平降低(P<0.01). 姜黄素能降低大鼠肝组织Visfatin水平、升高大鼠肝组织ZAG水平(与模型组Ⅱ相比, P<0.01), 且随着姜黄素浓度增高, 肝组织Visfatin水平下降、ZAG水平升高, 肝组织Visfatin、ZAG水平低、中、高剂量组间有明显差异(P<0.01), 姜黄素干预肝组织Visfatin水平未降至正常、ZAG水平未升至正常(P<0.05)(表3, 图3, 4).
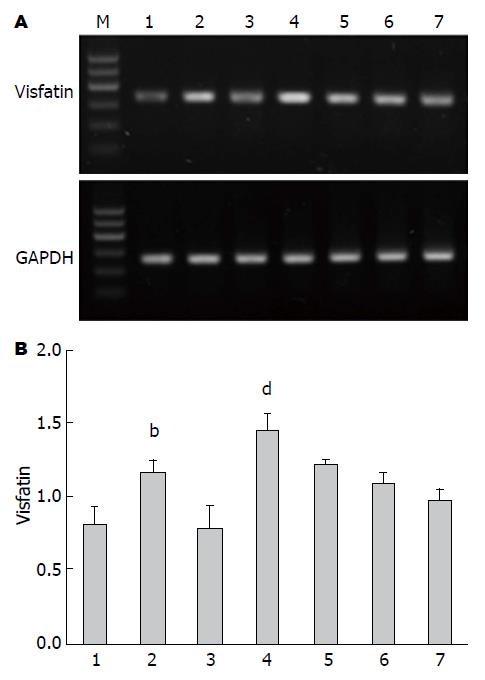
模型组大鼠较同时期正常组肝组织Visfatin mRNA水平明显升高(P<0.01). 随着造模时间的延长, 大鼠肝组织Visfatin mRNA水平升高(P<0.01). 姜黄素能降低大鼠肝组织Visfatin mRNA水平(与模型组Ⅱ相比, P<0.01), 且随着姜黄素浓度增高, 肝组织Visfatin水平下降, 肝组织Visfatin水平低、中、高剂量组间有明显差异(P<0.05), 姜黄素干预肝组织Visfatin mRNA水平未降至正常(P<0.05)(图5).
3.1.1 肝组织Visfatin表达与NAFLD: 2005年Fukuhara等[7]发现Visfatin可促进前脂肪细胞甘油三酯积累, 加快甘油三酯合成葡萄糖; 还可以诱使脂肪细胞分化; Visfatin治疗也可以诱使脂联素和脂肪酸合成酶(fatty acid synthetase, FAS)表达. 循环Visfatin具有烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide, NAD)生物合成活性[8], 可通过维持循环烟酰胺单核苷酸(nicotinamide Mononucleotide, NMN)的水平以调节胰岛β细胞功能[9]. Visfatin同时是炎症介质, 重组Visfatin可诱导促炎因子白介素-6(interleukin-6, IL-6)、肿瘤坏死因子-α(tumor necrosis factor, TNF-α), 表达增加[10]. Visfatin还能促进单核细胞趋化蛋白-1产生[11].
研究发现NAFLD组相较于正常组血清Visfatin浓度增高[12], NAFLD患者循环Visfatin水平和IL-6相互影响[13]. Visfatin可促使人单核细胞分泌IL-6, 而IL-6对Visfatin表达有负调控作用[14]. 两者交互作用, 促使前脂肪细胞分化成熟, 并加重胰岛素抵抗(insulin resistance, IR). 同时IR伴高胰岛素血症可导致IL-6和Visfatin增加, 促进肝细胞脂肪变, 最终导致NAFLD发生. Visfatin还可促使ROS产生[15], 进一步加重肝脏损害. 研究[16]发现NAFLD患者肝脏Visfatin表达增加, 其表达与肝纤维化分期呈正相关.
本实验示: 正常组大鼠肝脏可检测到Visfatin蛋白表达, 相较于正常组, 同时期模型组血清TC、TG升高(P<0.01), 促使肝脂肪变, 同时肝组织Visfatin表达增加(与正常组相比, P<0.01). 由此推测肝细胞脂肪变性可诱导Visfatin表达. 相较于同时期正常组, 模型组血清FBG、FINS和HOMA-IR升高(P<0.05), 提示明显IR. 随着高脂喂养时间延长, 大鼠肝组织脂肪变性程度进一步加重, Visfatin蛋白在肝组织表达也逐渐增加(P<0.01), 但模型组Ⅱ大鼠高胰岛素血症及肝组织病理改变情况进一步恶化. 由此可见肝细胞脂肪变性时, Visfatin蛋白表达代偿性升高, 调节胰岛β细胞功能, 但Visfatin蛋白过度表达后加重IR, 导致IL-6、活性氧等产生, 进一步损害肝脏功能.
3.1.2 肝组织ZAG表达与NAFLD: ZAG由脂肪细胞及上皮细胞分泌[17]. 研究[18]发现ZAG能减少小鼠脂肪, 增加血清FFA水平以及刺激脂肪细胞脂肪分解. ZAG通过肾上腺素β3受体上调cAMP水平实现脂解作用. 同时, 通过调节FAS活性, ZAG可以维持肝脏脂类代谢平衡[4]. ZAG还能抑制小鼠前脂肪细胞分化及刺激细胞增殖[19].
研究[4]表明肥胖小鼠脂肪组织内ZAG表达水平降低; 而诱使ZAG过表达, 肥胖小鼠体质量减轻. 肖新华等[20]发现正常小鼠较NAFLD模型小鼠肝脏ZAG mRNA表达水平高, 可能由于TNF-α表达增加减少ZAG表达[21]. 肝脏ZAG表达减少, 脂类分解通路中乙酰辅酶A羧化酶2(acetylcoa carboxylase2, ACC2)和脂酸β氧化的肉毒碱棕榈酰转移酶(carnitine palmitoyl transferase1, CPT1)活性减弱, 而脂类合成通路中, ACC1和苹果酸酶(malic enzyme, ME)活性增强[22], 上述酶活性改变致使肝脏脂质代谢紊乱, 肝内脂肪蓄积, 肝脂肪变性, 最终形成NAFLD.
本实验示: 与同时期正常组相比, 模型组大鼠肝组织ZAG表达明显降低(P<0.05), 随着高脂喂养时间的延长, 模型组大鼠肝组织ZAG表达量进一步下降(P<0.01), 伴高胰岛素血症、高脂血症、高糖血症及肝组织病理改变情况加重, 证明了肝组织ZAG在NAFLD病程的发展中发挥保护作用. 表明肝组织ZAG表达降低可导致肝脏脂代谢紊乱, 从而形成NAFLD.
NAFLD患者IR和脂质代谢紊乱严重程度与NAFLD病情进展呈正相关[23]. 研究[5]发现姜黄素能够调节肝星状细胞的活性, 从而改善肝细胞的功能, 能通过抑制内源性胆固醇合成, 降低脂肪肝细胞游离胆固醇[24]. 也有学者认为姜黄素对肝脏保护作用可能与降低单核细胞趋化蛋白-1、CD11b和基质金属蛋白酶组织抑制剂-1(tissue inhibitor of matrix metalloproteinase-1, TIMP-1)有关[25]以及影响TNF-α、转化生长因子-β1(transforming growth factor beta 1, TGF-β1)的表达[26,27]. 姜黄素能激活AMP激活的蛋白激酶(AMP-activated prorein kinase, AMPK)进而降低SREBP-1和Fas的表达, 最终抑制肝脂肪和提高肝脏抗氧化能力[28]. Vera-Ramirez等[29]发现姜黄素治疗NAFLD中对核因子-κB(nuclear factor-κB, NF-κB)影响有至关重要的作用. 麦静愔等[30]提出姜黄素能显著降低非酒精性脂肪肝血清学指标, 其机制与调节线粒体功能和维持肝细胞正常结构有关.
本研究示: 予以高脂饲料诱导的NAFLD大鼠姜黄素灌胃4 wk, 发现其可显著改善NAFLD大鼠的肝功能、减轻肝脂肪变及炎症, 从而证明了姜黄素在NAFLD中有治疗作用. 秦培洁等[31]在研究中发现姜黄素能够促进前脂肪细胞分化, 降低内脏脂肪素、抵抗素mRNA表达. 本研究发现姜黄素可改善IR、显著降低血清TG、TC水平, 还可升高ZAG含量和降低Visfatin活性, 伴血清 ALT、AST 显著下降和肝脏病理组织学的改善.
本实验于造模8、12 wk时可见肝脂肪变, 部分可见炎细胞浸润、肝细胞气球样变及坏死, ALT、AST明显升高(相较于同时期正常组, P<0.05), 提示大鼠高脂喂养后, 出现不同程度肝损害. 姜黄素治疗大鼠4 wk后, 肝指数下降(相较于模型组Ⅱ, P<0.01), 血清ALT、AST明显降低(相较于期模型组Ⅱ, P<0.01), 血清TC、TG水平降低(相较于模型组Ⅱ, P<0.05), 伴随肝组织Visfatin mRNA和Visfatin蛋白的表达下降(相较于模型组Ⅱ, P<0.01); 肝组织ZAG表达增加(相较于模型组Ⅱ, P<0.01), 同时FBG、FINS、HOMA-IR的降低(相较于模型组Ⅱ, P<0.01), 且低、中、高剂量组间有明显差异(P<0.05), 高剂量[200 mg/(kg•d)]治疗各项指标改善更为明显. 上述指标改变最终将减轻肝脂肪变、炎症反应及肝脏损害. 本研究证明: 姜黄素可以抗炎、调脂, 改善IR; 姜黄素可以通过下调肝组织Visfatin表达, 改善IR、减少ROS产生等降低炎症反应, 从而治疗NAFLD; 姜黄素可以通过上调肝组织ZAG的表达纠正脂质代谢紊乱, 从而治疗NAFLD.
本实验证明NAFLD大鼠肝组织Visfatin蛋白表达增加和ZAG表达减少促进了NAFLD发展, 可能是NAFLD发病机制之一. 姜黄素治疗NAFLD大鼠, 脂质代谢紊乱、IR及肝组织病变程度均有所改善, 肝功、血脂、血糖等各项指标均有明显下降. 同时发现不同剂量组在转氨酶、TC、胰岛素抵抗指数、ZAG、Visfatin等多项指标改善有明显差异, 随着姜黄素浓度上升, 其治疗效果越明显, 高剂量[200 mg/(kg•d)]治疗效果最佳.
研究发现内脏脂肪素(Visfatin)在非酒精性脂肪性肝病(non-alcoholic fatty liver disease, NAFLD)发病过程中作用尚有争议, 其可能使肝细胞脂肪变性, 促进NAFLD的发生. 锌-α2糖蛋白(Zinc-α2-glycoprotein, ZAG)可能在NAFLD发病过程中起到保护作用. 姜黄素对NAFLD有一定的治疗作用, 但其作用机制尚不清楚.
高泽立, 副教授, 周浦医院消化科, 上海交通大学医学院九院周浦分院
本文通过建立NAFLD模型来检测肝组织中Visfatin、ZAG表达, 探讨姜黄素对NAFLD大鼠影响及其机制, 以期为NAFLD治疗提供新的思路和策略.
目前研究发现姜黄素能够调节肝星状细胞的活性, 从而改善肝细胞的功能, 能抑制内源性胆固醇合成, 降低脂肪肝细胞游离胆固醇. 姜黄素对肝脏保护作用可能与降低单核细胞趋化蛋白-1、CD11b和基质金属蛋白酶组织抑制剂-1有关, 以及影响肿瘤坏死因子-α、转化生长因子β1的表达. 姜黄素能激活AMP激活的蛋白激酶进而降低SREBP-1和Fas的表达, 最终抑制肝脂肪和提高肝脏抗氧化能力.
黄素治疗NAFLD大鼠可能是通过调节肝Visfatin水平降低, ZAG水平升高发挥作用.
探讨姜黄素对NAFLD大鼠影响及其机制, 以期为NAFLD治疗提供新的思路和策略.
本文紧扣当前代谢性疾病非酒精性脂肪肝研究热点, 本研究经动物模型建立、从病理组织学到分子生物学不同角度证明: 姜黄素可以抗炎、调脂、改善胰岛素抵抗; 其机制可能是通过下调肝组织Visfatin表达, 改善胰岛素抵抗、减少ROS产生等降低炎症反应, 从而治疗NAFLD.
编辑: 郭鹏 电编: 都珍珍
| 1. | Lam B, Younossi ZM. Treatment options for nonalcoholic fatty liver disease. Therap Adv Gastroenterol. 2010;3:121-137. [PubMed] [DOI] |
| 2. | Wen H, Wang HJ, Dong B, Ma J. [Relationship between serum visfatin level and children and adolescent obesity and non-alcoholic fatty liver disease]. Zhonghua Liuxingbingxue Zazhi. 2012;33:269-272. [PubMed] |
| 3. | Akbal E, Koçak E, Taş A, Yüksel E, Köklü S. Visfatin levels in nonalcoholic fatty liver disease. J Clin Lab Anal. 2012;26:115-119. [PubMed] [DOI] |
| 4. | Gong FY, Deng JY, Zhu HJ, Pan H, Wang LJ, Yang HB. Fatty acid synthase and hormone-sensitive lipase expression in liver are involved in zinc-alpha2-glycoprotein-induced body fat loss in obese mice. Chin Med Sci J. 2010;25:169-175. [PubMed] |
| 5. | Cheng Y, Ping J, Xu LM. Effects of curcumin on peroxisome proliferator-activated receptor gamma expression and nuclear translocation/redistribution in culture-activated rat hepatic stellate cells. Chin Med J (Engl). 2007;120:794-801. [PubMed] |
| 6. | Nanji AA, Jokelainen K, Tipoe GL, Rahemtulla A, Thomas P, Dannenberg AJ. Curcumin prevents alcohol-induced liver disease in rats by inhibiting the expression of NF-kappa B-dependent genes. Am J Physiol Gastrointest Liver Physiol. 2003;284:G321-G327. [PubMed] |
| 7. | Fukuhara A, Matsuda M, Nishizawa M, Segawa K, Tanaka M, Kishimoto K, Matsuki Y, Murakami M, Ichisaka T, Murakami H. Visfatin: a protein secreted by visceral fat that mimics the effects of insulin. Science. 2005;307:426-430. [PubMed] |
| 8. | Revollo JR, Körner A, Mills KF, Satoh A, Wang T, Garten A, Dasgupta B, Sasaki Y, Wolberger C, Townsend RR. Nampt/PBEF/Visfatin regulates insulin secretion in beta cells as a systemic NAD biosynthetic enzyme. Cell Metab. 2007;6:363-375. [PubMed] |
| 9. | Revollo JR, Grimm AA, Imai S. The regulation of nicotinamide adenine dinucleotide biosynthesis by Nampt/PBEF/visfatin in mammals. Curr Opin Gastroenterol. 2007;23:164-170. [PubMed] |
| 10. | Moschen AR, Kaser A, Enrich B, Mosheimer B, Theurl M, Niederegger H, Tilg H. Visfatin, an adipocytokine with proinflammatory and immunomodulating properties. J Immunol. 2007;178:1748-1758. [PubMed] |
| 11. | Liu SW, Qiao SB, Yuan JS, Liu DQ. Visfatin stimulates production of monocyte chemotactic protein-1 and interleukin-6 in human vein umbilical endothelial cells. Horm Metab Res. 2009;41:281-286. [PubMed] [DOI] |
| 12. | Auguet T, Terra X, Porras JA, Orellana-Gavaldà JM, Martinez S, Aguilar C, Lucas A, Pellitero S, Hernández M, Del Castillo D. Plasma visfatin levels and gene expression in morbidly obese women with associated fatty liver disease. Clin Biochem. 2013;46:202-208. [PubMed] [DOI] |
| 13. | Jarrar MH, Baranova A, Collantes R, Ranard B, Stepanova M, Bennett C, Fang Y, Elariny H, Goodman Z, Chandhoke V. Adipokines and cytokines in non-alcoholic fatty liver disease. Aliment Pharmacol Ther. 2008;27:412-421. [PubMed] |
| 14. | Teoh N, Field J, Farrell G. Interleukin-6 is a key mediator of the hepatoprotective and pro-proliferative effects of ischaemic preconditioning in mice. J Hepatol. 2006;45:20-27. [PubMed] |
| 15. | Oita RC, Ferdinando D, Wilson S, Bunce C, Mazzatti DJ. Visfatin induces oxidative stress in differentiated C2C12 myotubes in an Akt- and MAPK-independent, NFkB-dependent manner. Pflugers Arch. 2010;459:619-630. [PubMed] [DOI] |
| 16. | Kukla M, Ciupińska-Kajor M, Kajor M, Wyleżoł M, Żwirska-Korczala K, Hartleb M, Berdowska A, Mazur W. Liver visfatin expression in morbidly obese patients with nonalcoholic fatty liver disease undergoing bariatric surgery. Pol J Pathol. 2010;61:147-153. [PubMed] |
| 17. | Bing C, Mracek T, Gao D, Trayhurn P. Zinc-α2-glycoprotein: an adipokine modulator of body fat mass. Int J Obes (Lond). 2010;34:1559-1565. [PubMed] [DOI] |
| 18. | Russell ST, Hirai K, Tisdale MJ. Role of beta3-adrenergic receptors in the action of a tumour lipid mobilizing factor. Br J Cancer. 2002;86:424-428. [PubMed] |
| 19. | Zhu HJ, Ding HH, Deng JY, Pan H, Wang LJ, Li NS, Wang XQ, Shi YF, Gong FY. Inhibition of preadipocyte differentiation and adipogenesis by zinc-α2-glycoprotein treatment in 3T3-L1 cells. J Diabetes Investig. 2013;4:252-260. [PubMed] [DOI] |
| 21. | Mracek T, Gao D, Tzanavari T, Bao Y, Xiao X, Stocker C, Trayhurn P, Bing C. Downregulation of zinc-{alpha}2-glycoprotein in adipose tissue and liver of obese ob/ob mice and by tumour necrosis factor-alpha in adipocytes. J Endocrinol. 2010;204:165-172. [PubMed] [DOI] |
| 22. | Choi JW, Liu H, Mukherjee R, Yun JW. Downregulation of fetuin-B and zinc-α2-glycoprotein is linked to impaired fatty acid metabolism in liver cells. Cell Physiol Biochem. 2012;30:295-306. [PubMed] [DOI] |
| 23. | Ying X, Jiang Y, Qian Y, Jiang Z, Song Z, Zhao C. Association between Insulin Resistance, Metabolic Syndrome and Nonalcoholic Fatty Liver Disease in Chinese Adults. Iran J Public Health. 2012;41:45-49. [PubMed] |
| 25. | Vizzutti F, Provenzano A, Galastri S, Milani S, Delogu W, Novo E, Caligiuri A, Zamara E, Arena U, Laffi G. Curcumin limits the fibrogenic evolution of experimental steatohepatitis. Lab Invest. 2010;90:104-115. [PubMed] [DOI] |
| 28. | Kang OH, Kim SB, Seo YS, Joung DK, Mun SH, Choi JG, Lee YM, Kang DG, Lee HS, Kwon DY. Curcumin decreases oleic acid-induced lipid accumulation via AMPK phosphorylation in hepatocarcinoma cells. Eur Rev Med Pharmacol Sci. 2013;17:2578-2586. [PubMed] |
| 29. | Vera-Ramirez L, Pérez-Lopez P, Varela-Lopez A, Ramirez-Tortosa M, Battino M, Quiles JL. Curcumin and liver disease. Biofactors. 2013;39:88-100. [PubMed] |