修回日期: 2014-01-16
接受日期: 2014-01-18
在线出版日期: 2014-03-08
目的: 回顾性分析内镜经黏膜下隧道肿瘤切除术(submucosal tunneling endoscopic resection, STER)治疗来源于固有肌层食管黏膜下肿瘤(submucosal tumors, SMTs)的安全性和有效性.
方法: 选取2012-04/2013-08行STER治疗, 来源于固有肌层食管SMTs的患者5例. 具体步骤如下: (1)建立黏膜下隧道暴露肿瘤; (2)完整剥离肿瘤; (3)移除肿瘤, 关闭隧道口.
结果: 采用STER成功切除所有黏膜下肿瘤, 完整切除率100%; 切除病灶直径1.0-2.5 cm, 平均1.6 cm; 操作时间80-138 min, 平均108.6 min; 住院天数5-7 d, 平均5.8 d; 关闭隧道口用金属钛夹5-9枚, 平均7枚. 术后病理诊断为平滑肌瘤4例, 间叶源性肿瘤1例, 切缘均为阴性. 发生皮下气肿1例, 予保守治疗好转. 4例完成6 mo、1例完成12 mo随访, 无一例出现病变残留或复发.
结论: STER治疗来源于固有肌层的食管SMTs是安全有效的, 值得临床推广并需进一步探究其适应症.
核心提示: 内镜经黏膜下隧道肿瘤切除术(submucosal tunneling endoscopic resection)技术在切除来源于固有肌层的食管黏膜下肿瘤(submucosal tumors)有着独特的优势, 是安全有效的, 但作为一种新技术在适应症的选择上仍需谨慎对待, 随着技术的发展和病例数的积累, 需要与外科手术方式进行前瞻性对照研究.
引文著录: 闵寒, 陈志荣, 龚菲, 王皓, 周俊东, 陈巍峰. 内镜经黏膜下隧道肿瘤切除术治疗源于固有肌层食管黏膜下肿瘤的回顾性分析. 世界华人消化杂志 2014; 22(7): 915-919
Revised: January 16, 2014
Accepted: January 18, 2014
Published online: March 8, 2014
AIM: To evaluate the safety and efficacy of submucosal tunneling endoscopic resection (STER) for esophageal submucosal tumors (SMTs) originating from the muscularis propria layer.
METHODS: Between April 2012 and August 2013, 5 patients with esophageal SMTs originating from the muscularis propria layer were treated by STER. The key steps were as follows: (1) creating a submucosal tunnel to uncover the tumor; (2) resecting the tumor en bloc by endoscopic resection techniques; and (3) closing the mucosal incision site after the tumor was removed.
RESULTS: STER was successfully performed in all 5 cases (success rate: 100%). The mean tumor size was 1.6 cm (range, 1.0-2.5 cm). The mean procedure time was 108.6 min (range, 80-138 min). The average hospital stay was 5.8 d (range, 5-7 d). The mean number of clips used was 7 (5-9). Pathological diagnosis of the tumors was leiomyoma (4/5) and mesenchymal tumor (1/5) with lateral and basal resection margins free of tumor tissue. During the procedure, one patient developed subcutaneous emphysema, who recovered after conservative treatment. No residual or recurrent tumors were detected during the 6-mo (4 patients) and 12-mo (1 patient) follow-up period.
CONCLUSION: STER seems to be a safe and effective procedure for treatment of esophageal SMTs originating from the muscularis propria layer, but its indications need to be further investigated.
- Citation: Min H, Chen ZR, Gong F, Wang H, Zhou JD, Chen WF. Submucosal tunneling endoscopic resection of esophageal submucosal tumors originating from the muscularis propria layer: A retrospective analysis. Shijie Huaren Xiaohua Zazhi 2014; 22(7): 915-919
- URL: https://www.wjgnet.com/1009-3079/full/v22/i7/915.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i7.915
随着消化内镜技术的发展, 特别是超声内镜检查的普及, 食管黏膜下肿瘤(submucosal tumors, SMTs)的诊断率逐年上升[1-4], 但对于其处理方式存在着较多争议. 鉴于其存在的潜在恶性和误诊可能, 目前较多文献倾向于早期切除, 但传统外科治疗创伤较大[5-7], 近年来, 各种内镜下手术方式开始应用于食管SMTs治疗. 传统的内镜下技术, 如内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)和内镜黏膜下挖除术(endoscopic submucosal excavation, ESE)若发生穿孔后果严重[3,4,8-12]. 为了能更安全有效地开展治疗, 2011年复旦大学附属中山医院首先报道了采用内镜经黏膜下隧道肿瘤切除术(submucosal tunneling endoscopic resection, STER)切除食管SMTs[13]. 近期相关研究证实与其他内镜下切除技术相比, 该技术能极大减少并发症的发生率, 保障了此类患者的治疗安全[14-16], 但对于这项技术开展的适应症仍存在争议[17]. 本研究回顾性分析2012-04/2013-08就诊于南京医科大学附属苏州医院消化内科的5例源于固有肌层食管SMTs的STER治疗病例, 为临床推广提供参考.
选择2012-04/2013-08南京医科大学附属苏州医院(苏州市立医院东区)消化内科经胃镜和超声胃镜诊断为食管SMTs患者28例. 超声胃镜证实来源于固有肌层的5例, 纳入本项研究. 其中男性3例, 女性2例, 年龄37-59岁, 平均47.2岁. 病变位于食管中段3例, 下段2例. 超声胃镜显示病变来源于浅肌层4例, 深肌层1例, 病变内部均呈低回声. 所有入组病例术前均签署知情同意书及手术同意书, 告知可能获得的益处和风险. GIF-Q260胃镜, D-201.11802透明帽, EU-M2000内镜超声系统: 微超声探头采用UM-2R(12 MHz)和3R(20 MHz), KD-640L三角刀, KD-620LR HOOK刀, KD-611L IT刀, NM- 200L-0423注射针, SD-5L/6L-1圈套器, FD-410LR热活检钳, HX-610-135L金属止血钛夹, 日本Olympus公司. ICC-200高频电切装置和APC2氩离子凝固器, 德国ERBE公司.
1.2.1 STER: 气管插管麻醉后患者轻度左侧卧位, 低流量吸氧2-3 L/min, 保持呼吸道通畅, 并在术前半小时予以静脉抗生素预防感染. 安装透明帽于胃镜头端, 具体操作步骤如下: (1)建立黏膜下隧道. 在肿瘤近口侧直线距离约5 cm处以2 mL靛胭脂、1 mL肾上腺素和100 mL生理盐水的混合液进行黏膜下注射, 黏膜隆起后以三角刀纵形切开约2 cm. 内镜借助透明帽沿切口进入黏膜下, 反复黏膜下注射并用三角刀逐步分离黏膜下层, 在黏膜层和肌层之间建立隧道直至暴露瘤体. 建立隧道过程中需反复退出隧道以及时了解病灶位置, 避免隧道偏离方向. 如无法寻找到瘤体, 需要重新读片排除其他原因, 必要时中止手术; (2)剥离肿瘤. 应用IT刀及Hook刀沿瘤体周围切开, 与周围组织分离, 完整剥离肿瘤, 注意要保持瘤体包膜的完整性, 避免损伤食管外膜, 术中监测气道压力及颈部有无皮下积气体征; (3)关闭隧道. 切除后瘤体以圈套器取出, 如瘤体过大无法取出隧道, 可扩大隧道口. 取出后使用灭菌蒸馏水反复冲洗隧道, 以热活检钳电凝或氩离子凝固术处理出血灶和显露的小血管. 确认隧道内无出血, 将隧道内液体和气体吸尽, 退出隧道, 直视下用6-10枚钛夹对缝黏膜切口, 关闭隧道口. 切除后病灶送病理.
1.2.2 术后处理和随访: 术后观察患者有无胸闷、气急, 监测血压、脉氧等生命体征. 使用质子泵抑制剂、抗生素和止血药. 术后禁食1 d, 如第2天无不适, 可进食流质. 术后6、12 mo复查胃镜及超声胃镜, 观察创面愈合情况及病变有无残留或复发.
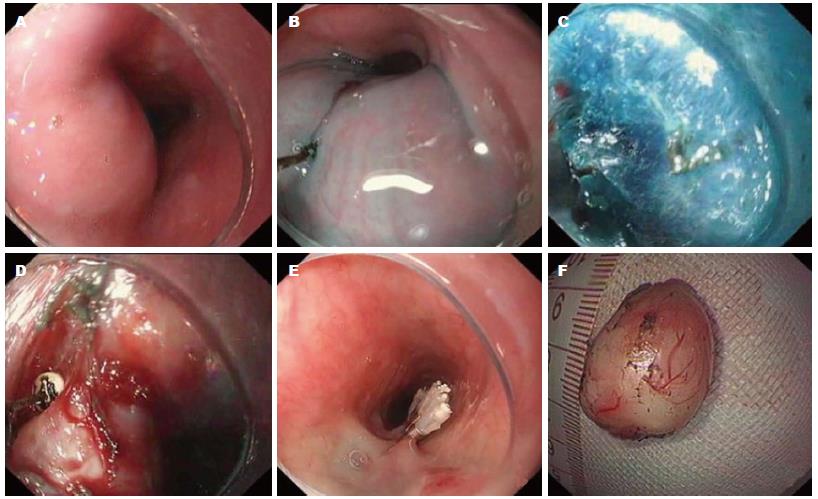
本研究5例病灶均通过STER成功切除(图1), 完整切除率为100%; 切除病灶直径为1.0-2.5 cm, 平均1.6 cm; 操作时间(从黏膜下注射至黏膜隧道切口缝合完成)为80-138 min, 平均108.6 min; 关闭隧道口所用金属钛夹5-9枚, 平均7枚. 术后病理诊断为平滑肌瘤4例, 间叶源性肿瘤1例(未行免疫组织化学), 切缘均为阴性.
术中均有少量出血, 出血量50-120 mL, 经过电凝和氩离子凝固术均成功止血. 1例出现皮下气肿, 予以低流量吸氧和抗感染治疗后3 d体征消失, 行胸片检查无异常. 术后无一例出现迟发性消化系出血或纵隔感染, 无一例出现隧道内积血或感染. 术后第2天患者均能进食流质, 住院天数5-7 d, 平均5.8 d. 4例完成6 mo的随访、1例完成12 mo的随访, 切口均愈合良好, 未发现病变残留或复发.
食管SMTs是一种常见的食管黏膜下肿物, 以平滑肌瘤为主. 食管SMTs患者一般临床无特殊症状, 常经胃镜及超声胃镜诊断. 尽管超声胃镜对病变的大小、层次有很高的评估价值[1-3], 但目前对于病变良恶性的鉴别尚缺乏有效的无创手段, 且存在误诊可能[18], 因此目前大都建议尽早切除明确病理[5,6,15].
对于来源于固有肌层食管SMTs的治疗以往一般采用外科手术[5-7], 但创伤较大, 对于无症状患者风险效益比争论较多. 近年来通过内镜技术的发展, 可以通过ESD、ESE等技术完成该类病变的内镜下切除[8-12]. 但由于病变与肌层关系密切, 极易发生穿孔, 且出现的穿孔创面难以进行有效闭合, 后果严重. 为了克服一般内镜切除技术的缺点, STER技术由经口内镜下贲门括约肌切断术发展而来[19-21]. 其通过隧道内剥离病灶, 既能完整切除肿瘤, 又能通过完整的"黏膜安全瓣"降低术后出现食管瘘和胸腔感染的可能[13,22-24]. 本研究5例病变均通过STER技术成功切除, 完整切除率100%, 且无一例术后严重并发症的发生, 这一结果和国内外相关研究结果是相符合的[13-16,25,26], 说明这项技术对于治疗来源于固有肌层的食管SMTs还是安全有效的. 但STER作为一种新兴的内镜技术, 发展时间较短, 仍存在一些值得继续探究的问题. 主要有以下几点: (1)适应症: 对于STER的适应症, 目前尚没有明确. 从现有的临床报道看有以下几点限制: 病变大小一般在3 cm以下, 如过大只能分片取出, 极易发生隧道内种植[16,17]. 本研究切除病灶直径1.0-2.5 cm, 平均1.6 cm, 均能完整切除并取出; 由于需要在病灶近口侧端约5 cm处建立隧道, 所以一般病灶位置以中下段为主, Choi等[17]认为病灶位置应低于食管上括约肌下方5 cm; 辅助检查提示肿瘤边界清楚, 质地均匀; 无消化系外侵犯和胸腹腔转移征象; (2)穿孔的处理: 术中如损伤食管外膜或穿孔常出现如皮下气肿、气胸或纵隔气肿等临床症状. 现有文献报道发生率约0-16.7%[15,16,26], 本项研究中1例出现皮下气肿, 可能与术中食管外膜损伤有关. 使用CO2气泵可以加快气体的吸收, 因此CO2气泵对于安全开展STER非常重要; (3)出血的估计和处理: 对于出血的估计, Kikuchi等[27]研究发现超声胃镜对于黏膜下血管的分级可以很好的估计胃ESD术中出血的可能性, 是否这也同样适用于食管SMTs还有待进一步研究. 对于出血的术中处理, 本研究出血量50-120 mL, 均成功止血, 但有个别报道出血量可达500 mL[28], 可能与病变位置有关, 但仍需要术中避免和及时处理大血管[29]; (4)保持"黏膜安全瓣"的完整性: 安全瓣的完整性是该技术开展的核心, 如果术中黏膜面发生破损, 病灶无法明确分离, 应及时中止手术或尽早采用黏膜缝合技术[14]. 同时避免为了定位肿瘤而进行的不必要的黏膜面注射和标记等操作, 以防造成潜在的穿孔风险.
总之, STER技术在切除来源于固有肌层的食管SMTs有着独特的优势, 是安全有效的, 但作为一种新技术在适应症的选择上仍需谨慎对待[17]. 本研究纳入的研究较少, 有一定局限性, 随着病例数的积累和技术的发展, 需要进一步与外科手术方式(如单纯胸腔镜、胃镜联合胸腔镜等)[30]进行前瞻性对照研究, 并对于远期疗效以及适应症不断探究.
食管黏膜下肿瘤(submucosal tumors, SMTs)的诊断率逐年上升, 但对于其处理方式存在着较多争议.传统外科治疗创伤较大, 近年来, 各种内镜下手术方式开始应用于食管SMTs治疗.
李小荣, 教授, 中南大学湘雅三医院普外二科
内镜经黏膜下隧道肿瘤切除术(submucosal tunneling endoscopic resection, STER)切除食管黏膜下肿瘤与其他内镜下切除技术相比, 能极大减少并发症的发生率, 保障了此类病人的治疗安全, 但对于这项技术开展的适应症仍存在争议.
Choi等认为尽管目前报道STER治疗食管SMTs是安全有效的, 但由于缺乏与外科手术方式的对照研究, 在选择上仍需要谨慎.
本文不仅对该技术应用的安全性和有效性进行了回顾性研究, 而且深入地对治疗适应症和存在的争议进行了探讨.
本文为微创治疗食管固有肌层肿瘤的推广应用提供了一定的临床研究依据.
编辑: 田滢 电编:鲁亚静
| 4. | Landi B, Palazzo L. The role of endosonography in submucosal tumours. Best Pract Res Clin Gastroenterol. 2009;23:679-701. [PubMed] [DOI] |
| 13. | 徐 美东, 姚 礼庆, 周 平红, 蔡 明琰, 钟 芸诗, 陈 巍峰, 张 轶群, 马 丽黎, 秦 文政, 胡 健卫. 经黏膜下隧道内镜肿瘤切除术治疗源于固有肌层的上消化道黏膜下肿瘤初探. 中华消化内镜杂志. 2011;28:606-610. |
| 14. | Inoue H, Ikeda H, Hosoya T, Onimaru M, Yoshida A, Eleftheriadis N, Maselli R, Kudo S. Submucosal endoscopic tumor resection for subepithelial tumors in the esophagus and cardia. Endoscopy. 2012;44:225-230. [PubMed] [DOI] |
| 15. | Ye LP, Zhang Y, Mao XL, Zhu LH, Zhou XB, He SQ, Chen JY, Jin X. Submucosal tunnelling endoscopic resection for the treatment of esophageal submucosal tumours originating from the muscularis propria layer: an analysis of 15 cases. Dig Liver Dis. 2013;45:119-123. [PubMed] [DOI] |
| 16. | Gong W, Xiong Y, Zhi F, Liu S, Wang A, Jiang B. Preliminary experience of endoscopic submucosal tunnel dissection for upper gastrointestinal submucosal tumors. Endoscopy. 2012;44:231-235. [PubMed] [DOI] |
| 17. | Choi HS, Chun HJ. Usefulness of tunnel dissection for upper gastrointestinal submucosal tumors. Endoscopy. 2012;44:801; author replies 802, 803. [PubMed] [DOI] |
| 19. | Inoue H, Minami H, Kobayashi Y, Sato Y, Kaga M, Suzuki M, Satodate H, Odaka N, Itoh H, Kudo S. Peroral endoscopic myotomy (POEM) for esophageal achalasia. Endoscopy. 2010;42:265-271. [PubMed] [DOI] |
| 22. | Sumiyama K, Gostout CJ, Rajan E, Bakken TA, Knipschield MA. Transesophageal mediastinoscopy by submucosal endoscopy with mucosal flap safety valve technique. Gastrointest Endosc. 2007;65:679-683. [PubMed] |
| 23. | Sumiyama K, Tajiri H, Gostout CJ. Submucosal endoscopy with mucosal flap safety valve (SEMF) technique: a safe access method into the peritoneal cavity and mediastinum. Minim Invasive Ther Allied Technol. 2008;17:365-369. [PubMed] [DOI] |
| 24. | Khashab MA, Saxena P, Valeshabad AK, Chavez YH, Zhang F, Akshintala V, Aguila G, Inoue H, Pasricha PJ, Neuhaus H. Novel technique for submucosal tunneling and endoscopic resection of submucosal tumors (with video). Gastrointest Endosc. 2013;77:646-648. [PubMed] [DOI] |
| 26. | 焦 春花, 杨 树平, 李 学良, 丁 静, 许 迎红, 陶 桂, 陈 莉, 张 道权, 何 湘. 经黏膜下隧道内镜切除术治疗食管中下段黏膜下肿瘤的初步探索. 中华医学杂志. 2013;93:2388-2391. |
| 27. | Kikuchi D, Iizuka T, Hoteya S, Yamashita S, Nakamura M, Kuroki Y, Mitani T, Fujimoto A, Matsui A, Nishida N. Usefulness of endoscopic ultrasound for the prediction of intraoperative bleeding of endoscopic submucosal dissection for gastric neoplasms. J Gastroenterol Hepatol. 2011;26:68-72. [PubMed] [DOI] |
| 28. | 徐 美东, 陆 巍, 李 全林, 周 平红, 钟 芸诗, 陈 巍峰, 张 轶群, 姚 礼庆. 内镜经黏膜下隧道肿瘤切除术在胃固有肌层肿瘤中的应用与评价. 中华胃肠外科杂志. 2012;15:671-674. |
| 29. | Yoshida N, Naito Y, Kugai M, Inoue K, Wakabayashi N, Yagi N, Yanagisawa A, Yoshikawa T. Efficient hemostatic method for endoscopic submucosal dissection of colorectal tumors. World J Gastroenterol. 2010;16:4180-4186. [PubMed] |