修回日期: 2014-01-23
接受日期: 2014-02-18
在线出版日期: 2014-04-28
目的: 观察同步放疗联合替吉奥/奥沙利铂(gimeracil and oteracil potassium capsules/oxaliplatin, S-1/L-OHP, SOX)方案与卡培他滨/奥沙利铂(capecitabine/oxaliplatin, CAP/L-OHP, XELOX)方案治疗术后复发老年胃癌的安全性和疗效.
方法: 66例老年胃癌术后复发患者, 随机分为2组, SOX组34例, 给予替吉奥(<1.25 m2, 40 mg; 1.25-1.5 m2, 50 mg; >1.5 m2, 60 mg), 早晚2次, 口服, d1-14; 奥沙利铂85 mg/m2, d1; 三维适应放疗45 Gy(1.8 Gy/d, 5 d/wk); XELOX组32例: 卡培他滨(2000 mg/m2, 早晚2次, 口服, d1-14), 奥沙利铂和放疗方案同SOX组, 21 d为1周期, 2周期后, 评价疗效和不良反应.
结果: SOX组和XELOX组总有效率(overall response rate, ORR)分别为55.9%和46.9%, 疾病控制率(disease control rate, DCR)分别82.4%和68.8%, 中位进展时间分别为6.3、5.8 mo, 中位生存时间分别为12.8、12.2 mo, 差异均无统计学差异(P>0.05). 两组主要不良反应为中性粒细胞减少、血小板减少等, 差异无统计学意义(P>0.05), XELOX组手足综合征发生率高于SOX组, 差异有统计学意义(P<0.05).
结论: 两组疗效相似, 但SOX方案同步三维适形放疗耐受性优于XELOX方案同步三维适形放疗, 手足综合征发生率较低, 值得进一步临床研究推广.
核心提示: 我们评价了替吉奥/奥沙利铂(gimeracil and oteracil potassium capsules/oxaliplatin, S-1/L-OHP, SOX)方案与卡培他滨/奥沙利铂(capecitabine/oxaliplatin)方案同步放疗治疗中老年胃癌术后复发的临床疗效和安全性, 结果表明两组临床疗效相似, 但SOX方案组手足综合征发生率较低, 耐受性更好, 可以作为老年局部复发晚期胃癌的一种有效治疗方案.
引文著录: 肖鹏, 栗敏, 梅家转, 白桦. SOX方案与XELOX方案同步放疗治疗术后复发胃癌的疗效. 世界华人消化杂志 2014; 22(12): 1720-1724
Revised: January 23, 2014
Accepted: February 18, 2014
Published online: April 28, 2014
AIM: To evaluate the efficacy and safety of SOX regimen (S-1 + L-OHP) versus XELOX regimen (capecitabine + L-OHP) in concurrent chemoradiotherapy for postoperative recurrent gastric carcinoma.
METHODS: Sixty-six elderly patients with postoperative recurrent gastric cancer were randomly divided into two groups: an SOX group (n = 34) and a XELOX group (n = 32). The SOX group received oral S-1 (< 1.25 m2, 40 mg; 1.25-1.5 m2, 50 mg; > 1.5 m2, 60 mg), twice daily, d1-14; L-OHP (85 mg/m2, d1); and three-dimensional conformal radiation (1.8 Gy/d, 5 d/wk and the total dose was 45 Gy). The XELOX group was treated with capecitabine (2000 mg/m2, separated to twice, d1-14), plus the same regimen of radiation and L-OHP as those in the SOX group. Each cycle lasted three weeks. The efficacy and toxicity were evaluated after two cycles of treatment.
RESULTS: The efficacy and toxicity could be evaluated in 66 cases. There were no significant differences in the overall response rate (55.9% vs 46.9%), median time to progression (TTP) (6.3 mo vs 5.8 mo) or median overall survival (OS) (12.8 mo vs 12.2 mo) (P > 0.05) between the two groups. The most common toxicities in the two groups were neutropenia, thrombopenia, nausea, vomiting and diarrhea, all of which could be tolerated. However, the incidence of hand-foot syndrome was significantly higher in the SOX group than in the XELOX group (P < 0.05).
CONCLUSION: The efficacy of chemoradiotherapy based on the SOX regimen for postoperative recurrent gastric carcinoma is better than that of concurrent chemoradiotherapy based on the XELOX regimen in terms of well-tolerated toxicity.
- Citation: Bai H, Mei JZ, Li M, Xiao P. Efficacy of SOX regimen versus XELOX regimen in concurrent chemoradiotherapy for postoperative recurrent gastric carcinoma. Shijie Huaren Xiaohua Zazhi 2014; 22(12): 1720-1724
- URL: https://www.wjgnet.com/1009-3079/full/v22/i12/1720.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i12.1720
胃癌是最常见的恶性肿瘤之一, 世界范围内, 发病率居男性第4位, 女性第5位, 我国胃癌发病率为33.14/10万, 世界人口标化率为23.09/10万, 居恶性肿瘤第2位, 死亡率为23.34/10万, 世界人口标化率为16.39/10万, 居恶性肿瘤死因第3位, 男性高于女性, 且胃癌死亡率随着年龄增长为上升, 65岁组以上发病率更高[1,2], 手术为主的综合治疗成为推荐的治疗模式之一, 5年生存率为20%-25%, 术后复发是死亡的主要原因, 循证医学证据表明, 术后放化疗可以进一步提高生存率[3,4]. 对于胃癌术后复发的老年患者, 考虑到特殊体质, 耐受性较差, 同步放化疗有利于提高局部控制率, 延长生存期. 我科采用奥沙利铂(oxaliplatin, L-OHP)联合替吉奥(gimeracil and oteracil potassium capsules, S-1)或卡培他滨(capecitabine, CAP)同步三维适形放疗方案治疗治疗66例胃癌术后复发患者, 取得较好的临床疗效, 现将临床结果报道如下, 为临床选择有效、安全的辅助治疗方案治疗胃癌术后复发的老年患者提供指导.
选择2008-06/2011-08我科收治66例的胃癌术后复发患者, 全部行全胃或胃次全切除并D2淋巴结清扫术; 男性36例, 女性32例; 年龄60-78岁, 中位年龄70岁; 高分化腺癌12例, 中分化腺癌16例, 低分化腺癌28例, 黏液腺癌8例, 印戒细胞癌2例; 既往术前未接受化疗和/或放疗, 术后接受化疗2到6周期, 但均未使用过奥沙利铂、卡培他滨和替吉奥, 与本试验间隔时间>1 mo, 治疗前均经组织病理学和CT(computed tomography, CT)、磁共振成像(magnetic resonance imaging, MRI)等检查证实至少有一个可测量的复发或转移病灶, 临床分期均为Ⅲ/Ⅳ期. Karnofsky评分>70分, 预计生存期≥3 mo, 心、肝、肾、肺等重要器官功能基本正常, 排除放化疗禁忌症, 无外周神经疾病; 采用双盲操作, 按临床试验随机对照原则, 分为SOX方案(替吉奥, 规格20 mg, 批号: H20080803, 山东新时代药业有限公/奥沙利铂, 规格50 mg, 批号: H20000337, 江苏恒瑞医药股份有限公司)组34例和XELOX方案(卡培他滨, 规格0.5 g, 批号: H2007302, 上海罗氏制药有限公司/奥沙利铂, 规格50 mg, 批号: H20000337, 江苏恒瑞医药股份有限公司)组32例, 两组患者临床资料间无显著性差异. 治疗前签知情同意书和放化疗知情同意书.
1.2.1 治疗: SOX组给予奥沙利铂联合替吉奥同步三维适形放疗, 奥沙利铂, 85 mg/m2, d1; 替吉奥根据体表面积给药40-60 mg(<1.25 m2, 40 mg; 1.25-1.5 m2, 50 mg; >1.5 m2, 60 mg), 早晚口服, d1-14, 停药7 d, 21 d重复; 三维适形放疗, 增强CT模拟定位, 明确病灶, 由放疗科、影像科及物理师共同勾画靶区, 靶体积(clinical target volume, CTV)包括吻合口和淋巴结引流区, 在CTV基础上外放0.5-0.8 cm为计划靶体积(planning target volume, PTV), 95%等剂量曲线包括PTV, 同时注意保护器官, 经三维重建, 以PTV几何中心为照射野中心, 应用西门子直线加速器6MV-X线照射, 1.8 Gy/次, 1次/d, 5次/wk 总剂量45 Gy. XELOX组: 给予卡培他滨: 2000 mg/(m2•d)早晚2次, 口服, 14 d, 停药7 d, 21 d重复]. 奥沙利铂和三维适形放疗方案同SOX组. 治疗期间常规应用保胃、保肝、止吐等支持治疗, 骨髓抑制着者给予人粒细胞集落自己因子注射, 出现手足综合征给予口服维生素B6、涂抹凡士林软膏, 腹泻较严重者给予思密达、易蒙停等对症治疗, 必要时延迟放化疗, 或适当减量, 疾病进展、患者拒绝、出现严重不良反应等不适合继续治疗则终止治疗, 2周期后评价疗效, 有效及稳定者继续SOX方案或XELOX方案化疗, 最多接受6个周期, 采用电话随访至2013-07, 每月随访1次.
1.2.2 观测指标: 疗效及不良反应评定标准: 按照WHO实体瘤客观评价标准, 分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、稳定(stable disease, SD)和进展(progressive disease, PD). 以CR+PR计算总有效率(overall response rate, ORR). 根据NCI-CTC2.0标准评价治疗不良反应. 总生存时间(overall survival, OS)为从本方案治疗的开始日期至死亡或末次随诊的时间, 疾病进展时间(time to progression, TTP)为从本方案治疗的开始日期至客观证据表明疾病进展的时间.
统计学处理 所有试验数据采用SPSS17.0版软件进行统计学分析, 组间差异比较采用χ2检验, 总体生存率采用Kaplan-Meier分析, 化疗反应的等级资料采用非参数秩和检验, 检验水准α = 0.05. P<0.05为差异有统计学意义.
66例患者均完成同步放化疗后又给予原化疗方案(SOX方案和XELOX方案)继续化疗1-5周期, 中位疗程为3个周期, 期间出现的不良反应经对症处理均可恢复或好转, 依从性较好, 并收集完整的临床资料进行相关评估.
66例均可评价疗效, SOX组CR 2例, PR 17例, SD 9例, PD 6例, XELOX组CR 1例, PR 14例, SD 7例, PD 10例, 两组总有效率(CR+PR)分别为55.9%和46.9%, 疾病控制率(CR+PR+SD)分别82.4%和68.8%, 但差异均无统计学差异(P>0.05).
两组患者均未出现治疗相关性死亡, 未见因严重不良反应而停药者, 两组共有常见的不良反应主要为中性粒细胞减少、血小板减少、恶心呕吐、乏力, 以Ⅰ-Ⅱ度为主, 差异无统计学意义(P>0.05), XELOX组手足综合征的发生率高于试验组, 差异有统计学意义(P<0.05)(表1).
| 不良反应 | XELOX组 | SOX组 | χ2 | P值 |
| 白细胞减少 | 0.106 | 0.745 | ||
| Ⅰ-Ⅱ度 | 19 | 17 | ||
| Ⅲ-Ⅳ度 | 2 | 4 | ||
| 血小板减少 | 0.030 | 0.862 | ||
| Ⅰ-Ⅱ度 | 8 | 9 | ||
| Ⅲ-Ⅳ度 | 3 | 2 | ||
| 恶心呕吐 | 0.229 | 0.632 | ||
| Ⅰ-Ⅱ度 | 15 | 13 | ||
| Ⅲ-Ⅳ度 | 1 | 2 | ||
| 手足综合征 | 10.616 | 0.001 | ||
| Ⅰ-Ⅱ度 | 15 | 5 | ||
| Ⅲ-Ⅳ度 | 3 | 1 | ||
| 腹泻 | 0.186 | 0.666 | ||
| Ⅰ-Ⅱ度 | 7 | 6 | ||
| Ⅲ-Ⅳ度 | 0 | 0 | ||
| 肝功能异常 | 0.194 | 0.660 | ||
| Ⅰ-Ⅱ度 | 6 | 5 | ||
| Ⅲ-Ⅳ度 | 0 | 0 |
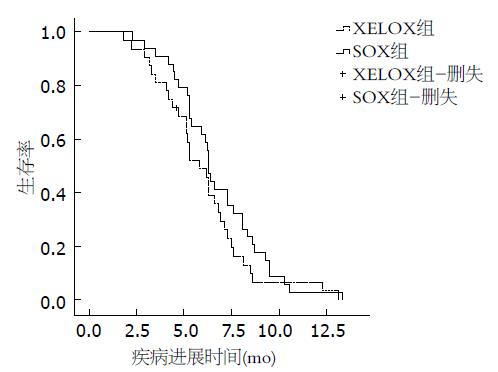
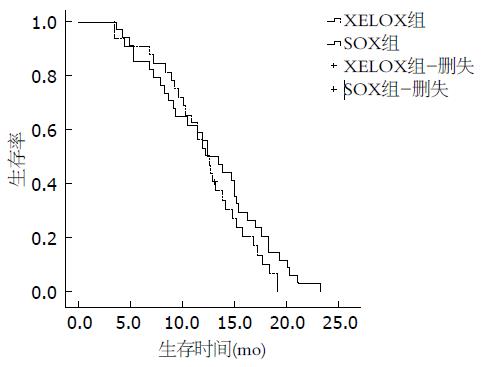
SOX组无失访病例, XELOX组1例失访, 平均随访时间12.6 mo, XELOX组、SOX组组中位TTP分别为5.8 mo(95%CI: 4.8-6.8 mo)、6.3 mo(95%CI: 6.0-6.6 mo), 中位OS分别为12.8 mo(95%CI: 10.9-14.6 mo)、12.2 mo(95%CI: 10.6-13.7 mo), 采用Log-rank检验对TTP和OS曲线进行分析, χ2分别为1.655和1.394(P>0.05), 差异均无统计学意义(图1, 2).
目前, 对于可切除的胃癌, D2根治性切除术成为推荐标准术式, 但术后复发后的挽救治疗, 还没有公认的标准方案之一, 基于美国INT0116试验, 肯定了氟尿嘧啶/亚叶酸钙方案联合放疗在胃癌术后辅助治疗中的价值[4], 而英国MAGIC试验表明ECF方案[表阿霉素(epirubicin)+顺铂(cisplatin)+氟尿嘧啶(5-fluorouracil, 5-FU)]化疗方案在胃癌围手术期化疗中的地临床获益[5], 基于日本ACTS-GC试验(adjuvant chemotherapy trial of S-1 for gastric cancer, ASTS-GC)和韩国CLASSIC临床试验结果, 胃癌D2根治性术后, 替吉奥或卡培他滨/奥沙利铂方案辅助化疗成为推荐的治疗模式[6-14].
替吉奥是二代5-FU类药物, 由替加氟、吉美嘧啶和奥替拉西钾组成的复方制剂, 生物利用度高, 并能降低5-FU引起的消化系不良反应[10]. 卡培他滨是一种新型靶向口服药物, 能在肿瘤组织内转化为氟尿嘧啶发挥抗肿瘤作用. 替吉奥和卡培他滨作为氟尿嘧啶的替代剂型, 在胃癌辅助治疗中, 临床疗效确切, 且给药更方便, 值得临床进一步研究[8,14]. Bang等[9]研究一项前瞻、多中心、随机、对照的Ⅲ期临床试验, 入组Ⅱ/Ⅲ期胃癌1035例, 行D2根治性切除术后, 随机分为两组, 试验组给予卡培他滨/奥沙利铂方案化疗, 对照组观察, 两组中位随访时间分别为34.2 mo、34.3 mo, 3年DFS分别为74%和59%, 不良反应主要为恶心、中性粒细胞减少和食欲下降, 可以耐受, 表明对于胃癌D2根治性切除术后, 卡培他滨/奥沙利铂方案化疗是合理的选择. ACTS-GC试验长期随访结果显示, 相对于单纯手术组, 术后S-1辅助化疗组, 5年总生存率分别为71.1%、61.1%, 5年无复发生存率分别为65.4%和53.1%, 结果表明, S-1辅助化疗延长了Ⅱ/Ⅲ期胃癌D2根治性术后的OS和RFS[11], 与Tatebe等[12]报道相似. 樊翠珍等[13]研究表明奥沙利铂/卡培他滨与奥沙利铂/S-1方案治疗进展期胃癌的疗效相当, 不良反应均可耐受. 刘芳等[15]研究也表明三维适形放疗联合卡培他滨/奥沙利铂方案治疗老年胃癌能降低局部复发率, 延长生存期, 可作为老年胃癌术后的一种有效治疗方法.
我们进一步研究评价SOX方案对比XELOX方案同步三维适形放疗治疗老年胃癌术后复发的疗效及其不良反应, 结果表明两组总有效率分别为55.9%和46.9%, 中位TTP分别为6.3 mo和5.8 mo, 中位OS分别为12.8 mo和12.2 mo, 尽管无统计学意义(P>0.05), 但也有一定的延长, 且XELOX组手足综合征发生率显著高于SOX组, 差异有统计学意义(P<0.05), 其他不良反应发生率无统计学意义.
总之, SOX方案联合放疗与XELOX方案联合放疗治疗老年胃癌术后复发, 临床疗效相似, 尽管没有统计学意义, 但也有一定的延长, 且安全性更高, 更易被老年患者耐受, 可以作为中老年直胃癌的一种有效治疗方案, 另外, 本试验由于样本量小、随访时间较短, 以及如何优放疗与化疗组合的方案等, 因此, 需要扩大样本, 进一步探究更有效、安全的辅助治疗方案, 不断提高术后复发老年胃癌患者的生活质量, 延长生存期.
如何提高中老年患者胃癌术后复发的疗效, 是困扰临床医生的难题, 循证医学证据表明同步放化疗可以提高其生存率, 我们进行了一项临床试验评价替吉奥/奥沙利铂(gimeracil and oteracil potassium capsules/oxaliplatin, S-1/L-OHP, SOX)方案与卡培他滨/奥沙利铂(capecitabine/oxaliplatin, CAP/L-OHP, XELOX)方案同步放疗在中老年晚期复发胃癌的临床疗效和安全性, 为中老年胃癌术后复发选择合理的治疗方案提供参考.
刘占举, 教授, 同济大学附属上海市第十人民医院
中老年患者胃癌术后复发的辅助治疗是胃癌临床研究的热点, 辅助化疗与辅助放化疗孰优孰劣还没有定论, 临床治疗中在注重疗效的同时, 更需要考虑治疗耐受性和患者的依从性, 如何选择最佳的化疗方案, 尤其是适合中老年患者的化疗方案以及联合放疗的时间选择和剂量选择等等, 都亟待得到更多的循证医学证据支持.
循证医学证据表明, SOX方案与XELOX方案在胃癌中显示出较好的临床疗效, 樊翠珍等研究表明奥沙利铂/卡培他滨与奥沙利铂/S-1方案治疗进展期胃癌的疗效相当, 不良反应均可耐受. 刘芳等研究表明三维适形放疗联合卡培他滨/奥沙利铂方案治疗老年胃癌能降低局部复发率,延长生存期,可作为老年胃癌术后的一种有效治疗方法. 我们研究表明SOX方案联合三维适形放疗组手足综合征发生率较低, 更易被老年患者耐受, 且经济费用相对低廉, 可以作为中老年胃癌术后复发的一种有效治疗方案.
我们研究主要评价SOX方案与XELOX方案联合放疗治疗中老年复发晚期胃癌的临床疗效及其不良反应, 结果表明两组疗效相似, 但SOX方案组手足综合征发生率较低, 易被老年患者耐受, 且经济费用相对低廉, 可以作为老年复发晚期胃癌的一种有效治疗方案.
本文主要评价SOX方案与XELOX方案同步三维适形放疗治疗中老年复发胃癌的临床疗效和安全性, 结果表明两组疗效相似, 但SOX方案组手足综合征发生率较低, 耐受性更好, 为中老年复发胃癌术后复发的临床治疗提供参考.
编辑: 郭鹏 电编:鲁亚静
| 2. | Guggenheim DE, Shah MA. Gastric cancer epidemiology and risk factors. J Surg Oncol. 2013;107:230-236. [PubMed] [DOI] |
| 3. | Meyer HJ, Wilke H. Treatment strategies in gastric cancer. Dtsch Arztebl Int. 2011;108:698-705; quiz 706. [PubMed] [DOI] |
| 4. | Macdonald JS, Smalley SR, Benedetti J, Hundahl SA, Estes NC, Stemmermann GN, Haller DG, Ajani JA, Gunderson LL, Jessup JM. Chemoradiotherapy after surgery compared with surgery alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med. 2001;345:725-730. [PubMed] [DOI] |
| 5. | Cunningham D, Allum WH, Stenning SP, Thompson JN, Van de Velde CJ, Nicolson M, Scarffe JH, Lofts FJ, Falk SJ, Iveson TJ. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med. 2006;355:11-20. [PubMed] [DOI] |
| 6. | Knight G, Earle CC, Cosby R, Coburn N, Youssef Y, Malthaner R, Wong RK. Neoadjuvant or adjuvant therapy for resectable gastric cancer: a systematic review and practice guideline for North America. Gastric Cancer. 2013;16:28-40. [PubMed] [DOI] |
| 7. | Taketa T, Sudo K, Wadhawa R, Blum MM, Ajani JA. Adjuvant therapy in gastric cancer: what is the optimal approach? Curr Oncol Rep. 2013;15:146-151. [PubMed] [DOI] |
| 8. | Park SC, Chun HJ. Chemotherapy for advanced gastric cancer: review and update of current practices. Gut Liver. 2013;7:385-393. [PubMed] [DOI] |
| 9. | Bang YJ, Kim YW, Yang HK, Chung HC, Park YK, Lee KH, Lee KW, Kim YH, Noh SI, Cho JY. Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): a phase 3 open-label, randomised controlled trial. Lancet. 2012;379:315-321. [PubMed] [DOI] |
| 10. | Miura K, Shirasaka T, Yamaue H, Sasaki I. S-1 as a core anticancer fluoropyrimidine agent. Expert Opin Drug Deliv. 2012;9:273-286. [PubMed] [DOI] |
| 11. | Sasako M, Sakuramoto S, Katai H, Kinoshita T, Furukawa H, Yamaguchi T, Nashimoto A, Fujii M, Nakajima T, Ohashi Y. Five-year outcomes of a randomized phase III trial comparing adjuvant chemotherapy with S-1 versus surgery alone in stage II or III gastric cancer. J Clin Oncol. 2011;29:4387-4393. [PubMed] [DOI] |
| 12. | Tatebe S, Tsujitani S, Nakamura S, Shimizu T, Yamane N, Nishidoi H, Kurisu Y, Kanayama H, Ogawa H, Ikeguchi M. Feasibility study of alternate-day S-1 as adjuvant chemotherapy for gastric cancer: a randomized controlled trial. Gastric Cancer. 2013; Aug 15. [Epub ahead of print]. [PubMed] [DOI] |