修回日期: 2013-01-10
接受日期: 2013-01-11
在线出版日期: 2013-01-28
目的: 探讨在糖尿病患者中采用胰周动脉超选择插管法用于灌注自体骨髓干细胞的安全性、可行性.
方法: 对24例糖尿病患者, 首先行腹腔干、肝动脉、脾动脉造影, 仔细观察、评价胰周动脉情况. 然后以同轴微导管对目标胰周动脉进一步行超选择插管. 成功后, 经导管缓慢注入含自体骨髓干细胞的分离液. 对于胰周动脉扭曲、细小, 插管困难者, 采用球囊辅助下灌注自体骨髓干细胞的分离液的方法. 观察超选择插管成功率、花费时间及相关并发症.
结果: 全部24例患者中, 23例成功完成胰周动脉超选择插管, 成功率95.8%. 其中, 胰背动脉超选择插管7例, 胰大动脉8例, 胰尾动脉4例, 胰头周围血管4例. 1例失败患者, 改行球囊辅助下灌注干细胞治疗. 全部患者未出现血管痉挛、穿孔、动脉夹层、血管闭塞、血栓形成等并发症. 插管花费时间25-190 min, 中位时间55 min.
结论: 本研究初步提示胰周动脉超选择插管是1种注入自体骨髓干细胞安全、可行的方法.
引文著录: 刘源, 何春水, 刘洋, 张丽峰, 曾伟, 陈秋. 胰周动脉超选择插管法灌注自体骨髓干细胞治疗糖尿病患者24例. 世界华人消化杂志 2013; 21(3): 272-277
Revised: January 10, 2013
Accepted: January 11, 2013
Published online: January 28, 2013
AIM: To evaluate the safety and feasibility of superselective peripancreatic arterial catheterization for infusion of autologous bone marrow stem cells in diabetic patients.
METHODS: A total of 24 patients with diabetes mellitus underwent celiac trunk, hepatic artery and splenic artery angiography, and peripancreatic arteries, which origin from these arteries, were carefully evaluated. One of these peripancreatic arteries was superselectively catheterized with a coaxial microcatheter. After the microcatheter reached the peripancreatic artery, autologous bone marrow stem cells were slowly injected into the artery transcatheterly. For distorted or small peripancreatic arteries that made catheterization difficult, balloon-assisted infusion of autologous bone marrow stem cells was utilized. Success rate, time required for the procedure and complications were evaluated.
RESULTS: Superselective peripancreatic arterial catheterization was successful in 23 of 24 patients, with a success rate of 95.8%. Superselective catheterization of the dorsal pancreatic artery was performed in 7 cases, the great pancreatic artery in 8 cases, the caudal pancreatic artery in 4 cases and the pancreatic artery supplying pancreatic head in 4 cases. The patient with the failed procedure was converted to balloon-assisted infusion of stem cells. Complications such as spasm, perforation, dissection, vascular occlusion and thrombosis were not observed. The time required for the procedure ranged from 25 to 190 min, with a median value of 55 min.
CONCLUSION: Superselective peripancreatic arterial catheterization is a safe and feasible method for infusion of autologous bone marrow stem cells in diabetic patients.
- Citation: Liu Y, He CS, Liu Y, Zhang LF, Zeng W, Chen Q. Superselective peripancreatic arterial catheterization for infusion of autologous bone stem cells in diabetic patients: An analysis of 24 cases. Shijie Huaren Xiaohua Zazhi 2013; 21(3): 272-277
- URL: https://www.wjgnet.com/1009-3079/full/v21/i3/272.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v21.i3.272
糖尿病已成为严重危害人类健康的主要疾病之一, 传统的口服降糖药和胰岛素治疗不能从根本上治愈糖尿病, 也不能完全阻止其并发症的发生和进展. 近年来自体骨髓干细胞移植治疗糖尿病被认为是具有较好前景的治疗手段[1-6]. 自体骨髓干细胞在体外培养、分离后移植到体内的部位有肝脏、脾脏、胰腺, 其中胰腺被认为是较好的移植部位, 但供应胰腺的胰周动脉血管细小、迂曲, 介入医师对该类血管插管的经验较少, 插管技术难度较大. 本文主要讨论经胰腺周围动脉超选择插管途径灌注自体骨髓干细胞在介入操作上的技术要点及安全性、可行性.
2010-3/2011-04, 在我院愿意接受自体骨髓干细胞移植的糖尿病患者共24例, 男13例, 女11例, 年龄13-62岁, 中位年龄54岁. 全部患者中, 1型糖尿病2例, 2型糖尿病22例, 糖尿病病史1-21年, 体质量指数18.9-30.1(23.14 kg/m2±4.42 kg/m2), 治疗前空腹血糖8.33 mmol/L±2.37 mmol/L, 糖化血红蛋白(HbA1c) 8.07%±2.93%, 空腹胰岛素(fasting serum lisulin, FINS)5.04 mIU/L±2.47 mIU/L, 餐后2 h(2 h INS)19.77 mIU/mL±7.96 mIU/mL. 所有患者均已经接受了胰岛素联合至少一种口服降糖药治疗, 包括二甲双胍、噻唑烷二酮类、磺脲类, 治疗前胰岛素用量为43-69 U/d(50.6 U/d±8.03 U/d). 术前行心电图、胸片、凝血、生化等检查, 排除绝对禁忌症, 并取得患者知情同意. 术前患者口腹降糖药物及饮食、运动治疗方案尽可能保持不变; 移植前6-12 h行双腹股沟、大腿、下腹部备皮.
1.2.1 骨髓血采集与分离: 患者术前3 d皮下注射集落细胞刺激因子, 刺激骨髓造血细胞. 手术当天先在外科无菌手术室接受骨髓穿刺, 多点穿刺双侧髂后上嵴或髂前上棘, 首次抽取骨髓0.5 mL行骨髓学和病原学检测, 继之用10 mL肝素注射器抽取骨髓血100-120 mL, 要求在60 min内完成. 将采集的骨髓血送干细胞分离室, 进行骨髓细胞分离、洗涤, 最后用生理盐水稀释单个核细胞悬液至20-30 mL, 进行细胞计数、活性检测. 整个操作过程严格实施无菌操作.
1.2.2 骨髓干细胞移植: 在自体骨髓干细胞分离、培养工作进行中, 根据实验室进度, 患者在骨髓干细胞培养成功前1 h左右被送往介入手术室进行胰周动脉超选择插管手术, 准备灌注自体骨髓干细胞. 血管造影设备为西门子落地式X线C型臂数字化平板探测器心血管造影系统(AXIOM Artis dFA). 患者先经股动脉入路行腹腔干数字减影血管造影(digital substraction angiography, DSA), 造影剂速率4 mL/s, 总量16 mL, 观察脾动脉、肝总动脉走行及分支情况, 并初步观察、评价胰周动脉情况, 包括胰背动脉、胰横动脉、胰大动脉、胰尾动脉等. 然后进一步分别行脾动脉和/或肝总动脉造影, 速率4 mL/s, 总量8 mL, 再次仔细确认胰周动脉开口及胰腺染色情况. 根据患者胰周动脉起源、管径、走行等特点, 选择管径较粗的胰周动脉作为目标动脉进行超选择插管. 超选择插管时, 根据目标血管开口及走行, 适当调整球管投照方向, 使得目标血管开口部位能够清楚显示, 便于操纵导丝进入目标血管. 通常选用SP微导管(Terumo公司), 以同轴方式进行. 以微导管插管成功后, 以0.5-1.0 mL/s流速、2-3 mL总量进行造影, 证实有胰腺实质染色后, 固定微导管, 经微导管缓慢注入自体骨髓干细胞分离液, 然后撤出导管及鞘, 结束手术. 术后患者平卧休息, 并监测生命体征情况. 对于胰周动脉扭曲、细小, 插管不能成功者, 采用球囊辅助下灌注自体骨髓干细胞的分离液的方法. 即将7F指引导管送至脾动脉近端, 然后沿指引导管送入球囊(6 mm×40 mm), 在脾动脉远端阻断脾动脉血流. 经指引导管造影显示脾动脉远端阻断, 而经脾动脉主干发出的胰周动脉及胰腺实质染色更加浓密. 此时在远端球囊阻断情况下, 再经指引导管注入自体骨髓干细胞分离液. 这样确保干细胞被灌注到胰腺实质内. 灌注完毕, 抽空球囊, 撤出导管系统.
1.2.3 观察指标: 观察胰周动脉超选择插管的成功率及其花费时间, 及其有无操作引起的血管痉挛、穿孔、血栓形成、夹层、闭塞等并发症, 观察自体骨髓干细胞灌注中及术后有无不良反应. 观察术后3 mo、6 mo患者血HbA1C、FINS及2 h INS变化情况.
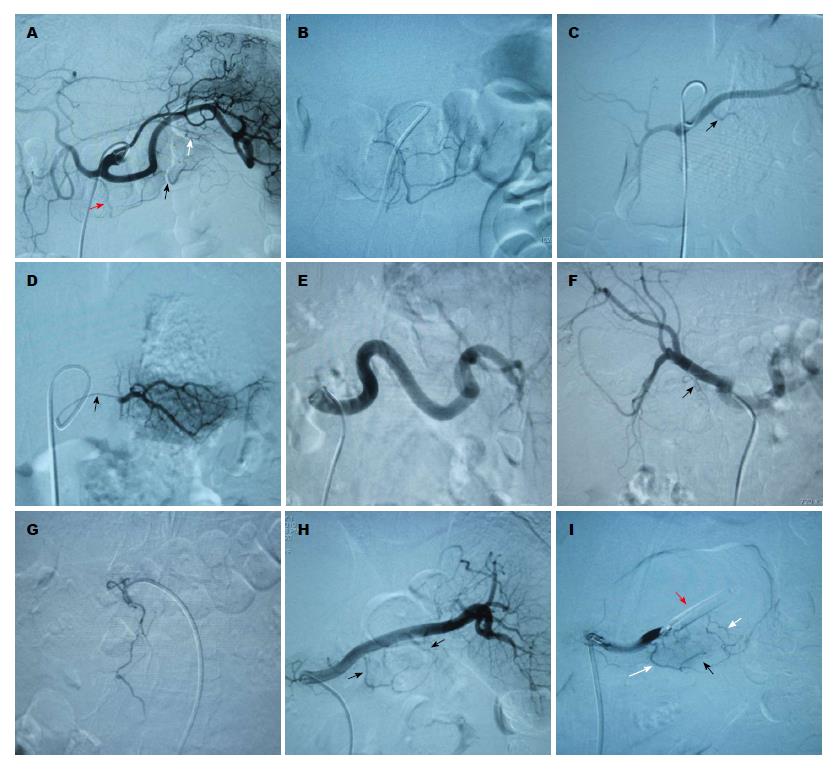
全部24例患者行腹腔干、脾动脉、肝动脉造影检查, 胰背动脉显示率54.17%(13/24), 胰大动脉显示率91.67%(22/24), 胰尾动脉显示率83.33%(20/24). 23例成功进行了胰腺动脉超选择插管灌注自体骨髓干细胞手术, 微导管超选择插管成功的血管分别如下: 胰背动脉7例, 胰大动脉8例, 胰尾动脉3例, 胰头周围血管4例. 插管成功后, 超选择造影显示胰腺实质为羽毛状染色, 勾画出该节段胰腺轮廓, 染色范围、大小与插管动脉的粗细及分支多少一致, 少数患者可见该动脉与其他胰周动脉的吻合支显示. 插管花费时间25-190 min, 中位时间55 min. 1例患者因胰周血管迂曲, 未能成功插管, 在球囊辅助下进行了自体骨髓干细胞灌注. 自体骨髓干细胞灌注时间5-10 min, 灌注中患者未诉特殊不适. 全部患者未观察到严重相关并发症. 无血管痉挛、穿孔、血栓形成、夹层、闭塞等并发症出现, (图1)自体骨髓干细胞移植治疗后3 mo、6 mo, HbA1c水平分别为7.28%±2.97%和7.56%±2.98%, FINS分别为6.90 mIU/L±3.15 mIU/L和7.40 mIU/L±3.33 mIU/L, 2 h INS分别为26.28 mIU/L±10.65 mIU/L和27.29 mIU/L±10.59 mIU/L, 与术前比较, 各组指标变化幅度有统计学意义(P<0.05).
虽然胰岛素治疗在一定程度上能够改善患者的糖代谢紊乱, 但并不能有效地防止或逆转糖尿病引起的血管病变及其并发症. 自体骨髓干细胞移植是治疗1型或2型糖尿病的一种有效方法, 不仅能够纠正糖代谢紊乱, 而且还能有效地防止或逆转糖尿病引起的血管病变及其并发症[7,8]. 自体骨髓干细胞移植主要途径有外周静脉灌注、经胰腺动脉内灌注移植到胰腺, 也有学者经肝动脉或门静脉, 将干细胞种植到肝脏, 也有经脾动脉将干细胞种植到脾脏[2,5,6,9-11]. 体内或体外细胞培养研究均已证实, 骨髓干细胞在胰腺微环境或模拟胰腺微环境下均可诱导分化为胰岛素分泌细胞, 植入胰腺局部的骨髓干细胞可刺激周围胰岛细胞的自我修复. 有学者提出植入胰腺的骨髓干细胞除了直接分化为胰岛素分泌细胞, 还能分化成血管内皮细胞遍布于胰岛周围, 分泌一些与生长及分化有关的因子, 诱导胰腺血管新生, 为胰岛细胞提供了复制信息, 促进胰岛细胞自我复制, 产生新的β细胞. 基于上述认识, 经胰腺动脉将自体骨髓干细胞灌注移植到胰腺组织被认为是较好的移植途径[2,5,6,12-14].
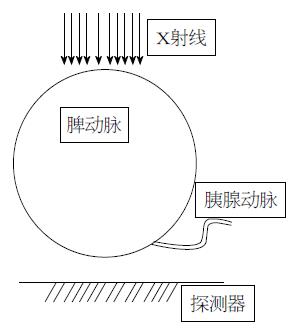
但是, 胰腺不同于肝、肺等内脏器官, 没有类似于"门"的解剖结构, 其供血动脉细小、变异多, 并分散起自于管径较粗的脾动脉和/或肝动脉. 这一解剖特点使得在血管造影时, 二维的图像不能清楚显示胰周动脉在肝或脾动脉的准确的开口部位, 容易导致手术医生误判胰腺动脉起源. 肝总动脉、脾动脉管径粗大, 胰周动脉管径细小, 这一解剖特点导致导丝在肝总/脾动脉内不容易探及胰周动脉开口. 肝总动脉、脾动脉走行常呈自然的迂曲、蜿蜒, 胰周动脉走行与其常呈直角甚至锐角, 导致导丝即使超选择进入到了胰周动脉, 也不易深入到胰周动脉末端, 微导管跟进困难, 且容易弹出. 而合并动脉粥样硬化或胰腺炎、胰腺萎缩的患者, 常有部分胰周动脉闭塞消失或胰周动脉开口的狭窄. 再加上临床上需要介入科医师对胰周动脉进行超选择插管、治疗的情况较少, 因而大多缺乏对这些细小血管超选择插管的经验. 基于这些因素, 一般认为胰周动脉选择插管困难, 耗时, 成功率较低[15,16].
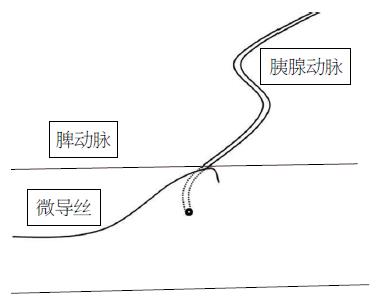
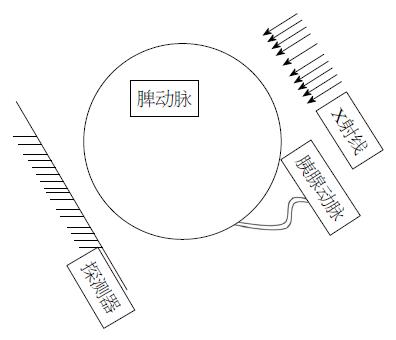
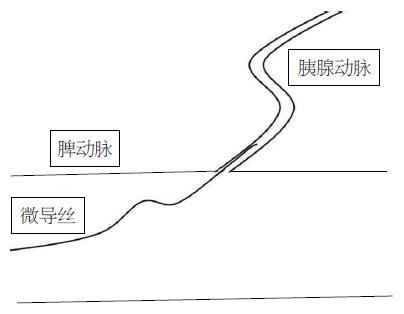
通过DSA本组患者胰周动脉显示情况为胰背动脉显示率54.17%(13/24), 胰大动脉显示率91.67%(22/24), 胰尾动脉显示率83.33%(20/24), 而Wu等[16]报道在102例糖尿病患者的胰周动脉的DSA及CT血管造影对比中, 50%(51/102)的胰背动脉单独显示, 21.6%(22/102)胰背、胰大动脉同时显示, 15.7%(16/102)胰大动脉单独显示, 胰横动脉显示率为10.8%(11/102), 64层增强CT能够显示95.1%(97/102)的胰腺体尾部的动脉. Lin等[17]报道胰背动脉的DSA及CT血管造影的显示率分别为85.7%(36/42)和83.3%(35/42). 提示通过动脉造影或CT血管成像, 胰腺周围动脉绝大多数能够清晰显示出来, 如果我们在手术操作过程中注意相应技巧, 通常能够成功插管、灌注干细胞. 手术操作时, 首先应多角度行腹腔干、脾(肝)动脉造影, 仔细观察胰周动脉分支及开口情况以及胰腺组织染色情况, 选择管径粗细、角度适合的分支作为插管的靶血管. 然后根据靶血管的形态, 对微导管、导丝适当塑形. 插管时应注意调整球管方向, 根据靶血管的起源作头位和/或足位倾斜, 让靶血管起始部与射线的投照方向成切线位, 操作者能够清楚看到靶血管的起始部位, 并能针对性地调整导丝角度进行插管, 这样则容易成功(图2-5). 必要时控制患者呼吸, 利用患者在吸气或呼气状态时, 内脏器官相应的下或上位移, 使靶血管的走行、角度有所改变, 利于导管、导丝通行. 如果采用的血管造影系统具有旋转减影或三维血管成像功能, 对于插管操作则更为有利. 具体操作是先进行旋转采集, 在后处理系统上仔细观察胰周动脉起源、走行情况, 并确定适合目标血管及适合的球管投照角度, 再按这一角度进行透视下插管. 这样手术者能够清楚看到目标血管的走行及起源动脉的情况, 能在短时间内插管成功. 超选择插管成功后, 微导管造影显示该血管供血部分的胰腺组织呈羽毛状染色, 即可经导管缓慢注入自体骨髓干细胞液. 此时, 干细胞即沿血流经该动脉分支漂移、种植于染色部位的胰腺组织内. 注射时勿速度过快, 否则可导致干细胞返流至上一级动脉分支, 并漂移至胰腺以外部位, 导致种植于胰腺的干细胞数目减少.
有学者认为胰头组织较为丰满, 应首选供应胰头的靶血管进行移植; 但我们观察胰头主要由胰十二指肠前、后动脉弓的分支供应, 周围侧支吻合过多, 干细胞培养液易经过吻合支进入十二指肠、网膜等部位. 而胰体、尾部的胰周动脉插管成功后, 造影则显示胰腺实质染色明显、确切. 在这一部位灌注, 能够保证干细胞最终被移植到胰腺组织内. 所以在目标血管的选择上应优先考虑选择胰体、尾的血管, 在胰体、尾没有合适的目标血管时, 再选择胰头的目标血管[17].
如果有些目标血管开口角度不利于微导管进入, 微导管反复尝试后不能成功, 可直接用眼镜蛇导管前端的弯曲弧度, 直接探、挂胰周动脉开口. 将导管尖端直接靠在目标动脉开口上, 造影往往能直接显示目标血管和胰腺染色. 此时妥善固定导管, 灌注干细胞, 也能确保干细胞能直接种植入胰腺组织. 因脾动脉主干近端、中段仅有胰大、胰尾动脉发出, 球囊在脾动脉远端阻断血流后, 造影证实胰腺组织染色增浓, 胰大、胰尾动脉管腔造影剂充盈明显, 说明造影剂主要进入了胰腺组织. 在球囊阻断脾动脉情况下灌注自体骨髓干细胞, 也能确保干细胞分离液进入胰腺组织. 但球囊辅助法操作较为繁琐, 脾动脉迂曲时, 球囊进入脾动脉也较困难, 且患者花费较高, 故宜作为最后的手段使用. 但优点在于干细胞培养液可同时经多支胰周动脉灌注, 种植到较广泛的胰腺组织内.
对于某些有急、慢性胰腺炎病史患者, 可在术前作胰周动脉影像学评价, 了解胰腺形态,和胰腺组织有无萎缩、破坏, 评价胰腺血供及胰周动脉粗细, 在术前提供更多信息, 推测胰周动脉插管难易程度[17,18]. 虽然胰周动脉细小, 走行迂曲, 若手术医生掌握一定技巧, 大多能够在较短时间内超选择插管成功, 且风险低并发症少. 该技术可以作为一种常规手段用于将自体骨髓干细胞灌注、移植到胰腺组织. 但自体骨髓干细胞经该途径进入到胰腺组织后, 其存活、增殖、胰岛素分泌功能等方面还需进一步研究.
自体骨髓干细胞移植治疗糖尿病被认为是具有较好前景的治疗手段. 通常认为经胰腺供血动脉将干细胞移植到胰腺是较为理想的移植部位, 但胰腺动脉细小, 变异多, 超选择插管技术耗时、难度大, 能否作为一个常规干细胞移植手段应用到临床, 还需要进一步研究.
门秀丽, 教授, 河北联合大学(原华北煤炭医学院)病理生理学教研室
微导管超选择插管技术在肝、肺肿瘤性病变及神经介入等方面应用较多, 但由于胰腺血管的特殊性及临床工作中较少用到胰腺动脉超选择插管技术, 介入医师大多缺乏该部位的超选择插管手术操作经验.
相关研究提示胰腺周围动脉起源较为广泛, 变异多, 走行迂曲, 但主要供血动脉如胰大动脉、胰背动脉、胰横动脉等均可经增强CT或数字减影血管造影(DSA)显示.
本研究介绍了以微导管超选择插管的技术在胰周动脉的具体应用, 并提出对于插管失败的患者, 可采用球囊辅助的方法移植干细胞.
在临床工作中, 可常规采用微导管超选择插管, 将自体骨髓干细胞经胰腺动脉安全可靠地移植到胰腺组织. 胰腺体、尾部是一个较好的干细胞移植部位. 该研究也可对胰腺某些富血供肿瘤的介入栓塞治疗有借鉴作用.
骨髓干细胞: 存在于骨髓中的多能干细胞, 包括造血干细胞和间充质干细胞. 骨髓间充质干细胞在体内或体外特定的诱导条件下, 可分化为脂肪、骨、肌肉、肌腱、韧带、神经、 肝、心肌、内皮等多种组织细胞, 可作为理想的种子细胞用于衰老和病变引起的组织器官损伤修复.
本文对自体骨髓干细胞移植治疗糖尿病提出了一个较新的灌注移植方法, 具有一定的临床应用价值, 值得临床医生阅读.
编辑: 田滢 电编: 鲁亚静
| 2. | Estrada EJ, Valacchi F, Nicora E, Brieva S, Esteve C, Echevarria L, Froud T, Bernetti K, Cayetano SM, Velazquez O. Combined treatment of intrapancreatic autologous bone marrow stem cells and hyperbaric oxygen in type 2 diabetes mellitus. Cell Transplant. 2008;17:1295-1304. [PubMed] [DOI] |
| 3. | Gangaram-Panday ST, Faas MM, de Vos P. Towards stem-cell therapy in the endocrine pancreas. Trends Mol Med. 2007;13:164-173. [PubMed] [DOI] |
| 4. | Sun Y, Chen L, Hou XG, Hou WK, Dong JJ, Sun L, Tang KX, Wang B, Song J, Li H. Differentiation of bone marrow-derived mesenchymal stem cells from diabetic patients into insulin-producing cells in vitro. Chin Med J (Engl). 2007;120:771-776. [PubMed] |
| 5. | Wang L, Zhao S, Mao H, Zhou L, Wang ZJ, Wang HX. Autologous bone marrow stem cell transplantation for the treatment of type 2 diabetes mellitus. Chin Med J (Engl). 2011;124:3622-3628. [PubMed] |
| 6. | Bhansali A, Upreti V, Khandelwal N, Marwaha N, Gupta V, Sachdeva N, Sharma RR, Saluja K, Dutta P, Walia R. Efficacy of autologous bone marrow-derived stem cell transplantation in patients with type 2 diabetes mellitus. Stem Cells Dev. 2009;18:1407-1416. [PubMed] [DOI] |
| 7. | Liu M, Han ZC. Mesenchymal stem cells: biology and clinical potential in type 1 diabetes therapy. J Cell Mol Med. 2008;12:1155-1168. [PubMed] [DOI] |
| 8. | Efrat S. Generation of insulin-producing cells from stem cells for cell replacement therapy of type 1 diabetes. Isr Med Assoc J. 2004;6:265-267. [PubMed] |
| 11. | 王 攀, 吴 正蓉, 田 景伦, 戚 龙. 经皮脾动脉自体骨髓细胞移植治疗2型糖尿病5例. 中国组织工程研究与临床康复. 2010;14:4355-4358. |
| 12. | Xie QP, Huang H, Xu B, Dong X, Gao SL, Zhang B, Wu YL. Human bone marrow mesenchymal stem cells differentiate into insulin-producing cells upon microenvironmental manipulation in vitro. Differentiation. 2009;77:483-491. [PubMed] [DOI] |
| 13. | Tang DQ, Cao LZ, Burkhardt BR, Xia CQ, Litherland SA, Atkinson MA, Yang LJ. In vivo and in vitro characterization of insulin-producing cells obtained from murine bone marrow. Diabetes. 2004;53:1721-1732. [PubMed] [DOI] |
| 14. | Hess D, Li L, Martin M, Sakano S, Hill D, Strutt B, Thyssen S, Gray DA, Bhatia M. Bone marrow-derived stem cells initiate pancreatic regeneration. Nat Biotechnol. 2003;21:763-770. [PubMed] [DOI] |
| 15. | Okahara M, Mori H, Kiyosue H, Yamada Y, Sagara Y, Matsumoto S. Arterial supply to the pancreas; variations and cross-sectional anatomy. Abdom Imaging. 2010;35:134-142. [PubMed] [DOI] |
| 16. | Wu ZX, Yang XZ, Cai JQ, Liao LM, Yang L, Lin YN, Tan JM. Digital subtraction angiography and computed tomography angiography of predominant artery feeding pancreatic body and tail. Diabetes Technol Ther. 2011;13:537-541. [PubMed] [DOI] |
| 17. | Lin Y, Yang X, Chen Z, Tan J, Zhong Q, Yang L, Wu Z. Demonstration of the dorsal pancreatic artery by CTA to facilitate superselective arterial infusion of stem cells into the pancreas. Eur J Radiol. 2012;81:461-465. [PubMed] [DOI] |