修回日期: 2013-07-10
接受日期: 2013-07-31
在线出版日期: 2013-09-08
目的: 系统评价恩替卡韦治疗乙型肝炎病毒相关性肝衰竭的疗效.
方法: 检索2005-01/2013-04有关在常规内科治疗基础上使用恩替卡韦后对患者生存率及DNA转阴率影响的随机对照试验, 应用Meta分析的方法以比值比(odds ratio, OR)为效应量进行合并分析.
结果: 共纳入18篇RCT, 生存率的合并效应量OR值及95%CI: 2.17(95%CI: 1.63-2.89), HBV-DNA转阴率的OR值的合并效应量及95%CI: 20.32(95%CI: 8.09-51.04).
结论: 与内科常规治疗比较, 加用恩替卡韦可显著抑制HBV的复制, 明显提高生存率.
核心提示: 恩替卡韦可以高效迅速抑制乙型肝炎病毒复制, 血清及肝组织中的病毒负荷降低, 肝细胞表面靶抗原的表达减轻, 使再生肝细胞免受病毒感染, 减轻肝内炎症活动和坏死程度, 减少死亡率.
引文著录: 马莎莎, 吴继周, 宁秋悦, 钟大妮, 吴健林. 恩替卡韦治疗HBV相关性肝衰竭随机对照试验的Meta分析. 世界华人消化杂志 2013; 21(25): 2594-2600
Revised: July 10, 2013
Accepted: July 31, 2013
Published online: September 8, 2013
AIM: To evaluate the effect of entecavir on survival of patients with HBV-related liver failure.
METHODS: This meta-analysis collected the randomized control trails that used entecavir to treat liver failure induced by hepatitis B virus from January 2005 to April 2013. All these clinical trials were carried out by comparing entecavir treatment with routine medical treatment for liver failure. Odds ratio (OR) was used to evaluate the effect of entecavir on survival and reduction in HBV-DNA levels in patients with HBV-related liver failure.
RESULTS: A total of 18 studies were included. OR for the survival rate was 2.17 (95% CI: 1.63-2.89) and OR for reduction in HBV-DNA levels was 20.32 (95%CI: 8.09-51.04).
CONCLUSION: Routine medical treatment in combination with entecavir is more effective than routine medical treatment alone in improving survival and inhibiting HBV replication in patients with HBV-associated liver failure.
- Citation: Ma SS, Wu JZ, Ning QY, Zhong DN, Wu JL. Effect of enticavir on survival of patients with HBV-related liver failure: A Meta-analysis. Shijie Huaren Xiaohua Zazhi 2013; 21(25): 2594-2600
- URL: https://www.wjgnet.com/1009-3079/full/v21/i25/2594.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v21.i25.2594
肝衰竭是以肝性脑病、肝肾综合征、凝血功能障碍和黄疸等为主要临床表现的一组临床症候群[1], 病死率高. 其病理生理改变在于肝炎病毒、药物、乙醇等多种因素导致严重的肝脏功能损害, 合成、解毒、排泄和生物转化等功能发生严重障碍或失代偿. 我国是乙型肝炎病毒感染高发国家之一, 乙型肝炎病毒(hepatitis B virus, HBV)感染引起的肝衰竭目前已成为乙型肝炎患者的主要死因之一. 目前, 肝移植仍被认为是治疗肝衰竭的首选治疗方案, 但是肝源的缺乏以及高昂的治疗费用使得其在临床上的应用受到了极大地限制. 近几年来, 人工肝技术成为肝衰竭患者的重要支持疗法, 但同样受到费用及血源的限制. 恩替卡韦(entecavir, ETV)作为一种强有效而低耐药率的抗病毒药物已被广泛应用于乙型肝炎相关性肝衰竭的治疗中, 虽然相关的临床研究报道较多, 但结论不尽一致, 而且在目前相关的肝衰竭治疗指南中仅作为专家的推荐意见(证据级别仅为Ⅲ级), 可见, 从循证医学的角度对ETV治疗HBV相关性肝衰竭的临床试验进行系统评价是有必要的. 本研究致力于对ETV是否能提高乙型肝炎相关性肝衰竭患者的生存率及降低HBV-DNA水平的效果进行Meta分析, 以期发现较新的科学、客观的循证医学证据, 用于指导HBV相关性肝衰竭临床治疗.
以"liver failure"、"hepatic failure"、"entecavir"、"Baraclude"、"severe hepatitis B"为主题词, 检索语种为英语, 对在2005-01/2013-04公开发表在Medline, Pubmed, Embase, the Cochrane Center Register of Controlled Trials等数据库的文献进行检索; 对2005-01/2013-04公开发表在重庆维普数据库(VIP)、中文科技数据库、CNKI全文数据库、万方数据库等的文献, 以"恩替卡韦"、"博路定"、"肝衰竭"、"乙型重型肝炎"、"慢加急性肝衰竭"等为主题词, 以汉语为检索语种进行检索, 同时以文献追述和手工检索的方法为辅助, 纳入相关的参考文献.
1.2.1 入选标准: (1)研究设计: 随机对照试验(randomized control trial, RCT); (2)研究对象: 符合我国2000年《病毒性肝炎防治方案》或2006年《肝衰竭诊疗指南》诊断标准; 均有急性乙型肝炎、慢性乙型肝炎或乙型肝炎后肝硬化的疾病史; HBV-DNA阳性(>103 copy/mL); (3)纳入研究前发现乙型肝炎表面抗原超过6 mo, 入选前未使用任何抗病毒药物, 或之前使用过, 但已停用至少6 mo以上者; (4)干预措施: 试验组在内科常规综合治疗的基础上加用ETV, 对照组除单纯内科常规综合治疗外不加用任何抗病毒药物, 在年龄、性别、病情等方面的差异无统计学意义; (5)选择最详细、最近发表的重复报道的文献进行分析.
1.2.2 剔除标准: (1)合并其他病毒的感染, 包括甲、丙、丁、戊型肝炎病毒或EB病毒、巨细胞病毒; 或合并其他容易引起肝衰竭的疾病, 如自身免疫性肝炎、药物性肝炎、酒精性肝炎等; (2)合并有严重免疫系统疾病、血液系统疾病、或恶性肿瘤、明显精神病史; (3)存在样本资料交待不清楚、诊断及疗效判定标准不统一等问题; (4)在治疗或随访期间辅助人工肝或糖皮质激素治疗者; (5)在分析时无法转化或应用提供的数据的文献.
1.2.3 质量控制: 2名研究者接受统一培训后对文献进行检索, 并对比检索结果防止文献遗漏. 对第一作者、标题、刊物名称、发表时间、患者年龄、性别、治疗方式、治疗时间、结局指标等资料进行提取归纳. 对纳入文献采用Jadad评分标准进行质量评分[2], 低质量文献≤2分, 高质量文献≥3分.
统计学处理 采用Cochrane协作网提供的Revman5.0软件包. 比值比(odds ratio, OR)及95%CI作为系统评价的指标. 异质性检验采用χ2检验进行, 根据异质性检验结果评估是否合并效应量及使用哪种模型进行估计; 存在同质性则应用固定效应模型(Mantel-Haenszel), 存在异质性时则用随机效应模型(Dersimonian-Laird). 根据森林图判定结果: OR = 1提示ETV治疗对生存率及HBV-DNA降低水平无影响; 当OR<1时提示ETV治疗对生存率及HBV-DNA转阴率无益; 当OR>1时表明ETV治疗有利于提高生存率及降低DNA水平. 发表偏倚的评估采用漏斗图, 并对结果进行敏感性分析. 以P<0.05为差异具有统计学意义.
根据入选标准及剔除标准进行筛选, 共检索到120篇与ETV治疗乙型肝炎病毒相关性肝衰竭相关的文献. 入选文献均以ETV和常规治疗进行分组, 其中有两篇文献分组中包括拉米夫定治疗组, 疗程均在4 wk以上. 最终纳入Meta分析的RCT文献共18篇. 其中, 英文文献3篇, 中文文献15篇, 所有的RCT均在中国大陆地区进行, 如表1所示.
| 文献来源 | 样本含量 | ETV剂量(mg/d) | 疗程 | 治疗结束时存活例数 | Jadad评分 | ||
| ETV组 | 常规组 | ETV组 | 常规组 | ||||
| 郭玉香[3] | 37 | 45 | 0.5 | 8 wk | 32 | 30 | 2 |
| 杨海敏等[4] | 55 | 55 | 0.5 | 30 d | 40 | 26 | 3 |
| 韩志启等[5] | 20 | 16 | 0.5 | 4 wk | 20 | 16 | 2 |
| 赵蕊[6] | 40 | 40 | 0.5 | 48 wk | 38 | 27 | 2 |
| 钟旬华等[7] | 30 | 30 | 0.5 | 1年 | 21 | 13 | 2 |
| Chen等[8] | 55 | 74 | 0.5 | 3 mo | 36 | 55 | 2 |
| Cui等[9] | 33 | 37 | 0.5 | 3 mo | 16 | 15 | 2 |
| 赵红等[10] | 63 | 58 | 0.5 | 12 wk | 46 | 39 | 2 |
| Chen等[11] | 42 | 34 | 0.5 | 3 mo | 26 | 12 | 2 |
| 王朝辉[12] | 22 | 20 | 0.5 | 12 wk | 12 | 4 | 2 |
| 李芳等[13] | 16 | 14 | 0.5 | 6 wk | 12 | 6 | 2 |
| 朱爱红等[14] | 23 | 23 | 0.5 | 12 wk | 22 | 21 | 2 |
| 袁锦林等[15] | 71 | 50 | 0.5 | 30 d | 71 | 50 | 2 |
| 廖炯[16] | 25 | 25 | 0.5 | 12 wk | 25 | 25 | 2 |
| 徐春华[17] | 27 | 25 | 0.5 | 6 wk | 27 | 25 | 2 |
| 杨澍等[18] | 32 | 32 | 0.5 | 8 wk | 32 | 32 | 2 |
| 林峰等[19] | 20 | 17 | 0.5 | 8 wk | 20 | 17 | 2 |
| 郭翔[20] | 40 | 38 | 0.5 | 12 wk | 22 | 12 | 2 |
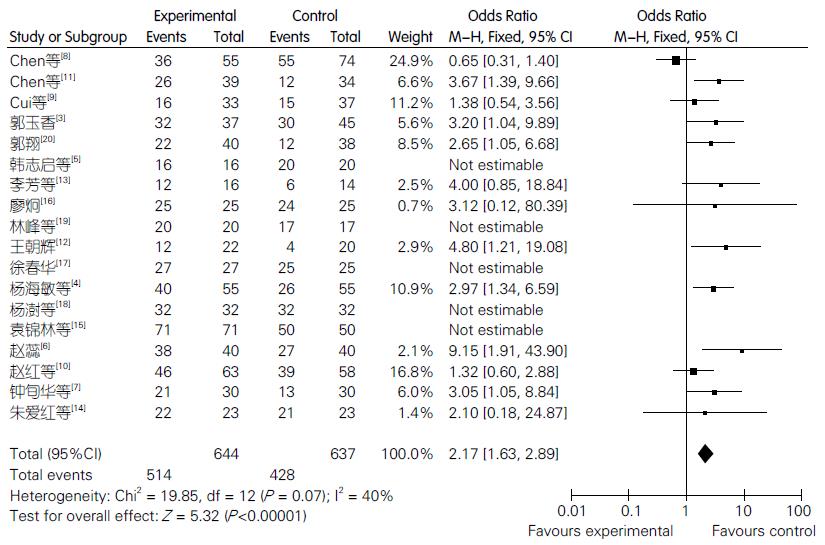
共有18篇文献入选, 其中ETV组共纳入644例, 常规治疗组共纳入637例, χ2检验提示存在同质性(χ2 = 19.85, I2 = 40%, P = 0.07), 效应量的合并采用固定效应模型进行, OR值及95%CI为2.17(95%CI: 1.63-2.89), 提示ETV治疗组的生存率是常规治疗组生存率的2.17倍, 存在统计学差异(Z = 5.32, P<0.00001, 图1).
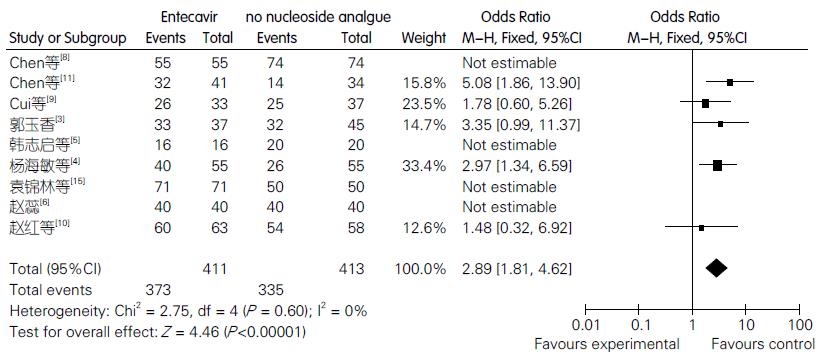
共有9篇文献涉及ETV治疗1 mo(4 wk)后的生存例数, 其中ETV组共纳入411例, 常规治疗组共纳入413例, 经异质性检验后提示存在同质性(χ2 = 2.75, I2 = 0%, P = 0.06), 合并效应后OR值及95%CI为2.89(95%CI: 1.81-4.62), 表明ETV治疗组的1 mo生存率相较于常规治疗组升高, 具有统计学意义(Z = 4.46, P<0.00001, 图2).
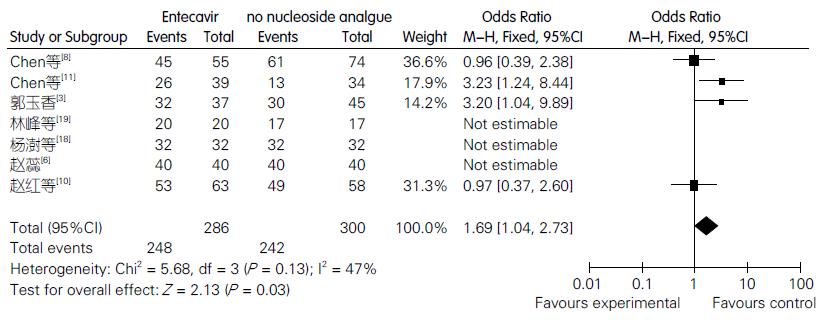
共有7篇文献涉及ETV治疗2 mo(8 wk)后的生存例数, 其中ETV组共纳入286例, 常规治疗组共纳入300例, 异质性检验结果认为存在同质性(χ2 = 5.68, I2 = 47%, P = 0.13), OR值的合并效应量及95%CI为1.69(95%CI: 1.04-2.73), 表明ETV治疗组的2 mo生存率亦高于常规治疗组, 差异具有统计学意义(Z = 2.13, P = 0.03, 图3).
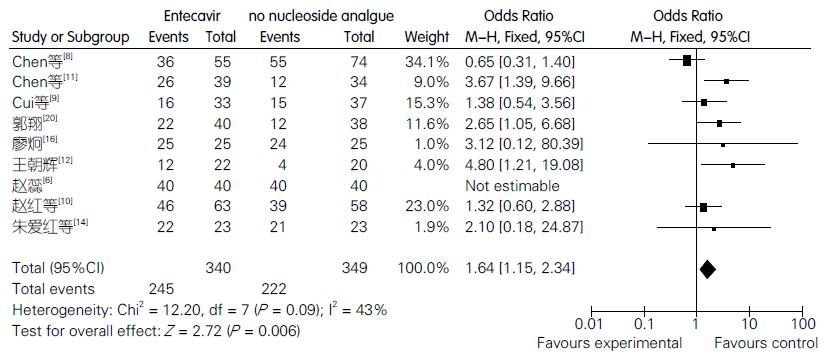
共有9篇文献涉及ETV治疗3 mo(12 wk)后的生存例数, 其中ETV组共纳入340例, 常规治疗组共纳入349例, χ2检验表明存在同质性(χ2 = 12.20, I2 = 43%, P = 0.09), OR值及95%CI为1.64(95%CI: 1.15-2.34), 表明ETV治疗组的3 mo生存率亦明显高于常规治疗组的生存率, 存在统计学差异(Z = 2.72, P = 0.006, 图4).
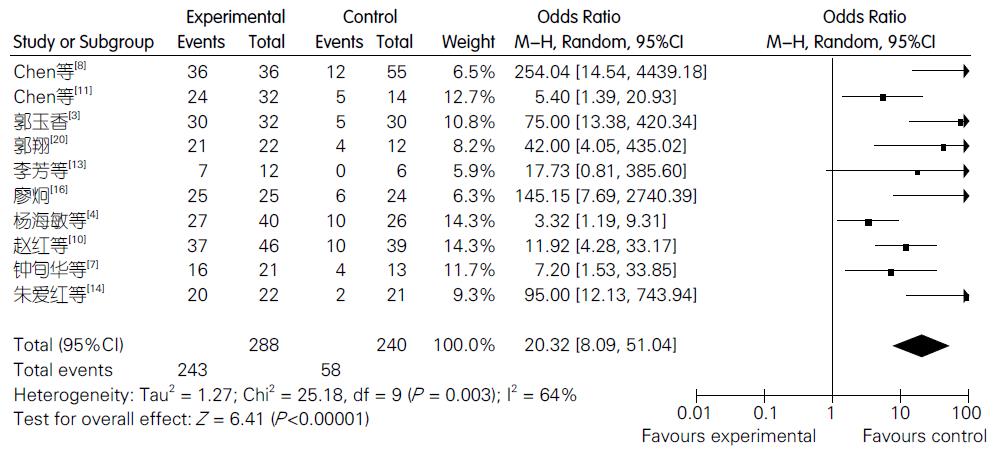
共10篇文献提供了治疗结束时各组HBV-DNA转阴的例数(HBV-DNA<103copy/mL), 其中ETV组共纳入288例, 常规治疗组共纳入240例, 文献的异质性检验结果认为各研究之间存在异质性(χ2 = 25.18, I2 = 64%, P = 0.003), 因此采用随机效应模型, OR值的合并效应量及95%CI为20.32(95%CI: 8.09-51.04), 表明ETV治疗组中患者HBV-DNA转阴率显著高于常规治疗组, 差异具有统计学意义(Z = 6.41, P<0.00001, 图5).
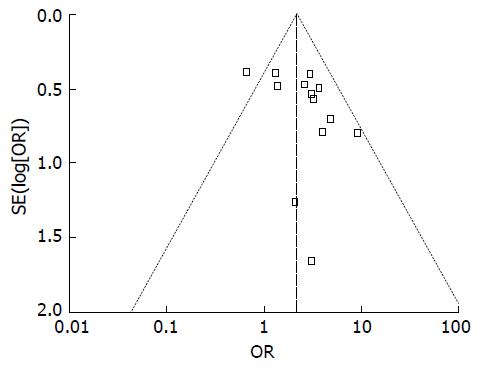
漏斗图分析纳入的研究分布不对称, 提示可能存在较大偏倚(图6). 分别采用固定效应模型和随机效应模型对研究结果进行敏感性分析进一步考察Meta分析的可靠性, 前后两次结论基本一致.
肝衰竭是一组临床症候群, 以凝血机制障碍和黄疸、肝性脑病、肝肾综合征等为主要临床表现. 其病因主要为各种肝炎病毒感染(A、B、C、D)、自身免疫性肝病、酒精性肝病、药物性肝病、Wilson病等, 可以分为急性、亚急性、慢加急性(亚急性)及慢性肝衰竭四型, 其中以慢加急性(亚急性)肝衰竭多见. 相较于欧美国家肝衰竭多因药物(乙酰氨基酚类)及酒精所致, 乙型肝炎病毒感染是我国肝衰竭主要因素, 但HBV相关性肝衰竭的定义目前尚不一致[21]. 发病机制也很复杂, 现认为其发生机制以HBV感染引起的肝细胞免疫病理损伤及T淋巴细胞毒性反应为主[22], HBV的高复制及其蛋白抗原在肝细胞表面的表达, 诱发以细胞毒性T淋巴细胞(cytotoxic T lymphocyte, CTL)和迟发型变态反应性T细胞(T delayed type hypersensitivity cell, TD)为主要效应细胞的细胞免疫反应, 导致大片肝细胞坏死, 是其致病的主要途径之一[23]. HBV的感染是肝功能损害的始动因素, 肝衰竭(重型肝炎) 是肝细胞在肝炎基础上再次受病毒特异的免疫攻击后机内毒素血症直接或间接损害肝细胞所致[24,25]. 抗乙型肝炎病毒治疗能使HBV的复制迅速得到抑制, 血清及肝细胞中的病毒负荷降低, 减轻肝细胞表面靶抗原的表达, 降低细胞毒性T淋巴细胞对感染乙型肝炎病毒的肝细胞的攻击, 避免了反复多次的免疫损伤, 使再生肝细胞免受病毒再感染, 从而减轻肝内炎症活动和坏死程度, 成为乙型肝炎病毒相关性肝衰竭治疗的关键[26].
乙型肝炎病毒相关性肝衰竭的临床治疗现以综合内科治疗为主, 肝移植虽仍被认为是治疗肝衰竭的首选治疗方案, 但是肝源的缺乏以及高昂的治疗费用使得其在临床上的应用受到了极大地限制. 近几年来, 人工肝技术成为肝衰竭患者的重要支持疗法, 但同样受到费用及血源的限制. 这些都促使临床专家去寻求一种新的途径来控制肝衰竭的进展. 抗乙型肝炎病毒药物可以使机体病毒载量降低, 过强的免疫反应得到缓解, 使其成为治疗乙型重型肝炎的一种方法.
ETV是一种有效的、选择性抑制乙型肝炎病毒复制的脱氧鸟嘌呤核苷类似物, 可抑制病毒DNA多聚酶的活性, 作用于病毒逆转录的3个环节: 多聚酶的启动、前基因组逆转录负链的形成、HBV-DNA正链的合成[27], 掺入到HBV-DNA链上, 从而终止DNA链的延伸和病毒的复制. 体内外试验[28,29]均已证明ETV的抗病毒能力强、耐药发生率低, 并且能够减轻慢性乙型肝炎及代偿期肝硬化患者的肝纤维化程度, 改善预后[30], 因此更适合作为重型乙型肝炎或肝硬化患者的优先选择. 目前已有众多文献报道了ETV对HBV相关性肝衰竭的治疗, 但对于其能否改善生存率, 结论不一. 因此, 本研究选择ETV治疗HBV相关性肝衰竭的随机对照试验进行Meta分析, 以期明确ETV对改善乙型肝炎相关性肝衰竭生存率的影响, 为肝衰竭的治疗提供依据.
Meta分析的结果表明, 在常规内科治疗基础上加用ETV治疗HBV相关性肝衰竭后的患者生存率明显高于常规内科治疗组, 差异具有统计学意义(P<0.0001), 其合并效应量OR值及95%CI为2.17(95%CI: 1.63-2.89), 表明ETV的治疗可以改善HBV相关性肝衰竭患者的生存率. 同时, 本Meta分析具体分析了ETV治疗对1 mo(4 wk)、2 mo(8 wk)及3 mo(12 wk)生存率的影响, 发现ETV治疗组的生存率均明显高于常规治疗组, 均具有统计学差异, 其OR值分别为2.89、1.69及1.64. 此外, 针对于HBV-DNA转阴率的分析发现, ETV组HBV-DNA转阴率明显高于常规治疗组, OR值的合并效应量及95%CI为20.32(95%CI: 8.09-51.04), 表明ETV治疗组患者的HBV-DNA转阴率显著高于常规治疗组, 存在统计学差异(Z = 6.41, P<0.00001). 综上可以得出结论, ETV抗病毒治疗能显著提高患者生存率的原因可能在于ETV可以高效迅速抑制HBV复制, 血清及肝组织中的病毒负荷降低, 肝细胞表面靶抗原的表达减轻, 使再生肝细胞免受病毒感染, 减轻肝内炎症活动和坏死程度, 减少死亡率. 因此, ETV应该能够成为除肝移植、人工肝血浆置换术外治疗HBV相关性肝衰竭的主要手段, 并应该推荐在疾病的早期尽早使用, 降低病毒载量, 减轻免疫反应, 挽救患者的生命, 并为肝移植的进行争取时间. 由于Meta分析的客观性和准确性主要依赖于全面而高质量的原始文献的支持, 该Meta分析虽将RCT应用在研究中, 但由于具体盲法的实施、分配方案隐藏、随机方法及失访情况等描述的不全面使得Jadad评分普遍不高, 此外, 本次Meta分析可能存在发表偏倚, 其可能的原因为样本量小的研究方法学质量低下以及阴性结果不易发表导致数据偏差. 因此, 上述结论尚需纳入更多高质量的前瞻性、大样本、多中心的随机对照试验进一步验证.
乙型肝炎病毒感染引起的肝衰竭目前已成为乙型肝炎病人的主要死因之一, 除了内科综合治疗措施, 人工肝治疗以及肝移植等治疗手段外, 新的治疗手段和药物一直是临床关注热点.
白浪, 副教授, 四川大学华西医院感染性疾病中心
通过Meta分析评估恩替卡韦是否能提高乙型肝炎相关性肝衰竭患者的生存率及降低HBV-DNA水平的效果.
抗乙型肝炎病毒药物如拉米夫定、恩替卡韦可以改善乙型肝炎病毒感染相关性的肝衰竭患者的生存率.
通过文献检索纳入18篇文献进行Meta分析,结果表明恩替卡韦的治疗可以改善HBV相关性肝衰竭患者的生存率.
对于指导临床治疗,增强临床应用恩替卡韦抗病毒信心具有重要的指导意义.
本文表明恩替卡韦的治疗可以改善HBV相关性肝衰竭患者的生存率, 对指导临床治疗具有重要意义.
编辑: 田滢 电编: 鲁亚静
| 2. | Jadad AR, Moore RA, Carroll D, Jenkinson C, Reynolds DJ, Gavaghan DJ, McQuay HJ. Assessing the quality of reports of randomized clinical trials: is blinding necessary? Control Clin Trials. 1996;17:1-12. [PubMed] |
| 3. | 郭 玉香. 恩替卡韦治疗慢性重型乙型病毒性肝炎临床观察. 中国慢性病预防与控制. 2008;16:289-290. |
| 8. | Chen J, Han JH, Liu C, Yu RH, Li FZ, Li QF, Gong GZ. Short-term entecavir therapy of chronic severe hepatitis B. Hepatobiliary Pancreat Dis Int. 2009;8:261-266. [PubMed] |
| 9. | Cui YL, Yan F, Wang YB, Song XQ, Liu L, Lei XZ, Zheng MH, Tang H, Feng P. Nucleoside analogue can improve the long-term prognosis of patients with hepatitis B virus infection-associated acute on chronic liver failure. Dig Dis Sci. 2010;55:2373-2380. [PubMed] [DOI] |
| 10. | 赵 红, 王 桂爽, 谢 雯, 闫 杰, 王 艳斌, 程 丹颖, 欧 蔚妮, 冯 亮, 成 军. 恩替卡韦治疗慢性乙型肝炎肝衰竭的疗效观察. 中华实验和临床感染病杂志(电子版). 2011;5:188-194. |
| 11. | Chen T, He Y, Liu X, Yan Z, Wang K, Liu H, Zhang S, Zhao Y. Nucleoside analogues improve the short-term and long-term prognosis of patients with hepatitis B virus-related acute-on-chronic liver failure. Clin Exp Med. 2012;12:159-164. [PubMed] [DOI] |
| 15. | 袁 锦林, 宋 晓敏, 史 建国, 张 雪明. 恩替卡韦治疗慢性重型乙型肝炎71例疗效观察. 苏州大学学报(自然科学版). 2009;29:1205-1206. |
| 21. | Canbay A, Tacke F, Hadem J, Trautwein C, Gerken G, Manns MP. Acute liver failure: a life-threatening disease. Dtsch Arztebl Int. 2011;108:714-720. [PubMed] [DOI] |
| 24. | Leifeld L, Cheng S, Ramakers J, Dumoulin FL, Trautwein C, Sauerbruch T, Spengler U. Imbalanced intrahepatic expression of interleukin 12, interferon gamma, and interleukin 10 in fulminant hepatitis B. Hepatology. 2002;36:1001-1008. [PubMed] |
| 25. | Liu Q. Role of cytokines in the pathophysiology of acute-on-chronic liver failure. Blood Purif. 2009;28:331-341. [PubMed] [DOI] |
| 26. | Villeneuve JP, Condreay LD, Willems B, Pomier-Layrargues G, Fenyves D, Bilodeau M, Leduc R, Peltekian K, Wong F, Margulies M. Lamivudine treatment for decompensated cirrhosis resulting from chronic hepatitis B. Hepatology. 2000;31:207-210. [PubMed] |
| 27. | Seifer M, Hamatake RK, Colonno RJ, Standring DN. In vitro inhibition of hepadnavirus polymerases by the triphosphates of BMS-200475 and lobucavir. Antimicrob Agents Chemother. 1998;42:3200-3208. [PubMed] |
| 30. | Schiff E, Simsek H, Lee WM, Chao YC, Sette H, Janssen HL, Han SH, Goodman Z, Yang J, Brett-Smith H. Efficacy and safety of entecavir in patients with chronic hepatitis B and advanced hepatic fibrosis or cirrhosis. Am J Gastroenterol. 2008;103:2776-2783. [PubMed] [DOI] |