修回日期: 2013-06-24
接受日期: 2013-07-03
在线出版日期: 2013-07-28
血管活性肠肽瘤(vasoactive-intestinal polypeptide-secreting tumors, VIPomas)是罕见的胰腺内分泌肿瘤. 临床上以大量水样腹泻, 顽固性低血钾, 胃酸缺乏为主要特征性表现. 此病非常罕见, 临床上较易误诊. 本文报道血管活性肠肽瘤1例, 通过病史及实验室、影像学、内镜学、组织学检查结合相关文献进行分析讨论, 提高对该病的认识.
核心提示: 本文报道血管活性肠肽瘤1例, 通过病史及实验室、影像学、内镜学、组织学检查结合相关文献进行分析讨论, 提高对该病的认识.
引文著录: 张丽平, 吴会超, 罗兰. 血管活性肠肽瘤1例. 世界华人消化杂志 2013; 21(21): 2117-2120
Revised: June 24, 2013
Accepted: July 3, 2013
Published online: July 28, 2013
Vasoactive intestinal polypeptide-secreting tumor (VIPoma) of the pancreas is a rare type of pancreatic endocrine neoplasm. The main clinical features of VIPoma include large amount of watery diarrhea, hypokalemia and achlorhydria. Due to extreme rarity of this disease, it is easily misdiagnosed. Here we report such a case to raise the awareness of this clinical entity. We also performed a review of the literature to summarize its clinical manifestations, diagnosis and treatment.
- Citation: Zhang LP, Wu HC, Luo L. Pancreatic vasoactive intestinal polypeptide-secreting tumor: A case reporty. Shijie Huaren Xiaohua Zazhi 2013; 21(21): 2117-2120
- URL: https://www.wjgnet.com/1009-3079/full/v21/i21/2117.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v21.i21.2117
血管活性肠肽瘤(vasoactive-intestinal polypeptide-secreting tumors, VIPomas)是一组定义明确的罕见的胰腺内分泌肿瘤, 该病每年的发病率为千万分之一. 平均发病年龄为49岁. 该病也称为胰性霍乱、Verner-Morrison综合征, 其典型临床表现是水样腹泻、低钾血症、低/无胃酸,因此也称为WHDA综合症[Watery (secretory) diarrhea, hypokalemia, and achlorhydria]. 下面就本院收治的1例VIPoma患者做简要的诊断分析, 旨在提高临床医生对该病的认识.
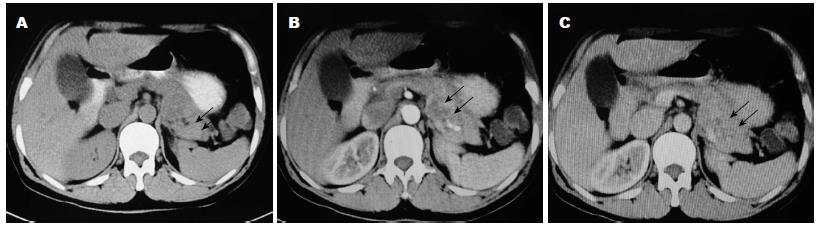
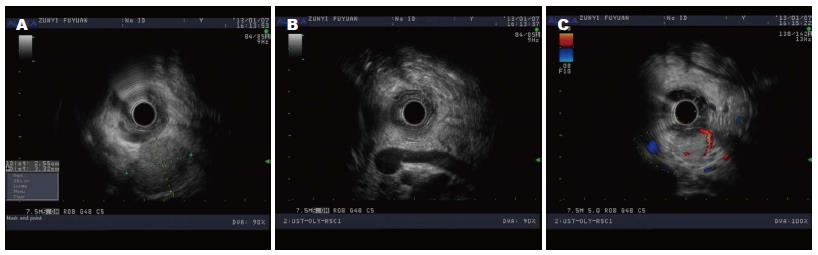
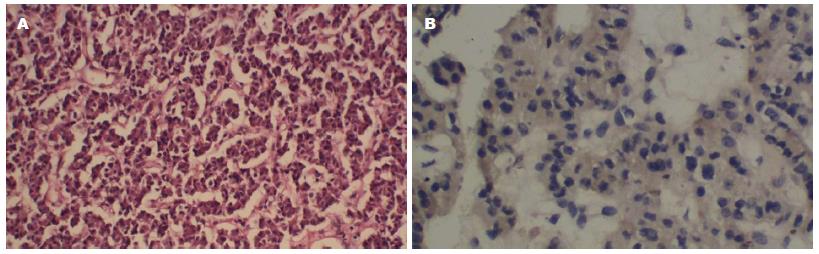
本院病例资料, 48岁女性患者, 因"反复腹泻2年"入院, 2年来无明显诱因出现腹泻, 黄稀便, 2-3次/d, 量少, 无腹痛腹胀, 无恶心呕吐, 有自愈倾向, 无关节疼痛. 于多家医院以"慢性胃肠炎"对症治疗可好转, 期间病情间断发作. 2012-12-30上述症状再发加重, 腹泻次数增至10次/d, 黄稀便, 无黏液脓血便, 伴纳差, 恶心呕吐, 反酸、嗳气、乏力. 无皮肤潮红、瘙痒, 无腰背部疼痛, 无呕血, 黑便, 无胸闷胸痛, 对症治疗无明显好转, 后以"慢性结直肠炎、慢性胃炎"收入我院消化科. 患者精神, 饮食, 睡眠欠佳. 自发病起体重减轻5 kg, 小便正常. 否认"肝炎, 结核, 伤寒"等传染疾病史, 否认"高血压, 糖尿病, 高血脂"等病史. 查体: 全身皮肤黏膜干燥, 口唇脱皮. 腹软, 无压痛, 反跳痛及肌紧张, 肝脾未触及, 未扪及包块, 肠鸣音正常. 实验室检查: 血常规: WBC 10.27×109/L, RBC 4.34×1012/L, HGB 137 g/L, PLT 344×109. 电解质: 钾2.23 mmol/L, 磷0.77 mmol/L, 血糖7.34 mmol/L; 肝肾功能未见异常. 每日监测电解质: 钾2.28-4.16 mmol/L(3.5-5.5 mmol/L)之间, 磷0.38-1.18 mmol/L(0.84-1.82 mmol/L)之间. 复查空腹及餐后血糖分别为: 4.42 mmol/L(3.89-6.11 mmol/L)和7.00 mmol/L(3.89-7.8 mmol/L). CA199、CEA、NSE、AFP、CA125均在正常范围. 游离三碘甲状腺原氨酸、游离甲状腺素、促甲状腺激素正常. 大便常规+潜血, 大便细菌培养阴性. 全段甲状旁腺激素8.5 pmol/L(0.7-8.5 pmol/L), 昼夜皮质醇, 醛固酮, 人生长激素, 泌乳素L均未见异常. 24 h尿微量白蛋白: 6 mg/24 h. 放免法测得腹泻时查血浆血管活性肠肽: 260.6 pg/mL, 腹泻间歇期35.625 pg/mL(正常2.0-36.8 pg/mL). 影像学检查: 胸部平片、腹部彩超未见异常. 上腹CT平扫+增强(图1): 肝左外叶侧段见约30 mm×27 mm稍低密度影, 增强扫描动脉期未见强化, 静脉期边缘结节状强化, 余肝内见多个小类圆形无强化低密度区. 胰尾后部见一大小约27 mm×31 mm密度不均肿块, 增强扫描不均匀强化. 意见: (1)肝左叶外侧段血管瘤, 肝内多发小囊肿; (2)胰尾肿瘤(胃泌素瘤?); (3)双侧少量胸腔积液. 心电图提示ST-T改变. 心脏彩超: 左房左室饱满; 二尖瓣, 三尖瓣轻度返流, 心包微量积液, 左心室功能正常, 心包积液. 内镜学表现: 胃镜: 慢性浅表性胃炎. 肠镜: 所见回肠末端、结直肠黏膜未见明显器质性病变. 超声内镜(endoscopic ultrasound, EUS)(图2): 胰腺尾部可见2.55 cm×3.32 cm类圆形低回声区, 边界清楚, 内部回声均匀. 胰腺头体部未见异常, 胰管不扩张. 血管分布走向清晰, CDFI低回声区内可见条点状血流信号. 治疗: 入院后予常规蒙脱石散、复方消化酶等止泻药物、纠正低钾血症等对症治疗, 仍出现顽固性低钾不能纠正, 结合CT及EUS结果, 顽固性低钾考虑血管活性肠肽瘤可能性大. 予生长抑素类似物奥曲肽0.1 mg皮下注射Q 12 h试验性治疗, 腹泻停止, 血钾纠正. 停用奥曲肽2 d后, 再次出现腹泻, 3次/d, 为水样便. 待患者低钾纠正后, 2013-01-28于我院行胰尾切除+脾切除术+肝左外叶血管瘤切除术, 术中胰体尾部可触及一包块, 直径约5 cm, 活动, 与周围组织无粘连. 术后患者即停止腹泻, 查电解质未见异常. 术后第3天查血浆血管活性肠131.7 pg/mL. 病理结果(图3A): (1)肝海绵状血管瘤; (2)脾脏呈淤血性改变, 部分区域被膜下淋巴管扩张; (3)胰腺高分化内分泌肿瘤>2 cm, 行为不确定性高分化内分泌肿瘤. 免疫组织化学CD10(-), CD56(弱+), CK7(-), CK8(+), CgA(个别+), NSE(+); Syn(+), VIP(++)(图3B). 术后患者即停止腹泻, 查电解质未见异常. 术后第3天查血浆血管活性肠131.7 pg/mL. 随诊: 术后2 mo因多浆膜腔(心包, 胸腔, 腹腔)积液再次就诊于我院, 查白蛋白33.3 g/L, 血钾4.16 mmol/L. 复查胸部CT及腹部CT平扫+增强可见多浆膜腔积液, 未见转移病灶. ECT未见骨转移, 多浆膜腔积液原因考虑术后低蛋白血症所致.
第1例VIPoma是1958年由Verner和Morrison首次报道的, 迄今全世界已报道有800多例[1]. 血管活性肠肽(vasoactive-intestinal polypeptide, VIP)可促进胰液、小肠液的产生和分泌, 大量VIP分泌解释了水样腹泻, 脱水, 低血钾, 酸中毒等症状. VIP亦可抑制胃酸分泌, 致低/无胃酸. 刺激肝糖原的释放, 导致血糖增高; 舒张外周血管, 致血压降低, 脸色潮红. 部分患者出现高血钙, 低磷血症与VIP促进甲状旁腺激素分泌有关[2].
VIPoma术前较难诊断, 易与导致腹泻的全身性、炎症性及器质性疾病混淆, 本院该患者即以肠炎治疗2年之久, 但入院后查甲状腺功能, 血糖, 胃肠镜、腹部CT及大便培养、血清CEA、CA125等实验室检查已予排斥. 根据该病的典型临床表现结合放免法测血浆VIP是术前最重要的定性依据, 腹泻时超过正常值上限2倍即可诊断, 但因VIP为非持续性分泌, 因此需多点多次检测. 本院该患腹泻时测得血管活性肠肽260.6 pg/mL(可能与腹泻不严重有关), 但仍高于腹泻间隙35.625 pg/mL. 术后第3天血管活性肠肽131.7 pg/mL, 已缓慢下降. 血浆VIP也是评价术后是否复发、手术是否彻底的重要指标. 术后病理学及免疫组织化学也是另一重要的定性方法, 并且现今在病理学的基础上对评价内分泌肿瘤的性质及预后有了重要发展. 使用免疫组织化学KIT/CK19进行危险度分级, 低度危险(KIT-/CK19-), 中度危险(KIT+/CK19-), 高度危险(KIT+/CK19+). Zhang等[3]对于97例有完整资料的胰腺内分泌肿瘤进行病理形态学和临床结果分析; 高度危险组中肿瘤的大小, 核分裂像, 肿瘤性坏死和肿瘤边缘情况等参数均高于低度危险组. 该作者提出了新的3级分级系统(1级: 0和1分、2级2分、3级3和4分)评价胰腺内分泌肿瘤, 根据核分裂像(0分: 0/50 HPE、1分1-3个/50 HPE、>4个/50 HPE)、肿瘤性坏死(0分: 无坏死、1分: 有坏死)、肿瘤边缘浸润(0分: 无浸润、1分: 有浸润). 结合KIT/CK19免疫组织化学结果, 能更好地评价胰腺内分泌肿瘤的性质. 不过遗憾的是, 本患者的病理学检查没有进一步的描述.
B超和CT是VIPoma术前定位的主要方法, 大部分胰腺内分泌肿瘤是高度富血管性的, 主要位于胰尾部, 与正常组织分界清, 增强CT扫描强化明显, 少数为少血管性; 而胰腺癌是少血管性肿瘤, CT增强扫描密度增加不明显, 因此CT对于两者的鉴别有重要价值. 同时CT还可了解肿块的大小, 数量, 及周围组织浸润, 远处转移及淋巴结侵犯等情况. B超对于<2 cm的胰腺占位诊断不明, 该患者行B超检查即未发现胰尾部占位, 可能与肠腔气体干扰有关. EUS对于诊断<2.5 cm的内分泌肿瘤的敏感性为82%, 发现最小的病变为2 mm, 是目前定位诊断最有效的手段[4]. 生长抑素闪烁成像依赖于生长激素受体表达, 80%-90%该受体表达阳性, 因此在大部分患者中有效.
外科手术切除是治疗本病的根本方法. 生长抑素类似物(奥曲肽)是缓解症状的最有效手段, 且对于发生远处转移的患者, 也可减小肿块体积, 改善体内激素水平和症状. 生长抑素类似物也用于术前诊断及术前准备, 但长久应用将会导致耐药性产生. 干扰素-α、糖皮质激素也可改善治疗效果.
虽然VIPoma的主要治疗方式是外科手术, 但该病误诊率极高, 该患者从出现症状到明确诊断长达2年. 因此, 临床医生在碰到难治性, 反复发作性腹泻, 伴有顽固性低钾血症, 糖耐量异常的患者应警惕该病, 早期诊断可明显提高该病的生存率与预后.
血管活性肠肽瘤(vasoactive-intestinal polypeptide-secreting tumor, VIPoma)是一种临床上罕见的疾病, 发病率低, 大量水样腹泻、低血钾、低/无胃酸综合征为其典型表现, 极易误诊.
肖文华, 主任医师, 中国人民解放军总医院第一附属医院肿瘤科
VIPoma在全世界已报道800多例, 人群中发病率为千万分之一, 病变主要位于胰尾部, 50%-60%的患者发现时已转移, 最常见转移至肝脏.
对于禁食72 h腹泻仍不能缓解的大量水样腹泻, 难治性低钾血症, 糖耐量异常的患者应高度怀疑该病, 同时结合血浆血管活性肠肽(vasoactive -intestinal polypeptide, VIP)水平, 影像学、内镜检查明确诊断, 并予以手术治疗, 可降低误诊率.
该病例也叫胰腺内分泌肿瘤, 发病率较低, 其临床表现较特殊, 应该引起临床医师, 特别是消化科大夫的高度重视.
| 1. | Peng SY, Li JT, Liu YB, Fang HQ, Wu YL, Peng CH, Wang XB, Qian HR. Diagnosis and treatment of VIPoma in China: (case report and 31 cases review) diagnosis and treatment of VIPoma. Pancreas. 2004;28:93-97. [PubMed] [DOI] |
| 2. | Ghaferi AA, Chojnacki KA, Long WD, Cameron JL, Yeo CJ. Pancreatic VIPomas: subject review and one institutional experience. J Gastrointest Surg. 2008;12:382-393. [PubMed] [DOI] |
| 3. | Zhang L, Lohse CM, Dao LN, Smyrk TC. Proposed histopathologic grading system derived from a study of KIT and CK19 expression in pancreatic endocrine neoplasm. Hum Pathol. 2011;42:324-331. [PubMed] [DOI] |
| 4. | Rösch T, Lightdale CJ, Botet JF, Boyce GA, Sivak MV, Yasuda K, Heyder N, Palazzo L, Dancygier H, Schusdziarra V. Localization of pancreatic endocrine tumors by endoscopic ultrasonography. N Engl J Med. 1992;326:1721-1726. [PubMed] [DOI] |