修回日期: 2011-12-30
接受日期: 2012-02-27
在线出版日期: 2012-03-28
目的: 比较不同的肝血流阻断方法在肝切除术中应用的有效性及安全性.
方法: 回顾性分析我院2004-2009年117例行肝切除术的肝癌患者的相关资料. A组: 自制肝断面血流阻断器局部血流控制(n = 42); B组: 解剖性半肝血流阻断(n = 35); C组: 第一肝门阻断(Pringle法, n = 40). 比较3组患者术中出血量和手术时间、术后肝功能的恢复以及术后并发症的发生率.
结果: 术中出血量和手术时间A组均明显少于B(P = 0.026, P<0.001)、C(P<0.001, P<0.001)组. A组术后第3、7天肝功能(TB、ALT)的明显好于C组(TB: P = 0.014, = 0.009; ALT: P<0.001, P<0.001). C组术后有29例出现不同程度的腹水, 术后腹水发生率显著高于A组(P<0.001); 2例发生肝功能衰竭, 1例出现胃肠道出血, 死亡1例.
结论: 肝切除术中采用肝断面血流阻断器能有效控制出血、缩短手术时间, 对肝功能影响小, 是一种简便、安全有效的方法.
引文著录: 周松, 薛小军, 李冉冉, 陈达丰, 陈文有, 刘广欣, 柯恩明, 郑硕云. 肝断面血流阻断器在肝癌切除术中的应用. 世界华人消化杂志 2012; 20(9): 790-794
Revised: December 30, 2011
Accepted: February 27, 2012
Published online: March 28, 2012
AIM: To compare a new tool named hepatic blood blocker versus the Pringle maneuver and hemihepatic vascular exclusion in controlling bleeding during hepatectomy for liver cancer.
METHODS: The clinical data for 117 patients who underwent hepatectomy for liver cancer from 2004 to 2009 were analyzed retrospectively. Of these patients, 42 underwent local hepatic blood occlusion with hepatic blood blocker (group A), 35 underwent hemihepatic vascular exclusion (group B), and 40 underwent the Pringle maneuver (group C). The blood loss, operative time, postoperative hepatic function and complications were compared among each group.
RESULTS: The average blood loss and operative time were significantly less in group A than in groups B (P < 0.05, 0.001) and C (both P < 0.001). Significant differences were seen between group A and group C in serum total bilirubin (TB) and alanine transaminase (ALT) on postoperative days 3 and day 7, and group A showed better hepatic function (TB: P = 0.014, 0.009; ALT: both P < 0.001). The Pringle maneuver significantly increased the rate of postoperative abdominal dropsy when compared to group A (P < 0.001). In group C, two patients suffered from liver failure, one suffered from alimentary tract hemorrhage and one died.
CONCLUSION: Using hepatic blood blocker during hepatectomy could effectively control bleeding, reduce operative time and preserve hepatic function, representing a safe and feasible technique.
- Citation: Zhou S, Xue XJ, Li RR, Chen DF, Chen WY, Liu GX, Ke EM, Zheng SY. Application of hepatic blood blocker to control bleeding during hepatectomy. Shijie Huaren Xiaohua Zazhi 2012; 20(9): 790-794
- URL: https://www.wjgnet.com/1009-3079/full/v20/i9/790.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i9.790
如何控制术中出血一直是肝脏手术中的关键问题, 出血量的多少和血流阻断引起的肝脏缺血再灌注损伤是影响术后肝功能的重要因素[1], 直接关系到患者的预后. 在以下的研究中, 我们采用自制的肝断面血流阻断器控制术中出血. 该研究回顾性地分析了我院近年收治的117例原发性肝癌患者的病例资料, 其中采用肝断面血流阻断器行局部血流控制实施肝切除术42例、半肝血流阻断法肝切除术35例、Pringle法肝切除术40例, 现分析报道如下.
2004-03/2009-06我院因原发性肝癌行肝切除手术患者117人, 其中用自制肝断面血流阻断器法(A组)42例, 男32例, 女10例, 年龄12-76岁(平均51.3岁); 病灶长径3-20cm(平均8.2 cm); 肝功能Child分级A级32例, B级10例. 半肝血流阻断法(B组)35例, 男28例, 女性7例, 年龄18-74岁(平均52.1岁); 病灶长径4-22 cm(平均7.9 cm); 肝功能Child分级A级30例, B级5例. Pringle法(C组)40例, 男31例, 女性9例, 年龄20-75岁(平均50.8岁); 病灶长径4-20cm(平均7.8 cm); 肝功能Child分级A级30例, B级10例. 3组患者术前外周血白蛋白(albumin, A)、总胆红素(total bilirubin, TB)、谷丙转氨酶(alanine aminotransferase, ALT)、肝功能Child分级、手术范围均无显著差异(P = 0.143, 0.630, 0.068, 0.047). 术后病理学检查均为原发性肝细胞癌或胆管细胞癌.
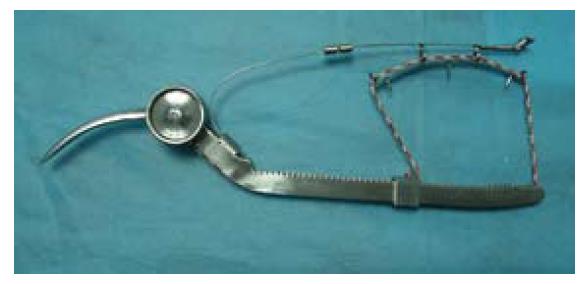
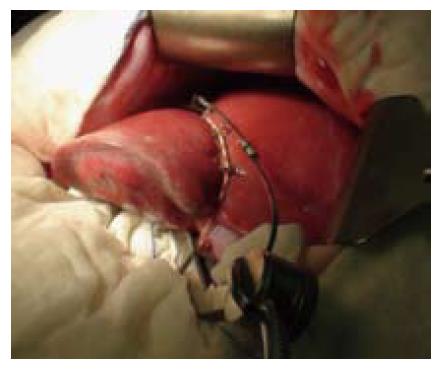
1.2.1 治疗: 自制肝断面血流阻断器组: 根据病灶所在部位, 按"无瘤术"原则距病灶≥2 cm用电刀在肝表面作切线标记, 于预定切线近侧2-3 cm用自制肝断面血流阻断器(图1, 2)收紧行局部肝血流控制, 随后用钳夹法断肝[2]. 半肝血流阻断法组: 根据病变部位解剖出供应左半肝或右半肝的肝动脉、门静脉分支, 预置半肝血流阻断带, 游离病侧半肝后收紧半肝血流阻断带, 结合肝面缺血线和肿瘤部位用电刀在肝表面作切线标记, 钳夹法断肝. Pringle法组: 游离肝脏并游离第一肝门预先放置阻断带, 明确癌灶位置及拟切除方式, 进行肝切除的同时进行第一肝门的血流阻断, 切除过程中每15-20 min开放一次, 每次约5 min, 以减少肝脏的热缺血损伤.
1.2.2 肝功能检测: 所有患者在术前、术后3 d和术后7 d分别测定外周A、TB和ALT.
统计学处理 计量资料以mean±SD表示, 术前A、TB、ALT水平采用单因素方差分析法检验; 术后A、TB、ALT水平采用Nemenyi检验; 肝功能Child分级差异采用Kruskal-Wallis H检验, 检验水准a = 0.05; 术后并发症发生率采用χ2检验, 检验水准经校正后a' = 0.0125, 用SPSS13.0软件进行统计学分析.
所有患者肿瘤均完整切除, 无手术死亡, 手术切除范围组间差异无统计学意义(P = 0.620, 表1). 术中出血量和手术时间A组均明显少于B组(P = 0.026, P<0.001)、C组(P<0.001, P<0.001; 表2), 差异有统计学意义. A、B两组的术后肝功能以及胸水、腹水、胃肠道出血、肝功能衰竭等并发症的发生率均无显著差异(P>0.05; 表2, 表3). C组术后第3、7天血TB、ALT水平与A组相比较高, 差异有统计学意义(TB: P = 0.014, = 0.009; ALT: P<0.001, <0.001; 表2). C组术后有29例出现不同程度的腹水, 术后腹水发生率显著高于A组(72.5% vs 33.3%, P = 0.001; 表3); C组中有2例发生肝功能衰竭, 1例出现胃肠道出血, 死亡1例.
| 分组(n) | mean±SD(95%CI) | Value | P值 | ||
| A(42) | B(35) | C(40) | |||
| A(g/L) | 34.87±4.15(33.58, 36.16) | 35.96±4.60(34.38,37.54) | 36.90±5.10(35.26,38.53) | 1.977 | 0.143 |
| TB(μmol/L) | 14.27±3.61(13.14,15.39) | 13.44±4.22(11.99,14.48) | 13.80±3.59(12.65,14.95) | 0.464 | 0.630 |
| ALT(U/L) | 35.98±6.00(34.11,37.85) | 36.53±7.00(34.13,38.93) | 33.43±5.69(31.61,35.25) | 2.748 | 0.068 |
| 肝功能(Child A/B/C) | 32/10/0 | 30/5/0 | 30/10/0 | 1.508 | 0.470 |
| 切除范围(n) | 2.671 | 0.620 | |||
| 肝单段切除 | 7 | 5 | 5 | ||
| 联合肝段切除 | 25 | 20 | 27 | ||
| 半肝切除 | 10 | 10 | 8 | ||
| 分组(n) | mean±SD(95%CI) | P值 | |||
| A(42) | B(35) | C(40) | A vs B | A vs C | |
| 出血量(mL) | 532.86±77.34 (508.76, 556.96) | 638.00±160.05(583.02, 692.98) | 1121.25±265.33(1036.39, 1206.11) | 0.026 | <0.001 |
| 手术时间(min) | 175.62±25.56 (167.65, 183.59) | 210.60±31.73(190.70, 212.50) | 210.82±31.18 (200.85, 220.80) | <0.001 | <0.001 |
| A(g/L) | |||||
| 术后第3天 | 31.11±4.02 (29.83, 32.37) | 30.43±3.43 (29.26, 31.61) | 31.75±3.92(30.40, 33.10) | 0.672 | 0.069 |
| 术后第7天 | 30.65±4.03 (29.39, 31.70) | 29.45±3.62 (28.21, 30.60) | 29.34±3.94(28.08, 30.60) | 0.307 | 0.227 |
| TB(μmol/L) | |||||
| 术后第3天 | 30.91±6.14 (29.00, 32.83) | 32.63±5.99 (30.58, 34.69) | 36.20±12.45(32.22, 40.18) | 0.605 | 0.014 |
| 术后第7天 | 20.84±6.20 (18.96, 22.71) | 23.76±7.23 (21.28, 26.25) | 25.00±6.32(22.98, 27.03) | 0.094 | 0.009 |
| ALT(U/L) | |||||
| 术后第3天 | 159.53±10.30 (156.32, 162.74) | 164.75±18.11(158.53, 170.97) | 236.88±44.32(223.94, 249.82) | 0.599 | <0.001 |
| 术后第7天 | 50.10±5.84 (48.28, 51.92) | 53.14±6.90 (50.77, 55.51) | 72.91±11.89(69.11, 76.71) | 0.221 | <0.001 |
| 分组(n) | n(%) | P值 | |||
| A(42) | B(35) | C(40) | A vs B | A vs C | |
| 胸腔积液 | 5(11.9) | 4(11.4) | 5(12.5) | 1.000 | 1.000 |
| 腹腔积液 | 14(33.3) | 13(37.1) | 29(72.5) | 0.913 | 0.001 |
| 消化系出血 | 0 | 0 | 1(2.5) | 0.980 | |
| 肝功能衰竭 | 0 | 0 | 2(5.0) | 0.453 | |
| 死亡 | 0 | 0 | 1(2.5) | 0.980 | |
肝脏是双血供器官, 每分钟大约有1 500 mL血液流经肝脏. 肝切除术中, 如何控制出血是首要问题. 良好的血流阻断, 不仅能减少出血, 易于手术的操作, 更能减少术后并发症, 利于患者恢复, 降低病死率[3,4]. 一百多年前, Pringle[5]提出阻断第一肝门处的肝动脉、门静脉血流可以明显减少肝切除术中的出血, 采用间断阻断法可以满足长时间手术的要求. 但是也存在一些不足, 如间歇期出血; 只阻断了入肝血流, 肝静脉回流出血无法控制; 由于抑制了肝脏的血供, 对肝功能影响较大[6,7], 增加了肝功能异常特别是肝硬化患者术后肝衰竭的风险; 对经门静脉回流血液的腹腔器官功能也有不同程度的影响[8,9], 同时对全身血流动力学也有较明显的影响[10]. 但因其操作简单、实用, 除肝门区肿瘤外, 几乎可用于各种类型的肝切除术, 所以至今仍被临床广泛使用.
我国是肝炎高发区, 肝癌患者大多合并有不同程度的肝硬化, 限制了Pringle法的应用. 半肝血流阻断法不仅能达到和Pringle相同的阻断效果, 同时不影响残肝血供, 减轻了肝功能损害, 更适合于合并有肝功能异常的患者[11,12], 同时由于保证了胃肠道血液的回流, 保护肠屏障功能[13]. 但肝硬化患者肝门部有大量曲张的侧支血管, 肝门部解剖时出血较多, 而且费时, 需要较高的技术水平.
在A组病例中, 我们采用自制的肝断面血流阻断器阻断预切除区的血供, 手术时, 充分游离需切除的肝脏, 自肝脏脏面、下腔静脉旁放置阻断器底座, 然后从肝脏上方及膈面(于预定切线近侧2-3 cm)将软绳固定于底座上的绳卡上, 收紧软绳, 使阻断器与肝包膜完全贴附, 范围从一个肝段到左右半肝都可采用. 由于采用了软绳和可滑动的绳卡, 软绳收紧后能与肝脏表面充分接触, 能适应肝脏形态的变化, 不易滑脱, 即使肝实质较厚本法局部血流控制的效果也较确切.
从理论上讲, 局部血流控制是一种最理想的肝血流控制方法, 其优点如下: (1)血流阻断彻底, 采用肝血流阻断器可完全阻断了肝断面来自于肝动脉、门静脉、肝静脉的血流, 术中出血明显减少, 同时可避免因术中挤压导致的肿瘤肝内播散和远处转移, 更加符合无瘤术的原则; (2)由于只对需要切除的组织进行阻断, 可持续阻断, 断肝时不受时间限制, 由于操作简单、术野清晰, 总的手术时间反而缩短, 减轻了手术创伤; (3)选择性高, 能选择性阻断拟被切除的肝叶(段), 对肝功能影响小, 不影响胰腺、胃肠道等器官的血液回流, 患者术后并发症少、恢复快[14,15]; (4)由于阻断范围相对较小, 对全身血流动力学无明显影响.
通过对照分析可以看出, 与Pringle法和半肝血流阻断法相比, 采用肝断面血流阻断器进行局部血流阻断具有器械固定牢固、操作简单、血流阻断彻底、最大限度保护肝功能、对全身血流动力学小等优点, 是一种控制出血的有效简便的方法, 除不适合紧邻第二、三肝门的肿瘤及合并肝静脉和下腔静脉癌栓的肝肿瘤等高难度肿瘤的切除外, 可满足绝大多数肝切除术, 对肝功能异常甚至肝硬化患者也适用. 然而肝癌的治疗包括严格掌握手术适应证, 充分术前准备, 认真仔细的手术操作, 术后密切观察病情及时有效的支持治疗, 血流阻断只是辅助手术操作的手段, 其具体方法的选择要综合考虑患者肝功能、术前影像学检查结果及术中探查的具体情况.
肝血流阻断方法众多, 各有优缺点, 如技术要求高、使用器械昂贵、血流阻断不彻底等. 本研究采用自制的肝断面血流阻断器实施局部血流阻断, 目的是尽可能减少对正常肝组织的副损伤, 最大限度地保护肝功能.
施晓雷, 副主任医师, 南京大学医学院附属鼓楼医院
目前对肝脏血流阻断引起的肝脏缺血再灌注损伤、门静脉系统脏器功能改变及预缺血处理对肝功能的保护作用机制研究较多, 如何既能有效控制出血又能最大限度地保护肝功能, 是肝脏血流阻断技术要同时兼顾又相互冲突的两个方面.
该研究在肝切除术中使用肝血流阻断器行肝脏血流阻断, 这是一个自制的手术器械, 能对拟切除的肝组织施行全血阻断, 效果良好.
肝断面血流阻断器在临床实际应用中有良好的血流阻断效果, 并在多家医院的使用中受到一致的好评; 由于其使用简便, 且可反复使用、价格便宜, 对经济状况不佳的患者是良好的选择.
肝断面血流阻断器: 是在"L"形的底座上套装一个绳卡, 绳卡可自由滑动, 与底座对应的弹片上有固定软绳的金属环, 软绳经底座的引导槽自末端引出, 通过金属环固定于绳卡. 通过转动摇柄可收紧软绳, 实施血流阻断.
本研究采用自制的肝断面血流阻断器能达到控制局部血流, 减少术中出血, 缩短手术时间, 减少肝脏损伤, 减少术后系列并发症, 在肝切除应用中具有良好价值.
编辑: 李军亮 电编: 闫晋利
| 3. | Dixon E, Vollmer CM, Bathe OF, Sutherland F. Vascular occlusion to decrease blood loss during hepatic resection. Am J Surg. 2005;190:75-86. [PubMed] [DOI] |
| 4. | Batignani G, Zuckermann M. Inferior approach for the isolation of the left-middle hepatic veins in liver resections: a safe way. Arch Surg. 2005;140:968-971. [PubMed] [DOI] |
| 5. | Pringle JH. V. Notes on the Arrest of Hepatic Hemorrhage Due to Trauma. Ann Surg. 1908;48:541-549. [PubMed] [DOI] |
| 6. | Brooks AJ, Hammond JS, Girling K, Beckingham IJ. The effect of hepatic vascular inflow occlusion on liver tissue pH, carbon dioxide, and oxygen partial pressures: defining the optimal clamp/release regime for intermittent portal clamping. J Surg Res. 2007;141:247-251. [PubMed] [DOI] |
| 7. | Pietsch UC, Herrmann ML, Uhlmann D, Busch T, Hokema F, Kaisers UX, Schaffranietz L. Blood lactate and pyruvate levels in the perioperative period of liver resection with Pringle maneuver. Clin Hemorheol Microcirc. 2010;44:269-281. [PubMed] |
| 8. | Ypsilantis P, Lambropoulou M, Grapsa A, Tentes I, Tsigalou C, Panopoulou M, Simopoulos C. Pringle maneuver deteriorates gut barrier dysfunction induced by extended-liver radiofrequency ablation. Dig Dis Sci. 2011;56:1548-1556. [PubMed] [DOI] |
| 9. | Unalp OV, Aydin U, Yazici P, Nart D, Yenisey C, Kavak T, Zeytunlu M, Coker A. The effects of the Pringle maneuver on the pancreas: can octreotide be protective? JOP. 2009;10:284-291. [PubMed] |
| 10. | Furka A, Nemeth N, Gulyas A, Brath E, Peto K, Takacs IE, Furka I, Sapy P, Miko I. Hemorheological changes caused by intermittent Pringle (Baron) maneuver in beagle canine model. Clin Hemorheol Microcirc. 2008;40:177-189. [PubMed] |
| 12. | Nakazawa T, Ohara H, Ando T, Hayashi K, Naitoh I, Okumura F, Tanaka H, Sano H, Joh T. Clinical course and indications for steroid therapy of sclerosing cholangitis associated with autoimmune pancreatitis. Hepatogastroenterology. 2009;56:584-588. [PubMed] |
| 14. | Moug SJ, Smith D, Leen E, Angerson WJ, Horgan PG. Selective continuous vascular occlusion and perioperative fluid restriction in partial hepatectomy. Outcomes in 101 consecutive patients. Eur J Surg Oncol. 2007;33:1036-1041. [PubMed] [DOI] |