修回日期: 2011-11-30
接受日期: 2011-12-23
在线出版日期: 2012-01-08
目的: 评价双歧三联活菌对三硝基苯磺酸钠(TNBS)诱导的大鼠结肠炎的疗效, 并探讨其作用机制.
方法: 成年♀SD大鼠(n = 50), 随机分为健康对照组A、未治疗组B、双歧三联活菌治疗组C、奥沙拉秦治疗组D、双歧三联活菌和奥沙拉秦联合治疗组E(n = 10). 观察大鼠的一般情况, 检测各组大鼠血清肿瘤坏死因子-a(TNF-a)、结肠组织TNF-a细胞阳性率, 比较结肠组织炎症程度.
结果: A组大鼠DAI(P<0.001)、血清TNF-a(P<0.001)水平、肠组织TNF-a细胞阳性率(P<0.05)、肠组织学评分(P<0.05)显著低于未治疗组B; B组大鼠DAI、血清TNF-a水平、肠组织学评分、肠组织TNF-a细胞阳性率最高(P<0.05); 3个治疗组C、D、E的大鼠DAI、血清TNF-a、肠组织TNF-a细胞阳性率明显下降, 肠组织炎症明显消散, 以E组最显著(P<0.05), 肠组织TNF-a的表达与结肠炎病情轻重呈正相关.
结论: 双歧三联活菌能有效治疗TNBS诱导的大鼠结肠炎, 其作用机制可能与抑制肠黏膜免疫系统效应细胞TNF-a的表达有关.
引文著录: 万岳梦, 朱尤庆, 杨晋辉, 尤丽英, 杨婧, 罗俊. 微生态制剂对TNBS诱导的大鼠结肠炎的疗效. 世界华人消化杂志 2012; 20(1): 66-69
Revised: November 30, 2011
Accepted: December 23, 2011
Published online: January 8, 2012
AIM: To evaluate the therapeutic effect of a probiotic compound on colitis in rats induced with trinitrobenzenesulfonic acid (TNBS) and to investigate the underlying mechanisms.
METHODS: In total, 50 female adult Sprague-Dawley rats were randomized into five groups: healthy control group (A), untreated group (B), probiotics group (C), olsalazine group (D) and combined treatment group (E). Except for group A, rats in the other groups were subjected to induction of colitis. Each group received a corresponding therapeutic regimen. After treatment, the general status of all rats was observed; serum levels of tumor necrosis factor-alpha (TNF-a) and positive rate of colonic TNF-a expression in the colon were detected; and histopathologic changes in the colon were examined.
RESULTS: The disease activity index (DAI), serum levels of TNF-a, positive rate of TNF-a expression in the colon, and histopathologic score were significantly lower in group A than in group B (all P < 0.05). Group B exhibited most severe colonic inflammation and highest DAI, serum TNF-a, and positive rate of TNF-a expression in the colon (all P < 0.05). The three treatment groups (C, D and E) showed marked remission of colonic inflammation and significantly decreased serum TNF-a and positive rate of TNF-a in the colon when compared to group B (all P < 0.05), with group E being most prominent. Colonic TNF-a expression correlates positively with the severity of colitis.
CONCLUSION: The tested probiotic compound could effectively reduce TNBS-induced colitis in rats possibly via mechanisms associated with the inhibition of TNF-a expressed by the effector cells of intestinal mucosal immune system.
- Citation: Wan YM, Zhu YQ, Yang JH, You LY, Yang J, Luo J. Therapeutic effect of a probiotic compound on TNBS-induced colitis in rats. Shijie Huaren Xiaohua Zazhi 2012; 20(1): 66-69
- URL: https://www.wjgnet.com/1009-3079/full/v20/i1/66.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i1.66
目前认为, 肿瘤坏死因子-a(tumor necrosis factor-alpha, TNF-a)在肠黏膜炎症反应中起着最重要的作用, 很可能是炎症性肠病(inflammatory bowel disease, IBD)炎症瀑布反应效应的中心点[1]. 国内有研究报道双歧杆菌能有效治疗三硝基苯磺酸钠(TNBS)诱导的鼠类结肠炎, 但其作用机制尚不清楚[2], 故本研究通过观察其对实验性大鼠结肠炎的疗效, 旨在探讨TNF-a与其疗效的关系.
5%三硝基苯磺酸钠溶液(5% TNBS, Sigma-Aldrich公司)、双歧三联活菌(上海医药有限公司信谊制药总厂)、奥沙拉秦(天津力生制药股份有限公司)、TNF-a ELISA 检测试剂盒(欣博盛生物科技有限公司)、Envision两步法免疫组化试剂盒(上海拜力)、兔抗大鼠TNF-a单克隆抗体(北京中杉金桥, 1:100稀释)、Rayto-6000酶标仪(美国Rayto公司). 健康雌性SD大鼠50只, SPF级, 体质量175-215 g, 由武汉大学中南医院动物实验中心提供, 许可证号: SCXK(鄂)2008-0004, 每日光照12 h, 室温条件下常规饲养.
1.2.1 药物配制: 将 5%TNBS 20 mL溶于50%乙醇溶液20 mL, 制成 2.5% TNBS(V/V)溶液, 10粒双歧三联活菌胶囊溶于20 mL生理盐水, 1片奥沙拉秦(250 mg)溶于20 mL生理盐水, 将10粒双歧三联活菌胶囊(每粒含活菌数不低于1×107 CFU)和1片奥沙拉秦(250 mg)同时溶于20 mL生理盐水.
1.2.2 造模: 据文献[3], 大鼠禁食48 h后, A组采用25%乙醇溶液灌肠, 1.0 mL/只, 其他组用2.5% TNBS(V/V)溶液灌肠, 1.0 mL/只(含TNBS 25 mg). 24 h后, A、B组: 每天无菌生理盐水灌胃, 2.0 mL/只; C组: 每天双歧三联活菌溶液灌胃, 1×107 CFU/只; D组: 每天奥沙拉秦溶液灌胃, 125 mg/kg; E组: 每天混合药液灌胃, 双歧三联活菌及奥沙拉秦的剂量同C及D组, 共10 d. 每日观察并记录大鼠精神、活动、毛发、粪便、体重, 据文献[4]分析疾病活动指数(DAI).
1.2.3 取材: 所有大鼠20%乌来糖腹腔注射(1.5 mL/只)麻醉后经腹主动脉无菌取血约2.0 mL, 提取血清, -20 ℃保存, 用于检测TNF-a水平. 从距肛门1.0 cm向结肠近端切取6.0 cm肠段, 取2.0 cm肠段送病理科进行病理学分析和免疫组化染色分析TNF-a的表达.
1.2.4 血清TNF-a测定: 按试剂盒说明书操作.
1.2.5 肠组织病理分析: 肠组织经HE染色后, 据文献[5]进行病理学评分.
1.2.6 肠组织TNF-a检测: 按试剂盒说明书操作, 采用两步法免疫组化方法检测大鼠结肠组织中TNF-a, 光镜下胞浆着棕黄色为阳性细胞: 每例取5个高倍视野(×400), 通过HPIAS2000型病理图文分析系统, 算出TNF-a的细胞阳性率.
统计学处理 采用SPSS16.0统计学软件, 实验数据以mean±SD表示, 本实验中各组大鼠血清TNF-a、肠组织TNF-a细胞阳性率、肠组织学评分采用单因素方差分析(One-way ANOVA), 大鼠疾病活动指数(DAI)采用2个重复测量因素的方差分析, P<0.05为差异有统计学意义.
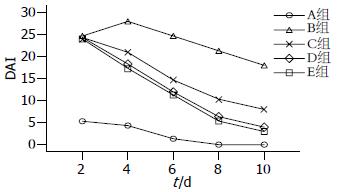
5组大鼠间的DAI明显不同(组间比较), 对照组A最低, 未治疗组B最高, P = 0.000; 治疗组C、D、E的DAI明显低于未治疗组B(P = 0.000); 与联合治疗组E相比, 治疗组C的DAI显著偏高(P = 0.002), 而治疗组D的DAI与之相比无显著差异(P = 0.309); 治疗组C的DAI显著高于治疗组D的DAI(P = 0.002, 图1).
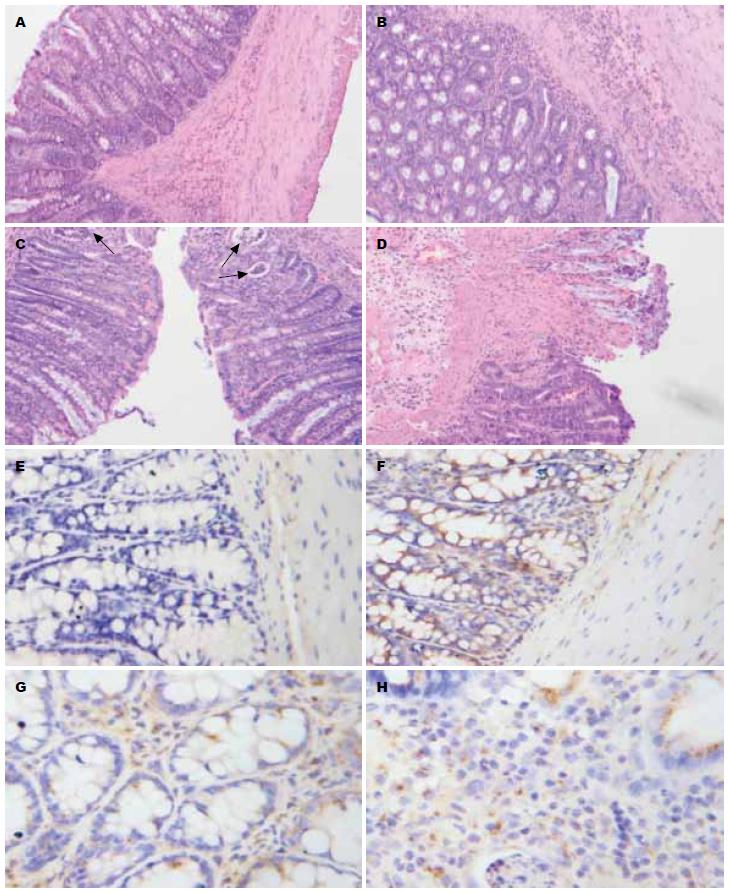
A组大肠腺体规则, 可见大量胞质富含黏液的杯状细胞, 黏膜固有层、黏膜下层未见炎性细胞浸润(图2A); 未治疗组B肠组织炎症程度较重, 可见肠黏膜和黏膜下组织大量中性粒细胞、淋巴细胞、浆细胞及嗜酸性粒细胞浸润, 杯状细胞胞质黏液分泌减少, 肠黏膜隐窝变形(图2B), 隐窝脓肿形成, 可见肠壁坏死、变薄, 几近穿孔(图2C), 肠黏膜溃疡多见, 黏膜下组织充血、水肿, 伴急性小血管炎症、出血和纤维素样坏死(图2D). 与B组相比, 治疗组C、D、E组均可见不同程度的炎症消散, 表现为炎性细胞浸润减少、隐窝变形恢复和杯状细胞胞质黏液增多, 溃疡缩小和肉芽组织增生修复, E组炎症最轻. 各组大鼠肠组织病理学评分见表1.
TNBS灌肠后10-24 h, 所有大鼠(B、C、D、E组)均有不同程度的腹泻、72.5%(29/40)的大鼠解黏液血便, 至用药后第2天, 各组大鼠的临床表现相似, 疾病活动指数(DAI)间差别不明显. 随着实验的进行, C、D、E组大鼠的疾病活动指数(DAI)开始下降, 至第4天药物治疗组C、D、E的DAI显著低于未治疗组B, 以联合治疗组E的DAI最低, 这种趋势持续到第10天, 表明培菲康、5-ASA及两者联合对TNBS诱导的结肠炎治疗有效, 且联合治疗的效果更佳. C组的DAI高于D组, 表明5-ASA的疗效优于培菲康. E组的DAI低于D组, 但两组的DAI差别无显著性(P = 0.309), 可能与用药时间偏短有关.
经培菲康、5-ASA及两者联合治疗后, 肠组织炎症明显消散, 表明培菲康、5-ASA及两者联合均能有效治疗TNBS诱导的结肠炎. C、D两组的肠组织病理学评分无显著差别, 表明培菲康与5-ASA的抗炎效果相似. 联合治疗组E肠组织病理学评分明显低于C、D两组, 表明培菲康与5-ASA联合应用, 能提高培菲康及5-ASA的抗炎效果.
TNF-a是一个致炎细胞因子, 其在IBD的发病中有重要作用, 抗TNF-a单克隆抗体(infliximab)能有效治疗CD[6]. 因此, 调节TNF-a水平, 理论上可以改变肠组织炎症程度. 本研究发现, 未治疗组B经2.5% TNBS/乙醇(V/V)溶液灌肠后, 血清TNF-a、肠组织TNF-a蛋白水平均明显升高, 提示TNBS诱导的结肠炎与TNF-a密切相关. 经培菲康、5-ASA及两者联合治疗后, 血清TNF-a、肠组织TNF-a蛋白水平呈不同程度下降, 以联合治疗组E的TNF-a水平下降最显著, 表明培菲康、5-ASA及两者联合都能有效降低TNF-a的表达. 治疗组C、D、E的结肠炎症都有明显好转, TNF-a水平与结肠炎症程度呈正相关(数据未列出), 提示培菲康、5-ASA及两者联合治疗TNBS诱导的结肠炎的疗效机制均与降低TNF-a的表达有关.
总之, 我们的研究表明双歧三联活菌能有效治疗TNBS诱导的大鼠结肠炎, 其疗效与降低肠组织TNF-a表达有关, 我们的研究为临床用培菲康治疗UC或设计随机、盲法、对照临床能有效治疗TNBS诱导的大鼠结肠炎, 其疗效与降低肠组织T研究提供了理论依据.
已知肠道黏膜免疫系统异常反应所导致的炎症反应在IBD发病中起重要作用, 认为这是由多因素相互作用所致, 主要包括环境、遗传、感染和免疫因素. 因为病因不明确, 治疗十分困难, 只能控制急性发作期的症状, 缓解后极易复发. 目前常见的治疗选择十分有限, 疗效也不尽如人意, 急需探索新的治疗方法.
施瑞华, 教授, 南京医科大学第一附属医院消化科
国内外有文献报道微生态制剂能有效治疗IBD的报道, 但确切机制尚不明确, TNF-α是一个致炎细胞因子, 其在IBD的发病中有重要作用.
陈宁等用益生菌治疗的实验性结肠炎取得一定疗效; Fedorak等用益生菌治疗醋酸诱导的结肠炎, 取得较好疗效.
本研究为临床用培菲康治疗UC或设计随机、盲法、对照临床研究提供了理论依据.
本文观察了微生态制剂培菲康治疗大鼠TNBS诱导的结肠炎的疗效, 有一定临床研究价值, 设计科学合理, 实验方法正确, 实验数据真实可信, 结论正确.
编辑: 李军亮 电编:何基才
| 1. | Schreiber S, Nikolaus S, Hampe J, Hämling J, Koop I, Groessner B, Lochs H, Raedler A. Tumour necrosis factor alpha and interleukin 1beta in relapse of Crohn's disease. Lancet. 1999;353:459-461. [PubMed] [DOI] |
| 3. | Siddiqui A, Ancha H, Tedesco D, Lightfoot S, Stewart CA, Harty RF. Antioxidant therapy with N-acetylcysteine plus mesalamine accelerates mucosal healing in a rodent model of colitis. Dig Dis Sci. 2006;51:698-705. [PubMed] [DOI] |
| 4. | Vowinkel T, Kalogeris TJ, Mori M, Krieglstein CF, Granger DN. Impact of dextran sulfate sodium load on the severity of inflammation in experimental colitis. Dig Dis Sci. 2004;49:556-564. [PubMed] [DOI] |
| 5. | Fedorak RN, Empey LR, MacArthur C, Jewell LD. Misoprostol provides a colonic mucosal protective effect during acetic acid-induced colitis in rats. Gastroenterology. 1990;98:615-625. [PubMed] |