修回日期: 2009-12-16
接受日期: 2009-12-21
在线出版日期: 2010-02-28
目的: 研究伊托必利、多潘立酮和甲氧氯普胺联合应用对功能性消化不良(FD)患者胃肠功能和Ghrelin含量的影响.
方法: 以FD患者为研究对象, 依据罗马Ⅱ标准, 将符合纳入标准的患者120例随机分为6组, 分别给予盐酸伊托必利, 多潘立酮, 甲氧氯普胺, 以及联合用药给予盐酸伊托必利+多潘立酮, 盐酸伊托必利+甲氧氯普胺和多潘立酮+甲氧氯普胺, 观察用药前后各临床症状积分改善程度、胃肠排空率及血清Ghrelin的水平改变.
结果: 各组FD患者服药后消化不良等症状均明显改善, 在症状缓解率, 联合用药组明显优于单独用药组(P<0.01); 在胃排空率, 各联合用药组明显优于单独用药组(54.26%±18.57%, 55.12%±18.22%, 47.17%±15.21% vs 36.23%±11.68%, 32.16%±10.08%, 32.24%±10.12%, 均P<0.01); 在肠排空率, 联合用药组中伊托必利+多潘立酮组和伊托必利+甲氧氯普胺组明显优于多潘立酮+甲氧氯普胺组(89.27%±11.36%, 88.67%±13.25% vs 69.16%±19.26%, 均P<0.01); 单独用药组中伊托必利明显优于多潘立酮或甲氧氯普胺(78.23%±12.56% vs 58.96%±12.20%, 58.33%±12.57%, P<0.01); 但伊托必利单独用药明显优于多潘立酮+甲氧氯普胺联合用药(P<0.05). FD患者血清Ghrelin水平明显降低(P<0.05). 经药物治疗后Ghrelin水平明显回升, 联合用药组明显高于单独用药组(P<0.05或0.01).
结论: 伊托必利、多潘立酮和甲氧氯普胺联合用药比单独用药更有效, 可显著改善FD患者的胃肠动力, 该功能可能与血清ghrelin水平改变有关.
引文著录: 李娜, 徐珞. 伊托必利、多潘立酮和甲氧氯普胺联合用药对FD患者胃肠功能和Ghrelin表达的影响. 世界华人消化杂志 2010; 18(6): 596-600
Revised: December 16, 2009
Accepted: December 21, 2009
Published online: February 28, 2010
AIM: To investigate the effects of combined treatment with itopride, domperidone and metoclopramide on digestive function, gastrointestinal emptying and serum ghrelin level in patients with functional dyspepsia (FD).
METHODS: One hundred and twenty FD patients were divided into six groups according to the Rome II criteria: those treated with itopride, domperidone and metoclopramide, alone or in double combination. The clinical symptoms, gastrointestinal emptying rate and serum ghrelin level were observed before and after treatment.
RESULTS: The symptoms of FD patients were significantly improved after each treatment. The symptomatic relief rates achieved in the combination groups were much better than those in single-drug groups (all P < 0.01). The gastric emptying rates achieved in the combination groups were also much better than those in single-drug groups (54.26% ± 18.57%, 55.12% ± 18.22% and 47.17% ± 15.21% vs 36.23% ± 11.68%, 32.16% ± 10.08% and 32.24% ± 10.12%, respectively; all P < 0.01). The intestinal emptying rates in the itopride plus domperidone group and the itopride plus metoclopramide group were much better than that in the domperidone plus metoclopramide group (89.27% ± 11.36% and 88.67% ± 13.25% vs 69.16% ± 19.26%, respectively; both P < 0.01). The intestinal emptying rate in the itopride group was much better than those in the domperidone group and the metoclopramide group (78.23% ± 12.56% vs 58.96% ± 12.20% and 58.33% ± 12.57%, respectively; both P < 0.01). The level of serum ghrelin in FD patients was significantly lower than that in normal controls (P < 0.05). After drug treatment, the level of serum ghrelin rose obviously. The levels of serum ghrelin in combination groups were higher than those in single-drug groups (all P < 0.05 or 0.01).
CONCLUSION: Treatment with itopride, domperidone and metoclopramide in double combination achieves better efficacy in FD patients than treatment with these drugs alone. Combination therapy significantly improves dyspepsia and gastric motility in FD patients perhaps by altering the level of serum ghrelin.
- Citation: Li N, Xu L. Combined treatment with itopride, domperidone and metoclopramide improves gastrointestinal function and upregulates serum ghrelin level in patients with functional dyspepsia. Shijie Huaren Xiaohua Zazhi 2010; 18(6): 596-600
- URL: https://www.wjgnet.com/1009-3079/full/v18/i6/596.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v18.i6.596
功能性消化不良(functional dyspepsia, FD)是一种常见的临床疾病, 占消化系疾病患者的20%-40%, 一直是人们研究的热点. 但目前FD发病机制尚未明确, 可能涉及多种因素. 近年来国内外研究表明, 胃肠动力功能障碍是FD的主要发病机制, 并且胃肠动力异常伴有胃肠激素变化与异常. Ghrelin是1999年Kojima等[1]发现的由28个氨基酸组成的小分子多肽. 其具有促进胃酸分泌、胃肠运动、促进摄食和调控能量代谢等功能. 为明确胃动力药对FD的治疗效果, 指导临床用药, 本实验采用胃肠排空检测法和放射免疫法, 结合临床观察探讨单用或联合应用伊托必利、多潘立酮和甲氧氯普胺对FD患者的胃肠运动和Ghrelin含量的影响.
按罗马Ⅱ标准诊断FD患者. 选择以上腹胀、早饱、暖气、恶心和呕吐为主要表现, 早饱和/或上腹胀的临床症状评分达2级或2级以上, 年龄为18-60岁的动力障碍型FD患者为研究对象. 实验前72 h停用抗胆碱药、解痉药、抑酸药及促动力药. 入选FD患者120例, 男66例, 女54例. 同期选择性别和年龄配对的健康志愿受试者10例(男6例, 女4例)作为对照组. 以上两组人群均征得本人同意, 且符合以下条件: (1)排除妊娠或哺乳期妇女, 伴有其他心、肝、肾、内分泌等疾病, 或合并精神疾病; (2)排除不能表达主观不适症状, 过敏体质, 以及有腹部手术史者; (3)FD患者在入选时和药物治疗后分别记录上腹胀、早饱、嗳气、恶心、呕吐等症状, 并给以评分. 症状评分标准按0-3级记录: 0级为无症状, 记0分; 1级为有轻度感觉但不明显, 记为1分; 2级为症状稍重, 但不影响工作, 记为2分; 3级为症状严重, 难以坚持工作, 记为3分
1.2.1 分组及治疗: 将符合纳入标准的患者分为6组(n = 20), 分别给予盐酸伊托必利50 mg, tid; 多潘立酮10 mg, tid; 甲氧氯普胺5 mg, tid; 盐酸伊托必利+多潘立酮(50 mg+10 mg), tid; 盐酸伊托必利+甲氧氯普胺(50 mg+5 mg), tid; 多潘立酮+甲氧氯普胺(10 mg+5 mg), tid. 药物均在餐前30 min服用, 疗程4 wk, 并以10名健康志愿者作为对照组.
1.2.2 胃肠排空检测: 所有受试者均采用统一的标准试餐, 包括50 g火腿肠和80 g油炸方便面, 用500 mL白开水冲泡. 要求受试者在10 min内吃完标准试餐. 标准试餐的总能量为1 966 kJ, 其中碳水化合物46%, 脂肪42%, 蛋白质12%. 受试者空腹至少8 h以上. 经期妇女应在月经周期的卵泡期(约为月经干净之后的2 wk内)进行检查, 以减少激素对胃排空的影响. 检查前至少3 d未使用可能影响胃排空功能的药物和其他措施(包括烟酒等). 受试者在进食标准试餐的10 min内分次均匀地口服下不透X光的钡条(长10 mm, 直径1 mm), 共计20根. 注意应整吞服下钡条, 不可嚼碎. 于餐后5 h, 72 h各透视并拍摄腹平片一张. 5 h透视时同时口服20%稀钡溶液20 mL, 以确定胃内钡条排空情况. 统计胃肠内不透X标记物残留数, 计算排空率. 排空率 = (20-胃或肠内残留钡条数)/20×100%. 检测用药前后胃排空率及肠排空率的大小, 并进行比较.
1.2.3 Ghrelin放射免疫测定: Ghrelin放射免疫分析试剂盒由北京科美东雅生物技术有限公司提供. 灵敏度<50 ng/L, 批内差异<7.0%, 批间差异<15%. 放免检测严格按说明书进行操作. 即配制Ghrelin标准液, 1:8 000抗Ghrelin血清和I125-Ghrelin液. 各管加I125-Ghrelin 100 µL, 抗Ghrelin血清100 µL. 样品管加200 µL, 标准管加Ghrelin 100 µL, 最后以磷酸缓冲液补足总反应体积为500 µL; 4 ℃冰箱内孵育24 h; 各管加1:3羊抗兔血清100 µL, 继续孵育24 h, 4 000 g离心20 min, 弃上清液, 测沉淀物的cpm, 根据同批测定管的Ghrelin竞争抑制曲线, 求取每升血清Ghrelin免疫反应阳性物的含量(ng/L).
统计学处理 采用SPSS统计软件包处理. 计量数据采用mean±SD的形式, 两组间均数比较采用成组t检验, 缓解率的比较采用卡方检验, 多个样本均数间比较采用Newman-Keuls法. P<0.05定义为显著性差异, P<0.01表示有极显著差异.
6组FD患者口服药物后各种症状均有减轻或缓解, 上腹痛、腹胀、早饱、嗳气、呕吐等临床症状较用药前均有统计学意义(P<0.05-0.01, 表1). 在症状缓解率, 联合用药组明显优于单独用药组(P<0.01); 单独用药组中伊托必利明显优于多潘立酮和甲氧氯普胺(P<0.05), 但多潘立酮与甲氧氯普胺组间无明显差异(P>0.05); 在联合用药组, 伊托必利+多潘立酮组和伊托必利+甲氧氯普胺组明显优于多潘立酮+甲氧氯普胺组(P<0.05-0.01), 而伊托必利+多潘立酮组与伊托必利+甲氧氯普胺组无明显差异(P>0.05).
| 疼痛 | 腹胀 | 早饱 | 反酸 | 嗳气 | 恶心 | 呕吐 | 总分 | |
| 伊托必利 | ||||||||
| 用药前 | 2.16±0.61 | 2.05±0.43 | 1.55±0.36 | 0.96±0.15 | 1.36±0.37 | 0.32±0.10 | 0.25±0.08 | 8.65±2.10 |
| 用药后 | 1.06±0.23b | 0.93±0.08b | 0.62±0.12b | 0.38±0.07b | 0.26±0.07b | 0.25±0.08a | 0.17±0.05b | 3.61±0.70 |
| 缓解率(%) | 50.93 | 54.63 | 60.00 | 60.42 | 80.88 | 21.88 | 32.00 | 58.27c |
| 多潘立酮 | ||||||||
| 用药前 | 2.13±0.69 | 2.21±0.54 | 1.56±0.51 | 1.06±0.34 | 1.42±0.39 | 0.22±0.07 | 0.26±0.08 | 8.86±2.62 |
| 用药后 | 1.33±0.43b | 1.37±0.37b | 0.55±0.17b | 0.97±0.30 | 0.65±0.17b | 0.16±0.05b | 0.18±0.05b | 5.21±1.54 |
| 缓解率(%) | 37.56 | 38.01 | 64.74 | 8.49 | 54.23 | 27.27 | 30.77 | 41.20 |
| 甲氧氯普胺 | ||||||||
| 用药前 | 2.17±0.66 | 2.16±0.57 | 1.65±0.42 | 1.01±0.33 | 1.38±0.34 | 0.26±0.08 | 0.24±0.07 | 8.87±2.47 |
| 用药后 | 1.26±0.35b | 1.25±0.32b | 0.74±0.21b | 0.86±0.27 | 0.77±0.21b | 0.22±0.07 | 0.16±0.05b | 5.26±1.48 |
| 缓解率(%) | 41.94 | 42.13 | 55.15 | 14.85 | 44.20 | 15.38 | 33.33 | 40.70 |
| 伊托必利+多潘立酮 | ||||||||
| 用药前 | 2.16±0.57 | 2.20±0.49 | 1.64±0.32 | 1.03±0.27 | 1.39±0.31 | 0.31±0.08 | 0.25±0.06 | 8.98±2.10 |
| 用药后 | 0.17±0.02b | 0.12±0.03b | 0.15±0.03b | 0.05±0.01b | 0.08±0.02b | 0.24±0.07b | 0.15±0.03b | 0.96±0.21 |
| 缓解率(%) | 92.13 | 94.55 | 90.85 | 95.15 | 94.24 | 22.58 | 40.00 | 89.31f |
| 伊托必利+甲氧氯普胺 | ||||||||
| 用药前 | 2.14±0.67 | 2.16±0.47 | 1.56±0.28 | 0.98±0.18 | 1.42±0.32 | 0.32±0.10 | 0.25±0.07 | 8.83±2.09 |
| 用药后 | 0.18±0.05b | 0.12±0.02b | 0.17±0.03b | 0.07±0.01b | 0.09±0.02b | 0.25±0.08a | 0.15±0.03b | 1.03±0.24 |
| 缓解率(%) | 91.59 | 94.44 | 89.10 | 92.86 | 93.66 | 21.88 | 40.00 | 88.34e |
| 甲氧氯普胺+多潘立酮 | ||||||||
| 用药前 | 2.15±0.56 | 2.17±0.57 | 1.48±0.21 | 1.01±0.26 | 1.37±0.31 | 0.33±0.10 | 0.22±0.07 | 8.73±2.08 |
| 用药后 | 0.57±0.14b | 0.48±0.11b | 0.38±0.07b | 0.25±0.05b | 0.13±0.02b | 0.25±0.08b | 0.16±0.05b | 2.22±0.52 |
| 缓解率(%) | 73.49 | 77.88 | 74.32 | 75.25 | 90.51 | 24.24 | 27.27 | 74.57 |
FD患者餐后钡条胃肠排空率明显低于健康正常对照组(P<0.01, 表2), 经伊托必利、多潘立酮或甲氧氯普胺单独或联合治疗后, 胃肠排空率明显改善, 且联合用药组优于单独用药组(P<0.05-0.01), 但胃排空率各单独用药组间和各联合用药组间无显著差异(P>0.05); 在肠排空率, 联合用药组中伊托必利+多潘立酮组和伊托必利+甲氧氯普胺组明显优于多潘立酮+甲氧氯普胺组(P<0.01), 而伊托必利+多潘立酮组与伊托必利+甲氧氯普胺组相比无明显差异(P>0.05); 单独用药组中伊托必利明显优于多潘立酮和甲氧氯普胺(P<0.01), 但多潘立酮与甲氧氯普胺组间无明显差异(P>0.05); 伊托必利单独用药优于多潘立酮+甲氧氯普胺联合用药(P<0.05). 伊托必利促肠排空作用明显优于多潘立酮和甲氧氯普胺.
| 胃排空率(5 h) | 肠排空率(72 h) | ||
| 对照组(n = 10) | 健康者 | 92.00±9.28 | 94.00±8.06 |
| FD组(n = 120) | 治疗前 | 6.67±2.12b | 56.38±15.13b |
| 伊托必利组 | 治疗前 | 6.76±2.17 | 56.33±14.57 |
| 治疗后 | 36.23±11.68 | 78.23±12.56 | |
| 多潘立酮组 | 治疗前 | 6.58±2.06 | 57.27±15.21 |
| 治疗后 | 32.16±10.08 | 58.96±12.20 | |
| 甲氧氯普胺组 | 治疗前 | 6.64±2.08 | 57.12±18.33 |
| 治疗后 | 32.24±10.12 | 58.33±12.57 | |
| 伊托必利+ 多潘立酮组 | 治疗前 | 6.72±2.15 | 56.56±14.37 |
| 治疗后 | 54.26±18.57e | 89.27±11.36e | |
| 伊托必利+ 甲氧氯普胺组 | 治疗前 | 6.69±2.17 | 57.28±17.07 |
| 治疗后 | 55.12±18.22e | 88.67±13.25e | |
| 多潘立酮+ 甲氧氯普胺组 | 治疗前 | 6.54±2.07 | 54.27±16.92 |
| 治疗后 | 47.17±15.21e | 69.16±19.26cg |
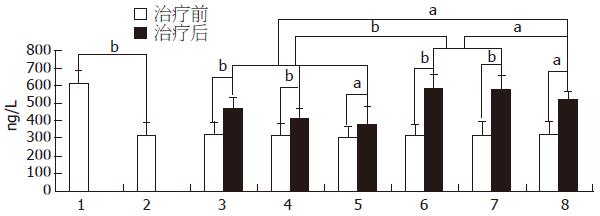
图1显示放射免疫研究结果. FD患者血清Ghrelin水平明显低于正常对照组(P<0.01), FD患者各组治疗后较治疗前Ghrelin含量显著增高(P<0.05-0.01); 联合用药各组则明显高于单独用药组(P<0.05-0.01).
FD是以餐后上腹不适或疼痛、早饱、恶心、呕吐、嗳气等为主要表现的症候群. 胃肠测压、胃排空、胃电图等研究表明, 空腹、餐后均存在着胃肠运动的异常及排空障碍,空腹时胃窦、十二指肠运动减弱, 餐后胃窦、十二指肠动力低下, 胃固体、液体及混合餐排空延迟.
至今FD的病因及发病机制仍不清楚, 其症状的产生并非单一因素引起的疾病, 而是诸多因素经不同的机制所导致的一组症候群. 目前认为FD发病机制[2]可能其一是内脏感觉过敏. 表现为近端胃对机械扩张的敏感性增加, 与患者餐后疼痛、打嗝及体质量下降有关. 其二是30%-80% FD患者有消化运动异常. 常见胃排空减慢, 近端胃受纳性舒张功能减弱, 胃窦移行性复合波(MMC)减少或缺如, 胃十二指肠协调运动减弱, 小肠MMC减少, 小肠消化间期无传导性暴发收缩活动增加等. 其三是幽门螺杆菌感染. 幽门螺杆菌是否为FD发病因素一直存在争议. 其四是精神应激. 应激可使中枢促皮质释放因子分泌增加, 引起胃排空减缓, 内脏感觉呈高敏状态. 常规应用促动力药、黏膜保护剂、抑酸剂、抗幽门螺杆菌及中成药等治疗可使部分患者得到缓解. 但有不少患者经上述常规治疗后无明显疗效. 最近有文献报道, 胃动力障碍与脑-肠轴功能障碍有关, 特别是和多巴胺受体功能异常有着直接密切的联系. 本研究发现伊托必利、多潘立酮和甲氧氯普胺均可改善FD患者胃肠运动和消化不良症状, 且伊托必利促进胃肠运动和改善消化不良症状明显优于多潘立酮和甲氧氯普胺.
多巴胺受体分为D1和D2受体, 多巴胺可显著抑制胃肠运动功能. 甲氧氯普胺可通过作用于D1和D2受体产生抗多巴胺的作用. 多潘立酮是一种合成的苯咪唑类衍生物, 为一种多巴胺受体拮抗剂, 通过拮抗胃肠道多巴胺受体, 特异性地作用于上消化道, 可显著增强胃蠕动, 促进胃排空, 增加胃窦收缩次数, 协调胃十二指肠运动, 恢复胃窦十二指肠协调性, 有效解除上消化系动力障碍症状[3,4]. 盐酸伊托必利为一种新型胃肠促动力药, 系甲基酰胺衍生物, 具有多巴胺D2受体阻断剂及乙酰胆碱酯酶抑制剂的双重作用, 通过刺激内源性乙酰胆碱释放并抑制乙酰胆碱水解, 可增加胃的内源性乙酰胆碱, 增强胃十二指肠的运动, 而解除消化系动力障碍症状[5].
虽然单独用药可减少多种药物的不良反应, 但长期单用一种药物, 机体对该药会产生耐受性[6]且作用单一. 联合用药能增加疗效降低毒性, 例如中医传统用药, 自古至今擅长于配伍使用药物, 西医虽然不这样分, 但往往根据疾病的需要也常常使用多种药物配合治疗, 通过综合用药发生综合治疗作用, 有利于疾病的恢复. 本研究发现联合应用伊托必利, 多潘立酮组或甲氧氯普胺, 患者消化不良临床症状的改善(如上腹痛、腹胀、早饱、嗳气等)和胃肠排空率均显著优于其单独用药组. 提示, 联合用药更有利于临床消化不良患者功能恢复和改善.
胃肠激素是胃肠运动功能的重要调节因素. 当今胃肠激素完全超出了单一的内分泌激素的范畴, 而是一类具有多种来源的多种成分、多种作用方式和功能的激素. Ghrelin是一种具有生长激素释放活性的脑肠肽. 随着研究的不断深入, 发现他还与食欲调节、能量平衡和肥胖、心脏、胃肠功能及睡眠等有关[7-11]. Masuda等研究发现, 静脉注射Ghrelin能剂量依赖性地增强胃肠道活动, 刺激胃酸分泌, 此作用会被阿托品的前处理和双侧迷走神经切断术所消除[12,13]. Ghrelin能促进大鼠胃的排空, 减少大鼠手术后的胃梗阻[14]; Sibilia等给小鼠脑室或腹膜注射Ghrelin, 发现摄食后1 h. 2 h胃食物残留量明显减少, 提示胃排空率的增快[15]. 有文献报道, Ghrelin可促进糖尿病大鼠胃排空增快[16], 其作用机制可能通过促进乙酸胆碱释放所致. 本研究发现, FD患者血清Ghrelin水平明显低于正常对照组; FD患者经治疗后, Ghrelin水平显著增高; 本研究还发现, 联合用药Ghrelin水平较单独用药显著增高(P<0.05-0.01). 提示, 这些促胃动力药物, 可能通过Ghrelin水平改变, 改善胃运动, 但具体机制不清, 尚有待于进一步研究.
功能性消化不良是以餐后上腹不适或疼痛、早饱、恶心、呕吐、暖气等为主要表现的症候群. 其发病率较高, 严重危害着人们生活质量, 是当今临床上亟待解决的问题之一.
刘正稳, 教授, 西安交通大学医学院第一附属医院
功能性消化不良是一常见的临床疾病, 是当今研究的热点之一. 其发病机制复杂, 涉及多种因素, 胃肠动力障碍和胃肠激素变化异常是发病的主要原因.
以往研究显示伊托必利、多潘立酮和甲氧氯普胺单独用药均有改善患者消化功能不良等症状. 该症状的改善与消化不良患者胃肠激素分泌变化研究较少.
以往研究主要焦点集中在单独选用一种药物疗效进行观察. 本研究同时观察和比较了伊托必利、多潘立酮和甲氧氯普胺这三代药在症状改善、胃肠排空和血清Ghrelin水平改变, 使医师对这些药物的临床应用有更加清楚的选择.
本研究通过对伊托必利、多潘立酮和甲氧氯普胺单独用药和联合用药比较, 可使临床医师对这些药物的临床应用做出更加准确的选择.
本文不仅比较了每种药物的单独作用, 而且比较了他们的联合作用. 因此, 该研究结果对临床药物的联合应用具有一定参考意义.
编辑: 李军亮 电编:何基才
| 1. | Kojima M, Hosoda H, Date Y, Nakazato M, Matsuo H, Kangawa K. Ghrelin is a growth-hormone-releasing acylated peptide from stomach. Nature. 1999;402:656-660. [PubMed] [DOI] |
| 7. | 王 淑珍, 尚 宏伟, 王 兴翠, 李 冰, 张 斌, 丁 惠国. 肝硬化患者Ghrelin、生长激素释放素的变化及其临床意义. 世界华人消化杂志. 2008;16:3230-3233. [DOI] |
| 9. | Gasco V, Beccuti G, Marotta F, Benso A, Granata R, Broglio F, Ghigo E. Endocrine and Metabolic Actions of Ghrelin. Endocr Dev. 2010;17:86-95. [PubMed] [DOI] |
| 10. | Kitazawa T, Maeda Y, Kaiya H. Molecular cloning of growth hormone secretagogue-receptor and effect of quail ghrelin on gastrointestinal motility in Japanese quail. Regul Pept. 2009;158:132-142. [PubMed] [DOI] |
| 11. | Lee KJ, Cha DY, Cheon SJ, Yeo M, Cho SW. Plasma ghrelin levels and their relationship with gastric emptying in patients with dysmotility-like functional dyspepsia. Digestion. 2009;80:58-63. [PubMed] [DOI] |
| 12. | Masuda Y, Tanaka T, Inomata N, Ohnuma N, Tanaka S, Itoh Z, Hosoda H, Kojima M, Kangawa K. Ghrelin stimulates gastric acid secretion and motility in rats. Biochem Biophys Res Commun. 2000;276:905-908. [PubMed] [DOI] |
| 13. | Johnson AW, Canter R, Gallagher M, Holland PC. Assessing the role of the growth hormone secretagogue receptor in motivational learning and food intake. Behav Neurosci. 2009;123:1058-1065. [PubMed] [DOI] |
| 14. | Trudel L, Tomasetto C, Rio MC, Bouin M, Plourde V, Eberling P, Poitras P. Ghrelin/motilin-related peptide is a potent prokinetic to reverse gastric postoperative ileus in rat. Am J Physiol Gastrointest Liver Physiol. 2002;282:G948-G952. [PubMed] |
| 15. | Sibilia V, Rindi G, Pagani F, Rapetti D, Locatelli V, Torsello A, Campanini N, Deghenghi R, Netti C. Ghrelin protects against ethanol-induced gastric ulcers in rats: studies on the mechanisms of action. Endocrinology. 2003;144:353-359. [PubMed] [DOI] |
| 16. | Qiu WC, Wang ZG, Wang WG, Yan J, Zheng Q. Therapeutic effects of ghrelin and growth hormone releasing peptide 6 on gastroparesis in streptozotocin-induced diabetic guinea pigs in vivo and in vitro. Chin Med J (Engl). 2008;121:1183-1188. [PubMed] |