修回日期: 2008-12-25
接受日期: 2008-12-29
在线出版日期: 2009-02-18
目的: 寻求基于64层螺旋CT断层图像在个人电脑重建大肠三维数字模型及虚拟内镜检查的方法.
方法: Philips/Brilliance 64对胸9至股骨中段沿横断面平扫及动脉期和静脉期连续跟踪扫描. 基于空气灌肠造影平扫CT数据, 使用VGL 3.2共享软件包用Ray-Casting光线投射算法对肠管进行体绘制, Mimics软件用MC(marching cubes)算法对肠管进行面绘制及用虚拟内镜法(VE)重建三维图像. Mimics软件基于CTA二维图像对大肠及周围结构等各种组织进行三维重建.
结果: 成功建立了较精确的大肠体绘制和面绘制模型及大肠及周围结构三维数字模型, 包括骨骼系统, 动脉系统, 泌尿系, 皮肤, 大肠及部分小肠. 实现了三维交互式浏览和虚拟内镜的应用.
结论: 大肠可视化模型准确反映其复杂的解剖结构及空间毗邻关系, 不但为临床诊断提供可靠的解剖资料, 也为今后的虚拟手术打下了良好的基础.
引文著录: 俞金龙, 黄宗海, 陈海金, 方驰华. 基于64层螺旋CT断层图像的影像后处理-大肠三维重建及虚拟内镜. 世界华人消化杂志 2009; 17(5): 524-528
Revised: December 25, 2008
Accepted: December 29, 2008
Published online: February 18, 2009
AIM: To find a method to reconstruct a large intestine three-dimensional digital model and virtual endoscopic examination based on 64-slice helical CT image in personal computer.
METHODS: We used Philips/Brilliance 64 CT to complete plain scan from the 9th thoracic vertebra to middle-femur and continuously tracked scan of arterial phase and venous phase. Based on the CT plain scan after air pressure enema, we used the VGL 3.2 sharewares to carry on the volume rendering of intestine with the Ray-Casting light projection algorithm. Mimics software for the surface was used to render intestines with the Marching Cubes algorithm then three dimensional graphics were reconstructed using virtual endoscopy (VE). We reconstructed three-dimensional large intestine and surrounding structures with the Mimics software separately based on the CTA two-dimensional graphics.
RESULTS: We have established a more precise model of volume rendering and surface rendering of large intestine and surrounding structures, including skeletal system, arterial system, urinary tract, skin, large intestine and part of small intestine. We have achieved a three-dimensional interactive browsing and virtual endoscopic applications.
CONCLUSION: The large intestine visualization model could show precisely complex anatomical structure and spatial adjoining relations, which not only offers clinic doctors reliable anatomical information, but also a good base for later virtual surgery.
- Citation: Yu JL, Huang ZH, Chen HJ, Fang CH. Image post-processing based on 64-slice helical CT sectional images: three-dimensional reconstruction and virtual endoscopy of large intestine. Shijie Huaren Xiaohua Zazhi 2009; 17(5): 524-528
- URL: https://www.wjgnet.com/1009-3079/full/v17/i5/524.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i5.524
随着计算机技术向影像学领域渗透和应用, CT、MRI等断层影像技术实现了数字化图像处理, 医学图像信息的采集、储存、传输、处理、显示等发生了前所未有的变革. 由此形成全新医学图像处理和诊断模式, 诞生了仿真影像学[1]. 仿真影像学以仿真内镜(virtual endoscope, VE)[2]为核心, 包括各种数字化图像三维重建技术和后处理技术. 利用CT、MRI等二维断层图像为数据源, 应用计算机软件重建直观地显示人体器官, 尤其是管腔器官内表面解剖及病变三维仿真图像[3-8], 能够准确地直观反映人体三维结构, 进行疾病诊断、立体定位、模拟手术等. 大肠及周围结构是普通外科重要的解剖结构, 基于CT、MRI工作站对断层影像处理主要用于疾病诊断, 目的比较单一, 对CT、MRI等断层影像有效信息挖掘不够深入, 为此, 我们基于64层螺旋CTA断层数据集在个人电脑重建大肠体绘制和面绘制模型, 大肠和周围解剖结构空间毗邻关系模型及大肠虚拟内镜, 为深入挖掘断层影像有效信息做了有益尝试. 建立的模型为解剖教学、手术培训提供教学平台. 临床医师根据患者的数字化仿真模型, 可制订个体化术前规划和手术模拟.
Dicom 3.0格式[9-13]CTA扫描断层数据. 64层螺旋CT(Philips/Brilliance 64, 飞利浦公司, 荷兰). JS-818电脑遥控灌肠整复机(今健医疗器械有限公司, 中国广州). 优维显(德国先灵广州药业有限公司). 计算机硬件: AMD Athlon64 3200+中央处理器, 2G内存, 200G硬盘, 256M显存Radeon X1600Pro显卡, 19寸液晶显示器; 计算机环境: Windows XP/Professional 操作系统. 医学3D图像编辑处理软件Mimics 11.02(Materialise Software, Belgium). VGL 3.2共享软件包(volume graphics Software, Germany).
1.2.1 原始数据的采集: 选1名健康志愿者, 男, 31岁, 检查前3 d进流质饮食, 检查前晚服蓖麻油30 mL, 当日禁食, 检查前2 h作清洁灌肠, 直到排出液澄清为止, 术前15 min肌注阿托品0.5 mg. 使用JS-818电脑遥控灌肠整复机行空气灌肠使肠管膨胀. 经肛门插入Foley氏18F气囊管(代肛管), 插入深度为10 cm, 注入30 mL空气膨胀气囊, 防止气囊管脱落. 以12 kPa压力向直肠内注入空气30 s, 以患者感到轻度腹涨为度, 夹闭气囊管. 空气灌肠成功后行CT平扫及动脉造影. 平扫采用平卧位及俯卧位两次采集数据. CTA动脉造影方法: 经右侧肘前静脉以5 mL/s流率用双筒高压注射器注射优维显(370 mgI/mL)80 mL, 再以3.0 mL/s的流率静脉注射0.9%的生理盐水30 mL. CT的扫描条件: 使用Philips 64层螺旋CT, 扫描范围从胸9至股骨中段平面, 动脉造影沿横断面在动脉期及静脉期连续跟踪扫描, 选择腹部扫描条件, 软组织窗, 准直器宽33 mm×0.625 mm, 管电压120 kV. 原始数据的重建层厚0.5 mm, 间隔0.5 mm, 矩阵512×512. 平扫, 动脉期及静脉期各812层, 扫描数据以Dicom 3.0标准存储.
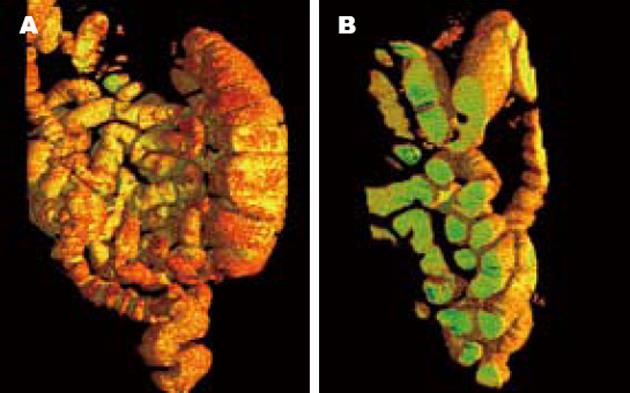
1.2.2 肠管体绘制: 体绘制[14-16]是对体数据进行直接绘制的过程. 我们用Ray-Casting光线投射算法[17]对肠管进行体绘制. 光线投射法是基于图像空间扫描生成高质量图像体绘制算法, 该方法能很好地反映物质边界的变化, 在医学上可将各组织器官的性质属性、形状特征表现出来. 在VGL 3.2软件包载入体数据后, 激活Classification工具控制面板, 在该面板内调节体绘制的参数. 主要定义以下2个传递函数: (1)灰度-不透明度传递函数. 该函数确定各体素或单位长度值的不透明度; (2)灰度-颜色传递函数. 该函数确定体素的颜色值或者灰度值. 体绘制的最终效果很大程度上由传递函数决定的, 在VGL对这两类传递函数进行调节以达到体素模型最佳视度效果. 在Clipbox工具可对体素模型进行三个正交平面的三维裁剪, 在Clipplane工具可对任意平面进行三维裁剪.
1.2.3 肠管面绘制和外显镜: Mimics软件[18-19]读入Dicom格式CT断层图像, 软件自动设定CT原始扫描参数, 每层原始图像灰度值以内插值处理, 达到亚体素的精度. 调整窗位窗宽, 对比度达到最佳视度. 空气灌肠使肠管充气膨胀, 肠道面绘制模型[20-21]按空气阈值建模, 界定阈值在-1024至1024亨氏单位, 并膨胀1-2个像素达到选择像素充满全部肠腔, 区域增长工具分割出直肠及乙状结肠, 升结肠, 横结肠及部分小肠, 去除冗余数据, 经MC(marching cubes)[22-27]算法计算建立肠道的三维数字模型. 面绘制模型以三角面片显示.
1.2.4 肠管空间毗邻关系: 在动脉期数据集重建骨骼系统, 动脉系统及皮肤, 前列腺三维模型. CTA血管造影技术使动脉显影, 密度造影剂和骨骼结构密度值相近. 按傅栋 et al[28]的方法建立骨性结构和动脉数字模型, 界定阈值在145-1061亨氏单位, Mimics软件自动形成各层面骨组织和动脉表面轮廓线, 图像经编辑处理, 去除无关边缘杂点和冗余数据, 经区域增长工具分割骨骼和动脉, 用Mimics软件二维, 三维修改工具及布尔计算分割后分别3D计算建立骨骼结构和动脉三维数字模型. 界定皮肤阈值在-718至-177亨氏单位建立皮肤三维数字模型. 在110层及82层二维图像分别手动分割出膀胱及前列腺, 3D计算建立膀胱及前列腺三维数字模型. 在静脉期数据集根据残余造影剂浓度重建输尿管三维模型, 阈值在220-1641亨氏单位, 经区域增长3D计算建立输尿管三维模型, 以STL格式导出在动脉期数据集根据输尿管和双肾及膀胱解剖结构关系行三维模型立体配对.
1.2.5 虚拟内镜: 对基于CT断层图像建立的肠管面绘制模型, 用虚拟内窥镜技术可对肠腔解剖和病变进行观察, 观看三角面片内部信息能够获得有效肠道内解剖图像和诊断信息. 可在二维平面图像进行大体观察来指导内镜重点观察目标, 给合多平面裁剪功能可以综合分析. 在肠腔内"漫游"可观察全结肠. 对观察到的病变对发现病变后, 变换视角、视距, 甚至反向观察. 返回到二维平面图像测量其最大径作为直径.
体数据应用体绘制光线投射(Ray-Casting)算法绘制出组织表面的真实感图像, 体绘制以体素作为基本单元, 直接由切片数据集生成三维体的图像, 能够较好地表示对象的内部信息, 并可从任意方向观看(图1).
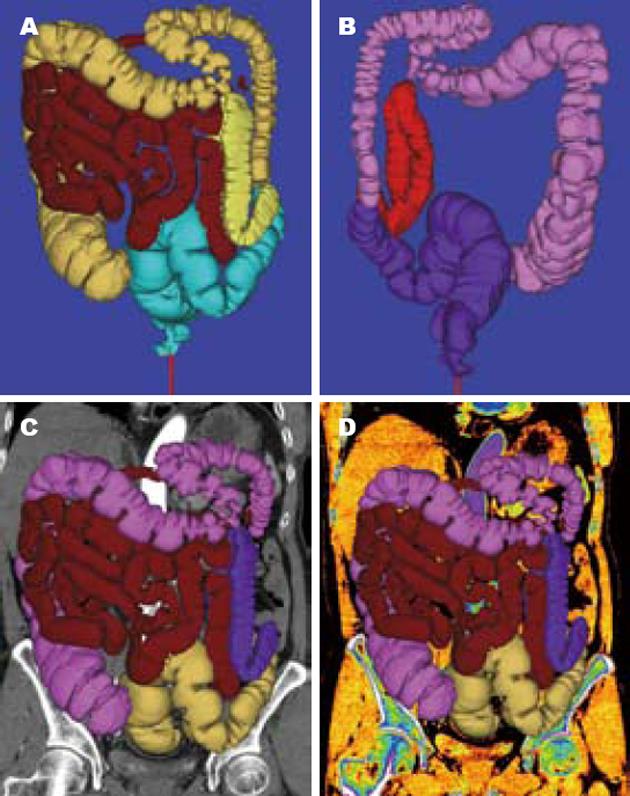
用面绘制MC算法对直肠, 肛管, 乙状结肠, 升结肠, 横结肠及部分小肠进行面绘制, 数字模型以三角面片表示(图2). 建立的模型几何外型逼真, 具有较佳的视觉效果, 可以多彩色、透明或任意组合显示, 整体清晰、实体感强. 通过不同平面的切面可以观察各组件的内部结构关系, 能够任意角度的旋转及缩放观察. 在同一平面上, 可用不同色彩分别显示直肠, 小肠、结肠等, 并根据需要, 从不同角度, 构建出所需绘制模型, 如结肠和部分小肠前面观(图2A), 结肠和直肠后面观(图2B), 结肠和部分小肠切面观等(图2C-D).
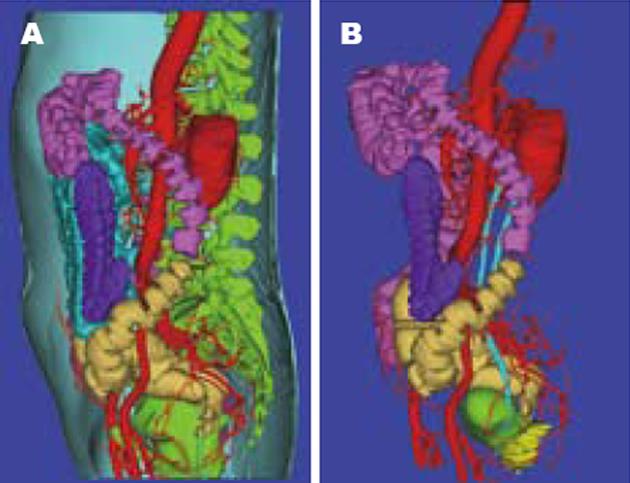
成功建立骨骼系统, 动脉系统及皮肤, 直肠, 结肠, 部分小肠, 输尿管, 膀胱和前列腺三维数字模型(图3). 并可从不同角度观看毗邻脏器的空间结构关系, 不同脏器用不同色彩展现, 便于分辨.
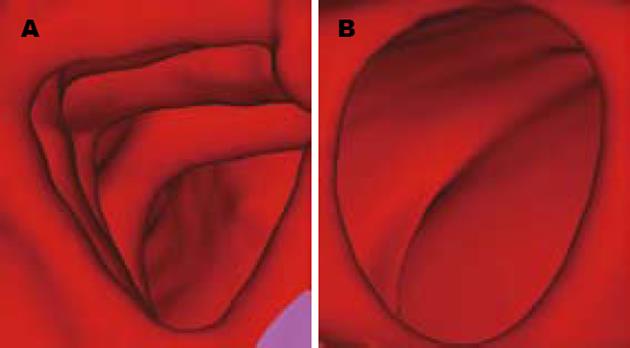
基于64层螺旋CT断层图像用虚拟内窥镜技术对肠腔的解剖和病变进行了观察. 能成功内镜样展现结肠的任何部位与转角处, 并能从狭窄、梗阻处两端观察肠腔的解剖和病变, 可靠地显示了病变部位和大小(图4). 动态显示可制作成AVI格式电影存储、输出, 画面清晰流畅.
可视化技术[29]是运用计算机图形学和图像处理技术, 把二维平面图像重构出具有立体效果的空间三维形态结构图像. 他涉及到计算机图形学、图像处理、计算机视觉、计算机辅助设计及人机交互技术等多个领域. 由于非侵入诊断技术如CT、MRI和正电子放射断层扫描(PET)的发展, 获得患者有关部位的二维断层图像变得很容易. 我们根据CT二维图像序列, 配合图像轮廓提取技术, 基于空气灌肠造影及CTA血管造影技术, 更精确还原骨骼, 肠管及动脉, 输尿管在活体内的原有真实结构形态, 简便、高效地建立直肠及周围结构三维模型. 以三维可视化的方式从不同角度进行展示, 可以根据需要设置不同的透明度, 透视观察骨骼结构, 动脉系统, 皮肤, 肠管, 输尿管, 膀胱, 前列腺的相互关系, 结合传统教材的图像与实体解剖, 能更好地理解真实的三维人体结构, 克服了解剖学教学中不能很好还原其真实解剖位置的不足, 是对传统教材中的完善和补充. 三维重建图像利于整体直观地显示病变, 帮助明确诊断并指导手术. 在可视化技术的基础上可以进一步实现计算机模拟及手术规划. 通过对人体器官的三维模型虚拟重建可加深对临床解剖学的理解, 是促进外科发展的有效途径. 肠管柔软易变形, 离体后不易定形, 其在人体的真实外形不易理解, 本研究以三维可视化的形式, 通过任意角度的旋转, 全方位显示直肠及其周围结构, 便于对周围结构的观察理解, 对临床医师理解掌握直肠周围结构的解剖关系有极大帮助.
虚拟内窥镜技术[30-33](VE)是计算机技术、计算机图形学、计算机图像处理尤其是虚拟现实等技术结合的一种独特医学图像后处理技术. 利用计算机专用软件, 将螺旋CT或MR获得的原始容积数据进行后处理, 对空腔器官内表面具有相同像素值范围部分进行三维重建, 利用计算机的模拟导航技术(navigation)或漫游技术(flythrough)进行腔内观察, 并赋予不同的光照强度和人工伪彩连续回放, 逼真地模拟腔道内窥镜直视观察肠腔的动态重建图像. 基于CT断层图像的虚拟内镜技术源于螺旋CT连续扫描获得的容积数据, 和传统的内窥镜技术相比, 虚拟内窥镜和CT工作站仿真内窥镜有着共同独特的优点: (1)无接触式无创性检查, 患者无不适感, 检查过程中不会产生穿孔、出血或感染等副作用; (2)常规的纤维镜存在视野的局限和无法评价腔外解剖与病变等缺点. 虚拟内窥镜可以从任意的角度和方位对病灶进行观察, 并能从狭窄、梗阻处两端观察肠腔的解剖和病变, 可靠地显示了病变部位和大小. 并能同时提供腔内腔外的情况; (3)可以针对不同要求, 制定不同的漫游计划, 任意地重复检查过程; (4)降低了医疗检查复杂性、危险性和医疗成本; (5)可用于教学目的, 可以三维可视化的方式从不同角度进行展示, 可以根据需要设置不同的透明度, 指导患者了解自己的病情.
CT或MR图像精度不够, 导致虚拟内窥镜图像分辨率不够理想; 不能反映器官腔内的真实颜色, 因此不能诊断黏膜的充血水肿及炎性病变; 肠腔内的扁平性病变、轻度渐进性长段的狭窄, 虚拟内窥镜的效果不够理想; 组织特异性较差, 不能采取标本活检, 或腔内介入性治疗; 会受肠道内残留气体或残留的粪便等影响, 产生伪影, 并可能有假阳性病灶产生. 这些都是VE的固有缺陷. 但由于虚拟内窥镜具有传统内镜不具备的独特优点, 无创性、简便性和灵活性使得他的应用很广泛, 也很有吸引力, 成为一个重要的医疗诊断和医疗普查的辅助手段. 相信随着医学三维成像技术的发展和虚拟内窥镜技术自身的发展, 虚拟内窥镜必将在越来越多的疾病诊断中占据着越来越重要的地位.
CT、MRI工作站对断层影像处理目的比较单一, 基于64层螺旋CTA断层数据集建立的三维重建模型为解剖教学、手术培训提供教学平台. 临床医师根据患者的数字化仿真模型, 可制订个体化术前规划和手术模拟.
戈之铮, 教授, 上海交通大学医学院附属仁济医院消化科
肠管柔软易变形, 其在人体的真实外形不易理解. 本研究以三维可视化的形式展示肠管, 对临床医师理解掌握结肠及其周围结构在体内的解剖关系有极大帮助.
基于医学图像进行三维重建己广泛应用于口腔生物力学、康复工骨生物力学等多个领域, 作为形态学、解剖学分析和力学分的基础. 文章将CT图像、MIMICS和有限元软件相结合, 并可以扩展到建立其他各个部位三维有限元模型, 进一步应用于临床和生物力学研究.
虚拟内窥镜具有传统内镜不具备的独特优点, 无创性、简便性和灵活性使得他的应用很广泛, 也很有吸引力, 成为一个重要的医疗诊断和医疗普查的辅助手段.
本文设计合理, 文字表达清晰, 研究结果为今后临床, 教学和科研打下了一定的基础.
编辑: 李军亮 电编:何基才
| 3. | Duan SY, Zhang DT, Lin QC, Wu YH. Clinical value of CT three-dimensional imaging in diagnosing gastrointestinal tract diseases. World J Gastroenterol. 2006;12:2945-2948. [PubMed] |
| 4. | Horton KM, Fishman EK. Current role of CT in imaging of the stomach. Radiographics. 2003;23:75-87. [PubMed] [DOI] |
| 5. | Ba-Ssalamah A, Prokop M, Uffmann M, Pokieser P, Teleky B, Lechner G. Dedicated multidetector CT of the stomach: spectrum of diseases. Radiographics. 2003;23:625-644. [PubMed] [DOI] |
| 6. | Patak MA, Mortele KJ, Ros PR. Multidetector row CT of the small bowel. Radiol Clin North Am. 2005;43:1063-1077, viii. [PubMed] [DOI] |
| 7. | Qalbani A, Paushter D, Dachman AH. Multidetector row CT of small bowel obstruction. Radiol Clin North Am. 2007;45:499-512, viii. [PubMed] [DOI] |
| 8. | Ramachandran I, Sinha R, Rajesh A, Verma R, Maglinte DD. Multidetector row CT of small bowel tumours. Clin Radiol. 2007;62:607-614. [PubMed] [DOI] |
| 11. | Liu S, Liao W, Yu Q, Cheng X, Dai N, Zhang X. [The development of a system for 3D reconstruction from DICOM data and collaborative visualization]. Shengwu Yixue Gongchengxue Zazhi. 2007;24:1152-1156. [PubMed] |
| 12. | Kling-Petersen T, Rydmark M. Modeling and modification of medical 3D objects. The benefit of using a haptic modeling tool. Stud Health Technol Inform. 2000;70:162-167. [PubMed] |
| 13. | Durand LG, Garcia D, Sakr F, Sava H, Cimon R, Pibarot P, Fenster A, Dumesnil JG. A new flow model for Doppler ultrasound study of prosthetic heart valves. J Heart Valve Dis. 1999;8:85-95. [PubMed] |
| 18. | Escott EJ, Rubinstein D. Free DICOM image viewing and processing software for your desktop computer: what's available and what it can do for you. Radiographics. 2003;23:1341-1357. [PubMed] [DOI] |
| 19. | Zhu XY, Fang CH, Bao SS, Quan XY, Zhong SZ. [Image segmentation and three-dimensional reconstruction of the liver based on 64-slice spiral CT scanning data]. Nanfang Yike Daxue Xuebao. 2008;28:345-347. [PubMed] |
| 20. | Cline HE, Dumoulin CL, Hart HR Jr, Lorensen WE, Ludke S. 3D reconstruction of the brain from magnetic resonance images using a connectivity algorithm. Magn Reson Imaging. 1987;5:345-352. [PubMed] [DOI] |
| 21. | Lee TY, Lin CH. Growing-cube isosurface extraction algorithm for medical volume data. Comput Med Imaging Graph. 2001;25:405-415. [PubMed] [DOI] |
| 22. | Wang K, Denney T, Morrison E, Vodyanoy V. Construction of volume meshes from computed tomography data. Conf Proc IEEE Eng Med Biol Soc. 2005;5:5168-5171. [PubMed] |
| 23. | Delibasis KS, Matsopoulos GK, Mouravliansky NA, Nikita KS. A novel and efficient implementation of the marching cubes algorithm. Comput Med Imaging Graph. 2001;25:343-352. [PubMed] [DOI] |
| 24. | Lesk VI, Sternberg MJ. 3D-Garden: a system for modelling protein-protein complexes based on conformational refinement of ensembles generated with the marching cubes algorithm. Bioinformatics. 2008;24:1137-1144. [PubMed] [DOI] |
| 25. | Teferi S. Visualization, volume and surface area calculation of three dimensional (3D) ultrasound images. Ethiop Med J. 2007;45:383-390. [PubMed] |
| 26. | Niu Q, Chi X, Leu MC, Ochoa J. Image processing, geometric modeling and data management for development of a virtual bone surgery system. Comput Aided Surg. 2008;13:30-40. [PubMed] [DOI] |
| 27. | Schreiner J, Scheidegger CE, Silva CT. High-quality extraction of isosurfaces from regular and irregular grids. IEEE Trans Vis Comput Graph. 2006;12:1205-1212. [PubMed] [DOI] |
| 28. | 傅 栋, 靳 安民. 应用CT断层图像快速构建人体骨骼有限元几何模型的方法. 中国组织工程研究与临床康复. 2007;11:1620-1623. |
| 29. | 陈 新, 陈 良琴, 徐 伟. 三维可视化技术及其在现代医学诊断中的应用. 中国高校科技与产业化(学术版). 2006;z1:306-309. |