修回日期: 2007-10-10
接受日期: 2007-10-28
在线出版日期: 2007-11-18
目的: 了解胰腺导管内乳头状黏液性肿瘤(IPMN)中MUC1, MUC2, MUC5AC及TFF1的表达意义.
方法: 采用免疫组织化学方法, 检测IPMN手术切除标本9例中MUC1, MUC2, MUC5AC及TFF1的表达, 分析不同组织学类型及不同性质IPMN之间黏液蛋白及TFF1表达的差异.
结果: MUC1表达率为44.4%, MUC2为66.7%, MUC5AC和TFF1为100%. 胃型IPMN黏液蛋白表达模式主要为MUC1-, MUC2-, MUC5AC+. 肠型IPMN为MUC1-, MUC2+, MUC5AC+. 嗜酸性细胞型IPMN为MUC1+, MUC2+, MUC5AC+. IPMN相关管状癌MUC1阳性, 胶质癌MUC2阳性. MUC5AC和TFF1共同表达, 在浸润癌中表达下降. 胃型IPMN常与其他类型IPMN同时出现并且不同上皮之间出现移行过渡, 提示胃型可能是其他类型IPMN的前期病变.
结论: 不同组织学亚型的IPMN具有不同的黏液蛋白表达模式. MUC1表达提示侵袭性生物学行为, MUC2与胶质癌浸润有关, MUC5AC与TFF1协同表达, 可能起保护作用.
引文著录: 何度, 张秀辉. 胰腺导管内乳头状黏液性肿瘤组织中MUC1, MUC2, MUC5AC和TFF1的表达意义. 世界华人消化杂志 2007; 15(32): 3423-3429
Revised: October 10, 2007
Accepted: October 28, 2007
Published online: November 18, 2007
AIM: To examine the expression of MUC1, MUC2, MUC5AC and TFF1 in intraductal papillary mucinous neoplasms (IPMNs) of the pancreas and its significance.
METHODS: Immunohistochemistry was used to detect the expression of MUC1, MUC2, MUC5AC and TFF1 in nine surgically resected specimens with different histological subtypes of IPMN.
RESULTS: The positive rates of MUC1, MUC2 and MUC5AC in all IPMNs were 44.4%, 66.7% and 100%, respectively. The common expression patterns of MUCs in different histological subtypes were: gastric type (MUC1-, MUC2-, MUC5AC+), intestinal type (MUC1-, MUC2+, MUC5AC+), and oncocytic type (MUC1+, MUC2+, MUC5AC+). Ductal type invasive carcinomas associated with IPMNs were MUC1+, whereas colloid carcinomas were MUC2+. MUC5AC and TFF1 were co-localized in IPMNs, and reduced expression appeared in invasive components. Gastric type IPMNs sometimes merged with other IPMN subtypes, and transition between different epithelia was present, implying that the gastric type might be a precursor of the other subtypes.
CONCLUSION: Different IPMN subtypes have their own MUC expression pattern. MUC1 suggests aggressive behavior, MUC2 is associated with colloid carcinoma, and MUC5AC and TFF1, which were co-expressed, might be protective factors.
- Citation: He D, Zhang XH. Expression of MUC1, MUC2, MUC5AC and TFF1 in intraductal papillary mucinous neoplasms of the pancreas and its significance. Shijie Huaren Xiaohua Zazhi 2007; 15(32): 3423-3429
- URL: https://www.wjgnet.com/1009-3079/full/v15/i32/3423.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v15.i32.3423
胰腺导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasm, IPMN)是发生在胰腺主导管或其主要分支导管的乳头状黏液分泌肿瘤[1], 占胰腺囊性肿瘤的第2位, 仅次于胰腺实性假乳头状肿瘤[2]. 其发病率自1990年代后期开始明显增加[3]. IPMN作为胰腺外分泌肿瘤的一种独特类型, 包括多种组织学形态及不同性质的肿瘤, 其导管起源、组织学形态、生物学行为及肿瘤发生途径与普通胰腺导管癌存在较大差别. IPMN的5年生存率(浸润型60%, 非浸润型100%)明显比普通胰腺导管癌高[4]. 黏液蛋白(mucin, MUC)是一类大分子量糖蛋白, 在正常生理状态下, 黏液蛋白的表达具有明确的组织特异性和时间特异性, 其表达稳态容易受到损伤因子的破坏. 黏液蛋白表达异常是许多炎症及肿瘤的显著特征, 在多种恶性肿瘤中, 黏液蛋白参与肿瘤的发生[5]. MUC1, MUC2及MUC5AC与IPMN关系密切, 对IPMN的诊断、鉴别、分型及生物学行为的提示具有重要作用. 三叶因子1(trefoil factor 1, TFF1)又称雌激素诱导蛋白pS2, 是三叶因子家族成员之一, 与黏液蛋白关系紧密. 人类TFF1直接与MUC5AC相互作用[6], 在正常胃肠道中TFF1与MUC5AC协同表达[7]. TFF1具有保护胃黏膜, 促进黏膜修复的功能[8], 还可能是肿瘤抑制基因[9]. 我们对IPMN进行临床病理分析, 目的在于了解不同类型IPMN中MUC1, MUC2, MUC5AC及TFF1的表达及意义, 并对TFF1及MUC5AC在IPMN中的关系进行探讨.
1998-2006年四川大学华西医院手术切除胰腺IPMN 9例, 按照WHO分类标准[1], 包括良性3例, 交界性1例, 恶性5例. 根据2005年国际专家组达成的IPMN组织学分型标准[10], 将病例分为胃型3例, 肠型4例和嗜酸性细胞型2例(本组病例中无胰胆管型). 由于在某些病例中存在一种以上的IPMN组织学类型, 因此将主要成分和次要成分同时列出, 另外将IPMN相关的浸润型癌成分也一并列出. 肿瘤周围正常胰腺组织5例作为正常对照. 患者年龄24-62(平均49.9)岁, 男5例, 女4例. 肿瘤部位: 胰腺头部6例, 尾部2例, 体部1例. 肿瘤最大直径1.2-9(平均4.41) cm. 大体多为囊性(7/9), 囊内容物为黏液, 其余2例表现为副胰管内新生物及胰管周变硬. 5例伴主胰管扩张, 2例无扩张, 2例主胰管有无扩张不清楚. 临床表现以腹痛、腹胀及腹部不适最常见(5例), 其次为腰背部胀痛不适或慢性腹泻. 2例无IPMN的相关症状, 其中1例是在行胃癌胃大部切除时, 术中发现脾动脉干处一"肿大淋巴结". 病理检查显示其来源胰腺的囊性肿瘤, 另1例为B超体检时意外发现胰腺后方占位. IPMN常伴胰外器官肿瘤, 本组中2例合并胰外器官肿瘤, 其中1例伴有十二指肠PJ息肉(临床诊断为Peutz-Jeghers综合征), 另1例伴胃窦癌(表1).
| 编号 | 年龄 | 性别 | 肿瘤部位 | 大体 | 大小(cm) | 主胰管扩张 | 相关症状 | 病理类型(WHO) | 胰外肿瘤 |
| 1 | 24 | 女 | 头 | 囊性 | 5 | 是 | 腹痛7 mo | 导管内乳头状黏液瘤 | 肠PJ息肉 |
| 2 | 56 | 男 | 头 | 副胰管内新生物 | 1.2 | 无 | 导管内乳头状黏液瘤 | 胃窦癌 | |
| 3 | 50 | 男 | 头 | 胰管周质硬 | 1.5 | 是 | 腹痛 | 导管内乳头状黏液瘤 | |
| 4 | 51 | 男 | 头 | 囊性 | 3 | 是 | 腹泻14 mo | 交界性导管内乳头状黏液瘤 | |
| 5 | 40 | 男 | 尾 | 囊性 | 9 | 否 | 腹痛6 mo | 浸润型导管内乳头状黏液癌 | |
| 6 | 62 | 男 | 头 | 囊性 | 5 | 腹胀3 mo | 浸润型导管内乳头状黏液癌 | ||
| 7 | 62 | 女 | 尾 | 囊性 | 8 | 否 | 无 | 浸润型导管内乳头状黏液癌 | |
| 8 | 48 | 女 | 体 | 囊性 | 2 | 是 | 腹部不适72 mo | 浸润型导管内乳头状黏液癌 | |
| 9 | 52 | 女 | 头 | 囊性 | 5 | 是 | 腰背部痛5 mo | 浸润型导管内乳头状黏液癌 |
采用免疫组化LsAB法. 标本经中性甲醛固定, 石蜡包埋, 切片厚4 μm. 分别进行HE染色及免疫组织化学标记, 其中1例进行AB-PAS染色. 切片常规脱蜡梯度水化, 过氧化氢处理切片25 min, 抗原修复, 血清封闭, 滴加一抗(表2). 一抗37℃孵育2 h, PBS洗片, 二三抗使用北京中杉金桥生物有限公司SP-9002试剂盒, 孵育时间均为45 min. PBS洗片, DAB显色, 苏木素复染, 脱水, 中性树胶封片. PBS代替一抗作为空白对照. MUC1及MUC5AC定位于细胞质和或细胞膜, MUC2及TFF1定位于细胞质; 阳性细胞数<10%为阴性, ≥10%为阳性. 细胞染色结果按照阳性强度分级: -(阴性), +(弱阳性), ++(中等强度阳性), +++(强阳性). 细胞外黏液染色强度按照阳性面积百分比分级: -(阴性), +(<1/3阳性), ++(1/3-2/3阳性), +++(>2/3阳性).
| 一抗 | 克隆类型 | 克隆系 | 工作浓度 | 抗原修复方法 | 购买公司 | 阳性对照组织 |
| MUC1 | 鼠抗人mAb | Ma695 | 即用型 | 高压锅; 枸櫞酸缓冲液; pH = 6.0 | 北京中杉金桥生物有限公 司(Zymed公司产品) | 乳腺癌 |
| MUC2 | 鼠抗人mAb | Ccp58 | 即用型 | 高压锅; 枸櫞酸缓冲液; pH = 6.0 | 北京中杉金桥生物有限公 司(Zymed公司产品) | 十二指肠 |
| MUC5AC | 鼠抗人mAb | 45M1 | 即用型 | 高压锅; 枸櫞酸缓冲液; pH = 6.0 | 福州迈新生物技术开 发有限公司 | 胃 |
| TFF1 | 鼠抗人mAb | BC04 | 1∶50 | 100℃水浴; EDTA缓冲液; pH = 9.0 | 北京中杉金桥生物有限公 司(Zymed公司产品) | 已知阳性乳腺癌 |
IPMN的组织学亚型分别为: 胃型3例, 肠型4例(包括2例肠型+胃型), 嗜酸性细胞型2例(包括1例嗜酸性细胞型+胃型). 4例为良性及交界性, 5例为恶性浸润型, 与IPMN相关的浸润成分为胶质癌(3/5)和管状癌(2/5)(表3).
| 编号 | IPMN类 型(WHO) | 肿瘤组 织学构成 | MUC1 | MUC2 | MUC5AC | TFF1 | |||||
| 胞膜 | 胞质 | 胞外黏液 | 胞质 | 胞外黏液 | 胞膜 | 胞质 | 胞外黏液 | 胞质 | |||
| 1 | 瘤 | 胃型IPMN | - | - | - | - | - | +++ | ++ | +++ | +++ |
| 2 | 瘤 | 胃型IPMN | - | - | - | - | - | +++ | +++ | +++ | +++ |
| 3 | 瘤 | 肠型(主)+ 胃型(次)IPMN | - | - | - | -/+++ | - | +++ | +++ | +++ | +++ |
| 4 | 交界性 | 肠型IPMN | - | - | - | +++ | - | - | +++ | +++ | +++ |
| 5 | 浸润型癌 | 胃型IPMN | +++ | - | ++ | - | - | +++ | ++ | +++ | +++ |
| 管状癌(高中分化) | +++ | + | ++ | - | - | -~+++ | -~+++ | +++ | -~+++ | ||
| 6 | 浸润型癌 | 肠型IPMN | - | - | - | +++ | + | +++ | +++ | ++ | +++ |
| 胶质癌 | - | - | - | +++ | - | -~+++ | -~+ | + | -~+++ | ||
| 7 | 浸润型癌 | 肠型(主)+胃型(次)IPMN | - | -~++ | - | +~+++ | - | +++ | +++ | +++ | +++ |
| 管状癌(中低分化) | -~++ | -~++ | - | -~+ | - | -~+++ | -~+ | +++ | -~+++ | ||
| 8 | 浸润型癌 | 嗜酸性细胞型IPMN | - | ++ | - | +++ | - | +++ | -~++ | +++ | +++ |
| 胶质癌 | - | - | - | +++ | - | +++ | ++ | +++ | +++ | ||
| 9 | 浸润型癌 | 嗜酸性细胞型(主) +胃型(次)IPMN | - | +++ | - | +++ | - | +++ | +++ | +++ | +++ |
| 胶质癌 | - | - | - | +++ | - | +++ | +++ | +++ | +++ | ||
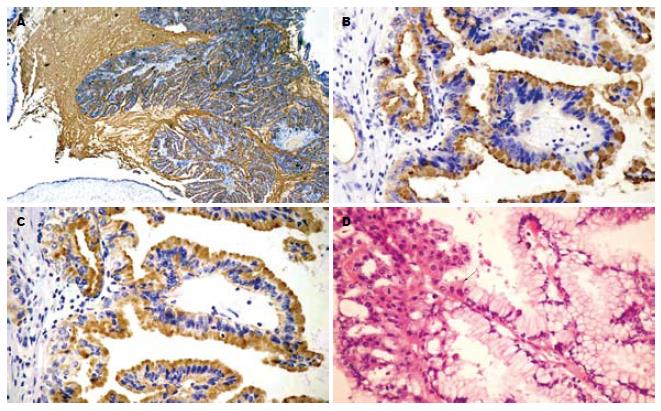
MUC1表达率为44.4%(4/9), 均为浸润型IPMN, 包括1例胃型, 1例嗜酸性细胞型, 1例嗜酸性细胞型+胃型及1例肠型+胃型, 良性和交界性病变不表达. MUC1在高中分化的浸润管状癌的顶端细胞膜上呈中-强阳性表达, 并出现胞质阳性表达. 低分化癌MUC1胞质表达增强呈中等强度阳性, 1例出现细胞外黏液阳性, 3例IPMN相关胶质癌MUC1呈阴性. MUC1在嗜酸性细胞型IPMN的胞质中呈中-强阳性表达, 细胞膜呈阴性表达. 正常胰腺组织内的小叶间导管及小叶内导管的上皮细胞顶端细胞膜MUC1呈细线状表达, 胞质阴性. MUC2阳性率为66.7%(6/9), 2例(2/4)为良性和交界性, 4例(4/5)为浸润型, 阳性信号定位于细胞质. 细胞膜及细胞外黏液(除1例外)均未见表达. 阳性IPMN包括2例肠型, 2例肠型+胃型, 1例嗜酸性细胞型及1例嗜酸性细胞型+胃型. 在1例良性肠型+胃型IPMN中, 肠型区域呈低乳头状生长, MUC2呈强阳性, 胃型区域MUC1和MUC2呈阴性. 浸润性管状癌呈阴性或部分阳性表达, 胶质癌(3/3)均呈强阳性表达. MUC2在正常胰腺的小叶间导管及小叶内导管均不表达. 所有IPMN呈MUC5AC阳性表达, 阳性定位于细胞质、顶端细胞膜及细胞外黏液(图1A). 然而管状浸润癌的表达下降, 部分低分化癌表达丧失. MUC5AC在正常胰腺的小叶间导管及小叶内导管上皮细胞中呈阴性或个别细胞质阳性. TFF1在所有IPMN的细胞质呈强阳性表达, 2例管状癌及1例胶质癌中表达部分丧失, 正常胰腺小叶间导管及小叶内导管上皮细胞呈阴性或个别上细胞阳性, 增生性病变呈阳性表达. TFF1与MUC5AC在表达强度和表达的细胞类型上具有相似性(图1B-C).
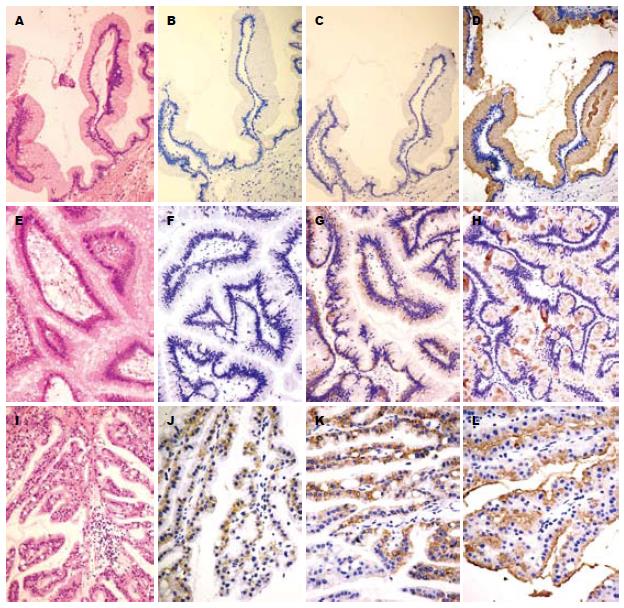
胃型IPMN多为良性病变, 常与其他类型IPMN同时出现, 某些区域的不同上皮细胞之间出现移行过渡(图1D), 提示胃型是其他类型的前体病变. 单纯胃型IPMN黏液蛋白表达模式主要为MUC1-, MUC2-, MUC5AC+(图2A-D). 肠型IPMN为MUC1-, MUC2+, MUC5AC+(图2E-H). 嗜酸性细胞型IPMN为MUC1+, MUC2+, MUC5AC+(图2I-L). 当肿瘤发生癌浸润时, 胃型IPMN出现MUC1表达.
近年来胰腺导管內乳头状黏液性肿瘤逐渐被认识, 在我国并不常见. Sohn et al[3]回顾了1987-2003年Johns Hopkins Hospital因IPMN手术切除病例136例, 发现自1990年代末期以后IPMN的发病率明显增加. 过去常将其归为胰腺黏液性囊性肿瘤(mucinous cystic neoplasm, MCN). 两者形态学相似, 但胰腺黏液性囊性肿瘤几乎均发生在女性, 位于胰腺体尾部, 卵巢型间质(ovarian-type stroma, OS)是目前区别两者的严格组织学指标[11]. 胰腺上皮内肿瘤(pancreatic intraepithelial neoplasia, PanIN)常发生于直径≤5 mm的导管[12], 常形成乳头状结构, 但高级别PanINs常进展成为恶性程度较高的胰腺导管癌(pancreatic ductal adenocarcinoma, PDAC). IPMN, MCN和PanIN均包括不同级别的病变, 在生物学行为及遗传学上具有异同, 3者都是侵袭性胰腺导管癌的癌前病变[13]. 黏液蛋白(mucin, MUC)是一类大分子糖蛋白, 在正常消化道、呼吸道及生殖道的上皮中广泛表达, 迄今为止已发现19种人类黏液蛋白[5]. 根据结构特点和生理学功能, 黏液蛋白分为两大类: 分泌型(secreted)和膜结合型(membrane-bound)[5]. 其分布具有器官、组织及时间特异性. 在疾病状态下, MUC异常表达或异常糖基化. 在肿瘤的演进过程中, MUC影响细胞的生长、分化、黏附、运动和机体的免疫监视功能. IPMN具有4种组织学亚型: 胃型、肠型、胰胆管型和嗜酸性细胞型. 每种亚型具有各自独特的MUC表达模式, 除形态学标准外, 2005年制定的新分型标准将MUC作为另一重要的辅助诊断标准, 不同组织学类型代表不同级别的IPMN[10].
MUC1是一种膜结合型黏液蛋白, 表达于正常乳腺上皮顶端细胞膜, 维持腺腔结构的稳定性[14], 在正常胰腺小叶间导管及小叶内导管的上皮细胞顶部呈细线状表达. 过表达MUC1导致细胞转化, 抑制损伤诱导的细胞凋亡[14-15]. MUC1削弱E-cadherin介导的细胞与细胞之间的黏附[16], 参与肿瘤浸润. 过表达MUC1使肿瘤细胞逃避细胞毒性效应细胞的杀伤作用[17]. MUC1阳性常见于胰胆管型和嗜酸性细胞型IPMN[18], 胃型及肠型MUC1常呈阴性[18], 当进展为管状浸润癌时, MUC1常为阳性[13]. 本组中2例浸润型IPMN的浸润成分为管状癌, 均有不同程度MUC1表达. 高-中分化管状癌的腺管上皮细胞顶端呈强阳性表达, 胞质呈阴性或弱阳性表达, 低分化癌胞质表达增强, 呈中等强度阳性. 2例嗜酸性细胞型IPMN, MUC1呈细胞质内中-强阳性表达, 细胞膜不表达, 提示此型为高级别肿瘤.
MUC2为分泌型黏液蛋白, 正常组织的杯状细胞高表达, 在正常胰腺的小叶间导管和小叶内导管不表达. 当MUC2基因敲除后, 小鼠发生胃肠道的腺瘤及腺癌, 提示MUC2是一种肿瘤抑制因子[19]. MUC2在肠型IPMN中常为阳性, 而MUC2在PanIN及胰腺导管癌中几乎不表达[13]. 除散在的杯状细胞外, MCNs不表达MUC2[20], 说明MUC2是IPMN的诊断、分型及提示生物学行为的重要指标. 嗜酸性细胞型IPMN非常少见, MUC2的表达情况各家报道不一. Terris et al[21]报道此型IPMN缺乏MUC2表达, 但Luttges et al[22]发现MUC1及MUC2均表达. 本组中4例肠型IPMN和2例嗜酸性细胞型IPMN均呈阳性表达, 3例IPMN相关性胶质癌MUC2呈强阳性表达, 而MUC1阴性. 由于胰腺胶质癌的预后明显较胰腺导管癌好, 两者MUC1和MUC2的表达模式恰恰相反, 因此Adsay et al[13]提出MUC1和MUC2代表两种不同的肿瘤演进方式: MUC2是"惰性"途径标志(代表IPMN和胶质癌), MUC1是"侵袭性"途径标志(代表从PanIN到导管腺癌). 本组中, 2例浸润型IPMN由肠型和胃型混合构成, 1例浸润型IPMN由嗜酸性细胞型和胃型(胃型MUC1+, MUC2+)混合构成. 随着肿瘤级别增高, 胃型IPMN出现MUC1及MUC2的表达, 提示胃型可能是其他类型IPMN的前期病变.
MUC5AC为胃型黏液蛋白, 与MUC2同属于分泌型黏液蛋白, 导管上皮细胞不表达或仅少数细胞表达. Jinfeng et al[23]发现浸润型胰腺导管癌的MUC5AC阳性表达率为63.6%, MUC5AC失表达与淋巴结转移和血管浸润相关, MUC5AC阳性病例的预后较好. 本研究9例IPMN均为阳性, 阳性率与其他报道一致[22-24]. 与IPMN相关的1例胶质癌及2例管状浸润癌部分区域MUC5AC表达丧失, 分化越低MUC5AC丧失越明显. 在所有病例中均发现肿瘤细胞外黏液MUC5AC强表达. 以上结果提示MUC5AC可能具有抑制肿瘤侵袭的功能.
TFF1在正常胃黏膜、慢性浅表性胃炎及胃溃疡中全部表达, 在不典型增生胃黏膜的表达率下降, 胃癌阳性率仅为20%[25]. Lefebvre et al[9]研究发现所有TFF1纯合子突变小鼠发生了胃窦幽门腺瘤, 30%小鼠发生上皮内或黏膜内癌, 提示TFF1可能是肿瘤抑制基因. Madsen et al[26]检测到正常胰腺组织中有中等水平TFF1 mRNA表达. TFF1蛋白在慢性胰腺炎导管上皮细胞中均呈强阳性[27], 在PanINs中随着其级别增高TFF1表达率降低[28], 在胰腺导管癌中仅半数表达TFF1[29]. 利用基因芯片技术已检测到IPMN存在多种基因表达异常, 其中TFF1和MUC5AC基因显著上调[30-31]. 人类TFF1能与MUC5AC结合, 稳定MUC5AC[6]. 我们通过免疫组化检测发现TFF1蛋白在正常导管中不表达或仅少数上皮细胞表达, IPMN的TFF1阳性率为100%. 在IPMN相关的2例管状癌及1例胶质癌中部分区域TFF1表达丧失, 其表达丧失区域与MUC5AC表达丧失区域的部位相似, 集中在低分化癌处, 提示TFF1与MUC5AC协同参与胰腺IPMN的发生, 共同抑制肿瘤侵袭.
我们的研究证实, 不同组织学亚型的IPMN具有其特有的黏液蛋白表达模式. MUC1是提示浸润型IPMN的有用指标, 与管状侵袭成分相关. MUC2提示"惰性"侵袭途径, 是肠型IPMN及胶质癌的标记, 且嗜酸性细胞型IPMN同样可表达. MUC5AC与TFF1共同表达于所有IPMN, 在浸润癌中表达不同程度丧失, 对机体而言两者可能是保护因素. 但TFF1与MUC5AC在IPMN中具体作用机制以及功能尚不清楚, 有待进一步深入研究.
胰腺导管内乳头状黏液性肿瘤(IPMN)是发生在胰腺主导管或其主要分支导管的乳头状黏液分泌肿瘤, 近20年来被逐渐认识. IPMN是胰腺外分泌肿瘤的一种独特类型, 包括多种组织学形态和不同性质的肿瘤, 其5年生存率显著高于普通胰腺导管癌. 目前IPMN被认为是侵袭性胰腺癌的癌前病变之一, 但其肿瘤发生途径与胰腺上皮内肿瘤-导管癌的途径不完全相同. 黏液蛋白(MUC)免疫组化研究发现不同组织学亚型的IPMN存在不同的表达模式, 并且在鉴别胰腺囊性肿瘤及提示肿瘤生物学行为方面具有重要作用.
本文验证了MUC1, MUC2, MUC5AC及TFF1在不同组织学亚型IPMN中的表达意义, 观察到胃型IPMN与其他类型IPMN在组织学上存在移行过渡, 并发现TFF1与MUC5AC的表达具有一致性.
不同组织学亚型的IPMN存在不同的MUC表达模式, MUC1与管状浸润癌有关, MUC2与胶质癌浸润有关. TFF1与MUC5AC在IPMN中高表达, 两者表达的区域一致. 对机体而言两者可能是保护因素, 但有待于进一步深入研究.
本文内容详尽, 资料丰富, 对提高胰腺癌的认识具有重要意义, 有一定的可读性.
编辑: 程剑侠 电编:郭海丽
| 1. | Organization classification of tumours. Pathology and genetics of tumors of the digestive system. Lyon: IRAC Press 2000; 237-240. |
| 2. | Kosmahl M, Pauser U, Peters K, Sipos B, Luttges J, Kremer B, Kloppel G. Cystic neoplasms of the pancreas and tumor-like lesions with cystic features: a review of 418 cases and a classification proposal. Virchows Arch. 2004;445:168-178. [PubMed] |
| 3. | Sohn TA, Yeo CJ, Cameron JL, Hruban RH, Fukushima N, Campbell KA, Lillemoe KD. Intraductal papillary mucinous neoplasms of the pancreas: an updated experience. Ann Surg. 2004;239:788-797; discussion 797-799. [PubMed] |
| 4. | Salvia R, Fernandez-del Castillo C, Bassi C, Thayer SP, Falconi M, Mantovani W, Pederzoli P, Warshaw AL. Main-duct intraductal papillary mucinous neoplasms of the pancreas: clinical predictors of malignancy and long-term survival following resection. Ann Surg. 2004;239:678-685; discussion 685-687. [PubMed] |
| 5. | Andrianifahanana M, Moniaux N, Batra SK. Regulation of mucin expression: mechanistic aspects and implications for cancer and inflammatory diseases. Biochim Biophys Acta. 2006;1765:189-222. [PubMed] |
| 6. | Ruchaud-Sparagano MH, Westley BR, May FE. The trefoil protein TFF1 is bound to MUC5AC in human gastric mucosa. Cell Mol Life Sci. 2004;61:1946-1954. [PubMed] |
| 7. | Longman RJ, Douthwaite J, Sylvester PA, Poulsom R, Corfield AP, Thomas MG, Wright NA. Coordinated localisation of mucins and trefoil peptides in the ulcer associated cell lineage and the gastrointestinal mucosa. Gut. 2000;47:792-800. [PubMed] |
| 8. | Taupin D, Podolsky DK. Trefoil factors: initiators of mucosal healing. Nat Rev Mol Cell Biol. 2003;4:721-732. [PubMed] |
| 9. | Lefebvre O, Chenard MP, Masson R, Linares J, Dierich A, LeMeur M, Wendling C, Tomasetto C, Chambon P, Rio MC. Gastric mucosa abnormalities and tumorigenesis in mice lacking the pS2 trefoil protein. Science. 1996;274:259-262. [PubMed] |
| 10. | Furukawa T, Kloppel G, Volkan Adsay N, Albores-Saavedra J, Fukushima N, Horii A, Hruban RH, Kato Y, Klimstra DS, Longnecker DS. Classification of types of intraductal papillary-mucinous neoplasm of the pancreas: a consensus study. Virchows Arch. 2005;447:794-799. [PubMed] |
| 11. | Tanaka M, Chari S, Adsay V, Fernandez-del Castillo C, Falconi M, Shimizu M, Yamaguchi K, Yamao K, Matsuno S. International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology. 2006;6:17-32. [PubMed] |
| 12. | Hruban RH, Takaori K, Klimstra DS, Adsay NV, Albores-Saavedra J, Biankin AV, Biankin SA, Compton C, Fukushima N, Furukawa T. An illustrated consensus on the classification of pancreatic intraepithelial neoplasia and intraductal papillary mucinous neoplasms. Am J Surg Pathol. 2004;28:977-987. [PubMed] |
| 13. | Adsay NV, Merati K, Andea A, Sarkar F, Hruban RH, Wilentz RE, Goggins M, Iocobuzio-Donahue C, Longnecker DS, Klimstra DS. The dichotomy in the preinvasive neoplasia to invasive carcinoma sequence in the pancreas: differential expression of MUC1 and MUC2 supports the existence of two separate pathways of carcinogenesis. Mod Pathol. 2002;15:1087-1095. [PubMed] |
| 14. | Li Y, Liu D, Chen D, Kharbanda S, Kufe D. Human DF3/MUC1 carcinoma-associated protein functions as an oncogene. Oncogene. 2003;22:6107-6110. [PubMed] |
| 15. | Yin L, Li Y, Ren J, Kuwahara H, Kufe D. Hu-man MUC1 carcinoma antigen regulates intracellular oxidant levels and the apoptotic response to oxidative stress. J Biol Chem. 2003;278:35458-35464. [PubMed] |
| 16. | Wesseling J, van der Valk SW, Hilkens J. A mechanism for inhibition of E-cadherin-mediated cell-cell adhesion by the membrane-associated mucin episialin/MUC1. Mol Biol Cell. 1996;7:565-577. [PubMed] |
| 17. | van de Wiel-van Kemenade E, Ligtenberg MJ, de Boer AJ, Buijs F, Vos HL, Melief CJ, Hilkens J, Figdor CG. Episialin (MUC1) inhibits cytotoxic lymphocyte-target cell interaction. J Immunol. 1993;151:767-776. [PubMed] |
| 18. | Adsay NV, Merati K, Basturk O, Iacobuzio-Donahue C, Levi E, Cheng JD, Sarkar FH, Hruban RH, Klimstra DS. Pathologically and biologically distinct types of epithelium in intraductal papillary mucinous neoplasms: delineation of an "intestinal" pathway of carcinogenesis in the pancreas. Am J Surg Pathol. 2004;28:839-848. [PubMed] |
| 19. | Velcich A, Yang W, Heyer J, Fragale A, Nicholas C, Viani S, Kucherlapati R, Lipkin M, Yang K, Augenlicht L. Colorectal cancer in mice genetically deficient in the mucin Muc2. Science. 2002;295:1726-1729. [PubMed] |
| 20. | Luttges J, Feyerabend B, Buchelt T, Pacena M, Kloppel G. The mucin profile of noninvasive and invasive mucinous cystic neoplasms of the pancreas. Am J Surg Pathol. 2002;26:466-471. [PubMed] |
| 21. | Terris B, Dubois S, Buisine MP, Sauvanet A, Ruszniewski P, Aubert JP, Porchet N, Couvelard A, Degott C, Flejou JF. Mucin gene expression in intraductal papillary-mucinous pancreatic tumours and related lesions. J Pathol. 2002;197:632-637. [PubMed] |
| 22. | Luttges J, Zamboni G, Longnecker D, Kloppel G. The immunohistochemical mucin expression pattern distinguishes different types of intraductal papillary mucinous neoplasms of the pancreas and determines their relationship to mucinous noncystic carcinoma and ductal adenocarcinoma. Am J Surg Pathol. 2001;25:942-948. [PubMed] |
| 23. | Jinfeng M, Kimura W, Hirai I, Sakurai F, Moriya T, Mizutani M. Expression of MUC5AC and MUC6 in invasive ductal carcinoma of the pancreas and relationship with prognosis. Int J Gastrointest Cancer. 2003;34:9-18. [PubMed] |
| 24. | Handra-Luca A, Flejou JF, Rufat P, Corcos O, Belghiti J, Ruszniewski P, Degott C, Bedossa P, Couvelard A. Human pancreatic mucinous cystadenoma is characterized by distinct mucin, cytokeratin and CD10 expression compared with intraductal papillary-mucinous adenoma. Histopathology. 2006;48:813-821. [PubMed] |
| 26. | Madsen J, Nielsen O, Tornoe I, Thim L, Holmskov U. Tissue localization of human trefoil factors 1, 2, and 3. J Histochem Cytochem. 2007;55:505-513. [PubMed] |
| 27. | Ebert MP, Hoffmann J, Haeckel C, Rutkowski K, Schmid RM, Wagner M, Adler G, Schulz HU, Roessner A, Hoffmann W. Induction of TFF1 gene expression in pancreas overexpressing transforming growth factor alpha. Gut. 1999;45:105-111. [PubMed] |
| 28. | Prasad NB, Biankin AV, Fukushima N, Maitra A, Dhara S, Elkahloun AG, Hruban RH, Goggins M, Leach SD. Gene expression profiles in pancreatic intraepithelial neoplasia reflect the effects of Hedgehog signaling on pancreatic ductal epithelial cells. Cancer Res. 2005;65:1619-1626. [PubMed] |
| 29. | Collier JD, Bennett MK, Bassendine MF, Lendrum R. Immunolocalization of pS2, a putative growth factor, in pancreatic carcinoma. J Gastroenterol Hepatol. 1995;10:396-400. [PubMed] |
| 30. | Terris B, Blaveri E, Crnogorac-Jurcevic T, Jones M, Missiaglia E, Ruszniewski P, Sauvanet A, Lemoine NR. Characterization of gene expression profiles in intraductal papillary-mucinous tumors of the pancreas. Am J Pathol. 2002;160:1745-1754. [PubMed] |
| 31. | Sato N, Fukushima N, Maitra A, Iacobuzio-Donahue CA, van Heek NT, Cameron JL, Yeo CJ, Hruban RH, Goggins M. Gene expression profiling identifies genes associated with invasive intraductal papillary mucinous neoplasms of the pancreas. Am J Pathol. 2004;164:903-914. [PubMed] |