修回日期: 2005-08-20
接受日期: 2005-08-26
在线出版日期: 2005-11-28
目的: 通过观察愈肝胶囊对2.2.15细胞分泌的HBsAg、HBeAg及HBV DNA的影响, 探讨在体外水平上愈肝胶囊的抗乙肝病毒作用.
方法: 将实验家兔(n = 6)随机分为3组: 正常血清组、乙肝宁颗粒组、愈肝胶囊组, 分别灌服洁净生理盐水5 mL/次, 乙肝宁颗粒3.4 g/(kg•d), 愈肝胶囊 0.7 g/(kg•d), 3次/d. 测定含不同浓度愈肝胶囊血清抗HBV活性情况. 2.2.15细胞培养上清液HBsAg、HBeAg测定采用ELISA法, HBV DNA检测采用PCR杂交试验法.
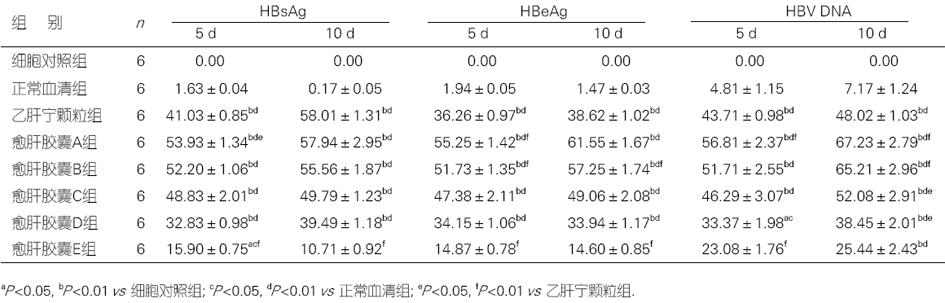
结果: 作用5 d时, 与乙肝宁颗粒组比较, 含愈肝胶囊血清1∶1组抗HBV作用优于乙肝宁颗粒组(HBsAg: 53.93±1.34 vs 41.03±0.85, P<0.05; HBeAg: 55.25±1.42 vs 36.26±0.97, P<0.01; HBV DNA: 56.81±2.37 vs 43.71±0.98, P<0.01); 1∶2组、1∶4组、1∶8组差异无显著性; 1∶16组则作用较乙肝宁颗粒组低. 药物作用10 d时, 与细胞对照组及正常血清组比较, 各含愈肝胶囊血清组抗HBV作用均比较显著. 与乙肝宁颗粒组比较, 含愈肝胶囊血清1∶1组抗HBV DNA作用优于乙肝宁颗粒组(67.23±2.79 vs 48.02±1.03, P<0.05); 1∶2组和1∶4组对HBeAg及HBV DNA的作用优于乙肝宁颗粒组; 1∶8组和1∶16组对HBV DNA作用低于乙肝宁颗粒组.
结论: 含愈肝胶囊血清在体外细胞培养中对2.2.15细胞分泌HBsAg、HBeAg及HBV DNA均有较好的抑制作用, 其抑制作用随其浓度增大而增强.
引文著录: 高萍, 程留芳, 谢朝良. 愈肝胶囊体外抗乙型肝炎病毒的作用. 世界华人消化杂志 2005; 13(22): 2693-2696
Revised: August 20, 2005
Accepted: August 26, 2005
Published online: November 28, 2005
AIM: To investigate the anti-hepatitis B virus effect of Yugan capsule in vitro.
METHODS: The experimental rabbits (n = 6) were randomly divided into 3 groups (2 for each), and then were treated with the normal serum, Yiganning granule and Yugan capsule, respectively. The blood samples were collected from the hearts and diluted into various concentrations. The effects of the serums on the 2.2.15 cell line were observed. Enzyme linked immunosorbent assay was used to detect the the contents of HBsAg and HBeAg, and polymerase chain reaction and hybridization were used to determine the contents of HBV DNA.
RESULTS: Five days after treatment, Yugan capsule of 1∶1 group had significant anti-HBV effect in comparison with Yiganning granule (HBsAg: 53.93±1.34 vs 41.03±0.85, P < 0.05; HBeAg: 55.25±1.42 vs 36.26±0.97, P < 0.01; HBV DNA: 56.81±2.37 vs 43.71±0.98, P < 0.01), while Yugan capsule of 1∶2, 1∶4, and 1∶8 group was not markedly different, and that of 1∶16 group had less anti-HBV effect. Ten days after treatment, Yugan capsule of different concentrations inhibited the proliferation of HBV significantly in comparison with cell control and normal serum group, while in comparison with Yiganning granule, Yugan capsule of 1∶1 group notably inhibited the replication of HBV DNA (67.23±2.79 vs 48.02±1.03, P < 0.05). Also Yugan capsule of 1∶2 and 1∶4 group was superior to Yiganning granule in inhibiting the secretion of HBeAg and replication of HBV DNA, but that of 1∶8 and 1∶16 group was inferior to Yiganning.
CONCLUSION: Yugan capsule serum can inhibit the secretion of HBsAg, HBeAg, and replication of HBV DNA in 2.2.15 cells cultured in vitro in a concentration-depended manner.
- Citation: Gao P, Cheng LF, Xie CL. Inhibitory effect of Yugan capsule on hepatitis B virus in vitro. Shijie Huaren Xiaohua Zazhi 2005; 13(22): 2693-2696
- URL: https://www.wjgnet.com/1009-3079/full/v13/i22/2693.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v13.i22.2693
乙型肝炎(hepatitis B)是乙型肝炎病毒(HBV)引起的一种严重的世界范围内危害人类健康的疾病. 中医药辨病与辨证相结合, 多途径, 多层次, 整体调控, 在乙型肝炎的治疗中发挥着独特的优势. 本实验应用中药含药血清药理学研究方法, 通过严格的体外实验. 对愈肝胶囊治疗乙肝的有效性进行进一步探讨.
1.1.1 实验动物: 取纯种♂日本大耳白兔6只, 体质量约3 kg, 由泸州医学院实验动物中心提供.
1.1.2 药物: 愈肝胶囊每克含生药14.7 g, 处方主要由茵陈、栀子、黄芪、党参、丹参、白术、虎杖等药组成. 泸州医学院附属第二医院制剂室生产, 批号: 990815; 乙肝宁颗粒 17克/包, 广西半宙制药股份有限公司生产, 批号: 22-5010-桂卫药准字(1990)第079023号.
1.1.3主要试剂: 2.2.15细胞株(由重庆医科大学病毒性肝炎研究所提供)、RPMI-1640培养基(Gibco BRL Co)、胎牛血清(由华西医科大学生物学教研室制备)、四甲基偶氮唑蓝(Sigma)、二甲基亚砜(Sigma)、HBsAg、HBeAg ELISA试剂盒(华美生物工程公司), HBV DNA PCR杂交试剂盒( 华美生物工程公司).
1.2.1 含药血清的制备: 实验家兔每2只一组, 分为正常血清组(Ⅰ组)、乙肝宁颗粒组(Ⅱ组)、愈肝胶囊组(Ⅲ组). 分别灌服洁净生理盐水5 mL/次, 乙肝宁颗粒, 3.4 g/(kg•d)(成人公斤体重用量的12倍[1], 相当于临床等效剂量), 愈肝胶囊0.7 g/(kg•d), (成人千克质量用量的12倍, 相当于临床等效剂量), 3/d, 第7日上午连续给药2次(间隔1 h)[2], 1 h后, 无菌采血, 3 000 r/min 离心20 min分离血清, 56℃灭活30 min[3], 抽滤除菌后-20℃冰箱保存备用.
1.2.2 体外培养实验分组方法: 每3孔为1组, 共分8组, 分别为细胞对照组(2.2.15细胞常规培养)、正常血清组(含Ⅰ组血清) 、 乙肝宁颗粒组(含浓度为1∶1 Ⅱ组药物血清)愈肝胶囊A组(含浓度为1∶1 Ⅲ组药物血清)、愈肝胶囊B组(含浓度为1∶2 Ⅲ组药物血清)、愈肝胶囊C组(含浓度为1∶4 Ⅲ组药物血清)、愈肝胶囊D组(含浓度为1∶8 Ⅲ组药物血清)、愈肝胶囊E组(含浓度为1∶16 Ⅲ组药物血清).
1.2.3 细胞培养: 将长满2.2.15细胞的培养瓶用2.5 g/L胰蛋白酶消化3 min左右; 培养液吹打使细胞分散, 配制成1×108/L种于细胞培养板中, 96孔板0. 2 mL/孔; 24孔板1.2 mL/孔, 37℃ 50 mL/L CO2培养.
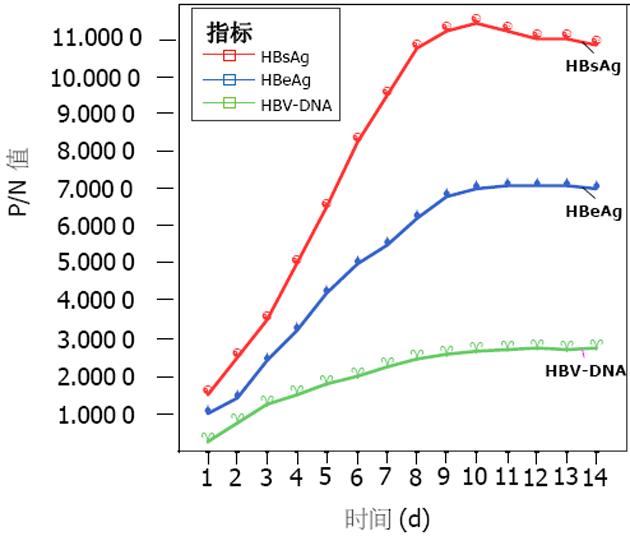
1.2.4 2.2.15细胞分泌HBsAg、HBeAg及HBV DNA规律的测定[3]: 将2.2.15细胞按1×108个/L的浓度传入多个培养瓶, 37℃ 50 mL/L CO2 培养, 每天收集培养液上清. 供测 HBsAg、HBeAg、HBV DNA用, 共14 d. 同法重复进行采样和检测2次.
1.2.5 含愈肝胶囊血清对2.2.15细胞存活率影响实验: 96孔板细胞培养24 h后, 含愈肝胶囊血清用培养液倍比稀释5个浓度, 加入细胞培养板, 每浓度3孔, 并设正常细胞(2.2.15细胞常规培养), 正常血清(含Ⅰ组血清)、阳性对照组(含浓度为1∶1 Ⅱ组药物血清), 每4 d换同浓度含药血清, 10 d后MTT染色法[4]测定细胞存活率. 加入MTT 400 mg/L, 100 μL/孔, 4-6 h后加二甲基亚砜, 完全溶解后测定570 nm波长A值. 细胞存活率计算公式为: 细胞存活率 = 药物处理细胞[A]/药物未处理细胞[A]×100%.
1.2.6 含愈肝胶囊血清体外抗HBV活性的测定: 24孔板细胞培养4 d后各组分别加入不同浓度的药物血清培养基, 继续培养5 d收集上清液, 供测HBsAg、HBeAg、HBV DNA用. 然后再加入相应不同浓度的药物血清培养基, 10 d后, 再收集上清液, 供测HBsAg、HBeAg、HBV DNA用. 重复2次, 取平均值.
1.2.7 样品检测与结果计算方法: 上清液HBsAg、HBeAg的检测: ELISA法. 上清液HBV DNA 的测定: PCR杂交试验法.
P/N值 = 试验孔cpm/阴性孔cpm
抑制率 = (细胞对照cpm值-给药组cpm值/细胞对照cpm值-空白对照cpm值)×100%
抑制率>50%判为有抑制作用.
统计学处理 用SPSS10.0统计软件处理. 所有计量资料以均值加减标准差(mean±SD)表示, 进行方差分析, 组间两两比较用SNK法; 两时间点前后均值比较用配对t检验, 检验水准α = 0.05.
含愈肝胶囊血清各组作用10 d后, 各组细胞存活率均>82%, 细胞生长良好, 结果显示: 含愈肝胶囊血清对细胞存活率无明显影响. 含愈肝胶囊血清对HBV抑制率测定(图2).
愈肝胶囊重用黄芪补益脾胃之气, 以纠正肝病脾气虚弱这一根本问题, 党参、白术、云苓健脾益气, 采用中药含药血清药理学研究方法, 以含有愈肝胶囊药物成分的血清代替中药粗提物进行体外实验, 不仅能反映愈肝胶囊中可吸收部分的直接作用, 且能反映药物成分在机体作用下形成的代谢产物和药物诱生的机体内源性物质的间接效果, 克服了中药制剂本身理化性质对实验结果的干扰[5-7]; 在动物选择、给药方案、采血时间[8], 血清灭活与保存[9-10], 血清添加及对照组设立[11]等各方面均按该实验方法研究的最新、最可靠的方法操作, 最大限度地保证了含药血清的质量和有效成分, 达到了体外实验和体内实验的完美结合.
1990年之前, 国外学者利用PLC/PRF/5细胞株作了大量抗HBV研究工作 [12-13], 1986年, Sereau et al[14]人利用电穿孔基因转移技术将克隆的环状DNA与带耐药新霉素基因的载体质粒重组, 转染近似正常肝细胞的HepG2细胞系, 获得2.2.15细胞系, 使HBV体外组织培养获得了真正的突破. 2.2.15细胞可以在体外无性繁殖, 能够长期稳定的向培养上清液中分泌HBsAg、HBeAg和完整的Dane颗粒, 而且还能产生大量的复制中间体, 细胞内含有整合型和游离型HBV DNA, 还有rcDNA和单链DNA似为病毒基因组的复制型, 但无cccDNA. 整合分子在培养期内始终稳定[15]. 在我们所用的培养条件下, 现有的2.2.15细胞株能稳定地分泌HBsAg、HBeAg、HBV DNA, 愈肝胶囊含药血清培养2 d即可稳定检出HBsAg、HBeAg, 各标志物的分泌量均随培养时间的延长而升高, 10 d达最高峰, 此后不再增加; 培养1 d可从上清液中检出HBV DNA, 并可持续至14 d, 11 d后处于高峰, 不再增加. 其复制规律与HBsAg、HBeAg分泌规律相似, 可用于抗HBV药物筛选实验. 任何药物在达到一定浓度作用一定时间时, 都会产生细胞毒性而造成死亡, 从而影响药物作用的判定. 本实验结果显示各不同浓度含药血清作用10 d后, 细胞的存活率均很高. 故本实验利用中药含药血清在体外实验中的优势避免了因细胞死亡造成的HBsAg、HBeAg、HBV DNA滴度下降, 更好地反映药物的抗HBV活性.
各组含愈肝胶囊血清与空白对照组及正常血清组比较认为愈肝胶囊不同浓度含药血清对乙肝病毒分泌HBsAg、HBeAg、HBV DNA均有一定的抑制作用, 各组含愈肝胶囊血清与乙肝宁颗粒组比较, 可以认为含愈肝胶囊血清A组抑制HBsAg、HBeAg及HBV DNA的作用均优于乙肝宁颗粒, 有统计学意义(P<0.05); 含愈肝胶囊血清B组则对HBeAg的作用可以优于乙肝宁颗粒(P<0.05); 而含愈肝胶囊血清E组抗乙肝病毒的作用则明显低于乙肝宁颗粒(P<0.05); 从而认为含愈肝胶囊血清抗乙肝病毒的作用呈剂量依赖性; 尤其值得重视的是其对HBV DNA的抑制作用, 含愈肝胶囊血清A组和B组作用10 d时, 抑制率可达65%-67%, 提示愈肝胶囊在抗乙肝病毒的治疗中具有较好的应用前景.
电编: 张勇 编辑: 张海宁
| 3. | 叶 下珠. 复方肝丹体外抗HBV作用特点的实验研究. 中国中医基础医学杂志. 1999;5:29-33. |
| 4. | Mosmann T. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. J Immunol Methods. 1983;65:55-63. [DOI] |
| 5. | Amagaya S, Harada K, Miyake A, Iwama H, Ogihara Y. A new pharmacological testing method-different effects of levamisole and the serum of mice orally treated with levamisole on mitogenic activity of lipopolysaccharide. Chem Pharm Bull. 1989;37:1117-1119. [PubMed] [DOI] |
| 6. | Umeda M, Amagaya S, Ogihara Y. Effects of certain herbal medicines on the biotransformation of arachidonic acid: a new pharmacological testing method using serum. J Ethnopharmacol. 1988;23:91-98. [PubMed] [DOI] |
| 12. | Yamashita Y, Koike K, Takaoki M, Matsuda S. Suppression of HBsAg production in PLC/PRF/5 human hepatoma cell line by interferons. Microbiol Immunol. 1988;32:1119-1126. [PubMed] [DOI] |
| 13. | Sells MA, Chen ML, Acs G. Production of hepatitis B virus particles in Hep G2 cells transfected with cloned hepatitis B virus DNA. Proc Natl Acad Sci USA. 1987;84:1005-1009. [PubMed] [DOI] |