修回日期: 2005-05-01
接受日期: 2005-05-23
在线出版日期: 2005-07-15
目的: 探讨磁共振血管造影(MRA)对肝移植术后血管解剖的显示及诊断并发症的价值.
方法: 11例原位肝移植术后患者均用磁共振(MR)快速自选回波(TSE)序列及快速小角度激发梯度回波(FLASH)序列常规扫描、钆喷替酸葡甲胺(Gd-DTPA)动态增强3D MRA检查, 分析各序列图像特点.
结果: 术后血管正常4例.血管并发症7 例: 肝动脉过长迂曲2例, 肝动脉供体端瘤样轻度扩张2例; 门静脉轻度狭窄2例, 位于吻合口; 肝静脉末梢分支杵状扩张 2例; 下腔静脉血栓1例.
结论: MRA可清楚显示肝移植术后血管解剖并准确、快速诊断肝移植术后出现的血管并发症, 对指导临床诊断及治疗具有重要意义.
引文著录: 郭友, 张雪林, 陈曌. 磁共振血管成像对肝移植术后血管的评价. 世界华人消化杂志 2005; 13(13): 1630-1632
Revised: May 1, 2005
Accepted: May 23, 2005
Published online: July 15, 2005
N/A
- Citation: N/A. N/A. Shijie Huaren Xiaohua Zazhi 2005; 13(13): 1630-1632
- URL: https://www.wjgnet.com/1009-3079/full/v13/i13/1630.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v13.i13.1630
肝移植是目前公认的肝脏终末期疾病治疗方法之一, 但与肝移植手术相关的术后并发症, 特别是血管并发症, 仍然是导致移植肝功能衰竭和患者死亡的主要原因之一.磁共振血管造影(MRA)作为一种安全、无创、精确的影像技术已成为早期发现肝移植后血管并发症的一种重要手段[1-5].我们分析11例原位肝移植术后MRA影像学表现, 并结合文献复习探讨MRA对肝移植术后血管解剖的显示及并发症的诊断价值.
收集东莞市人民医院和南方医院2002-07/2004-12同时具有MR和多普勒超声资料的11例肝移植患者, 全为男性, 年龄40-58岁, 平均49岁.术前临床诊断为原发性肝癌2例, 重症肝硬化9例.9例行原位经典式肝移植, 所有血管采用端端吻合, 2例行背驮式原位肝移植术, 其下腔静脉采用端侧吻合, 肝动脉及门静脉端端吻合.移植后至首次MRA检查最短时间为15 d, 最长为2年.复查间隔时间为每月1次, 3次以后根据病情延长为每2-3 mo 1次.所有患者均在MRA检查的同时行多普勒超声检查.
11例患者移植术后共作MR检查25次.MRA成像应用超导型Seimens 1.5 T系统及TORSOPA相控阵线圈.(1)MR平扫: 冠状面定位相: 真实稳态进动快速成像(true FISP)T2WI, TR 4.3 ms, TE 2.1 ms, 视野(FOV)42 cm×45 cm, 矩阵 360×512.上腹部轴面常规FLASH T1WI: TR 107 ms, TE 4.8 ms; TSE T2WI: TR 4 000 ms, TE 101 ms.FOV 26 cm×35 cm, 层厚6 mm, 层间距1.8 mm, 矩阵 230×512.T1WI包括不抑脂和抑脂序列, T2WI序列抑脂.所有序列均屏气扫描.(2)三维增强磁共振血管成像(3D-CE-MRA): 用高压注射器以3 mL/s流率经肘静脉注射0.3 mmol/kg对比剂钆喷替酸葡甲胺(Gd-DTPA)和30 mL生理盐水.采用团注对比剂测试时间以计算扫描延迟时间, 分三次扫描获得动脉期、门静脉期和下腔静脉期图像.原始图像行MIP和MPR重建.(3)增强扫描: 在MRA成像后, 迅速采用与平扫FLASH T1WI抑脂序列完全相同参数行轴面和冠状面扫描.
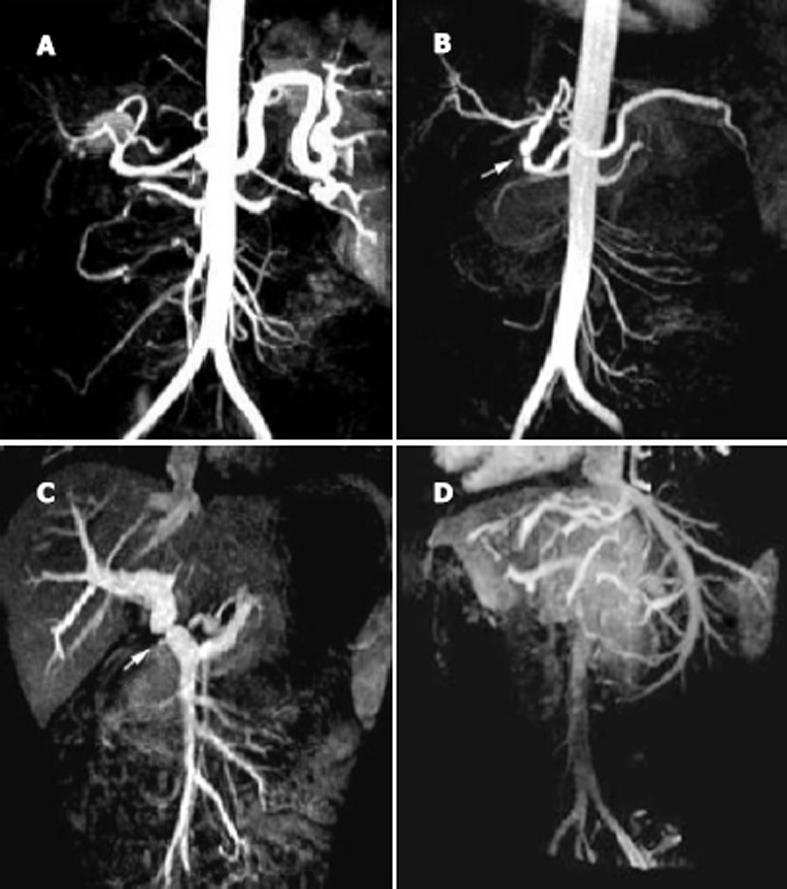
3D-CE-MRA原始图像MIP重建及容积或者曲面MPR重建可以很好显示血管吻合口以及迂曲血管走行.可显示从腹腔干到肝内动脉的近段分支(图1AB)、门静脉主干及分支、脾静脉、肠系膜上静脉(图1C)和肝静脉及下腔静脉(图1CD).
肝动脉、门静脉和下腔静脉吻合口通畅3例(图1A).1例供体门静脉管径略小于受体门静脉.肝移植术后早期MR T2WI图像见到门静脉周围高信号1例, 持续3 wk后消失.
肝动脉过长迂曲2例, 肝动脉供体端瘤样轻度扩张2例(图1B), 但肝动脉末梢分支显影正常.门静脉轻度狭窄2例, 位于吻合口(图1C), 且门静脉供体段与受体段的管径不相等, 门静脉肝内分支均正常.肝静脉末梢分支杵状扩张2例(图1D), 而其下腔静脉未见异常.下腔静脉血栓1例, MR表现为高信号血管腔内椭圆形低无信号区.追踪复查, 2例肝静脉末梢分支杵状扩张患者6 mo后肝静脉末梢分支扩张程度降低, 但仍有轻度扩张, 下腔静脉血栓治疗1 mo后多普勒超声及MRA复查血栓消失.其余血管并发症影像学表现均无明显变化.
1例肝动脉过长迂曲合并肝动脉供体端瘤样轻度扩张诊断为肝动脉过长迂曲.门静脉轻度狭窄1例诊断为正常, 1例诊断为可疑狭窄.肝静脉末梢分支杵状扩张未发现.其余诊断与MRA相符.
多普勒超声对肝移植术后并发症的检测价值已被广泛研究, 多数学者认为超声发现血栓形成和血管狭窄的灵敏度相当高, 然而其对血管吻合口的直接显示较困难[6].不同学者对多普勒超声诊断血栓形成和狭窄的结果不同.从本组实验看MRA对血管解剖的显示及并发症的诊断均优于多普勒超声, 所以MRA可有效弥补多普勒超声的缺陷.
MR检查比计算机断层成像(CT)或多普勒超声困难得多.但是, 在约40 min的MR检查过程中, 绝大多数患者能够配合检查.屏气时间通常为15-20 s.对于缺氧患者可适当调整扫描视野和空间分辨率等以降低扫描时间.MR可实现"一站式"检查, 即一次检查可获得腹部血管、胰胆管成像以及上腹部器官的形态学改变.而且, MR对比剂毒副作用很小.CT因为其X线辐射以及对比剂肝、肾毒性的限制, 不适合肝移植术后反复应用.数字减影血管造影术对血管分支显影良好, 但是对迂曲血管难以充分显示其走行的细节, 而且是有创性检查, 患者难以接受.
熟悉肝移植术后正常的MRA表现有助于正确评价肝移植术后并发症[3,5-6].肝移植术后最完美的血管表现是吻合口通畅, 血管分支移行正常.肝移植术后早期MR T2WI图像常可见到门静脉周围高信号, 可持续数周.门静脉周围异常高信号与移植手术阻断淋巴正常引流而导致淋巴水肿有关.肝移植术后早期肝门门静脉可有暂时狭窄, 可能与周围水肿有关.供体门静脉管径与受体门静脉不相等, 这也是肝移植术后较常见的表现.
3D-CE-MRA作为一种相对较新的影像技术, 其最优化的扫描参数还未统一.本组实验采用更薄层厚、更短的TR以缩短扫描时间, 屏气扫描, 因为屏气完全时运动伪影相对较少, 血管末梢分支显影更清楚.运用零插入内插法K空间填充技术、脂肪抑制扫描、部分重叠重建后处理可使图像质量获得质的提高[7].本组实验所有病例均采用团注对比剂测试时间以计算扫描延迟时间, 从而获得最佳扫描时期.
血管并发症主要包括血管吻合口狭窄和血栓形成.文献报道肝动脉狭窄的发生率为11%, 肝动脉血栓形成是最常见、最具破坏性的血管并发症[8], 其成人肝移植术后的发生率为4-12%, 而儿童肝移植术后的发生率高达42%.静脉并发症的发生率低于动脉并发症, 门静脉血栓形成和狭窄的发生率为1-2%, 下腔静脉并发症的发生率低于1%.但本组实验中仅见1例血栓形成, 可能与移植术前准备充分、术后预防措施得力有关.
本组实验中肝动脉过长迂曲及肝固有动脉供体段瘤样轻度扩张可能与手术操作有关.肝动脉动脉瘤文献报道仅有假性动脉瘤[2], 但是本例不支持假性动脉瘤的诊断, 因为该瘤壁在增强延迟期未见强化表现, 而且术后1 a内3次CE-MRA检查肝动脉改变无明显变化.另外肝静脉末梢分支杵状扩张, 可能与排斥反应有关.以上两种血管改变均未见文献报道类似并发症, 尚待进一步研究.
总之, 磁共振血管造影作为一种非侵袭性影像检查方法, 可清楚显示肝移植术后血管解剖并准确、快速诊断肝移植术后出现的血管并发症, 对指导临床诊断及治疗具有重要意义.
编辑: 王谨晖 审读:张海宁
| 1. | Pandharipande PV, Lee VS, Morgan GR, Teperman LW, Krinsky GA, Rofsky NM, Roy MC, Weinreb JC. Vascular and extravascular complications of liver transplantation: comprehensive evaluation with three-dimensional contrast-enhanced volumetric MR imaging and MR cholangiopancreatography. Am J Roentgernol. 2001;177:1101-1107. [PubMed] [DOI] |
| 2. | Glockner JF, Forauer AR, Solomon H, Varma CR, Perman WH. Three-dimensional gadolinium-enhanced MR angiography of vascular complications after liver transplantation. Am J Roentgernol. 2000;174:14471453. [PubMed] [DOI] |
| 3. | Ito K, Siegelman ES, Stolpen AH, Mitchell DG. MR imaging of complications after liver transplantation. Am J Roentgernol. 2000;175:11451149. [PubMed] [DOI] |
| 4. | Stafford-Johnson DB, Hamilton BH, Dong Q, Cho KJ, Turcotte JG, Fontana RJ, Prince MR. Vascular complications of liver transplantation: evaluation with gadolinium-enhanced MR angiography. Radiology. 1998;207:153160. [PubMed] [DOI] |
| 5. | Nghiem HV, Tran K, Winter TC 3rd, Schmiedl UP, Althaus SJ, Patel NH, Freeny PC. Imaging of complications in liver transplantation. Radiographics. 1996;16:825-840. [PubMed] [DOI] |
| 6. | Crossin JD, Muradali D, Wilson SR. US of liver transplants: normal and abnormal. Radiographics. 2003;23:1093-1114. [PubMed] [DOI] |